Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЭЛЕКТРОЛИЗ
Содержание
- 1. ЭЛЕКТРОЛИЗ
- 2. Цель: изучить сущность процесса электролизаЗадачи: раскрыть принцип
- 3. Пятница, 13…Вам страшно? А мне очень..!
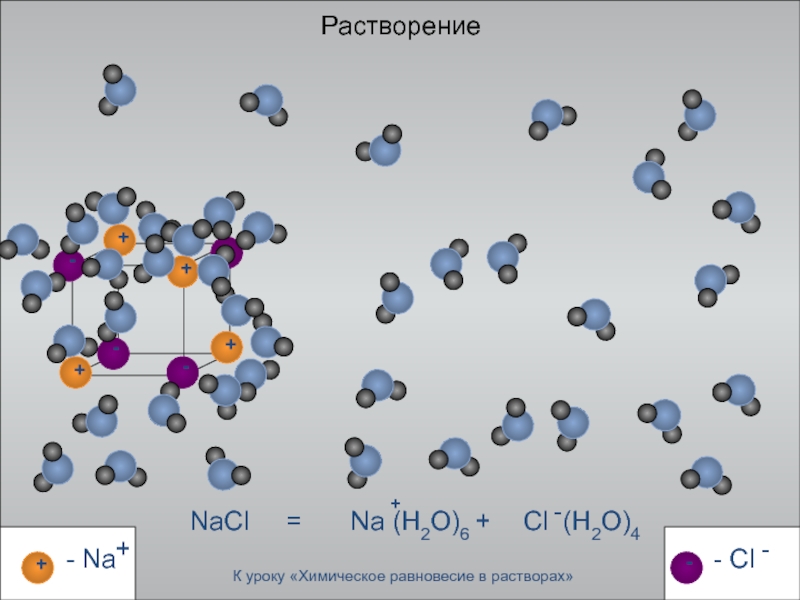
- 4. РастворениеNaCl =К уроку «Химическое равновесие в растворах»
- 5. Электролиз – дословно: «лизиз» - разложение, «электро» - электрическим током.
- 6. Электролиз. Электролиз – окислительно-восстановительный процесс, протекающий на
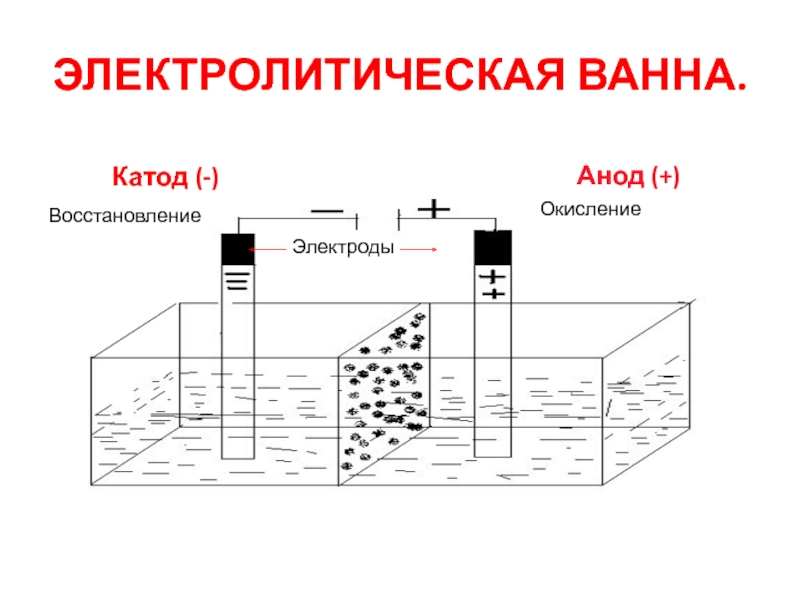
- 7. ЭЛЕКТРОЛИТИЧЕСКАЯ ВАННА. Катод (-)Анод (+)ВосстановлениеОкислениеЭлектроды
- 8. Окислительно-восстановительные процессы легко запомнить так:На АНОД
- 9. AuCl+-Электролиз раствора соли
- 10. Применение электролиза. Для получения щёлочных, щёлочноземельных
- 11. Применение ЭЛЕКТРОЛИЗАКыштымский Медеэлектролитный завод:- получение алюминия- получение
- 12. ИТЕРБИЙ - для изготовления оптоволоконных лазеров (стоимость
- 13. ЭЛЕКТРОЛИЗОМ получают два основных продукта : серную кислоту и цинк
- 14. Применение ЭЛЕКТРОЛИЗАОдно из новых направлений электролиза –
- 15. Другие применения электролиза. Кроме указанных выше электролиз
- 16. Спасибо за терпение!Спасибо за внимание!Спасибо за урок!
- 17. Скачать презентанцию
Цель: изучить сущность процесса электролизаЗадачи: раскрыть принцип работы электролизёра суть катодных и анодных процессов примеры электролиза применение электролиза
Слайды и текст этой презентации
Слайд 2
Цель: изучить сущность процесса электролиза
Задачи:
раскрыть принцип работы электролизёра
суть катодных и анодных процессов
Слайд 3Пятница, 13…Вам страшно?
А мне очень..!
Если в пятницу тринадцать
Календарь
вам показал, Интерес при этом к жизни До нуля у вас упал. Не
спеши трястись от страха, Кто сказал: тринадцать зло, Тем испортив эту дату, Всем нам сделав западло? Ну, а пятница тем болей - Просто божья благодать, Ведь не даром всю неделю Мы ее готовы ждать!Слайд 6Электролиз.
Электролиз – окислительно-восстановительный процесс, протекающий на электродах при прохождении
постоянного электрического тока через расплав или раствор электролита.
Электролиты: соли,
щёлочи, кислоты.Слайд 8Окислительно-восстановительные процессы легко запомнить так:
На
АНОД
идут
ОТРИЦАТЕЛЬНЫЕ
ионы,
там происходит
процесс
ОКИСЛЕНИЯ
На
КАТОД
идут
ПОЛОЖИТЕЛЬНЫЕ
ионы, там происходит
процесс
ВОССТАНОВЛЕНИЯ
Слайд 10
Применение электролиза.
Для получения щёлочных, щёлочноземельных металлов, алюминия, лантаноидов
Для получения точных
металлических копий, что называется гальванопластикой
Для защиты металлических изделий от коррозии
и для придания декоративного вида. Отрасль прикладной электрохимии, которая занимается покрытием металлических изделий другими металлами называется ГАЛЬВАНОСТЕГИЕЙ.Слайд 11Применение ЭЛЕКТРОЛИЗА
Кыштымский Медеэлектролитный завод:
- получение алюминия
- получение меди;
выпуск золота и
серебра в слитках;
получение металлов платиновой группы;
получение технического селена
Слайд 12ИТЕРБИЙ - для изготовления
оптоволоконных лазеров
(стоимость чистого составляет
250-300
долларов за килограмм)
Металлы платиновой группы :
палладиевая оправу для драгоценных
камней,не тускнеет и стоек к коррозии;
иридий обладает очень высокой твердостью
и его используют для изготовления
электроконтактов,
хирургических инструментов,
точных химических весов;
-рутений (Россия) - самый редкий из
платиновой группы,используют при изготовлении
проводов, контактов, электродов,
лабораторной посуды, ювелирных изделий.
Слайд 14Применение ЭЛЕКТРОЛИЗА
Одно из новых направлений электролиза – это косметология. Существует
несколько видов элекроэпиляции, один из которых основан на ЭЛЕКТРОЛИЗЕ. В
основу метода положено электрохимическое действие гальванического тока. В результате анодно-катодной реакции происходит образование соляной кислоты, которая, распадаясь, преобразуется в едкую щелочь. Именно эти два химических вещества приводят к электролитическому ожогу и разрушению волосяного фолликула.Слайд 15Другие применения электролиза.
Кроме указанных выше электролиз нашел применение и в
других областях. Укажем некоторые из них:
а) получение оксидных защитных
пленок на металлах (анодирование);б) электрохимическая обработка поверхности металлического изделия (полировка);
в) электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др.);
г) очистка воды – удаление из нее растворимых примесей. В результате получается так называемая мягкая вода (по своим свойствам приближающаяся к дистиллированной);
д) электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т.д.).