Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Гидролиз солей
Содержание
- 1. Гидролиз солей
- 2. Изменение цвета различных индикаторов при действии растворов кислот и щелочей
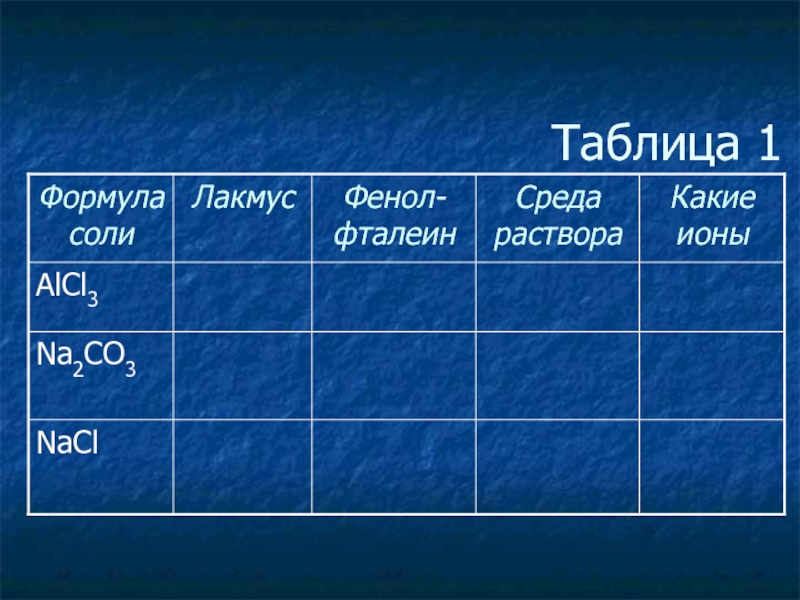
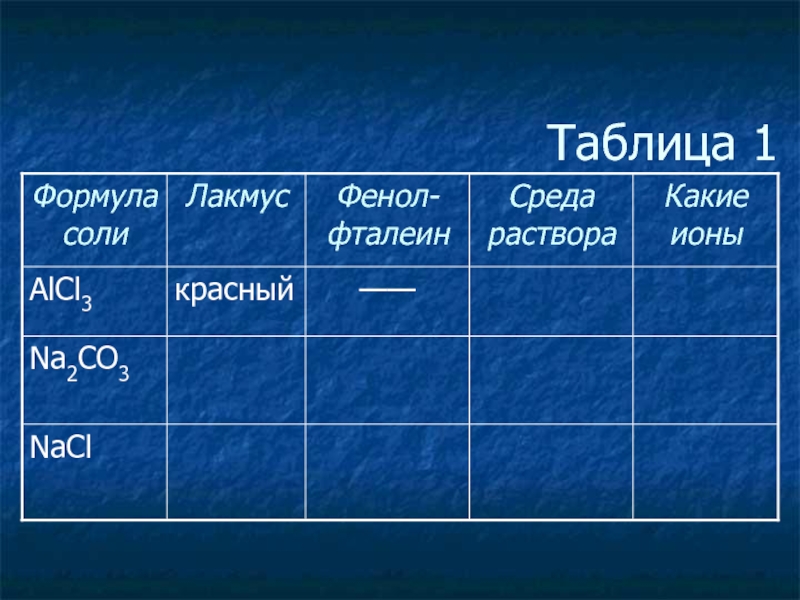
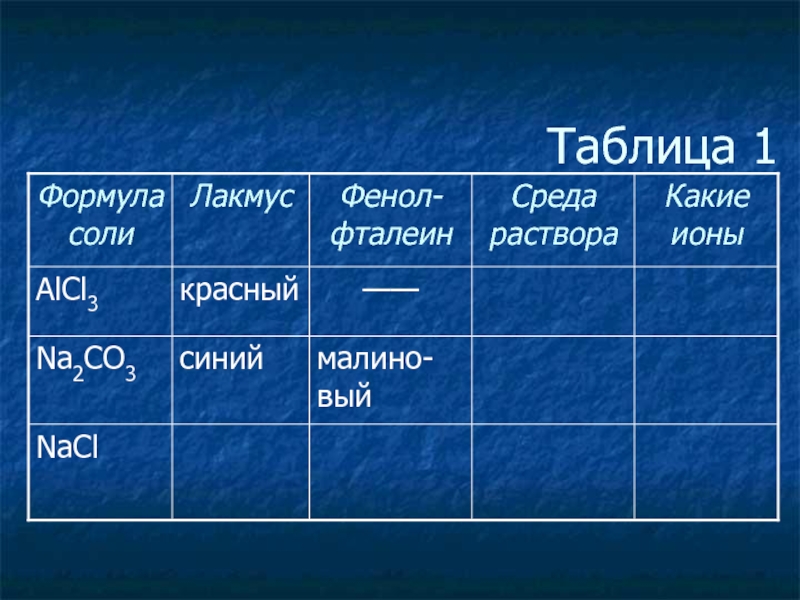
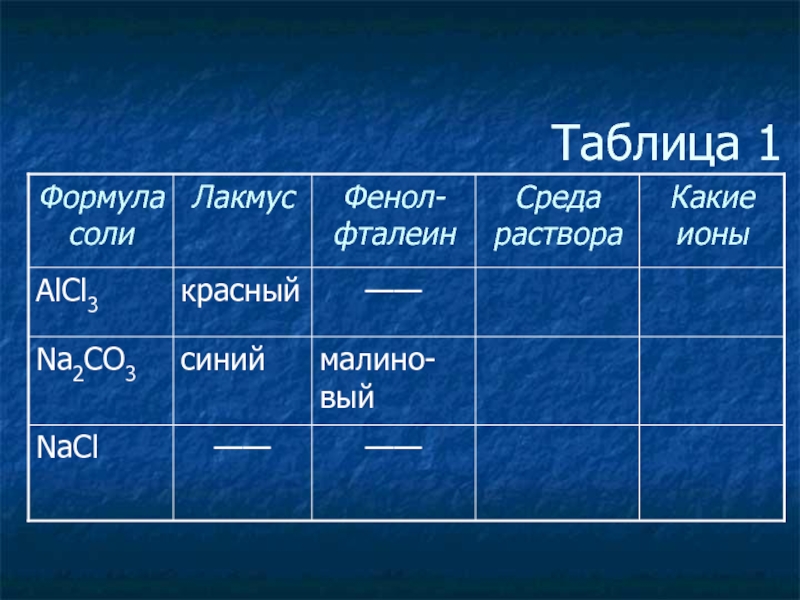
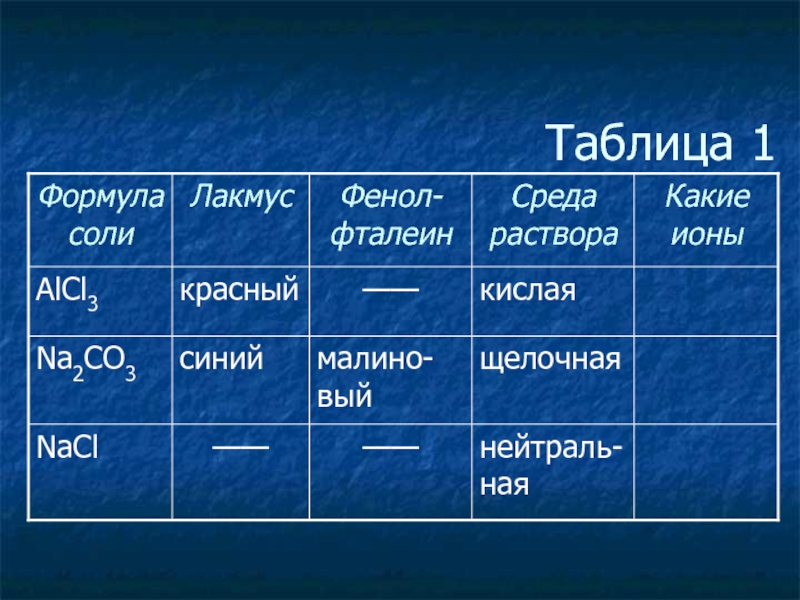
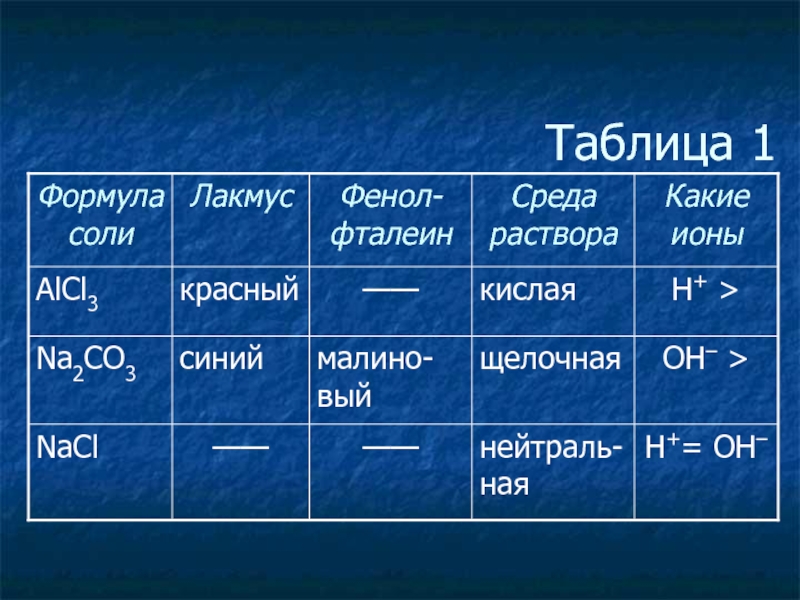
- 3. Таблица 1
- 4. Таблица 1
- 5. Таблица 1
- 6. Таблица 1
- 7. Таблица 1
- 8. Таблица 1
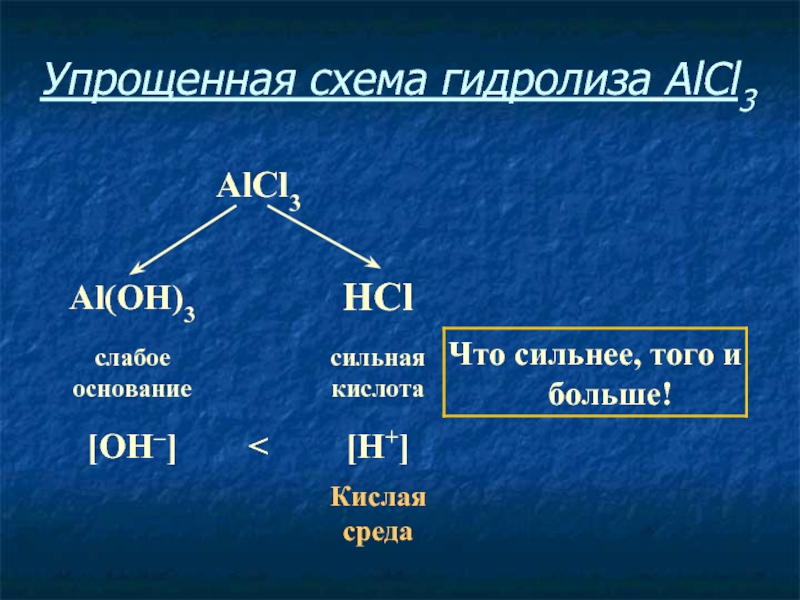
- 9. Упрощенная схема гидролиза AlCl3
- 10. Соль, образованная слабым основанием и сильной кислотой,
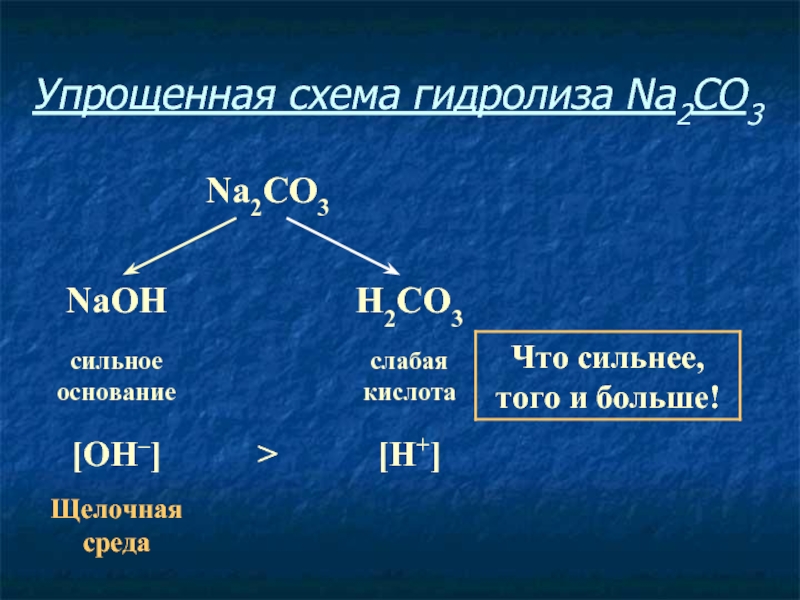
- 11. Упрощенная схема гидролиза Na2CO3
- 12. Соль, образованная сильным основанием и слабой кислотой, имеет щелочную среду, так как в растворе избыток гидроксид-ионов.
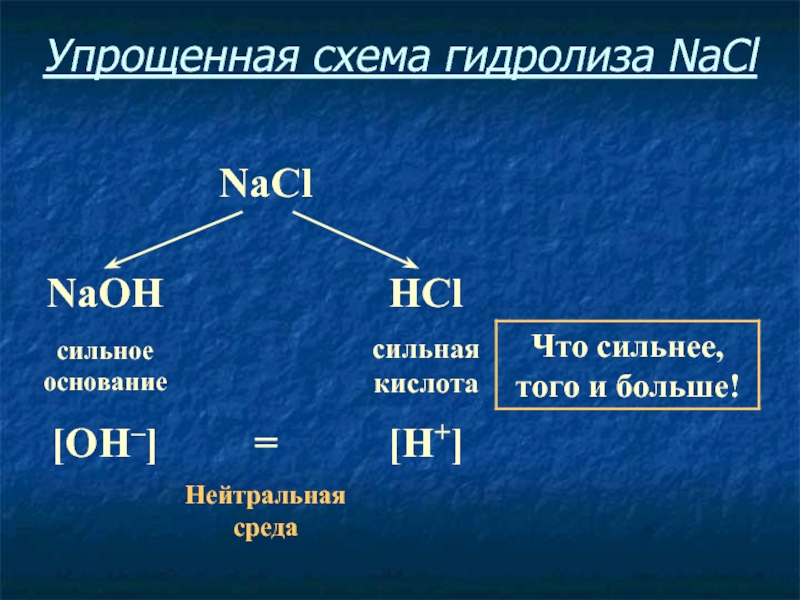
- 13. Упрощенная схема гидролиза NaCl
- 14. Соль, образованная сильным основанием и сильной кислотой,
- 15. Гидролиз — это реакция обмена между некоторыми солями и водой («гидро» — вода, «лизис» — разложение)
- 16. Уравнения гидролиза АlСl3 АlСl3 ↔ Аl3+ + 3Сl–
- 17. Уравнения гидролиза АlСl3АlСl3 ↔ Аl3+ + 3Сl–Н2O ↔ Н+ + ОН–
- 18. Уравнения гидролиза АlСl3АlСl3 ↔ Аl3+ + 3Сl–Н2O ↔ Н+ + ОН–_______________________________________________________________________________
- 19. Уравнения гидролиза АlСl3АlСl3 ↔ Аl3+ + 3Сl–Н2O
- 20. Уравнения гидролиза АlСl3АlСl3 ↔ Аl3+ + 3Сl–Н2O
- 21. Уравнения гидролиза АlСl3АlСl3 ↔ Аl3+ + 3Сl–Н2O
- 22. Уравнения гидролиза Na2CO3 Na2CO3 ↔ 2Na+ + СO32–
- 23. Уравнения гидролиза Na2CO3Na2CO3 ↔ 2Na+ + СO32–Н2O ↔ Н+ + ОН–
- 24. Уравнения гидролиза Na2CO3Na2CO3 ↔ 2Na+ + СO32–Н2O ↔ Н+ + ОН–____________________________________________________________________________
- 25. Уравнения гидролиза Na2CO3Na2CO3 ↔ 2Na+ + СO32–Н2O
- 26. Уравнения гидролиза Na2CO3Na2CO3 ↔ 2Na+ + СO32–Н2O
- 27. Уравнения гидролиза Na2CO3Na2CO3 ↔ 2Na+ + СO32–Н2O
- 28. Уравнения гидролиза NaClNaCl ↔ Na+ + Сl–Н2O
- 29. Какую среду будут иметь водные растворы следующих
- 30. Ответы
- 31. Zn(NO3)2 ↔ Zn2+ + 2NO3–Н2O ↔ Н+
- 32. K2SO4 ↔ 2K+ + SO42–Н2O ↔ Н+
- 33. Na2S ↔ 2Na+ + S2–Н2O ↔ Н+
- 34. О значении и применении гидролиза...
- 35. Домашнее задание.Пользуясь таблицей «Сильные и слабые электролиты»,
- 36. Урок окончен
- 37. Источники материаловКузьменко Н.Е., Еремин В.В., Попков В.А.
- 38. Скачать презентанцию
Изменение цвета различных индикаторов при действии растворов кислот и щелочей
Слайды и текст этой презентации
Слайд 1«Гидролиз солей»
Тема урока:
Новикова Ирина Петровна
учитель химии
МОУ Совхозная сош
Тамбовский район
Слайд 10Соль, образованная слабым основанием и сильной кислотой, имеет кислую среду,
так как в растворе избыток ионов водорода.
Слайд 12Соль, образованная сильным основанием и слабой кислотой, имеет щелочную среду,
так как в растворе избыток гидроксид-ионов.
Слайд 14Соль, образованная сильным основанием и сильной кислотой, имеет нейтральную среду,
так как в растворе одинаковое количество ионов водорода и гидроксид-ионов.
Слайд 15Гидролиз — это реакция обмена между некоторыми солями и водой
(«гидро» — вода, «лизис» — разложение)
Слайд 18Уравнения гидролиза АlСl3
АlСl3 ↔ Аl3+ + 3Сl–
Н2O ↔ Н+ +
ОН–
_______________________________________________________________________________
Слайд 19Уравнения гидролиза АlСl3
АlСl3 ↔ Аl3+ + 3Сl–
Н2O ↔ Н+ +
ОН–
_______________________________________________________________________________
Al3+ + 3Сl– + Н2O ↔ АlOН2+ + 3Сl– +
Н+Слайд 20Уравнения гидролиза АlСl3
АlСl3 ↔ Аl3+ + 3Сl–
Н2O ↔ Н+ +
ОН–
_______________________________________________________________________________
Al3+ + 3Сl– + Н2O ↔ АlOН2+ + 3Сl– +
Н+Аl3+ + Н2O ↔ АlOН2+ + Н+
Слайд 21Уравнения гидролиза АlСl3
АlСl3 ↔ Аl3+ + 3Сl–
Н2O ↔ Н+ +
ОН–
___________________________________________________________________
Al3+ + 3Сl– + Н2O ↔ АlOН2+ + 3Сl– +
Н+Аl3+ + Н2O ↔ АlOН2+ + Н+
Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет.
Слайд 24Уравнения гидролиза Na2CO3
Na2CO3 ↔ 2Na+ + СO32–
Н2O ↔ Н+ +
ОН–
____________________________________________________________________________
Слайд 25Уравнения гидролиза Na2CO3
Na2CO3 ↔ 2Na+ + СO32–
Н2O ↔ Н+ +
ОН–
____________________________________________________________________________
2Na+ + СO32– + Н2O ↔ 2Na+ + HCO3– +
ОН–Слайд 26Уравнения гидролиза Na2CO3
Na2CO3 ↔ 2Na+ + СO32–
Н2O ↔ Н+ +
ОН–
____________________________________________________________________________
2Na+ + СO32– + Н2O ↔ 2Na+ + HCO3– +
ОН–СO32– + Н2O ↔ НСO3– + ОН–
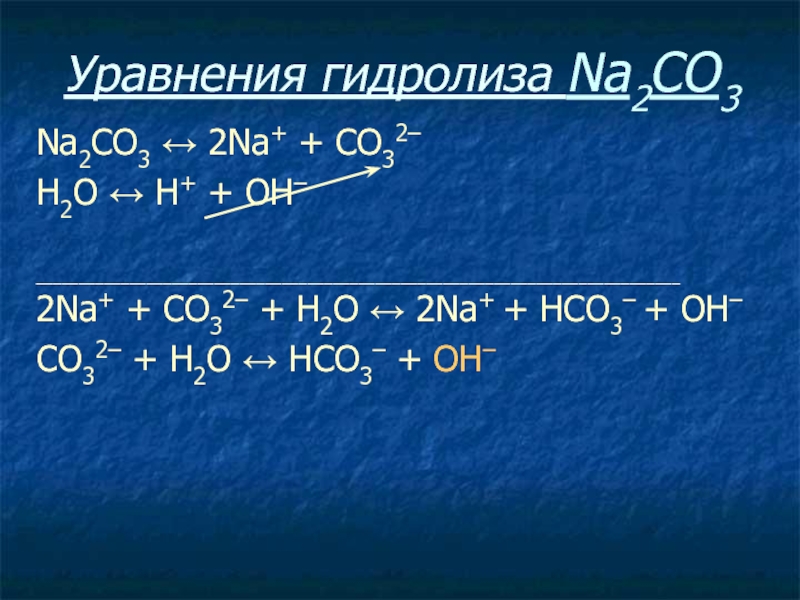
Слайд 27Уравнения гидролиза Na2CO3
Na2CO3 ↔ 2Na+ + СO32–
Н2O ↔ Н+ +
ОН–
____________________________________________________________________________
2Na+ + СO32– + Н2O ↔ 2Na+ + HCO3– +
ОН–СO32– + Н2O ↔ НСO3– + ОН–
Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым.
Слайд 28Уравнения гидролиза NaCl
NaCl ↔ Na+ + Сl–
Н2O ↔ Н+ +
ОН–
____________________________________________________________________________
Na+ + Сl– + Н2O ↔ Na+ + Cl– +
H2OОдинаковое количество гидроксид-ионов и ионов водорода дает соли нейтральную среду, поэтому индикаторы не меняют окраску (гидролизу не подвергается).
Слайд 29Какую среду будут иметь водные растворы следующих солей:
1 вариант
2 вариант
а) нитрата цинка (II) а) хлорида меди (II) б) сульфата калия б) сульфита натрия в) сульфида натрия в) нитрата бария
Составьте ионное уравнение гидролиза этих солей.
Слайд 31Zn(NO3)2 ↔ Zn2+ + 2NO3–
Н2O ↔ Н+ + ОН –
________________________________________________________
Zn2+
+ 2NO3– + Н2O ↔ ZnOН+ + 2NO3– + Н+
Zn2+
+ Н2O ↔ ZnOН+ + Н+ (среда кислая)2 вариант
CuCl2 ↔ Cu2+ + 2Сl –
Н2O ↔ Н+ + ОН –
_______________________________________________________________________________________________________________________
Cu2+ + Сl – + Н2O ↔ CuOH+ + Cl – + Н+
Сu2+ + Н2O ↔ СuOH+ + Н+ (среда кислая)
а) 1 вариант
Слайд 32K2SO4 ↔ 2K+ + SO42–
Н2O ↔ Н+ + ОН –
____________________________________________________________________________
2K+
+ SO42– + Н2O ↔ 2K+ + SO42– + H2O
(среда нейтральная)2 вариант
Na2SO3 ↔ 2Na+ + SO32–
Н2O ↔ Н+ + ОН –
____________________________________________________________________________
2Na+ + SO32– + Н2O ↔ 2Na+ + HSO3– + ОН
SO32– + Н2O ↔ НSO3– + ОН – (среда щелочная)
б) 1 вариант
Слайд 33Na2S ↔ 2Na+ + S2–
Н2O ↔ Н+ + ОН –
____________________________________________________________________________
2Na+
+ S2– + Н2O ↔ 2Na+ + HS– + ОН
–S2– + Н2O ↔ НS– + ОН – (среда щелочная)
2 вариант
Ba(NO3)2 ↔ Ba2+ + 2NO3–
Н2O ↔ Н+ + ОН –
___________________________________________________________________
Ba2+ + 2NO3– + Н2O ↔ Ba2+ + 2NO3– + Н2O
(среда нейтральная)
в) 1 вариант
Слайд 34О значении и применении гидролиза...
Под действием
биологических катализаторов — ферментов в организме человека происходит гидролиз крахмала,
целлюлозы, белка, жиров.В технике крахмал подвергают гидролизу при взаимодействии с разбавленной серной кислотой и превращают в глюкозу (это реакция Кирхгофа, 1811 г.). Продукты гидролиза крахмала широко используются в кондитерской промышленности, медицине, для технических целей.
В промышленности гидролизу подвергаются сложные эфиры и жиры обязательно в щелочной среде. Такая реакция называется омылением. На этой реакции основано производство мыла, однако в настоящее время на производство моющих средств идут главным образом продукты переработки нефти.
Продукты гидролиза целлюлозы в промышленности — это бумага, хлопчатобумажные ткани.
Слайд 35Домашнее задание.
Пользуясь таблицей «Сильные и слабые электролиты», приведите свои примеры
солей, которые будут иметь кислую, щелочную и нейтральную среду раствора,
и напишите к ним ионные уравнения гидролиза.Слайд 37Источники материалов
Кузьменко Н.Е., Еремин В.В., Попков В.А. Начала химии. —
М.: Экзамен, 2001.
Хомченко Г.П. , Хомченко И.Г. Сборник задач по
химии. — М., 2000 .http://hydorlysis.narod.ru/pages/teoria.htm
http://www.xumuk.ru/encyklopedia/1047.html
Теги