Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ион алмасу реакциялары ж?не оларды? ж?ру жа?дайлары
Содержание
- 1. Ион алмасу реакциялары ж?не оларды? ж?ру жа?дайлары
- 2. Сабақтың тақырыбы: Ион алмасу реакциялары және олардың жүру жағдайлары 9 сынып
- 3. Үй тапсырмасын бекіту
- 4. Электролиттік диссоциация Білім тексеру Ерітінділердегі электролиттердің дисоциациялауы
- 5. Қате Дұрыс Дұрыс Қате Дұрыс Дұрыс Күшті
- 6. Русецкая О.П.Жаңа сабақты меңгерту
- 7. ХИМИК –САРАМАН
- 8. Слайд 8
- 9. Тақырыбы: Ион алмасу реакциясының жүру жағдайы.I. Тұнба
- 10. Білім бекіту
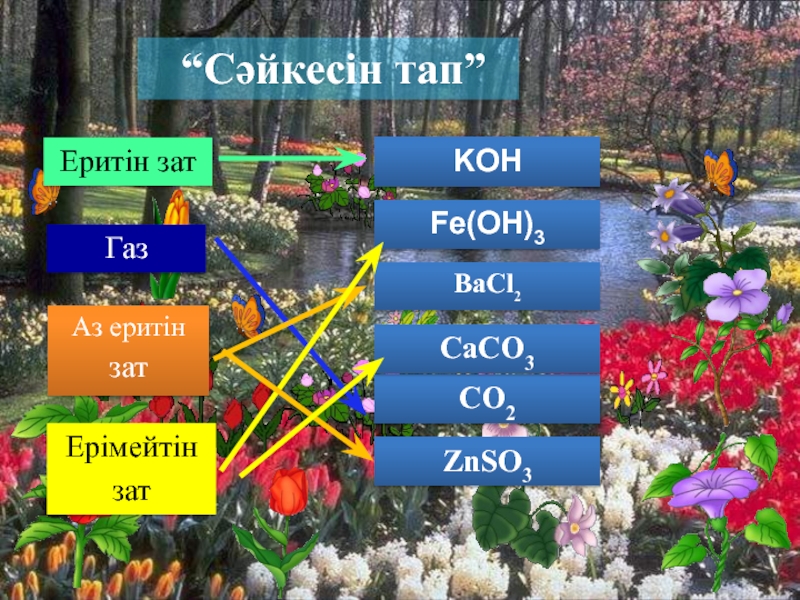
- 11. “Сәйкесін тап”KOHЕритін зат Аз еритін затГаз Ерімейтін зат Fe(OH)3BaCl2 CO2CaCO3ZnSO3
- 12. Берілген теңдеудің толық және
- 13. Төменде келтірілгендер реакция нәтижесінде қандай қосылыстар түзеді?Осы
- 14. Үйге тапсырма
- 15. Еңбегіне қарай өнбегіОқушыларды бағалау
- 16. Рефлексия «Білім тамшысы»
- 17. Үйге тапсырма: § 10. термин жаттау. А деңгей № 1С деңгей 1 нұсқа шығару.
- 18. Назарларыңызға рахмет!
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 4Электролиттік диссоциация
Білім тексеру
Ерітінділердегі электролиттердің дисоциациялауы нәтижесінде электролиттер ыдырайды__________
.
сұрақ 1
Ерітінділердегі электролиттердің электролиттік диссоциациялануы __________қатысында жүреді .
сұрақ
2
Әлсіз электролиттер _______ .
сұрақ 3
Электролиттер ________ .
сұрақ 4
Электролиттік диссоциация теориясының негізін салушы ______.
сұрақ 5
Слайд 5Қате
Дұрыс
Дұрыс
Қате
Дұрыс
Дұрыс
Күшті электролиттер
Ca(OH)2
Электролиттер
Бейэлектролиттер
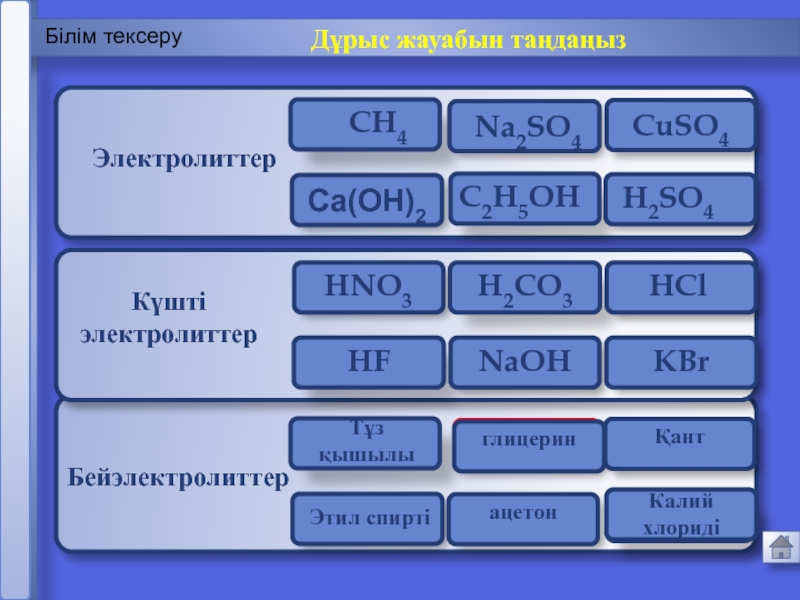
Білім тексеру
Дұрыс жауабын таңдаңыз
Слайд 9Тақырыбы: Ион алмасу реакциясының жүру жағдайы.
I. Тұнба түзілсе.
BaCl2 +
Na2SO4 BaSO4 + NaCl
Ba2+
2Cl-
+
+
2Na+
SO42-
+
2
BaSO4
+
2Na+
+
2Cl-
Ba2+
+
SO42-
BaSO4
Mg(NO3)2
+ Na2CO3 MgCO3 + NaNO3 Mg2+
2NO3-
+
+
2Na+
CO32-
+
2
MgCO3
+
2Na+
+
2NO3-
Mg2+
+
CO32-
MgCO3
II. Газ түзілсе.
Na2CO3 + H2SO4 Na2SO4 + H2CO3
H2O
CO2
2Na+
CO32-
+
+
2H+
SO42-
+
2Na+
SO42-
+
+
+
CO32-
+
2H+
H2O
CO2
+
III. Су немесе аз еритін зат түзілсе.
2NaOH + H2SO4 Na2SO4 + 2H2O
2H2O
2Na+
2OH-
+
+
2H+
SO42-
+
2Na+
SO42-
+
+
2OH-
+
2H+
2H2O
OH-
+
H+
H2O
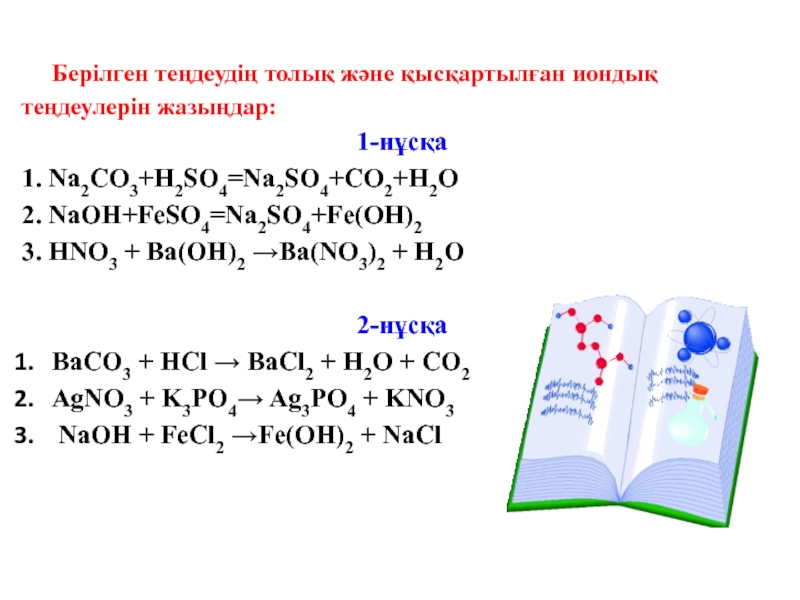
Слайд 12 Берілген теңдеудің толық және қысқартылған иондық теңдеулерін
жазыңдар:
1-нұсқа
1. Na2CO3+H2SO4=Na2SO4+CO2+H2O
2. NaOH+FeSO4=Na2SO4+Fe(ОН)2
3. HNO3 + Ba(OH)2 →Ba(NO3)2 +
H2O2-нұсқа
BaCO3 + HCl → BaCl2 + H2O + CO2
AgNO3 + K3PO4→ Ag3PO4 + KNO3
NaOH + FeCl2 →Fe(OH)2 + NaCl
Слайд 13Төменде келтірілгендер реакция нәтижесінде қандай қосылыстар түзеді?Осы реакция теңдеулері арқылы
қышқылдардың қасиеттері туралы қорытынды жаса.
Zn + HCI→ … +↑
а) NaCI2) CuO + H2SO4→ … + H2O ә) ZnCI2
3)NaOH + HCI→ … + 2H2O б) CuSO4
4) ZnCI2 + H2SO4→ … + 2HCI в) ZnSO4