Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
КОВАЛЕНТНАЯ СВЯЗЬ
Содержание
- 1. КОВАЛЕНТНАЯ СВЯЗЬ
- 2. Ковалентная связь - это химическая связь, возникающая между атомами за счет образования общих электронных пар.
- 3. Классификация КС1. По механизму образования Обменный механизмКаждый
- 4. Слайд 4
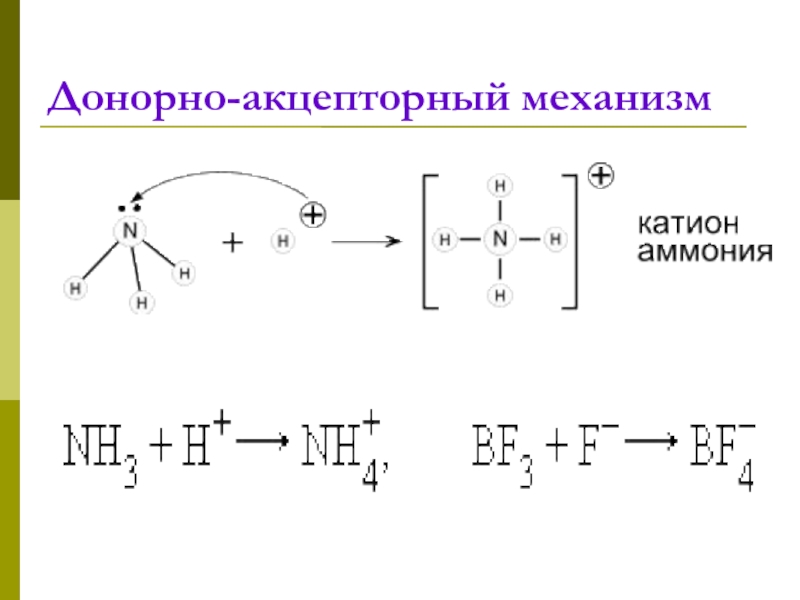
- 5. Донорно-акцепторный механизм
- 6. Донорно-акцепторный механизм
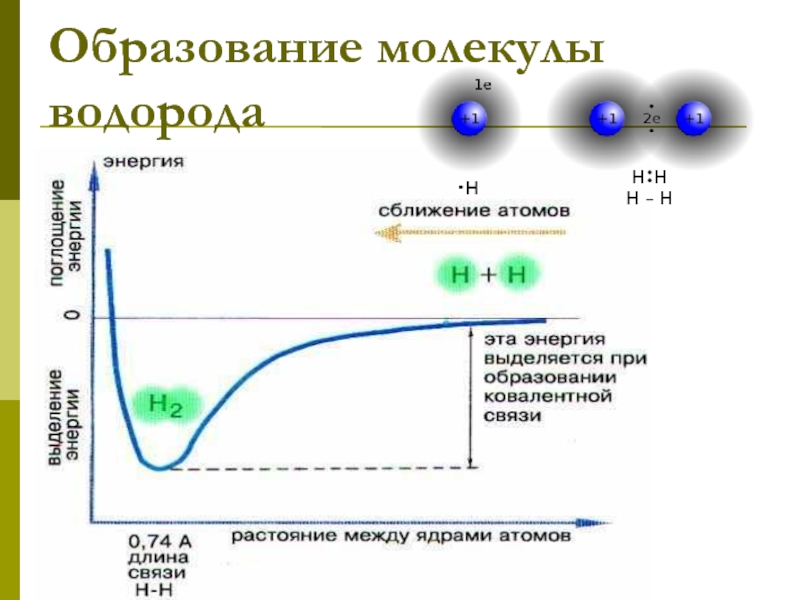
- 7. Образование молекулы водорода
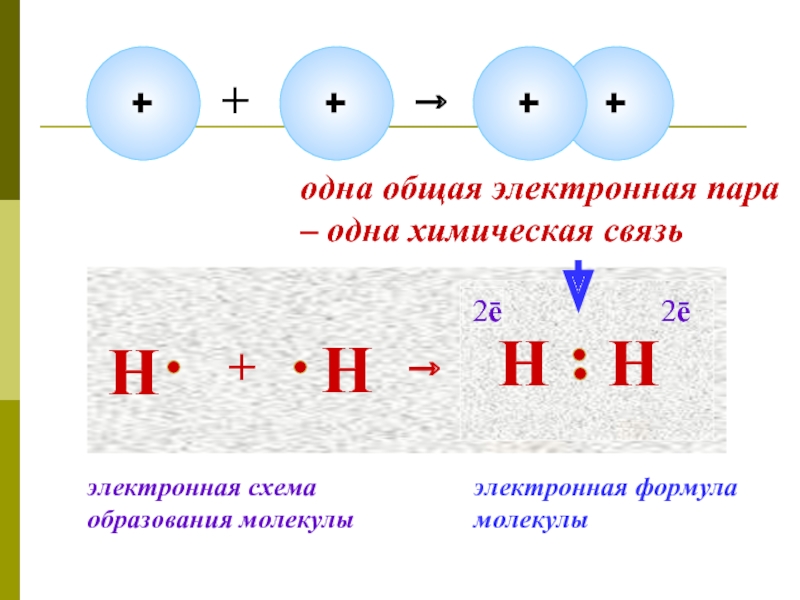
- 8. Н+Н→НН2ē2ēодна общая электронная пара – одна химическая связьэлектронная формула молекулыэлектронная схема образования молекулы
- 9. 2. По степени смещения общей электронной пары
- 10. 3. По способу перекрывания электронных орбиталей.σ (сигма-связь)-область
- 11. 3. По способу перекрывания электронных орбиталей
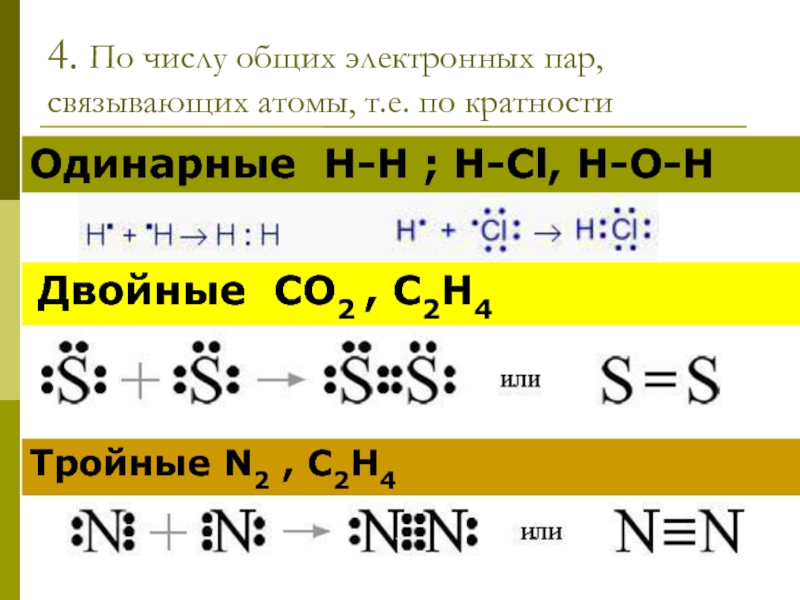
- 12. 4. По числу общих электронных пар, связывающих
- 13. Типы кристаллических решетокМолекулярнаяВ узлах находятся молекулы. Силы
- 14. Атомной кристаллической решёткой называется решётка, в узлах
- 15. Алмаз.
- 16. Слайд 16
- 17. Молекулярной кристаллической решёткой называется решётка, в узлах
- 18. Фрагмент кристаллов воды и серы.
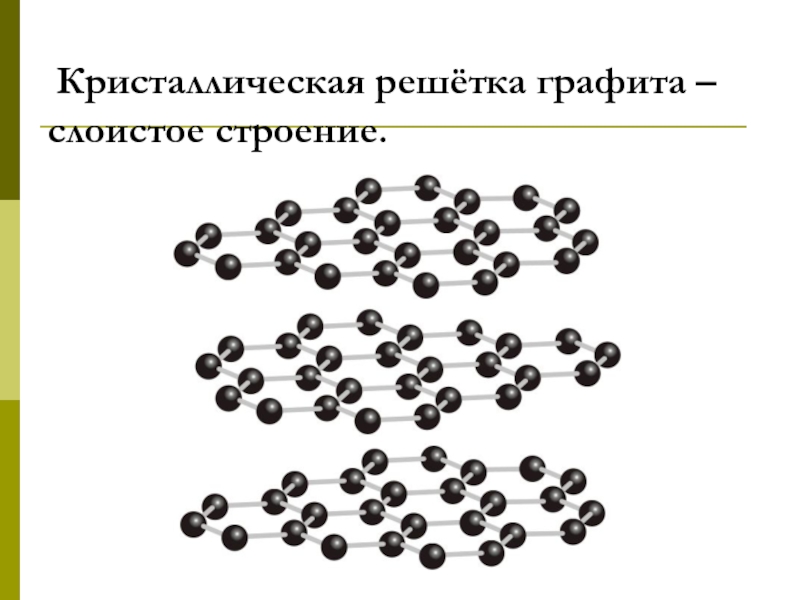
- 19. Кристаллическая решётка графита –слоистое строение.
- 20. Графит.
- 21. Домашнее заданиеГабриелян химия 11 базовый уровень§ 4
- 22. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Химическая связь 11 класс
КОВАЛЕНТНАЯ СВЯЗЬ
РАБОТА ВЫПОЛНЕНА
учителем химии средней школы №118
Выборгского района Санкт - Петербурга
Слайд 2Ковалентная связь
- это химическая связь, возникающая между атомами за
счет образования общих электронных пар.
Слайд 3Классификация КС
1. По механизму образования
Обменный механизм
Каждый из атомов
предоставляет неспаренный
( неспаренные) электроны для образования связи
Донорно-акцепторный механизм
Донор предоставляет
общую электронную пару, акцептор предоставляет свободную электронную орбиталь,которую эта пара может занятьСлайд 8
Н
+
Н
→
Н
Н
2ē
2ē
одна общая электронная пара – одна химическая связь
электронная формула молекулы
электронная
схема образования молекулы
Слайд 92. По степени смещения общей электронной пары
Ковалентная неполярная связь – общая электронная пара принадлежит обоим атомам
в равной степени. Ковалентная полярная связь –общая электронная пара смещена
к более электроотрицательному атому.
Слайд 103. По способу перекрывания электронных орбиталей.
σ (сигма-связь)-область перекрывания электронных орбиталей
находится на прямой, связывающей ядра атомов
S-S
P - P
S-P
d -d
Слайд 113. По способу перекрывания электронных орбиталей
π (пи-связь)-область перекрывания
электронных орбиталей лежит вне прямой, связывающей ядра атомов
p -d
d-d
Слайд 124. По числу общих электронных пар, связывающих атомы, т.е. по
кратности
Одинарные Н-Н ; H-Cl, H-O-H
Двойные СО2 , С2Н4
Тройные N2
, С2Н4Слайд 13Типы кристаллических решеток
Молекулярная
В узлах находятся молекулы. Силы притяжения слабые.
Вещества непрочные,
легкоплавкие, летучие.
Газы и жидкости в твердом состоянии, сера, иод, нафталин,
белый фосфор, углекислый газ(«сухой лёд»), органические веществаАтомная
В узлах находятся атомы. Силы притяжения сильные.
Вещества прочные, тугоплавкие, нелетучие, не проводят электрический ток ( кроме графита)
Алмаз, кремний кристаллический, бор, оксид кремния( кремнезем)
Слайд 14Атомной кристаллической решёткой называется решётка, в узлах которой расположены атомы,
соединённые между собой прочными ковалентными связями. Такие соединения имеют большую
прочность и тугоплавкость.В кристалле алмаза атомы углерода соединены в форме тетраэдра (каркасная структура).
Слайд 17Молекулярной кристаллической решёткой называется решётка, в узлах которой расположены молекулы,
удерживаемые силами межмолекулярного взаимодействия . Такие соединения легко плавятся. При
н.у. часто являются газами или подвижными жидкостями.Слайд 21Домашнее задание
Габриелян химия 11 базовый уровень
§ 4 стр.37 вопросы 1.
2, 3,6, 7,8
Габриелян , Лысова Химия 11
§ 6 стр.
46 – 51 стр. 56 вопросы 3,4,5Составьте формулу ионного фторида и молекулярного оксида с наименьшей молекулярной массой. Рассчитайте массовые доли фтора и кислорода в этих соединениях