Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Методическая разработка урока химии в 9 классе Фосфор как элемент мысли и жизни
Содержание
- 1. Методическая разработка урока химии в 9 классе Фосфор как элемент мысли и жизни
- 2. Цели урока:организовать деятельность учащихся по изучению особенностей
- 3. Мотивационно-ориентационный этап.Академик А.Е.Ферсман назвал
- 4. Какие сведения о фосфоре вам были известны до сегодняшнего урока?ФОСФОР
- 5. История открытия фосфора 1669 г- Х.Бранд-первооткрыватель
- 6. периодФосфор как химический элемент3группа5валентных электронов5степени окисления-3,0,+3,+5высший оксид Р2О5водородное соединениеРН3
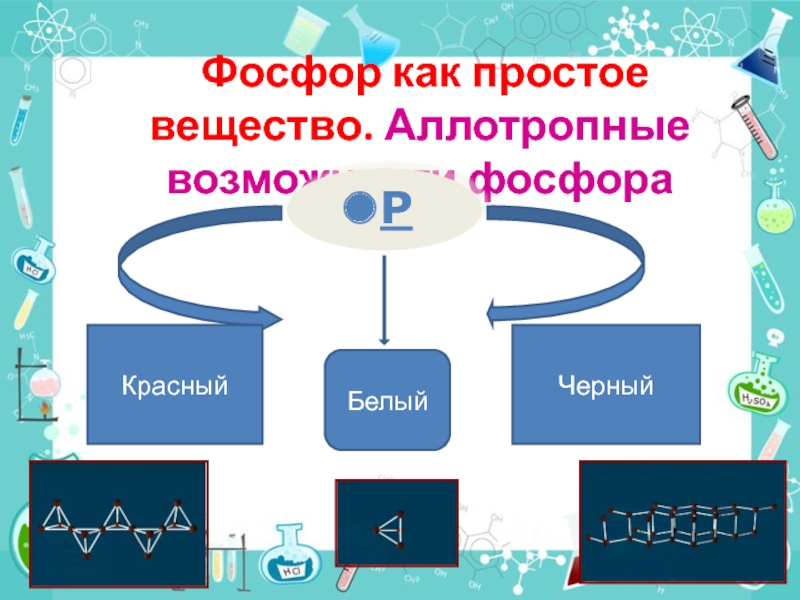
- 7. Фосфор как простое
- 8. Аллотропия фосфора
- 9. Прокомментируйте отрывок из романа А.Конан-Дойля
- 10. Химические свойства фосфора. ( Работа с учебником стр.160 и дополнительной литературой)
- 11. с бертолетовой солью при ударе взрывается, воспламеняется: 5KClO3 +6 P =3 P2O5 +5 KCl
- 12. « Сжигание красного фосфора и исследование продуктов его сгорания»
- 13. Видеоролик «Сгорание фосфора в хлоре»2 Р +
- 14. ПРИМЕНЕНИЕ ФОСФОРАРудобренияядохимикатыПроизводство спичекСоздание дымовых завесполупроводникиПроизводство красокЗащита от коррозииумягчение водымоющие средства
- 15. Войска СШАиспользовали фосфорныеБомбыв Ираке, 2004 г.
- 16. Первичное закрепление полученных знаний. Тест с использованием для голосования интерактивные индивидуальные устройства.
- 17. Тест1.Тип кристаллической решетки у белого фосфора…. а) молекулярный
- 18. Тест5. Причина свечения белого фосфора…. а)изменение агрегатного состояния
- 19. Домашнее задание:Учащиеся выбирают для выполнения задания разных
- 20. Итоги урока. Рефлексивно- оценочный этап. 1.Почему академик
- 21. СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ Учебник О.С.Габриеляна
- 22. Слайд 22
- 23. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1«Фосфор как элемент мысли и жизни»
Выполнила: учитель химии МАОУ «СОШ№1»г.Светлогорск
Кострикова
Ирина Анатольевна.
Слайд 2Цели урока:
организовать деятельность учащихся по изучению особенностей строения атома фосфора
на основании его положения в ПСХЭ Д.Менделеева
выяснить аллотропные возможности
фосфораизучить химические свойства фосфора как простого вещества на основе его строения
развивать познавательную самостоятельность учащихся при работе с учебником, дополнительной литературой, сайтами Интернета
формировать умения составления химических уравнений на основе химического эксперимента, навыки решения расчетных задач
воспитывать ответственность за конечный результат работы.
Слайд 3
Мотивационно-ориентационный этап.
Академик А.Е.Ферсман назвал этот элемент «
элементом мысли и жизни», без него невозможно существование на Земле
живого, в теле человека его примерно 0,8 кг. Он - основа нервных, мышечных, мозговых и костных тканей. Является жителем V-A подгруппы периодической системы химических элементов Д.И.Менделеева. О каком элементе идет речь?Слайд 5История открытия фосфора
1669 г- Х.Бранд-первооткрыватель
фосфора
1682г- Р.Бойль в химической лаборатории при работе с
фосфором.Слайд 6период
Фосфор как химический элемент
3
группа
5
валентных электронов
5
степени окисления
-3,0,+3,+5
высший оксид
Р2О5
водородное соединение
РН3
Слайд 9Прокомментируйте отрывок из романа А.Конан-Дойля
« Собака Баскервилей». Попытайте определить, где
правда, а где вымысел автора?
«...Да! Это была собака, огромная, черная, как смоль. Но такой собаки еще никто из нас, смертных, не видывал. Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь .Ее огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте. - Фосфор, – сказал я».
Слайд 14ПРИМЕНЕНИЕ ФОСФОРА
Р
удобрения
ядохимикаты
Производство
спичек
Создание
дымовых завес
полупроводники
Производство
красок
Защита от
коррозии
умягчение воды
моющие средства
Слайд 16Первичное закрепление полученных знаний.
Тест с использованием для голосования интерактивные индивидуальные
устройства.
Слайд 17Тест
1.Тип кристаллической решетки у белого фосфора….
а) молекулярный б) атомный
в) ионный
а) молекулярный Р4
2. У фосфора….. аллотропных модификаций
а) две б) три
в) четыре г) пятьв) четыре – белый, черный, красный, фиолетовый
3. В атоме фосфора неспаренных электронов -…
а) три б) четыре в) пять
а) три
4. В реакции…. Фосфор проявляет восстановительные свойства
а)4Р+5О2=2Р2О5 б)2Р+3Mg=Mg3P2 в)2Р+3Н2=2РН3
а)4Р+5О2=2Р2О5
Слайд 18Тест
5. Причина свечения белого фосфора….
а)изменение агрегатного состояния вещества
б) химическое явление
в) физическое явление
б) химическое явление
6.Как называются соединения фосфора
с металламиа) сульфаты б)фосфаты в) фосфиды
в) фосфиды
7.Какой тип связи в молекуле фосфина РН3
а) ковалентная неполярная б) ковалентная полярная в) ионная
а) ковалентная неполярная
8) Красный или белый фосфор ядовит?
а) красный б) белый
б) белый
9) Очень ядовит, с неприятным запахом, легко воспламеняется на воздухе, образует болотные блуждающие огни. О каком газе идет речь?
О фосфине РН3
Слайд 19Домашнее задание:
Учащиеся выбирают для выполнения задания разных уровней сложности:
1 уровень:
упр. №1 стр. 163 учебника
( О.С.Габриелян, «Химия-9»)2 уровень:упр.№2 стр. 163 учебника
3 уровень: решение расчетной задачи №5 стр.163 учебника.
Слайд 20Итоги урока. Рефлексивно- оценочный этап.
1.Почему академик Ферсман назвал фосфор «элементом
жизни и мысли?
2.Как ты оцениваешь знания, полученные сегодня?
3. Какое
значение для тебя лично имеютзнания и умения, полученные сегодня?
Слайд 21СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ
Учебник О.С.Габриеляна « Химия- 9», изд.»
Дрофа», 2007 год.
Виртуальная лаборатория. Открытая химия. 8-11 класс. [Электронный носитель].
– М.:Габриелян О.С. Настольная книга учителя. Химия. 9 класс. – М.: Дрофа, 2002.
Уроки химии Кирилла и Мефодия. 8-9 класс. [Электронный носитель]. – М.: «Кирилл и Мефодий», 2002.
httphttp://http://wwwhttp://www.http://www.alhimikhttp://www.alhimik.http://www.alhimik.ru
httphttp://http://himhttp://him.1http://him.1septemberhttp://him.1september.http://him.1september.ru.