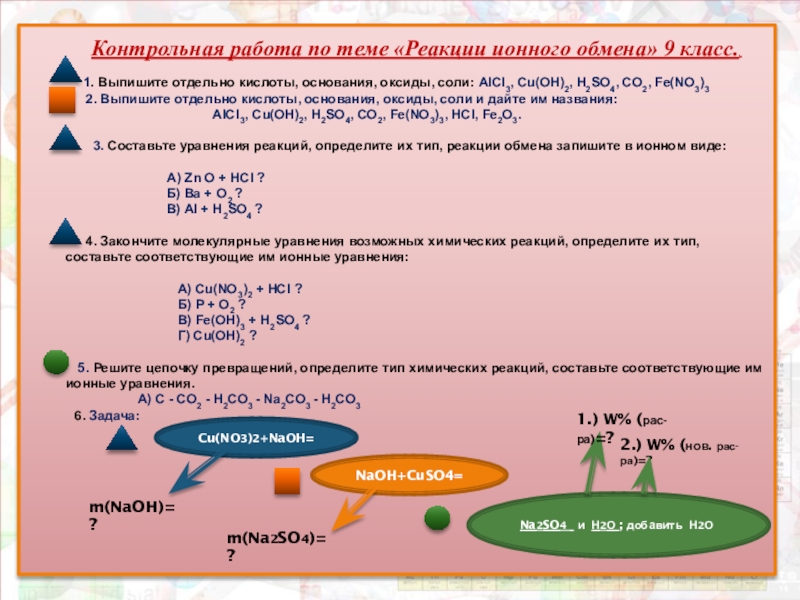
1. Выпишите отдельно кислоты,
основания, оксиды, соли: AlCl3, Cu(OH)2, Н2SO4, CO2, Fe(NO3)3
2. Выпишите отдельно кислоты, основания, оксиды, соли и дайте им названия:
AlCl3, Cu(OH)2, Н2SO4, CO2, Fe(NO3)3, HCl, Fe2O3.
3. Составьте уравнения реакций, определите их тип, реакции обмена запишите в ионном виде:
А) Zn O + HCl ?
Б) Ва + O2 ?
В) Al + H2SO4 ?
4. Закончите молекулярные уравнения возможных химических реакций, определите их тип,
составьте соответствующие им ионные уравнения:
А) Cu(NO3)2 + HCl ?
Б) P + O2 ?
В) Fe(OH)3 + H2SO4 ?
Г) Cu(OH)2 ?
5. Решите цепочку превращений, определите тип химических реакций, составьте соответствующие им
ионные уравнения.
А) С - СO2 - Н2СO3 - Na2CO3 - Н2СO3
6. Задача:
Cu(NO3)2+NaOH=
NaOH+CuSO4=
Na2SO4 и Н2О ; добавить Н2О
m(NaOH)=?
m(Na2SO4)=?
1.) W% (рас-ра)=?
2.) W% (нов. рас-ра)=?