Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Изготовление моделей веществ с водородной связью
Содержание
- 1. Изготовление моделей веществ с водородной связью
- 2. ГБОУ СОШ № 1981Акимова ВалерияПолякова АнжеликаРаботу выполнили
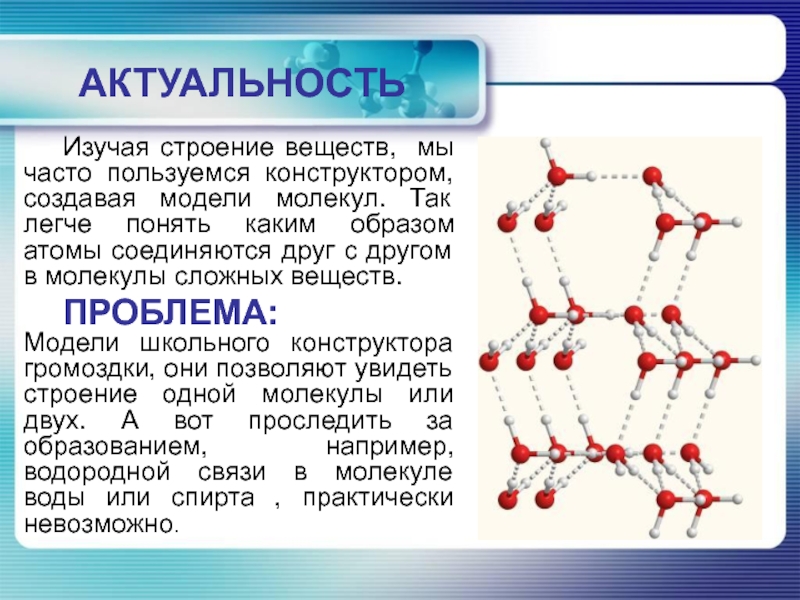
- 3. АКТУАЛЬНОСТЬИзучая строение веществ, мы часто пользуемся конструктором,
- 4. Создать модели веществ с водородной связью ЦЕЛЬ:
- 5. ОБЪЕКТ И ПРЕДМЕТ ИЗУЧЕНИЯ:ОБЪЕКТ ИЗУЧЕНИЯ:Мы хотим создать
- 6. ЗАДАЧИизучить природу, образования водородных связей;продумать процесс выполнения
- 7. РАБОЧАЯ ГИПОТЕЗАИз бисера можно создать модели веществ
- 8. НОВИЗНАМы увлекаемся бисероплетением и имеем огромное количество
- 9. Теоретический этап работы:изучение материалов, связанных с темой
- 10. ВОДА Ни одна из планет Солнечной системы
- 11. ВОДОРОДНЫЕ СВЯЗИ И ФИЗИЧЕСКИЕ СВОЙСТВАСледствием полярности связи
- 12. ВОДОРОДНАЯ СВЯЗЬДля возникновения водородных связей важно, чтобы
- 13. МЕЖМОЛЕКУЛЯРНАЯ ВОДОРОДНАЯ СВЯЗЬУчитывая заметную разницу зарядов на
- 14. СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫМолекула воды имеет следующее строение:Две
- 15. ПРОЯВЛЕНИЕ ВОДОРОДНЫХ СВЯЗЕЙЕще одно красивое проявление водородных
- 16. НАШИ РАБОТЫ
- 17. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2ГБОУ СОШ № 1981
Акимова Валерия
Полякова Анжелика
Работу выполнили ученицы 8,9 класса:
Руководители
работы:
Слайд 3АКТУАЛЬНОСТЬ
Изучая строение веществ, мы часто пользуемся конструктором, создавая модели молекул.
Так легче понять каким образом атомы соединяются друг с другом
в молекулы сложных веществ.ПРОБЛЕМА: Модели школьного конструктора громоздки, они позволяют увидеть строение одной молекулы или двух. А вот проследить за образованием, например, водородной связи в молекуле воды или спирта , практически невозможно.
Слайд 5ОБЪЕКТ И ПРЕДМЕТ ИЗУЧЕНИЯ:
ОБЪЕКТ ИЗУЧЕНИЯ:
Мы хотим создать изделия из бисера,
которые
бы отражали наличие водородной связи в веществах.
ПРЕДМЕТ ИЗУЧЕНИЯ:
Предметом нашего изучения
будут вещества, которые могут образовывать водородную связь. Слайд 6ЗАДАЧИ
изучить природу, образования водородных связей;
продумать процесс выполнения работы из бисера;
создать
модели веществ с водородной связью, используя бисер.
Слайд 7РАБОЧАЯ ГИПОТЕЗА
Из бисера можно создать модели веществ с водородной связью.
Эта работа будет иметь практическое значение и поможет в изучении
темы "Виды связи".Слайд 8НОВИЗНА
Мы увлекаемся бисероплетением и имеем огромное количество разнообразных работ. Подумалось,
что и из бисера можно изготовить модели молекул. И картину
образования связей будет легче представить, разглядывая нашу работу, так как молекулы там будут многократно повторены, так же как и образование водородной связи между молекулами.Слайд 9Теоретический этап работы:
изучение материалов, связанных с темой исследования.
Практическая часть работы:
изготовление
из бисера атомов с разной валентностью (учитывая, что в бисере
всего 2 отверстия);изготовление моделей веществ с водородной связью.
ЭТАПЫ РАБОТЫ
Слайд 10ВОДА
Ни одна из планет Солнечной системы не содержит на
своей поверхности такого большого количества воды, как наша Земля. Моря
и океаны, средняя глубина которых около 6 км, покрывают 71 % поверхности Земли. Огромное количество воды в виде снега и льда сосредоточено в приполярных районах.Этот удивительный факт пока не нашел однозначного объяснения. Безусловно, вода играет огромную роль в возникновении и существовании жизни на нашей планете. Во многом это связано со свойствами, которых нет у ее ближайших соседей и аналогов (H2S). Прежде всего нужно разобраться, почему вода может находиться в жидком и даже в твердом состоянии (лед) в условиях, в которых похожие соединения водорода с более тяжелыми элементами (серой, селеном и т.д.) газообразные.
Слайд 11ВОДОРОДНЫЕ СВЯЗИ И ФИЗИЧЕСКИЕ СВОЙСТВА
Следствием полярности связи О–Н и наличия
неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к
образованию водородных связей .Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т.кип. метанола +64,5°С). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.
Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена.
Ассоциация молекул ROH
Гидратация молекул ROH
Слайд 12ВОДОРОДНАЯ СВЯЗЬ
Для возникновения водородных связей важно, чтобы в молекулах вещества
были атомы водорода, связанные с небольшими, но электроотрицательными атомами, например:
O, N, F. Это создает заметный частичный положительный заряд на атомах водорода. С другой стороны, важно, чтобы у электроотрицательных атомов были неподеленные электронные пары. Когда обедненный электронами атом водорода одной молекулы (акцептор) взаимодействует с неподеленной электронной парой на атоме N, O или F другой молекулы (донор), то возникает связь, похожая на полярную ковалентную.Водородные связи между молекулами обозначены пунктиром
Слайд 13МЕЖМОЛЕКУЛЯРНАЯ ВОДОРОДНАЯ СВЯЗЬ
Учитывая заметную разницу зарядов на атомах Н и
О соседних молекул, дополнительную прочность этой межмолекулярной связи придает притяжение
разноименных зарядов. Водородные связи характерны для таких веществ, как вода H2O, аммиак NH3, фтороводород HFВ водных растворах аммиака или HF эти молекулы образуют водородные связи не только между собой, но и с молекулами воды. Благодаря водородным связям аммиак NH3 имеет фантастическую растворимость: в 1 л воды может растворяться 750 л газообразного аммиака! В органических веществах встречаются также внутримолекулярные водородные связи, сильно влияющие на пространственную форму этих молекул.
Энергия связи водородной связи Н---О в димере воды (H2O) составляет 21,5 кДж/моль, а ее длина 2,04 А. Таким образом, эти связи более длинные и примерно в 10-20 раз менее прочные, чем обычные ковалентные, но именно они заставляют воду быть жидкостью или льдом (а не газом) в обычных условиях. Водородные связи разрушаются только тогда, когда жидкая вода переходит в пар.
Слайд 14СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ
Молекула воды имеет следующее строение:
Две поделенные электронные пары
участвуют в образовании двух полярных ковалентных связей, а оставшиеся две
неподеленные пары электронов тоже играют важную роль в свойствах воды. Все заместители у атома кислорода, включая неподеленные пары, стремятся расположиться как можно дальше друг от друга. Это приводит к тому, что молекула приобретает форму искаженного тетраэдра с атомом кислорода в центре. В четырех вершинах этого "тетраэдра" находятся два атома водорода и две неподеленные пары электронов. Но если смотреть только по центрам атомов, то получается, что молекула воды имеет угловое строение, причем угол Н–О–Н составляет примерно 105 градусов.Слайд 15ПРОЯВЛЕНИЕ ВОДОРОДНЫХ СВЯЗЕЙ
Еще одно красивое проявление водородных связей – голубой
цвет чистой воды в ее толще. Когда одна молекула воды
колеблется, она заставляет колебаться и связанные с ней водородными связями другие молекулы. На возбуждение этих колебаний расходуются красные лучи солнечного спектра, как наиболее подходящие по энергии. Таким образом, из солнечного спектра "отфильтровываются" красные лучи – их энергия поглощается и рассеивается колеблющимися молекулами воды в виде тепла.В белом солнечном свете различные цвета как бы уравновешивают друг друга. Поэтому солнечный свет кажется глазу "белым" – лишенным цвета. Если "отфильтровать" лучи одного участка спектра, то начинает проступать другой – в данном случае голубой участок спектра. Он и окрашивает воду в красивый голубой цвет. Но для этого требуется, чтобы солнечный луч прошел не менее чем через 2-х метровую толщу чистой воды и "потерял" достаточно много красных лучей.