Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Неорганические и элементоорганические полимеры
Содержание
- 1. Неорганические и элементоорганические полимеры
- 2. Неорганические полимерыНеорганические полимеры – полимеры, которые имеют неорганические главные цепи и не содержат органических боковых радикаловАсбест
- 3. Красный фосфорКрасный фосфор — одна из аллотропных модификаций
- 4. Производство спичекКрасный фосфор применяется для производства спичек.
- 5. Черный фосфорЧёрный фосфор — еще одна аллотропная модификация
- 6. Карбин — аллотропная форма углерода, его линейный полимер. Может
- 7. Карбин представляет собой мелкокристаллический порошок чёрного цвета,
- 8. Элементоорганические полимерыЭлементоорганические полимеры — полимеры, не содержащие в повторяющемся
- 9. СиликоныСиликоны (полиорганосилоксаны) — кремнийорганические соединения. Силиконы имеют строение в
- 10. Cиликон используется для изготовления силиконовых прокладок, колец,
- 11. ПолифосфазеныОсновная цепь полифосфазена состоит из чередующихся атомов
- 12. Полигерманы и полистаннаныПолимерные цепочки могут состоять из
- 13. Спасибо за внимание
- 14. Скачать презентанцию
Неорганические полимерыНеорганические полимеры – полимеры, которые имеют неорганические главные цепи и не содержат органических боковых радикаловАсбест
Слайды и текст этой презентации
Слайд 2Неорганические полимеры
Неорганические полимеры – полимеры, которые имеют неорганические главные цепи
и не содержат органических боковых радикалов
Слайд 3Красный фосфор
Красный фосфор — одна из аллотропных модификаций элементарного фосфора. Он
представляет собой полимер со сложной структурой. В зависимости от способа получения и
степени дробления имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком, имеет металлический блеск. Химическая активность красного фосфора невысока, он нерастворим в воде, а также в бензоле, сероуглероде . Растворить его возможно лишь в некоторых расплавленных металлах (свинец и висмут). Красный фосфор на воздухе не самовоспламеняется, вплоть до температуры 240—250 °С, но самовоспламеняется при трении или ударе. Ядовитость его в тысячи раз меньше, чем у белого фосфора, поэтому он применяется гораздо шире.Слайд 4Производство спичек
Красный фосфор применяется для производства спичек. Из красного фосфора,
сульфида сурьмы (III), железного сурика (природного оксида железа (III) с примесью кварца) и клея
приготовляют смесь, которую наносят на боковые поверхности спичечной коробки. Головка спичек состоит главным образом из бертолетовой соли, молотого стекла, серы и клея. При трении головки о намазку спичечной коробки красный фосфор воспламеняется, поджигает состав головки, а от него загорается дерево.Слайд 5Черный фосфор
Чёрный фосфор — еще одна аллотропная модификация элементарного фосфора. Он
представляет собой чёрное вещество с металлическим блеском, жирное на ощупь
и весьма похожее на графит, с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Чёрный фосфор проводит электрический ток и имеет свойства полупроводника. Температура плавления – 1000 °С под давлением 18·105 Па. Черный фосфор наименее активный из всех видов фосфора, поэтому практически не применяется.Слайд 6Карбин — аллотропная форма углерода, его линейный полимер. Может иметь:
а) полииновое строение,
когда атомы углерода соединены в цепочки поочередно тройными и одинарными
связямиб) поликумуленовое строение, когда атомы углерода соединены в цепочки постоянно двойными связями
Карбин
Слайд 7Карбин представляет собой мелкокристаллический порошок чёрного цвета, обладает полупроводниковыми свойствами, причём под
воздействием света его проводимость сильно увеличивается. На этом свойстве основано
первое практическое применение — в фотоэлементах. Карбин – наиболее прочный и жесткий из всех известных материалов. После того как карбин был получен в лаборатории, его обнаружили в метеоритном кратере Рис (ФРГ) и в метеорите Новый Урей (СССР). Это наводит на мысль, что карбин образуется в специфических условиях, изучение которых поможет разгадать тайны космохимии.Слайд 8Элементоорганические полимеры
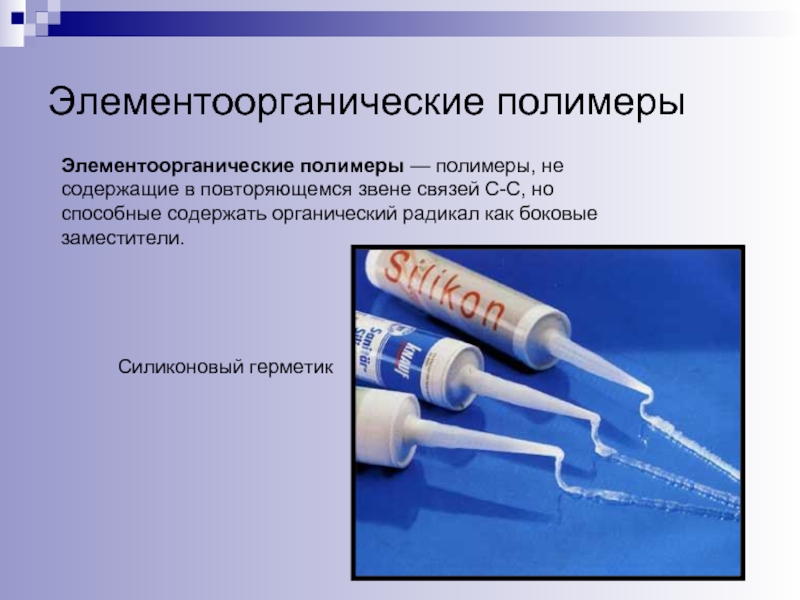
Элементоорганические полимеры — полимеры, не содержащие в повторяющемся звене связей C-C,
но способные содержать органический радикал как боковые заместители.
Силиконовый герметик
Слайд 9Силиконы
Силиконы (полиорганосилоксаны) — кремнийорганические соединения. Силиконы имеют строение в виде основной неорганической
кремний-кислородной цепи (…-Si-O-Si-O-Si-O-…) с присоединёнными к ней боковыми органическими группами,
которые крепятся к атомам кремния. В некоторых случаях боковые органические группы могут соединять вместе две или более кремнийорганических цепей.Силиконы обладают рядом уникальных качеств в комбинациях, отсутствующих у любых других известных веществ: гидрофобностью, способностью работать и сохранять свойства при экстремальных и быстроменяющихся температурах или повышенной влажности, диэлектрическими свойствами, эластичностью, долговечностью, экологичностью. Это обуславливает их высокую востребованность в разных областях.
Слайд 10Cиликон используется для изготовления силиконовых прокладок, колец, втулок и многого
другого. Изделия из силикона сохраняют свою работоспособность от −60 °C до
+200 °C. Они устойчивы к воздействию радиации, УФ излучения, электрических полей и разрядов, озона, морской и пресной воды (в т. ч. кипящей), спиртов, минеральных масел и топлив, слабых растворов кислот, щелочей и перекиси водорода.Из-за высокой стоимости силиконов, в продаже нередки их подделки. Для распознавания подделки в бытовых условиях достаточно поджечь небольшой кусочек проверяемого образца: в отличие от органических соединений на основе углерода, используемых для подделок, силиконовые материалы загораются с трудом, а при горении выделяют не черную сажу (углерод) а белую (диоксид кремния).
Слайд 11Полифосфазены
Основная цепь полифосфазена состоит из чередующихся атомов фосфора и азота.
Такая цепочка очень гибкая, поэтому полифосфазены являются эластомерами (резинами). Также
они хорошие электрические изоляторы. Полифосфазены самозатухают или не горят, поэтому на их основе получают негорючие и огнестойкие материалы.Полифосфазен - синтетический полимер нового поколения для изделий сердечно-сосудистой хирургии, хирургических шовных нитей, устранения косметических дефектов лица, в том числе для реабилитации инвалидов. Основополагающими свойствами для его широкого применения в медицине являются совместимость с живым организмом, обеззараживающее действие, высокая совместимость с кровью при отсутствии раздражающего, аллергенного или токсического действия.
Слайд 12Полигерманы и полистаннаны
Полимерные цепочки могут состоять из германия или олова.
Такие полимеры называются, соответственно, полигерманами и полистаннанами.
Эти полимеры уникальны, поскольку
они являются единственными известными полимерами, основная цепь которых сделана целиком из атомов металлов.Полигерманы и полистаннаны изучаются на предмет их использования в качестве проводников электричества.
Полидиметилгерман
Полидиметилстаннан
Теги