Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация для урока химии 11 класс "Электролитическая диссоциация"
Содержание
- 1. Презентация для урока химии 11 класс "Электролитическая диссоциация"
- 2. Процесс распада электролита на ионы называется электролитической диссоциацией.
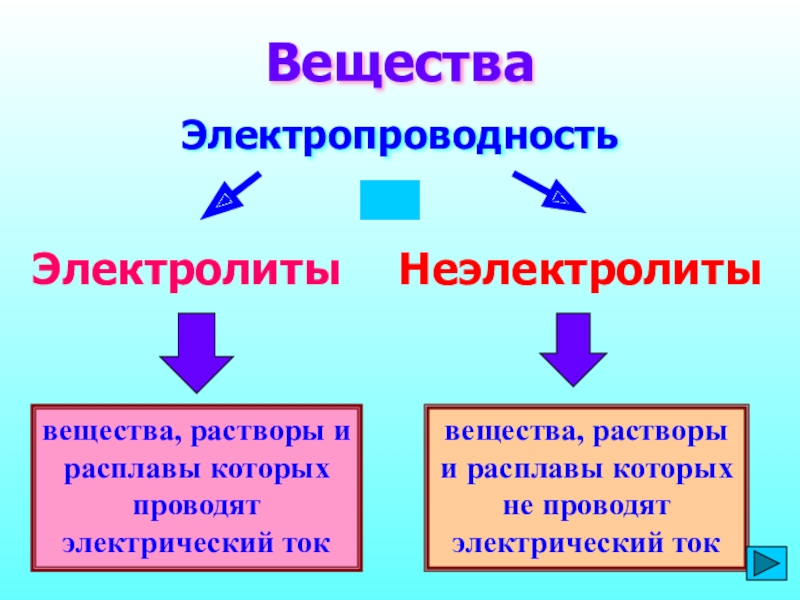
- 3. вещества, растворы и расплавы которых проводят электрический
- 4. Слайд 4
- 5. Ионная или сильнополярная ковалентная связьОснованияКислотыСолиКовалентная неполярная или малополярная связьОрганические соединенияГазыНеметаллыЭлектролитыНеэлектролиты
- 6. Теория электролитической диссоциацииС. А. Аррениус (1859-1927)процесс растворения
- 7. 1. Электролиты при растворении в воде распадаются
- 8. Слайд 8
- 9. Слайд 9
- 10. Причины распада вещества на ионы в расплавах
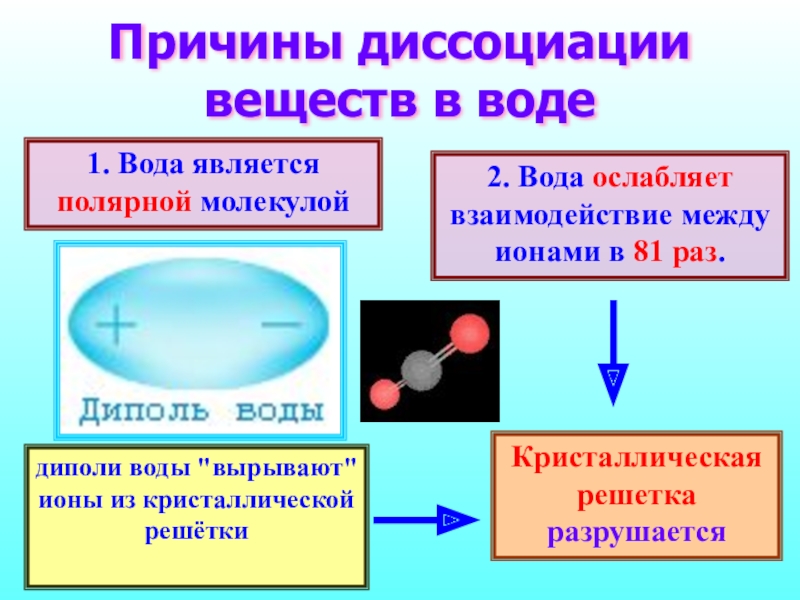
- 11. Причины диссоциации веществ в воде 1. Вода
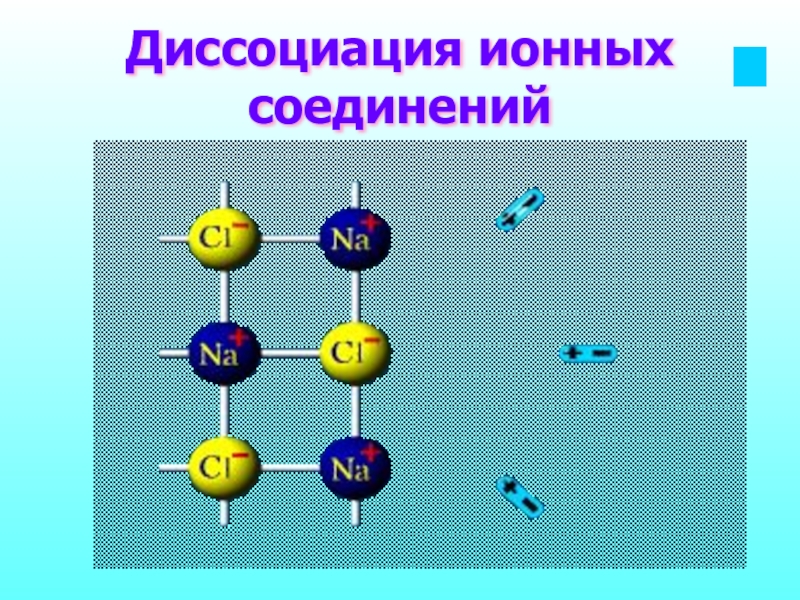
- 12. Диссоциация ионных соединений
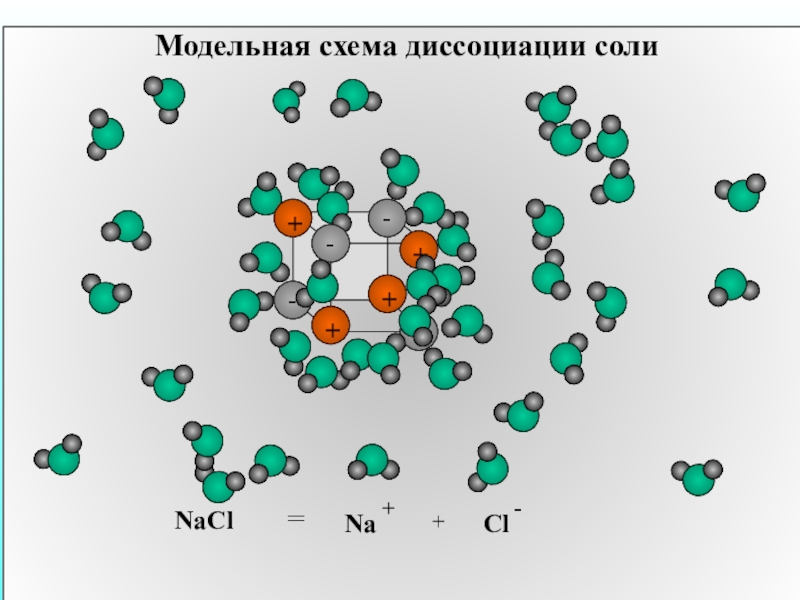
- 13. Модельная схема диссоциации солиNaCl = + Na+
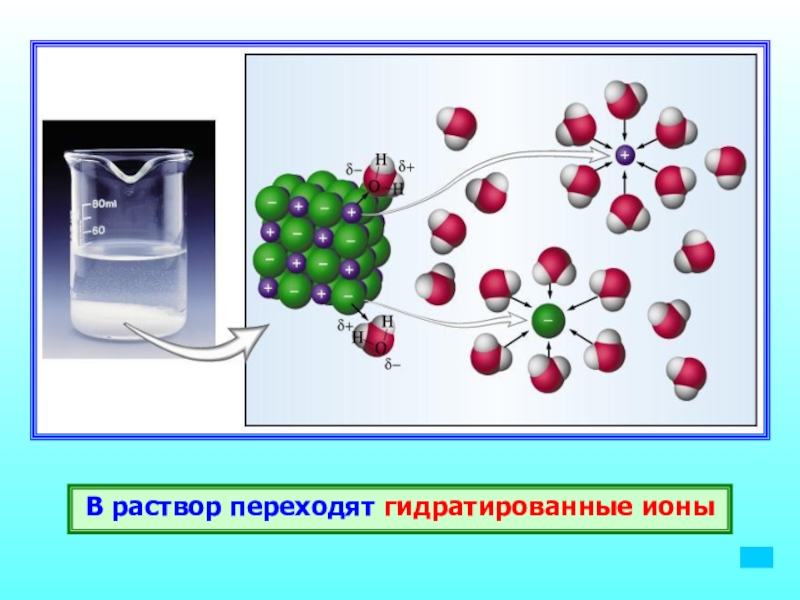
- 14. В раствор переходят гидратированные ионы
- 15. Диссоциация соединений с КП связью
- 16. Образование в результате распада электролитов гидратированных ионов
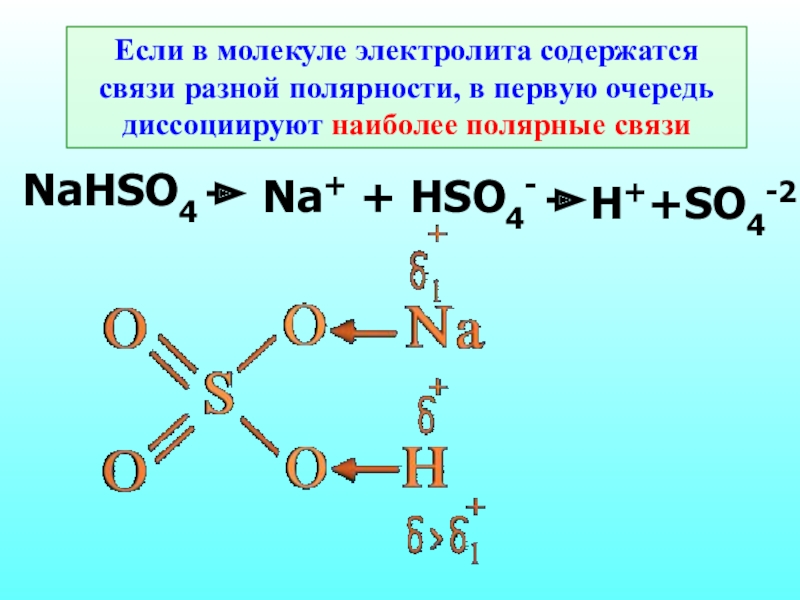
- 17. Если в молекуле электролита содержатся связи разной
- 18. Количественная характеристика процесса диссоциацииОтношение числа распавшихся молекул к общему числу молекул в раствореСила электролита
- 19. Слайд 19
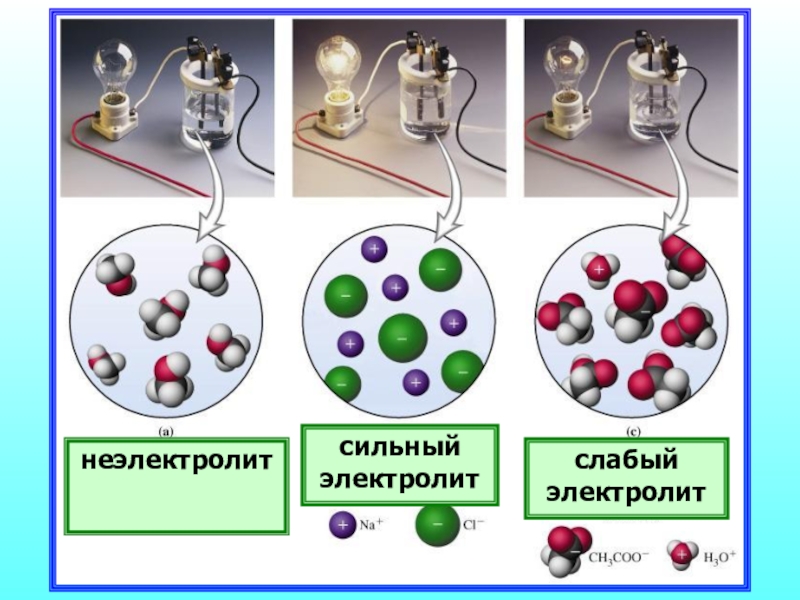
- 20. неэлектролитсильный электролитслабый электролит
- 21. Слайд 21
- 22. Слайд 22
- 23. Слайд 23
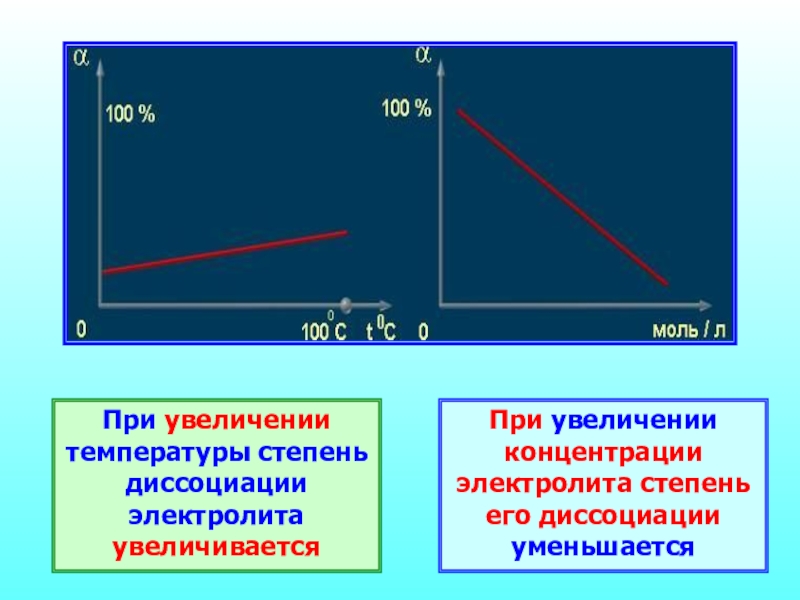
- 24. При увеличении температуры степень диссоциации электролита увеличиваетсяПри увеличении концентрации электролита степень его диссоциации уменьшается
- 25. Константа диссоциацииХарактеризует способность слабого электролита распадаться на ионы
- 26. Вильгельм Оствальд (Ostwald W.F.)(2.IX.1853 - 4.IV.1932)Закон разбавления
- 27. Задание для 1 группы: Впишите недостающие слова:
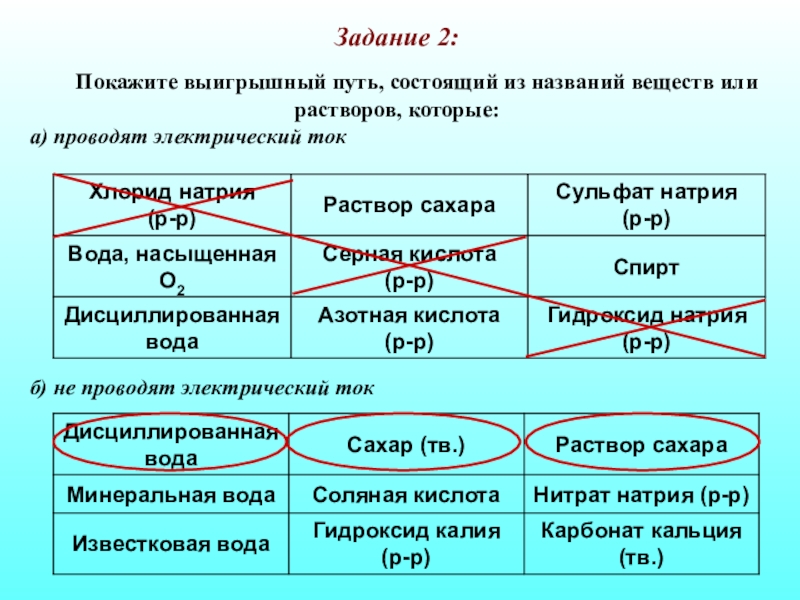
- 28. Задание 2: Покажите выигрышный путь, состоящий из названий
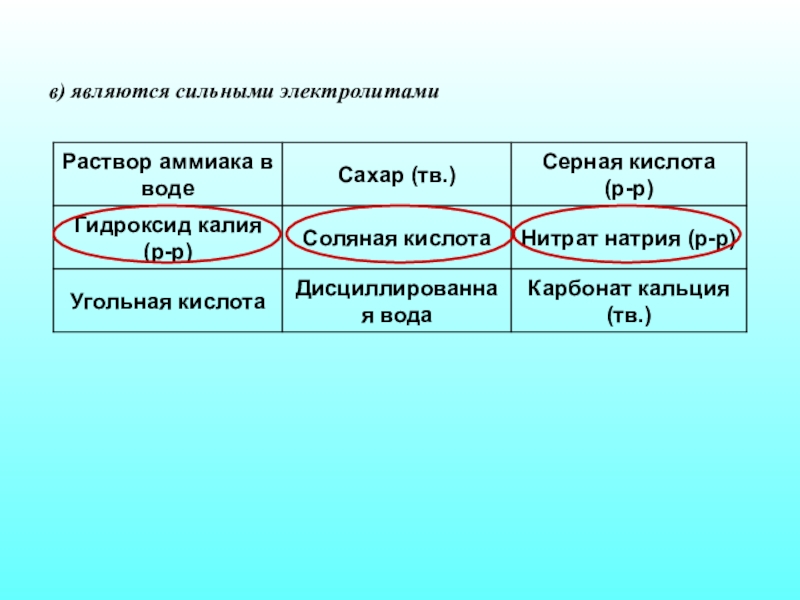
- 29. в) являются сильными электролитами
- 30. Задание 3:Соотнесите: 1.А) Электролиты
- 31. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3
вещества, растворы и расплавы которых проводят электрический ток
Вещества
Электропроводность
Электролиты
Неэлектролиты
вещества,
растворы и расплавы которых не проводят электрический ток
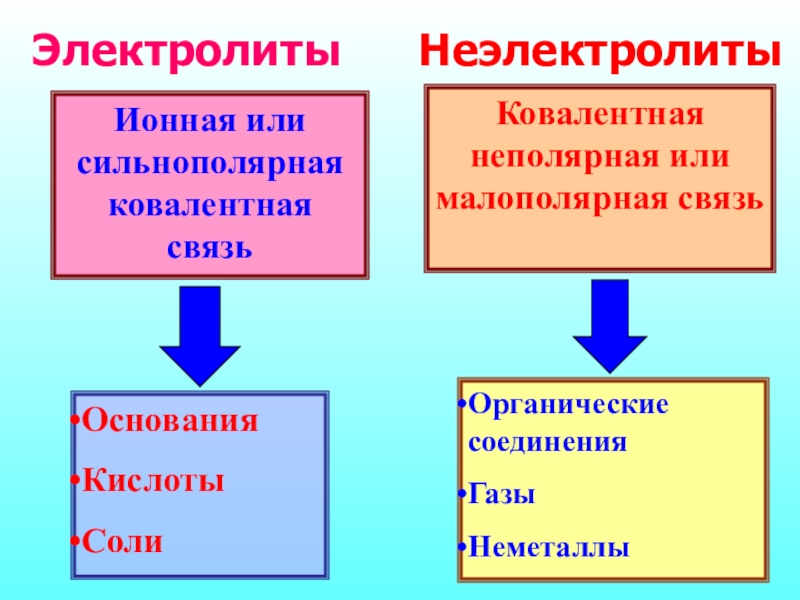
Слайд 5Ионная или сильнополярная ковалентная связь
Основания
Кислоты
Соли
Ковалентная неполярная или малополярная связь
Органические соединения
Газы
Неметаллы
Электролиты
Неэлектролиты
Слайд 6Теория электролитической диссоциации
С. А. Аррениус (1859-1927)
процесс растворения электролитов сопровождается образованием
заряженных частиц, способных проводить электрический ток
Процесс растворения или плавления электролитов
сопровождается образованием заряженных частиц , способных проводить электрический токСлайд 71. Электролиты при растворении в воде распадаются на положительные и
отрицательно заряженные ионы – электролитическая диссоциация.
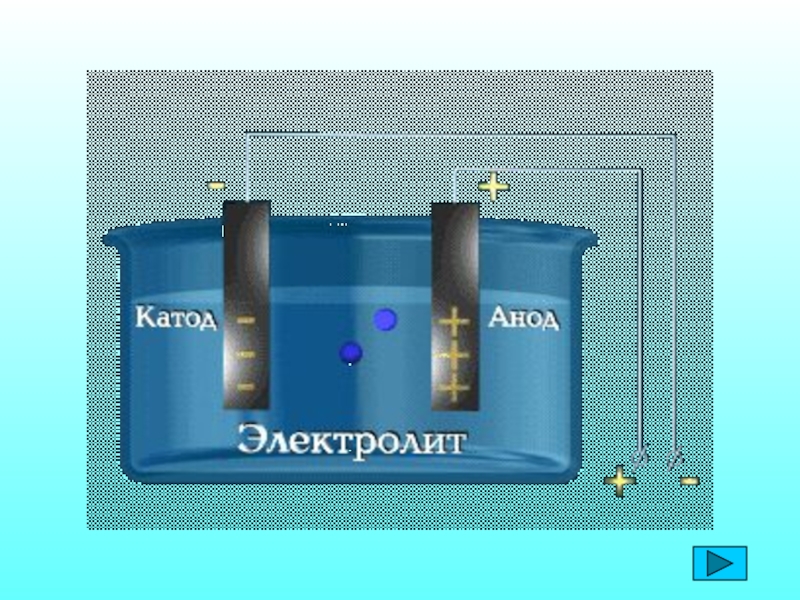
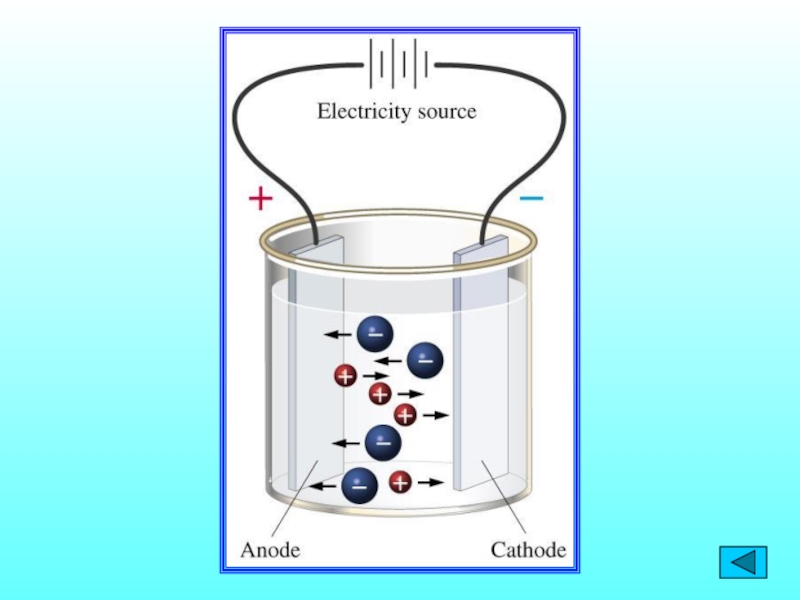
2. Под действием электрического тока
положительно заряженные ионы движутся к отрицательному полюсу – катоду (катионы), отрицательно заряженные ионы к положительному полюсу - аноду (анионы).
3. Диссоциация - обратимый процесс. Наряду с распадом молекул на ионы может протекать процесс соединения ионов в молекулы (ассоциация)
Слайд 10Причины распада вещества на ионы в расплавах
Нагревание усиливает колебания
ионов в узлах кристаллической решётки -кристаллическая решётка разрушается.
Слайд 11Причины диссоциации веществ в воде
1. Вода является полярной молекулой
2. Вода ослабляет взаимодействие между ионами в 81 раз.
диполи
воды "вырывают" ионы из кристаллической решёткиКристаллическая решетка разрушается
Слайд 16Образование в результате распада электролитов гидратированных ионов отражается при написании
уравнений диссоциации, однако, чаще эти уравнения записывают в более короткой
формеСлайд 17Если в молекуле электролита содержатся связи разной полярности, в первую
очередь диссоциируют наиболее полярные связи
NaHSO4
Na+ + HSO4-
H++SO4-2
Слайд 18Количественная характеристика процесса диссоциации
Отношение числа распавшихся молекул к общему числу
молекул в растворе
Сила электролита
Слайд 24При увеличении температуры степень диссоциации электролита увеличивается
При увеличении концентрации электролита
степень его диссоциации уменьшается
Слайд 26
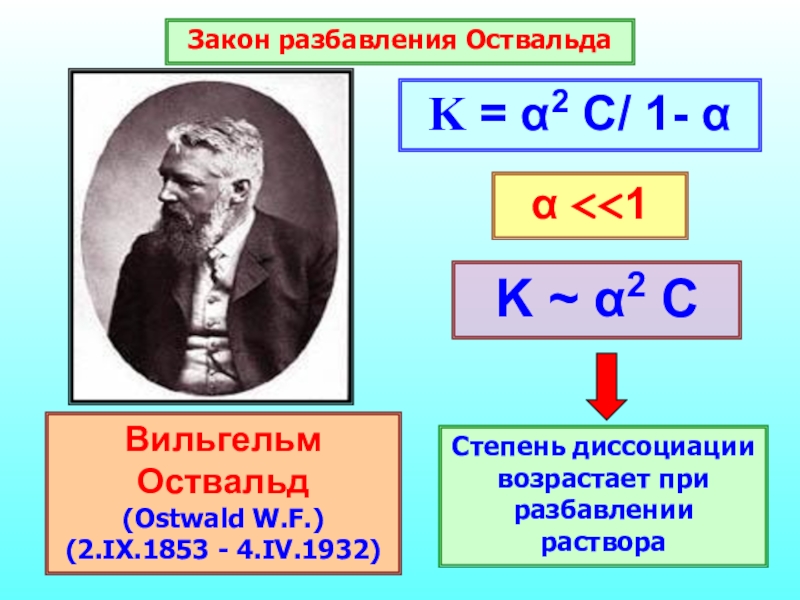
Вильгельм Оствальд
(Ostwald W.F.)
(2.IX.1853 - 4.IV.1932)
Закон разбавления Оствальда
K ~ α2 C
Степень
диссоциации возрастает при разбавлении раствора
K = α2 C/ 1- α
α
<<1Слайд 27Задание для 1 группы:
Впишите недостающие слова:
Все вещества по
их способности проводить электрический ток в растворах делятся на ______________
и ________________.Процесс распада электролита на ионы называется __________________ ______________.
В растворах электролиты диссоциируют на _______________ и ______________ ионы.
По степени электролитической диссоциации электролиты делятся на _________ и _______.
2) Все соли – электролиты, CuSO4 – ___________.
Все растворимые основания – сильные электролиты,
NaOH – ___________________.
электролиты
неэлектролиты
электролитической диссоциацией
положительные
отрицательные
сильные
слабые
электролит
сильный электролит
Слайд 28Задание 2:
Покажите выигрышный путь, состоящий из названий веществ или растворов,
которые:
а) проводят электрический ток
б) не проводят электрический ток
Слайд 30Задание 3:
Соотнесите:
1.
А) Электролиты
1) Кислоты
Б) Неэлектролиты 2) Оксиды
3) Простые вещества
4) Соли
5) Основания
2.
А) Сильные электролиты 1) Азотная кислот
Б) Слабые электролиты 2) Вода
3) Гидроксид натрия
4) Соляная кислота
5) Гидроксид алюминия
3.
Электролиты: Ионы в растворе электролита:
А) NaCl
Б) KOH
В) HNO3
1) OH¯ 4) K
2) H 5) NO3¯
+
+
3) Na 6)Cl
+
–