Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основания 8 класс
Содержание
- 1. Основания 8 класс
- 2. Определение. Основания – это сложные вещества, состоящие
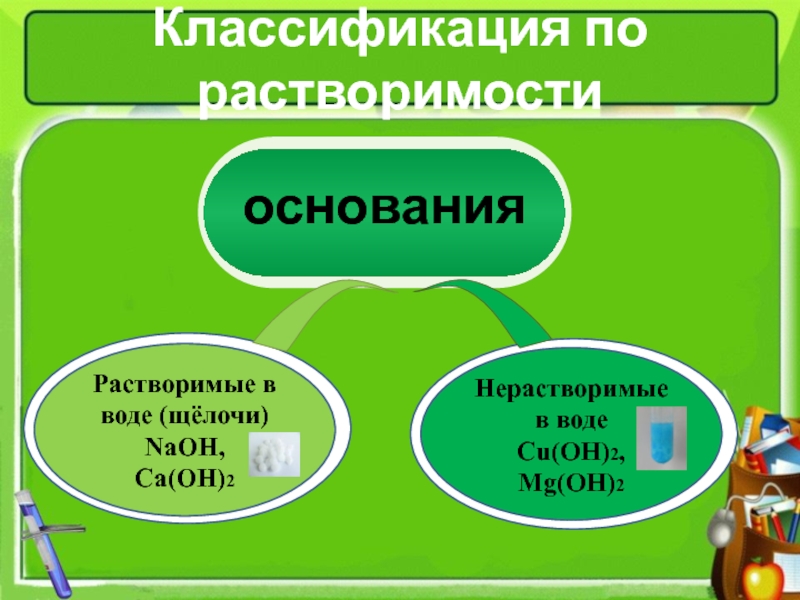
- 3. Классификация по растворимостиРастворимые в воде (щёлочи)NaOH, Ca(OH)2Нерастворимые в водеCu(OH)2, Mg(OH)2
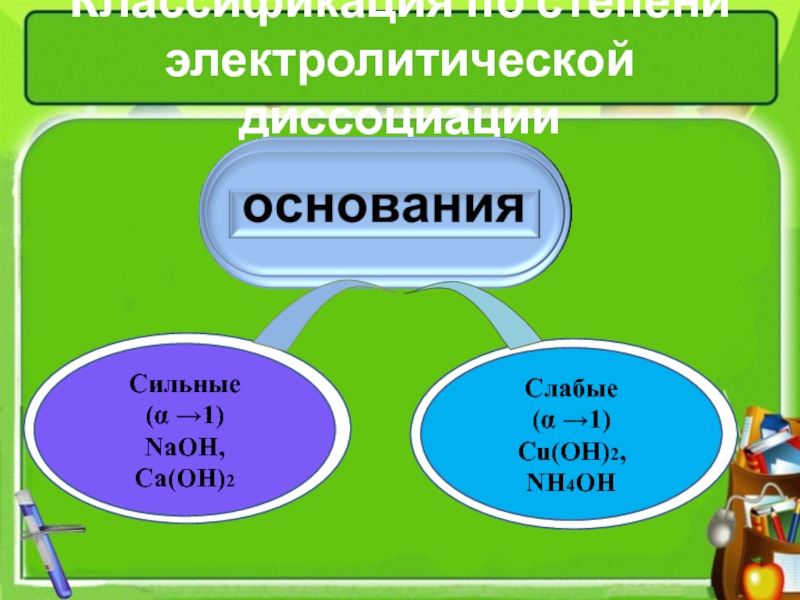
- 4. Классификация по степени электролитической диссоциацииСильные (α →1)NaOH, Ca(OH)2Слабые(α →1)Cu(OH)2, NH4OH
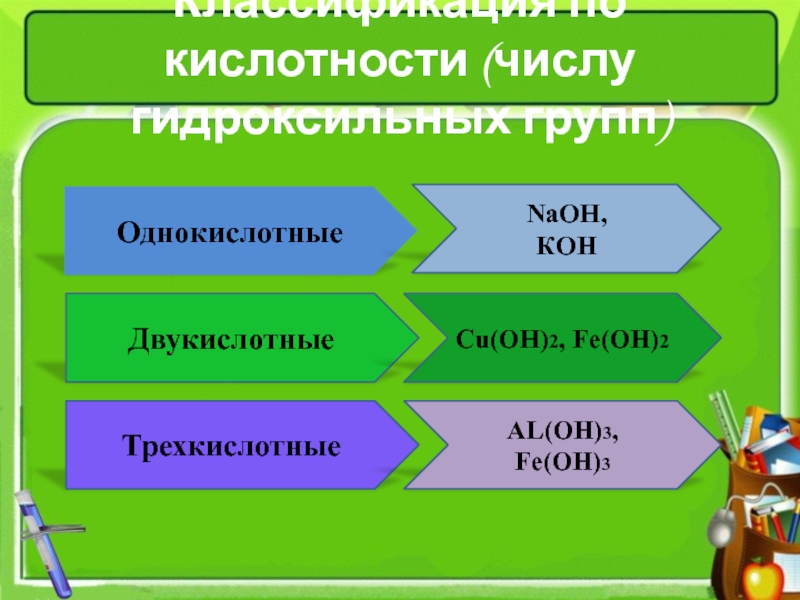
- 5. Классификация по кислотности (числу гидроксильных групп)ОднокислотныеДвукислотныеТрехкислотныеNaOH, КOHAL(OH)3, Fe(OH)3Cu(OH)2, Fe(OH)2
- 6. Химические свойства щелочейКачественные реакции для щелочеймалиновыйбесцветныйФенолфталеинжёлтыйоранжевыйМетиловый оранжевыйсинийфиолетовыйЛакмусЩелочная средаНейтральная средаИндикатор
- 7. Химические свойства щелочейЩелочь + кислота = соль
- 8. Химические свойства гидроксидовГидроксид + кислота = соль
- 9. Химические свойства амфотерных гидроксидовГидроксид + кислота =
- 10. Домашнее задание:§ 39, № 3-5 стр. 217-218.
- 11. Скачать презентанцию
Определение. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов.Основания – электролиты, при диссоциации которых образуются катионы металла и анионы кислотного остатка.
Слайды и текст этой презентации
Слайд 2Определение.
Основания – это сложные вещества, состоящие из ионов металлов
и связанных с ними гидроксид-ионов.
Основания – электролиты, при диссоциации которых
образуются катионы металла и анионы кислотного остатка.Слайд 3
Классификация по растворимости
Растворимые в воде (щёлочи)
NaOH,
Ca(OH)2
Нерастворимые в воде
Cu(OH)2, Mg(OH)2
Слайд 4
Классификация по степени электролитической диссоциации
Сильные
(α →1)
NaOH,
Ca(OH)2
Слабые
(α →1)
Cu(OH)2, NH4OH
Слайд 5Классификация по кислотности (числу гидроксильных групп)
Однокислотные
Двукислотные
Трехкислотные
NaOH,
КOH
AL(OH)3, Fe(OH)3
Cu(OH)2, Fe(OH)2
Слайд 6Химические свойства щелочей
Качественные реакции для щелочей
малиновый
бесцветный
Фенолфталеин
жёлтый
оранжевый
Метиловый оранжевый
синий
фиолетовый
Лакмус
Щелочная среда
Нейтральная среда
Индикатор
Слайд 7Химические свойства щелочей
Щелочь + кислота = соль + вода (нейтрализация)
NaOH + HCl = NaCl + H2O
Щёлочь (изб.) + кислотный оксид = соль + вода
2NaOH + CO2 = Na2CO3 + H2O
3. Щёлочь (нед.) + кислотный оксид = кислая соль
NaOH + CO2 = NaНCO3
4. Щёлочь + соль = гидроксид+ новая соль
2NaOH + CuSO4 = Na2SO4 +Cu(OH)2
Слайд 8Химические свойства гидроксидов
Гидроксид + кислота = соль + вода
Cu(OH)2 + 2HCl = CuCl2 + H2O
2. Разложение на оксид и воду
Cu(OH)2 =t СuO + H2O
Слайд 9Химические свойства амфотерных гидроксидов
Гидроксид + кислота = соль + вода
Zn (OH)2 + 2NaOH Na2ZnO2 + 2H2O