Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Подгруппа азота элективного курса Биогенные элементы нашей жизни 9 класс
Содержание
- 1. Подгруппа азота элективного курса Биогенные элементы нашей жизни 9 класс
- 2. Скажи мне - и я забуду
- 3. Существует много приемов воздействия на эмоциональную сферу
- 4. «Если ученик в школе не научился сам
- 5. научиться познаватьнаучиться делатьнаучиться жить вместенаучиться житьтехнологииИССЛЕДОВАТЕЛЬСКАЯПСИХОЛОГИЧЕСКАЯ самоопределенческаяРЕФЛЕКСИВНАЯИМИТАЦИОННОГОмоделированияДЕЯТЕЛЬНОСТНАЯКОММУНИКАТИВНАЯЧетыре столпа современного образования:
- 6. вне деятельности нет развития; знание учениками их
- 7. Стимулировать интерес обучающихся к определенным проблемам, предполагающим
- 8. Роли участниковобразовательного процессаУченик – активный субъект деятельностиУчитель
- 9. Цели занятия Надпредметные:1.Способствовать развитию:- логического
- 10. Структура занятиявводное слово учителя групповая работа выполнение заданийрецензии ответов оценка групповой работы подведение итогов
- 11. Правила совместной работы Нет “актеров” и “зрителей”, все – участники.
- 12. Подгруппа азотаI. Постановка целейВопрос учащимся: «Как сформулировать
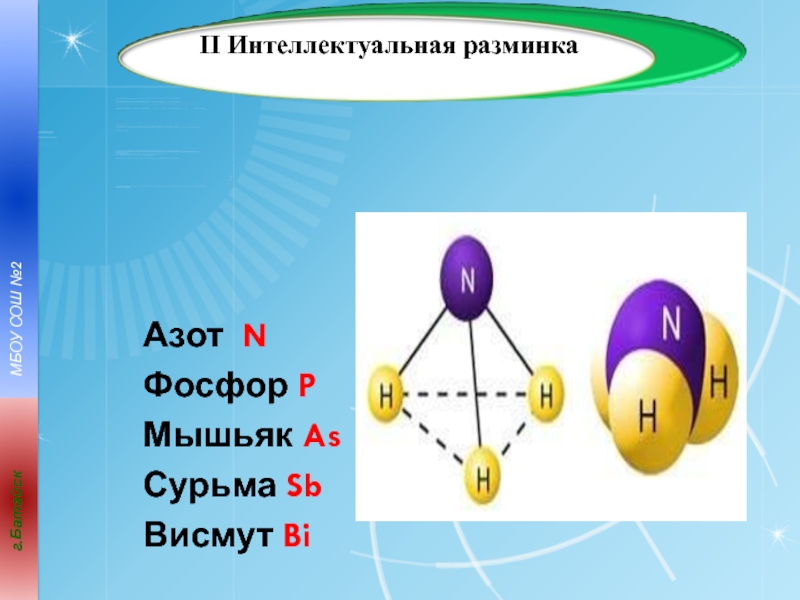
- 13. Азот NФосфор PМышьяк AsСурьма SbВисмут BiII Интеллектуальная разминка
- 14. Пять знаменитых химиков
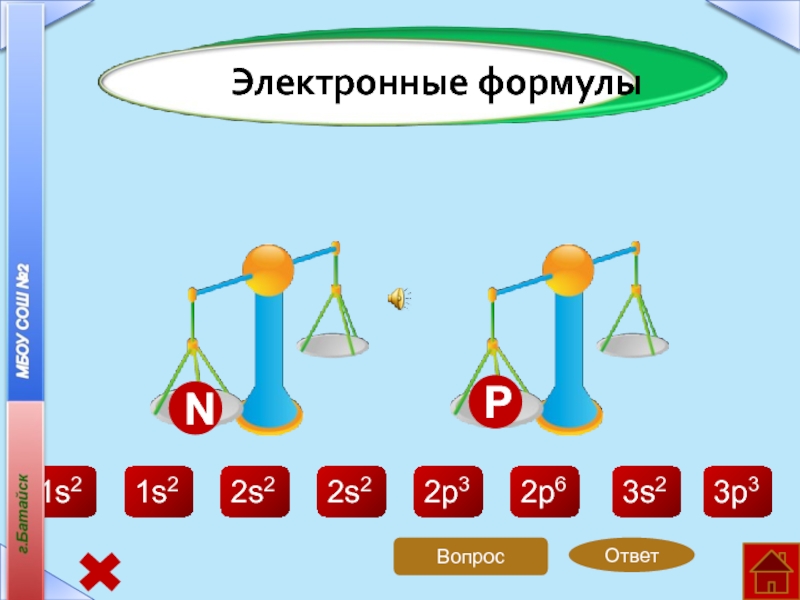
- 15. 1s21s22s22s22p32p63s23p3ОтветNPВопросЭлектронные формулы
- 16. 4ЗаданиеВыбери шар
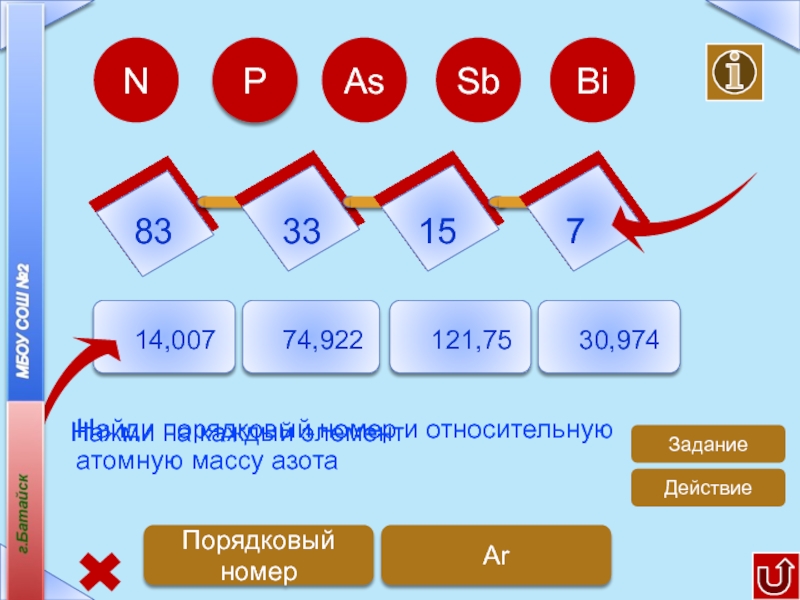
- 17. 833315714,00774,922121,7530,974NНайди порядковый номер и относительную атомную массу азотаЗаданиеArПорядковый номерPAsSbBiДействиеНажми на каждый элемент
- 18. Метафосфорная кислотаАзотистая кислотаАзотная кислотаФосфористая кислота
- 19. сооесНужная информация23456781втнответИллюстрацияЭтот элемент открыт совершенно случайноВ 1669
- 20. Нужная информацияответИллюстрацияСлово укоренилось только в русском и
- 21. Нужная информацияАзот открыт почти одновременно несколькими исследователямиНазвание
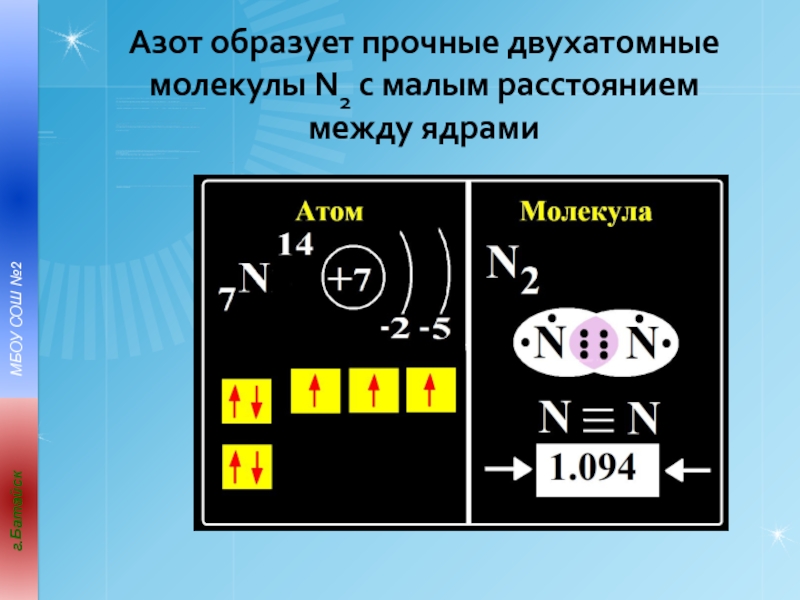
- 22. Азот образует прочные двухатомные молекулы N2 с малым расстоянием между ядрами
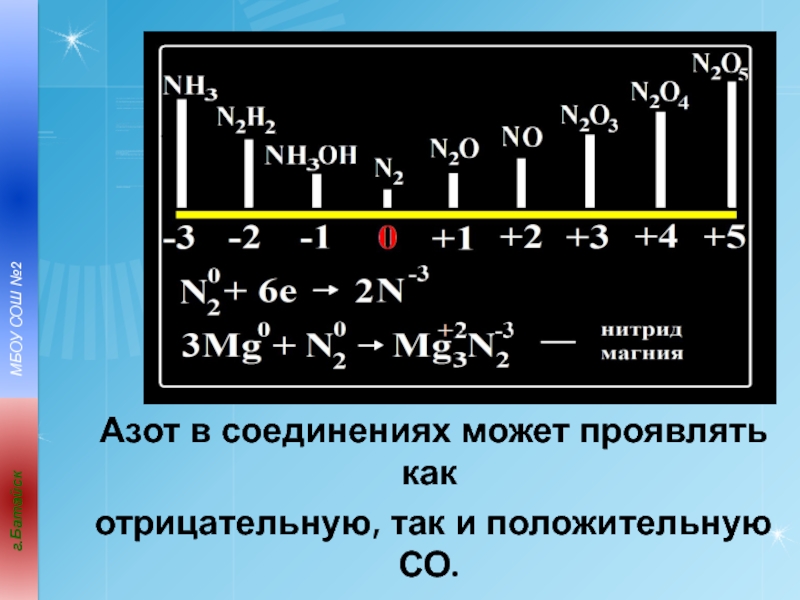
- 23. Азот в соединениях может проявлять
- 24. Почему Даниэль Резерфорд назвал открытый им
- 25. Как получают азот в промышленности? Почему
- 26. 1. Степень окисления азота в оксиде NO2
- 27. 4. С каким из указанных веществ взаимодействует
- 28. Степень окисления азота в оксиде азота N2O
- 29. 4. В молекуле азота связьА) одинарная; Л
- 30. 1. Степень окисления фосфора в оксиде Р2О5
- 31. III команда4. С каким из указанных веществ
- 32. IV. Защита полученных результатовПредставители команд защищают выполненные задания. Учитель подводит итог работы команд.
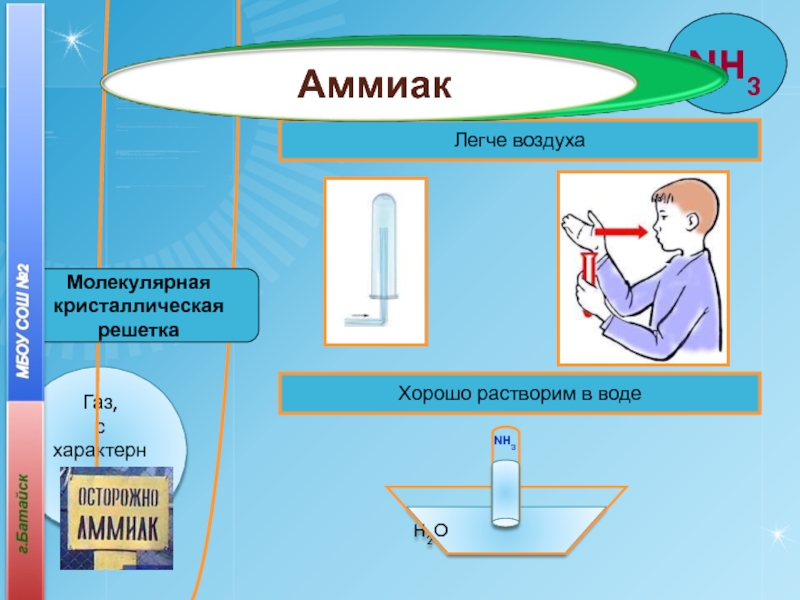
- 33. Легче воздухаХорошо растворим в водеH2ONH3Молекулярная кристаллическая решеткаАммиак
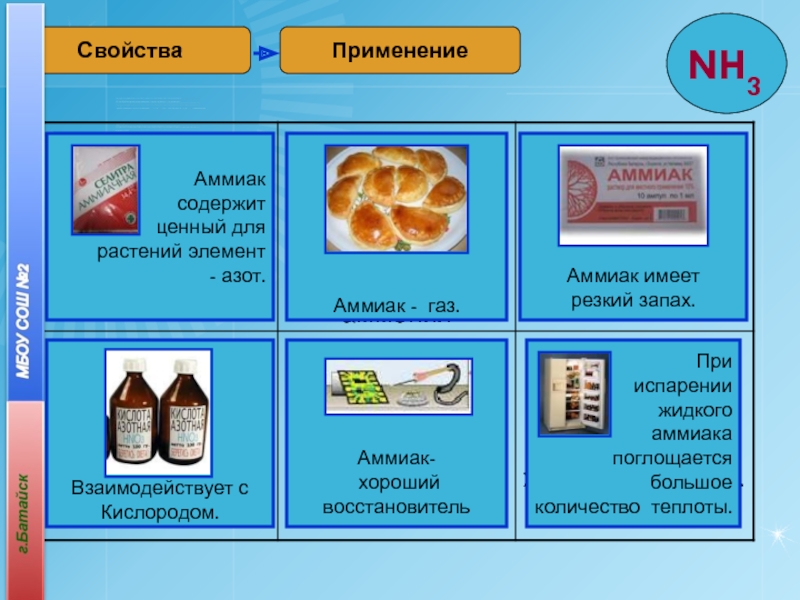
- 34. ПрименениеСвойства
- 35. Азотная кислота
- 36. Одна связь с кислородом образуется
- 37. Азотная кислота широко используется для производства азотных
- 38. неметалл, Ar=31V группа, главная подгруппа3 период, 3
- 39. Красный фосфор применяют для изготовления спичек и
- 40. V .РефлексияУчащиеся высказывают мнение об уроке. Учитель подводит итог урока, выставляет оценки.
- 41. БЛАГОДАРЮ ЗА ВНИМАНИЕ !!!
- 42. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Интегрированное занятие «Подгруппа азота» элективного курса «Биогенные элементы нашей жизни»
области
Слайд 2Скажи мне - и я забуду покажи мне – и я
запомню вовлеки меня в процесс - и я пойду отойди – и
я буду действовать. КонфуцийСлайд 3Существует много приемов воздействия на эмоциональную сферу обучающихся НО! есть
три универсальные познавательные эмоции, которые возникают у любого человека, когда
он сталкивается с противоречием при овладении новым материалом: удивление, недоумение, восхищениеЕсли нет желания учиться
Слайд 4«Если ученик в школе не научился сам ничего творить, то
и в жизни он всегда будет только подражать, копировать, так
как мало таких, которые бы, научившись копировать, умели сделать самостоятельное приложение этих сведений»Л.Н.Толстой
Слайд 5научиться познавать
научиться делать
научиться жить вместе
научиться жить
технологии
ИССЛЕДОВАТЕЛЬСКАЯ
ПСИХОЛОГИЧЕСКАЯ
самоопределенческая
РЕФЛЕКСИВНАЯ
ИМИТАЦИОННОГО
моделирования
ДЕЯТЕЛЬНОСТНАЯ
КОММУНИКАТИВНАЯ
Четыре столпа современного образования:
Слайд 6вне деятельности нет развития;
знание учениками их собственных возможностей и
результатов учения есть обязательные условия их дальнейшего психического развития;
ученик
становится субъектом учебной деятельности лишь на основе таких личностных самообразований, как активность, самостоятельность и общение.Принципы обучения
Слайд 7Стимулировать интерес
обучающихся к определенным
проблемам, предполагающим владение
определенной суммой
знаний
и через деятельность на уроке,
предусматривающую решение проблем,
показать практическое применение
полученных знаний
учителя
Задача
Слайд 8Роли участников
образовательного процесса
Ученик – активный
субъект деятельности
Учитель –организатор учебной деятельности,
способный к проектированию учебного процесса
Основу ФГОС составляет
методика сотрудничества с
учеником, использование системно-деятельностного
подхода, практико-
ориентированного метода
обучения
Слайд 9 Цели занятия
Надпредметные:
1.Способствовать развитию:
- логического мышления уч-ся,
- умений сравнивать,
обобщать данные и делать выводы,
- выбирать критерии для классификации.
2.
Создать условия для воспитания взаимопомощи, умения работать в группе.
3. Способствовать формированию личностных смыслов в усвоении
информации, касающейся бережного отношения к своему здоровью.
Предметные:
Обобщить, закрепить, систематизировать и проверить степень усвоения знаний о свойствах азота, фосфора и их соединений;
умение в составлении ионных уравнений, окислительно-восстановительных реакций;
навыки в решении расчётных и экспериментальных задач.
Цели занятия для ученика:
1. Учиться общаться, работать в группе.
2. Повторить состав, строение, свойства простых веществ, образованных элементами подгруппы азота
3. Проводить химический эксперимент.
4. Знать технику безопасности при работе с веществами.
Слайд 10Структура занятия
вводное слово учителя
групповая работа
выполнение заданий
рецензии ответов
оценка
групповой работы
подведение итогов
Слайд 12Подгруппа азота
I. Постановка целей
Вопрос учащимся: «Как сформулировать цель урока?» (учащиеся
предлагают свои варианты).
Цель урока написана на обратной стороне доски.
На столе
учителя набор фигур с цветовыми сигналами (красный, жёлтый, зелёный). Учащиеся выбирают фигуру и садятся в ту группу, где находится соответствующий сигнал.Слайд 14 Пять знаменитых химиков XVIII в. дали
некоему неметаллу, который в виде простого вещества представляет собой газ
и состоит из двухатомных молекул, пять разных имен.
- «ядовитый воздух»
- «дефлогистированный
воздух»
- «испорченный воздух»
- «удушливый воздух»
- «безжизненный воздух»
В 1772 году шотландский химик,
ботаник и врач Даниел Резерфорд
В 1772 году английский химик
Джозеф Пристли
В 1773 году шведский химик-
аптекарь Карл Шееле
В 1774 году английский химик
Генри Кавендиш
В 1776 году французский химик
Антуан Лавуазье
И это все об азоте
Слайд 1783
33
15
7
14,007
74,922
121,75
30,974
N
Найди порядковый номер и относительную атомную массу азота
Задание
Ar
Порядковый номер
P
As
Sb
Bi
Действие
Нажми на
каждый элемент
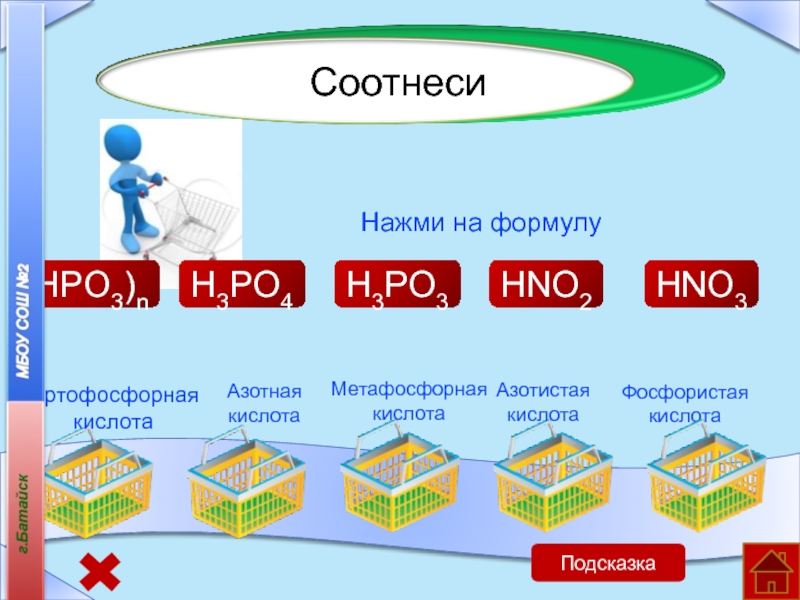
Слайд 18Метафосфорная кислота
Азотистая
кислота
Азотная
кислота
Фосфористая кислота
Ортофосфорная кислота
H3PO4
HNO2
(HPO3)n
Подсказка
HNO3
H3PO3
Нажми на формулу
Соотнеси
Слайд 19с
о
о
е
с
Нужная информация
2
3
4
5
6
7
8
1
в
т
н
ответ
Иллюстрация
Этот элемент открыт совершенно случайно
В 1669 году алхимиком Брандом
Назван
« phosphorus» - фосфор
Зашифрованное слово – это перевод слова фосфор
с греческогоЧасто встречается в русской химической литературе XIX века
Таинственный элемент
Слайд 20Нужная информация
ответ
Иллюстрация
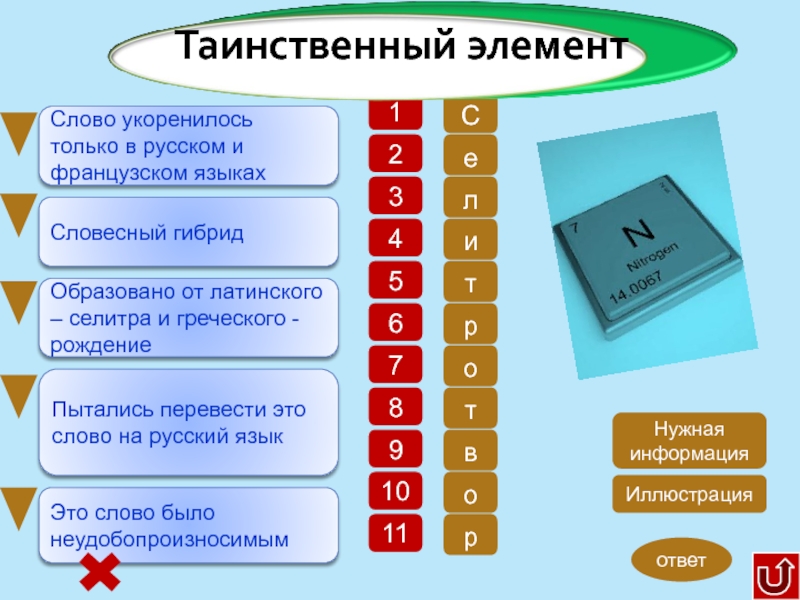
Слово укоренилось только в русском и французском языках
Словесный гибрид
Образовано
от латинского – селитра и греческого - рождение
Пытались перевести это
слово на русский языкЭто слово было неудобопроизносимым
2
3
4
5
6
7
8
1
9
10
11
е
р
С
в
о
р
е
л
и
т
р
о
т
С
в
о
р
Таинственный элемент
Слайд 21Нужная информация
Азот открыт почти одновременно несколькими исследователями
Название от греческой отрицательной
приставки «а» и слова «зоэ»
Название означало «безжизненный»
Название часто встречалось в
русской химической литературе начала XIX века2
3
4
5
6
7
8
1
ответ
Иллюстрация
9
в
л
т
р
о
Г
о
в
л
н
т
и
Таинственный элемент
Слайд 24 Почему Даниэль Резерфорд назвал открытый им газ «зловредным», а
Антуан Лавуазье дал ему общее название - азот, т.е. «безжизненный»?
Чем обусловлена химическая инертность азота?
В какое соединение превращается азот в верхних слоях атмосферы во время грозовых разрядов?
Слайд 25 Как получают азот в промышленности?
Почему азот называют
«элементом жизни»?
Что такое «нашатырный спирт»? Для чего его используют?
Какие свойства аммиака лежат в основе его применения в холодильных установках?
Слайд 261. Степень окисления азота в оксиде NO2 равна.
А) +2; К
Б) +4; А В) -4. Н
2. Как называются
соли азотной кислотыА) нитраты; М Б) нитриты; И В) нитриды. Л
3. В каких из указанных реакций азот N2 играет роль восстановителя?
А) N2 + 3Mg = Mg3N2; К Б) N2 + 3F2 = 2NF3; М В) N2 + 3H2 = 2NH3 Н
III. Прохождение маршрута командами
По результатам выполненных заданий должно получиться слово. Ответы закодированы буквами русского алфавита.
I команда
Слайд 274. С каким из указанных веществ взаимодействует конц. HNO3 с
образованием NO2?
А) Сu; И Б) ZnO; А В)
Ag. О5. Сумма коэффициентов в уравнении реакции NH3 + O2 = N2 +H2O равна:
А) 7; Т Б) 10; С В) 15. А
6. Сколько молей азотной кислоты расходуется на с 10 г карбоната кальция?
А) 0,1 моль; М Б) 2 моль; У В) 0,2 моль. К (АММИАК)
III. Прохождение маршрута командами
Слайд 28Степень окисления азота в оксиде азота N2O равна
А) +2; К
Б) +1; Н В) +4. О
2. Как называются
соли азотистой кислотыА) нитраты; А Б) нитриты; И В) нитриды. В
3. В каких из указанных реакций азот N2 играет роль окислителя?
А) N2 + 3Mg = Mg3N2; Т Б) N2 + 3F2 = 2NF3; Б В) N2 + O2 = 2NO В
II команда
Слайд 294. В молекуле азота связь
А) одинарная; Л Б) двойная;
С В) тройная. Р
5. Сумма коэффициентов в уравнении реакции
NH3 + O2 = NO + H2O равнаА) 19; А Б) 9; У В) 12. И
6. Какой объём углекислого газа выделяется в реакции азотной кислоты с 21,2 г карбоната натрия?
А) 2,24 л; М Б) 44,8 л; Х В) 4,48 л Т (НИТРАТ)
II команда
Слайд 301. Степень окисления фосфора в оксиде Р2О5 равна
А) +3; А
Б) +5;Ф В) – 3. К
2. Как
называются соли фосфорной кислоты?А) фосфиды; А Б) фосфориты; У В) фосфаты.О
3. В каких из указанных реакций фосфор играет роль восстановителя?
А) 2Р+8Н2О=2Н3РО4+5Н2 С Б) 3Са+2Р=Са3Р2 М В)3Nа+Р= Nа3Р Н
III команда
Слайд 31III команда
4. С каким из указанных веществ взаимодействует оксид фосфора
(V) Р2О5?
А) НNО3 Н Б) NаОН
Ф В)СО2 А5. Сумма коэффициентов в уравнении реакции РН3+О2=Р2О5+Н2О равна
А) 10 И Б) 6 А В) 4 О
6) Сколько граммов соли образуется в реакции фосфорной кислоты с 12г гидроксида натрия.
А) 16,4г Д Б)98г К В) 19,6г Т (ФОСФИД)
Слайд 32IV. Защита полученных результатов
Представители команд защищают выполненные задания. Учитель подводит
итог работы команд.
Слайд 36
Одна связь с кислородом образуется по донорно-акцепторному
механизму, но из-за близости расположения атомов в молекуле становятся равноценными.
Строение
Слайд 37Азотная кислота широко используется для производства азотных удобрений, искусственных волокон,
органических красителей, лаков и взрывчатых веществ.
Применение
Слайд 38неметалл,
Ar=31
V группа, главная подгруппа
3 период, 3 ряд
степени окисления -3.0,+1,+3,+5.
оксиды
Р2О3 и Р2О5 - оба оксида кислотные
Кислоты:
H 3PO3 –фосфористая кислота H3PO4 –фосфорная кислота
летучее водородное соединение РН3-газ фосфин ( связь ковалентная почти неполярная)
Р Фосфор
( Phosphorus-Cветоносец)
Фосфор