Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация для урока химии "Алканы"
Содержание
- 1. Презентация для урока химии "Алканы"
- 2. Алканы (предельные, насыщенные, парафины) – органические вещества,
- 3. Гомологический ряд алканов.
- 4. Гибридизация АО - это взаимодействие (смешение) разных
- 5. Строение молекулыВсе атомы углерода в молекулах алканов
- 6. Строение молекулыСвязи углерод-углерод являются неполярными и плохо
- 7. Строение алкановковалентная полярная связь. 109° 28’ –
- 8. ИзомерияСтруктурная Изомерия углеродного скелета
- 9. Строение алкановОтсутствие в молекулах алканов полярных связей
- 10. Физические свойства С 1 – С4 –
- 11. Химические свойстваДля алканов характерны следующие реакции:Реакции замещения
- 12. 1) Реакция галогенированияСН4 + Сl2 → СН3Сl
- 13. 2) Реакция нитрования (реакция М.И.Коновалова).Реакция Коновалова М.
- 14. ДегидрированиеПри пропускании нагретого алкана над
- 15. крекингПри нагревании до температуры выше 500°
- 16. 2) пиролизПри увеличении температуры можно достичь такой
- 17. 3) ароматизацияАлканы с 6 и более атомами
- 18. Под влиянием катализаторов при нагревании углеводороды нормального
- 19. При мягком окислении СН4 в присутствии катализатора
- 20. V. конверсия СН4+Н2O CO+3H2Так
- 21. Отношение алканов к растворам перманганата калия
- 22. Нахождение в природеОсновные источники алканов – нефть
- 23. Слайд 23
- 24. Слайд 24
- 25. Способы получения алканов1) Промышленные способыприродные источники;крекинг алканов;Метод
- 26. ПРОМЫШЛЕННЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКАНОВ
- 27. Способы получения алкановПолучение из природных источников: а)
- 28. Способы получения алканов Гидрирование угля: реакция идет
- 29. Способы получения алкановСН3-СН2-СН2-СН2-СН2 - СН2-СН2-СН2-СН2-СН3 СН3-СН2-СН2-СН2-СН2-
- 30. Способы получения алканов Синтез Фишера-Тропша, на основе
- 31. ЛАБОРАТОРНЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКАНОВ
- 32. 1. Реакция Вюрца - взаимодействие натрия с
- 33. 2) Реакция Дюма - сплавление солей карбоновых кислот со щелочью.Способы получения алканов
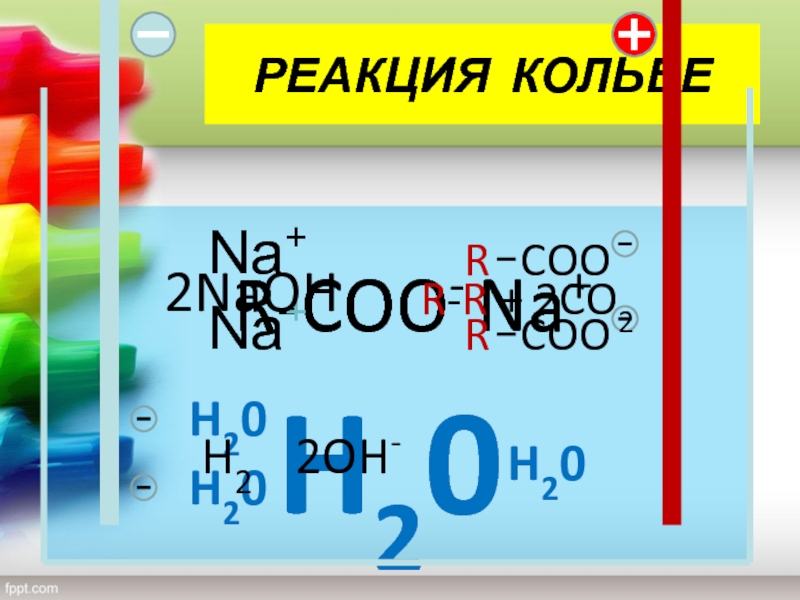
- 34. Способы получения алканов3) РЕАКЦИЯ КОЛЬБЕПротекает при прохождении
- 35. РЕАКЦИЯ КОЛЬБЕNaR-COOH20Na+R-COO-H20H20RCOORCOOR-R + 2CO2H20H22OH-Na+Na+2NaOH
- 36. Способы получения алкановГидролиз карбидов металлов.Al4C3 + 12H2O
- 37. СИНТЕЗ С ИСПОЛЬЗОВАНИЕМ РЕАКТИВА ГРИНЬЯРа Реактив Гриньяра
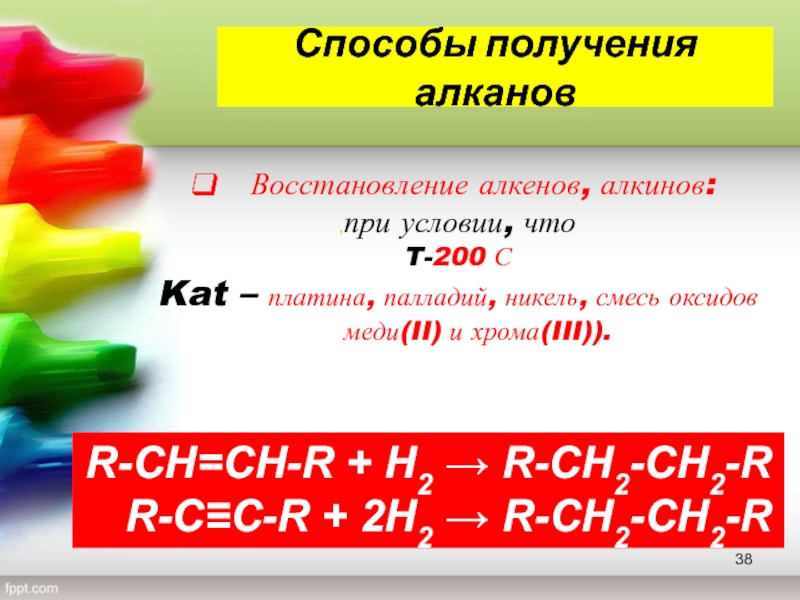
- 38. Способы получения алканов Восстановление алкенов, алкинов:,при условии,
- 39. Способы получения алкановВОССТАНОВЛЕНИЕ ГАЛОГЕНАЛКАНОВ И НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ:
- 40. ПРИМЕНЕНИЕ АЛКАНОВ Значение алканов для человечества огромно!
- 41. ПРИМЕНЕНИЕ АЛКАНОВВысшие алканы входят в состав смазочных масел, вазелина и парафина.
- 42. ПРИМЕНЕНИЕ АЛКАНОВ Газообразные алканы - ценное топливоЖидкие
- 43. ПРИМЕНЕНИЕ АЛКАНОВ Алканы в составе бензина, керосина, солярового масла, мазута используются в качестве топлива.
- 44. ПРИМЕНЕНИЕ АЛКАНОВ Смесь изомерных пентанов и гексанов
- 45. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2 Алканы (предельные, насыщенные, парафины) – органические вещества, состоящие из атомов
углерода и водорода, связанных между собой одинарными (сигма) связями.
Слайд 4Гибридизация АО - это взаимодействие (смешение) разных по типу, но
близких по энергии атомных орбиталей данного атома с образованием гибридных
орбиталейСЛОВАРЬ
Слайд 5Строение молекулы
Все атомы углерода в молекулах алканов находятся в состоянии
sp3-гибридизации, т.е. все четыре гибридные орбитали атома
углерода одинаковы по форме, энергии и направлены к вершинам равносторонней треугольной пирамиды – тетраэдра. Угол между направлениями связей составляет 109°28´, поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг), хотя молекулы алканов могут приобретать самую разнообразную форму, потому что вокруг одинарной углерод-углеродной связи возможно практически свободное вращение.
Слайд 6Строение молекулы
Связи углерод-углерод являются неполярными и плохо поляризуемыми, длина связи
C–C равна 0,154 нм. Связи C–H несколько короче и
являются слабополярными.
Слайд 7Строение алканов
ковалентная полярная связь.
109° 28’ – угол между связями
Длина
связи C-H 0.109 нм
C-C 0.154 нмСлайд 8Изомерия
Структурная
Изомерия углеродного скелета
СН3 – СН2
– СН2 – СН2 – СН3
н-пентан СН3СН3 – СН – СН2 – СН3 І
l СН3 ─ С ─ СН3
СН3 І
2-метилбутан СН3
2,2-диметилпропан
С5Н12 :
Пространственная: не характерна
Слайд 9Строение алканов
Отсутствие в молекулах алканов полярных связей приводит к тому,
что они плохо растворимы в воде, не вступают во взаимодействие
с ионами. Наиболее характерными для алканов являются реакции, протекающие по свободно-радикальному механизму.Слайд 10Физические свойства
С 1 – С4 – газ без цвета
и запаха
С 5 – С 17 – бесцветные жидкости
с запахом бензинаС 18 … -твердые вещества, белого цвета, жирные на ощупь
По мере увеличения числа атомов углерода в цепи возрастает температура кипения, плавления и плотность
Молекулы с разветвленным скелетом кипят и плавятся при более низкой температуре, чем молекулы с нормальным строением
Газообразные и жидкие алканы образуют взрывоопасные смеси с воздухом
Алканы практически не растворимы в воде, но растворяются в неполярных органических растворителях (бензол,тетрахлорметан)
Жидкие и твердые алканы смешиваются друг с другом
Слайд 11Химические свойства
Для алканов характерны следующие реакции:
Реакции замещения
Реакции элиминирования
(отщепления)
Реакции изомеризации
Реакции окисления
Слайд 121) Реакция галогенирования
СН4 + Сl2 → СН3Сl + НСl
СН4 +
Сl2 → СН2Сl2 + 2НСl
СН4 + 3Сl2 → СНСl3 +
3НСlСН4 + 4Сl2 → ССl4 + 4НСl
ЗАПОМНИ: Реакция начинается при освещении и носит радикально-цепной
характер, т.е. идет через образование свободных радикалов.
Реакции замещения
(по свободнорадикальному механизму) разрыв связей C – H и замещение атомов водорода
Слайд 132) Реакция нитрования (реакция М.И.Коновалова).
Реакция Коновалова М. И.: взаимодействие с
разбавленной азотной кислотой при 140°С и при повышенном или нормальном
давлении – образуется смесь изомерных нитросоединений (легче всего замещаются атомы водорода у третичного атома углерода, труднее – у вторичного, наиболее трудно – у первичного).СН4 + HO-NO2 = CH3-NO2 + H2O
Реакции замещения
(по свободнорадикальному механизму) разрыв связей C – H и замещение атомов водорода
Слайд 14
Дегидрирование
При пропускании нагретого алкана над платиновым или никелевым
катализатором может отщепиться водород. Этот процесс называется дегидрированием
C3H8
C3H6 + H22СН4 Н─С≡С─Н + 3Н2
СН3─СН3 Н2С═СН2 + Н2
II. Реакции отщепления
Слайд 15
крекинг
При нагревании до температуры выше 500° в молекулах алканов
происходит разрыв связей между атомами углерода.
C 10H22 C5H12+C5H10C10H22 C4H10+C6H12
Этот процесс называется термическим крекингом (от англ. tocrack– «колоть, расщеплять»).
II. Реакции отщепления
Слайд 162) пиролиз
При увеличении температуры можно достичь такой степени протекания реакции,
при которой органические вещества – углеводороды – полностью разлагаются на
углерод и водород. Такой процесс называется пиролизом.СН4 С+2Н2
2СН4 С2Н2 + 3Н2
II. Реакции отщепления
Слайд 173) ароматизация
Алканы с 6 и более атомами углерода вступают в
реакции дегидрирования с образованием цикла (дегидроциклизации)
С6Н14
С6Н6 + 4Н2II. Реакции отщепления
Слайд 18Под влиянием катализаторов при нагревании углеводороды нормального строения подвергаются изомеризации
- перестройке углеродного скелета с образованием алканов разветвленного строения.
CH3-CH2-CH2-CH3 AlCl3 CH3-CH-CH3
CH3
n-бутан 2-метил пропан
III. Реакции изомеризации
Слайд 19
При мягком окислении СН4 в присутствии катализатора кислородом при 200 °C
могут образоваться:
Метиловый спирт: 2СН4 + О2 → 2СН 3ОН;
формальдегид:
СН4 + О2 → СН 2О + Н 2O; Муравьиная кислота :
2СН4 + 3О2 → 2НСООН + 2Н2O.
IV. Реакции окисления
1) Горение
СН4 +2О2 →СО2 + 2Н2О
2) Каталитическое окисление
Слайд 20V. конверсия
СН4+Н2O CO+3H2
Так называют взаимодействия алканов, из
которых чаще всего используют природный газ с парами воды. При
высокой температуре около 1000 образуется смесь оксида углерода – угарного газа и водорода. Эту смесь называют синтез- газ.Часто ее не разделяют, а используют для получения разных органических веществ.
Слайд 21 Отношение алканов к растворам перманганата калия и бромной воды.
Чтобы
отличить предельные углеводороды от непредельных используют растворы бромной воды и
перманганата калияАлканы не обесцвечивают раствор перманганата калия и бромную воду
Слайд 22Нахождение в природе
Основные источники алканов – нефть и природный газ.
Метан составляет основную массу природного газа, в нем присутствуют также
в небольших количествах этан, пропан и бутан. Метан содержится в выделениях болот и угольных пластов. Наряду с легкими гомологами метан присутствует в попутных нефтяных газах. Эти газы растворены в нефти под давлением и находятся также над ней. Алканы составляют значительную часть продуктов переработки нефти. Содержатся в нефти и циклоалканы – они называются (от греч. naphtha – нефть). нафтенамиСлайд 23 В природе широко распространены также газовые гидраты алканов, в основном
метана, они залегают в осадочных породах на материках и на
дне океанов. Их запасы, вероятно, превышают известные запасы природного газа и в будущем могут случить источником метана и его ближайших гомологов.Нахождение в природе
Слайд 24
Нахождение в природе
Твердые алканы встречаются в природе в виде залежей
горного воска – озокерита, в восковых покрытиях листьев, цветов и
семян растений, входят в состав пчелиного воска.Слайд 25Способы получения алканов
1) Промышленные способы
природные источники;
крекинг алканов;
Метод Фишера- Тропша
2) Лабораторные
способы
реакция Вюрца,
реакция Дюма,
реакция Кольбе.
гидролиз реактива Гриньяра,
восстановление галогеноалканов
инепредельных соединений
Слайд 27Способы получения алканов
Получение из природных источников:
а) метан, этан, пропан,
бутан выделяют из природного газа, причем метана в нем 95-98
%об.б) Алканы от С5 до С11 выделяют из бензиновой фракции нефти
в) алканы от С12 до С16 из средней фракции нефти
г) высшие алканы, от С16 и выше, получают вакуумной перегонкой неперегоняемого остатка нефти.
Слайд 28Способы получения алканов
Гидрирование угля:
реакция идет при условиях:
T-400-600
С,
P-250атм.
Kat-FeO-Fe2O 3
С + 2H2 = CH4 – частный
случай для метанаСлайд 29Способы получения алканов
СН3-СН2-СН2-СН2-СН2 - СН2-СН2-СН2-СН2-СН3
СН3-СН2-СН2-СН2-СН2- + -СН2-СН2-СН2-СН2-СН3
СН3-СН2-СН2-СН2-СН3 + СН2=СН-СН2-СН2-СН3
С16Н34
С18Н38
СnH2n+2
CmH2m+2 + Cn-mH2n-2mКРЕКИНГ АЛКАНОВ
Реакции расщепления углеродного скелета крупных молекул при нагревании и в присутствии катализаторов.
При температуре 450 – 700 ° С алканы распадаются за счет разрыва связей С – С (более прочные связи С – Н при этом сохраняются) и образуются алканы и алкены с меньшим числом углеродных атомов.
Слайд 30Способы получения алканов
Синтез Фишера-Тропша, на основе синтез-газа (CO +
H2):
Kat - Ni или Co
T- 200 С
3CO + 7H2=C3H8
+ 3H2O – частный случай для пропана.
Слайд 321. Реакция Вюрца - взаимодействие натрия с галогенпроизводными алканов:
Приводит к
увеличению углеводородной цепи.
Если в реакцию вступают различные галогеналканы, то
образуется смесь алканов.Способы получения алканов
Слайд 34Способы получения алканов
3) РЕАКЦИЯ КОЛЬБЕ
Протекает при прохождении электрического тока через
расплав или раствор соли карбоновой кислоты.
2RCOONa + 2H2O =
R-R + 2CO2 +H2 + 2 NaOH
2RCOONa → R-R + 2CO2 + 2Na
Слайд 36Способы получения алканов
Гидролиз карбидов металлов.
Al4C3 + 12H2O → 4Al(OH)3 +
3CH4↑
карбид
алюминия
Слайд 37СИНТЕЗ С ИСПОЛЬЗОВАНИЕМ РЕАКТИВА ГРИНЬЯРа Реактив Гриньяра имеет формулу RMgX и
общее название алкилмагний-галогенид. Считается, что связь углерод — магний является
ковалентной, но сильно полярной; связь магний — галоген по существу ионная.
RHal + Mg → RMgHal
RMgHal + HCl → RH + MgClHal
Способы получения алканов
Слайд 38Способы получения алканов
Восстановление алкенов, алкинов:
,при условии, что
T-200 С
Kat
– платина, палладий, никель, смесь оксидов меди(II) и хрома(III)).
R-CH=CH-R
+ H2 → R-CH2-CH2-R
R-C≡C-R + 2H2 → R-CH2-CH2-RСлайд 39Способы получения алканов
ВОССТАНОВЛЕНИЕ ГАЛОГЕНАЛКАНОВ И НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ:
Восстановление галогеналканов:
RHal
+ H2 → RH + Hhal
Катализатор: палладий на карбонате бария.
Восстановление иодалканов иодоводородной кислотой: RI + HI → RH + I2
Слайд 40ПРИМЕНЕНИЕ АЛКАНОВ
Значение алканов для человечества огромно! Представить нашу жизнь
без алканов очень и очень сложно… Но тот факт, что
нефть на земле довольно скоро закончится ставит под вопрос столь простой и выгодный для человечества способ получения энергии, как сжигание алканов. Количество энергии, полученное человечеством от этих соединений очень велико. Как и области применения алканов.Слайд 42ПРИМЕНЕНИЕ АЛКАНОВ
Газообразные алканы - ценное топливо
Жидкие алканы – основа
в изготовлении косметики, медикаментов; разные растворители, моторное и ракетное топливо
и т. д.Твердые алканы – изготовление свечей, пропитка бумаги и т. д. Сырье для нефтехимических производств