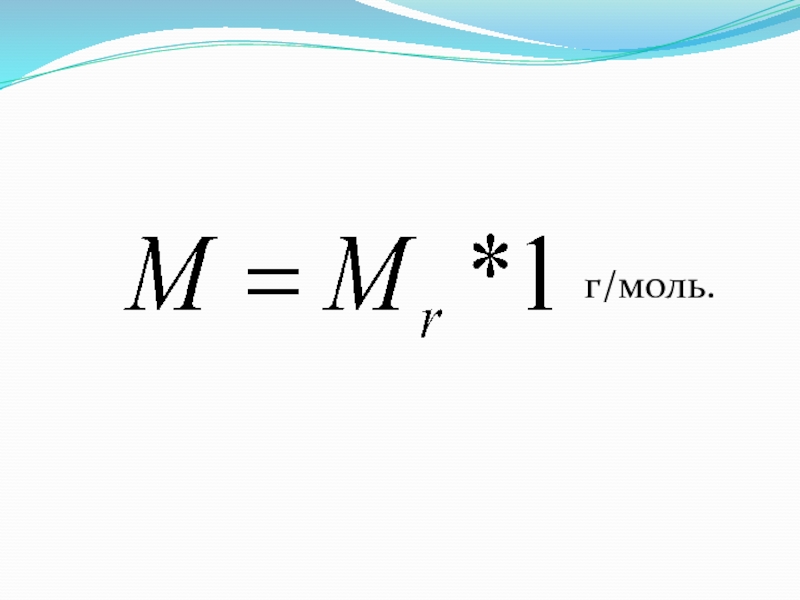Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку по химии
Содержание
- 1. Презентация к уроку по химии
- 2. Основные понятия химии.
- 3. Вещество – это совокупность атомов, ионов или молекул, состоящих из одного или нескольких химических элементов.
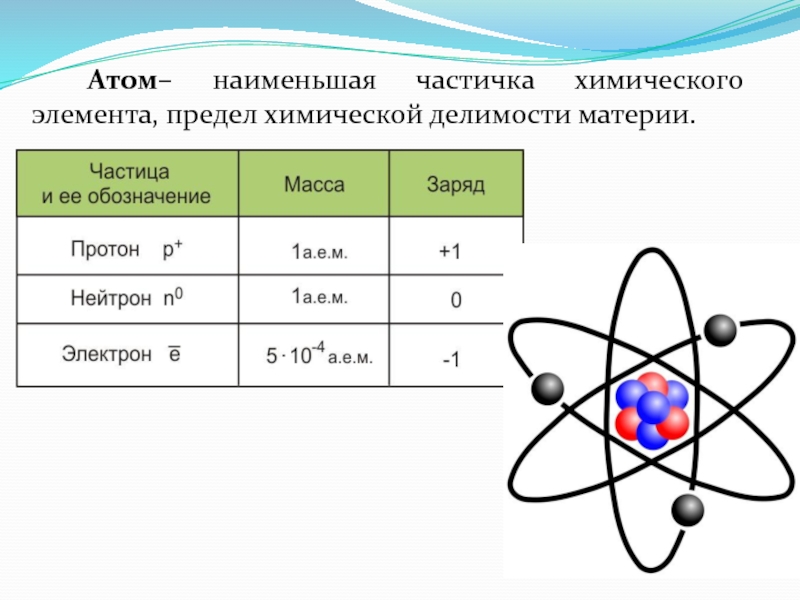
- 4. Атом– наименьшая частичка химического элемента, предел химической делимости материи.
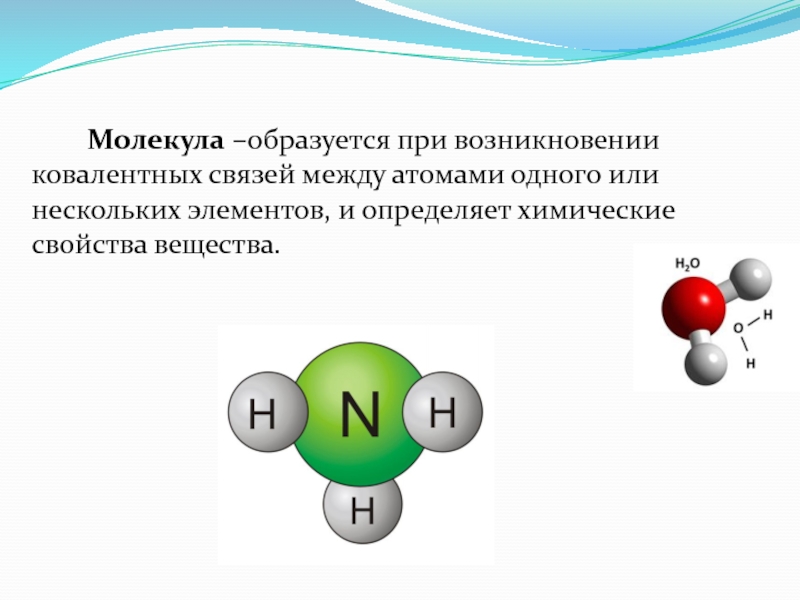
- 5. Молекула –образуется при возникновении ковалентных связей между
- 6. Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
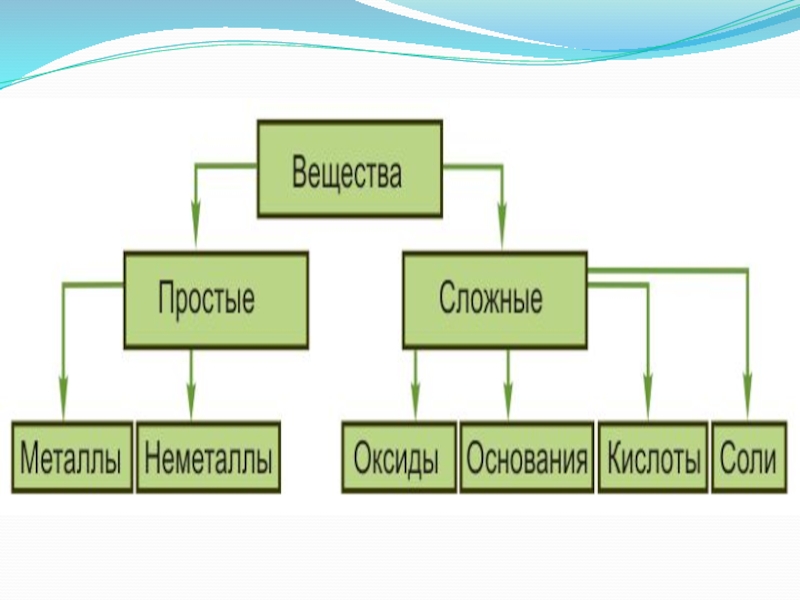
- 7. Состав веществ. Измерение веществ.
- 8. Слайд 8
- 9. Качественный состав – это совокупность химических элементов
- 10. Химический знак (символ)
- 11. Химическая формула
- 12. Валентность – это способность атомов одного химического
- 13. Простейшая (эмпирическая) формула показывает качественный состав и
- 14. Относительная атомная масса ( ) химического элемента
- 15. Mr (вещества) = Ar(э) + Ar(э)Относительная молекулярная масса ( )
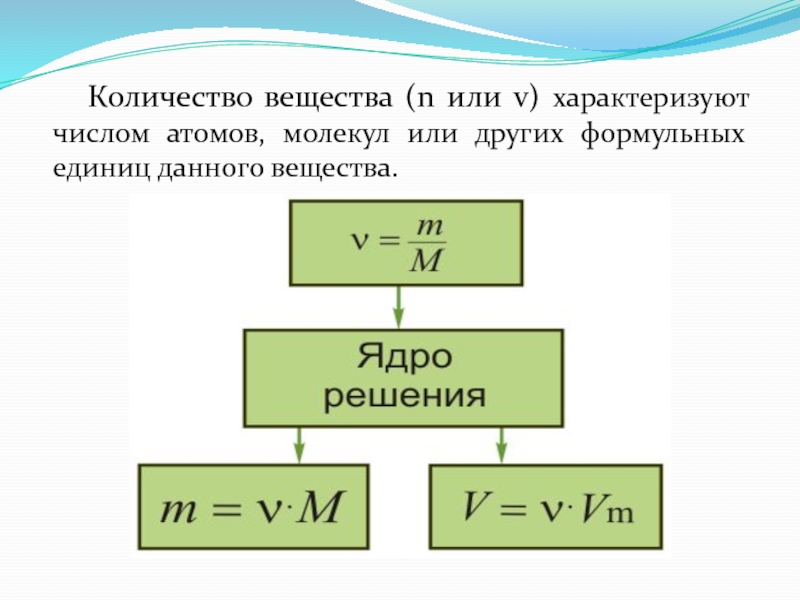
- 16. Количество вещества (n или v) характеризуют числом атомов, молекул или других формульных единиц данного вещества.
- 17. Слайд 17
- 18. Постоянная Авогадро ( ) –
- 19. Основные законы химии
- 20. Закон сохранения массы. Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции.
- 21. Стехиометрия – раздел химии, в котором рассматриваются
- 22. Закон постоянства состава вещества. Всякое чистое вещество независимо
- 23. Современная формулировка закона постоянства состава вещества таков: Состав
- 24. Вещества постоянного состава называют дальтонидами в честь
- 25. Закон Авогадро. В равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
- 26. Один моль любого газа при одинаковых условиях
- 27. Массы двух разных газов, занимающих одинаковый объем
- 28. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона).
- 29. Основные законы химии
- 30. Найдите относительные молекулярные массы веществ, состав которых
- 31. Сколько молекул содержится в 32 г сернистого
- 32. Скачать презентанцию
Основные понятия химии.
Слайды и текст этой презентации
Слайд 3
Вещество – это совокупность атомов, ионов или молекул, состоящих из
одного или нескольких химических элементов.
Слайд 5 Молекула –образуется при возникновении ковалентных связей между атомами одного или
нескольких элементов, и определяет химические свойства вещества.
Слайд 9
Качественный состав – это совокупность химических элементов и (или) атомных
группировок, составляющих данное химическое вещество.
Количественный состав – это показатели, характеризующие
количество или число атомов того или иного химического элемента и (или) атомных группировок, образующих данное химическое вещество.Слайд 12
Валентность – это способность атомов одного химического элемента соединятся со
строго определенным числом атомов другого химического элемента.
Слайд 13
Простейшая (эмпирическая) формула показывает качественный состав и соотношения ( НО,
NO).
Молекулярная (истинная) формула показывает качественный состав и число составляющих вещество
частиц, но не показывает порядок связей частиц в веществе. (H2O2)Графическая формула отражает порядок соединения атомов, т. е. связи между ними. (Н-О-О-Н).
Слайд 14
Относительная атомная масса ( ) химического элемента – это величина,
показывающая отношение средней массы атома природной изотопной смеси элемента к
1/12 массы атома углеродаСлайд 16 Количество вещества (n или v) характеризуют числом атомов, молекул или
других формульных единиц данного вещества.
Слайд 18
Постоянная Авогадро ( ) – число атомов или
молекул (или других формульных единиц), содержащихся в одном моле вещества;
она всегда равна
Слайд 20Закон сохранения массы.
Масса веществ, вступивших в реакцию, равна массе веществ,
образовавшихся в результате реакции.
Слайд 21
Стехиометрия – раздел химии, в котором рассматриваются массовые и объемные
соотношения между реагирующими веществами, вывод химических формул и составление уравнений
химических реакций.Слайд 22
Закон постоянства состава вещества.
Всякое чистое вещество независимо от способа его
получения всегда имеет постоянный качественный и количественный состав.
Однако уже в
начале XIX в. К. Бертолле показал, что элементы могут соединятся друг с другом в разных соотношениях в зависимости от массы реагирующих веществ.Слайд 23
Современная формулировка закона постоянства состава вещества таков:
Состав соединений молекулярной структуры
является постоянным независимо от способа их получения. Состав соединений немолекулярной
структуры (с атомной, ионной или металлической кристаллической решеткой) не является постоянным и зависит от способа их получения.Слайд 24
Вещества постоянного состава называют дальтонидами в честь английского физика и
химика Дж. Дальтона,
а вещества переменного состава –
бертоллидами в честь французского химика К. Бертолле.Слайд 25
Закон Авогадро.
В равных объемах различных газов при одинаковых условиях содержится
одинаковое число молекул.
Слайд 26
Один моль любого газа при одинаковых условиях занимает один и
тот же объем.
Этот объем, называемый
молярным ( ), при нормальных условиях (давление = 101325 Па и абсолютной температуре = 273,15 К) равен 22,4 л:
Слайд 27
Массы двух разных газов, занимающих одинаковый объем при одинаковых условиях,
относятся между собой как их молярные массы
Отношение масс двух газов,
занимающих равный объем при одинаковых условиях, называют относительной плотностью одного газа по другому и обозначают буквой D.Слайд 30Найдите относительные молекулярные массы веществ, состав которых описывается формулами:
Рассчитайте относительные
молекулярные массы медного купороса
и кристаллической содыЗадания
Слайд 31Сколько молекул содержится в 32 г сернистого газа
?
Какова масса
молекул аммиака ?Какова масса 5,6 (н. у.) углекислого газа? Сколько молекул содержится в этом объеме газа?
Каков объем 128 г сернистого газа при нормальных условиях? Сколько молекул содержится в 128 г этого газа?
Найдите массу кислорода, содержащегося в баллоне объемом 50 л при температуре и давлении 790 кПа.