Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Серная кислота
Содержание
- 1. Серная кислота
- 2. АВТОРЫ РАБОТЫ: ученица 11а класса ГБОУ школы
- 3. Характеристика кислотыПолучениеХимические свойстваСолиПрименениеВЫВОДСерная кислота в природеС О Д Е Р Ж А Н И ЕФизические свойства
- 4. По основности: двухосновнаяПо наличию кислорода: кислородосодержащаяПо силе:
- 5. Агрегатное состояние – жидкостьТяжелая маслянистая жидкость ("купоросное
- 6. Все, что по серной кислоте узнал –Запомни
- 7. Химические свойства H2SO4С металлами (в ряду активности
- 8. ОСОБОЕ СВОЙСТВО КОНЦЕНТРИРОВАННОЙ СЕРНОЙ КИСЛОТЫ – ВЗАИМОДЕЙСТВИЕ
- 9. Автоцистерна для перевозки серной кислоты
- 10. Соли H2SO4Они могут быть как растворимыми, так
- 11. В природе встречается 180 минералов сульфатов, и
- 12. Сульфат кальцияСульфат барияВ Мексике не так давно
- 13. Применение H2SO41. В производстве минеральных удобрений2. Как
- 14. Промышленное получение H2SO4S SO2
- 15. Серная кислота в природеКислые озёра
- 16. Существуют предположения, что кислотное озеро возникло
- 17. Озеро шириной 500 м и глубиной 140
- 18. Серная кислота – очень активная жидкость, особенноконцентрированная,
- 19. Нет кислоты, которая была бы нужнее и
- 20. Ссылки на источники:1.http://www.sigmatec.ru/main/prod/sernaya_kislota/nature2. http://dobavkam.net/dobavki/e5133. Учебник для общеобразовательных учреждений – 9 класс, О.С.Габриелян4. Википедия (электронная энциклопедия)
- 21. Автоцистерна для перевозки http://www.avtomash.ru/pred/graz/ack5612.htm Цистерна на слайде
- 22. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Характеристика кислоты
Получение
Химические свойства
Соли
Применение
ВЫВОД
Серная кислота в природе
С О Д Е Р
Ж А Н И Е
Физические свойства
Слайд 4По основности: двухосновная
По наличию кислорода: кислородосодержащая
По силе: сильный электролит
Это тяжёлая
жидкость, которая в любом соотношении смешивается с водой, имеет молекулярную
решётку и ковалентную полярную связьH2SO4
Характеристика:
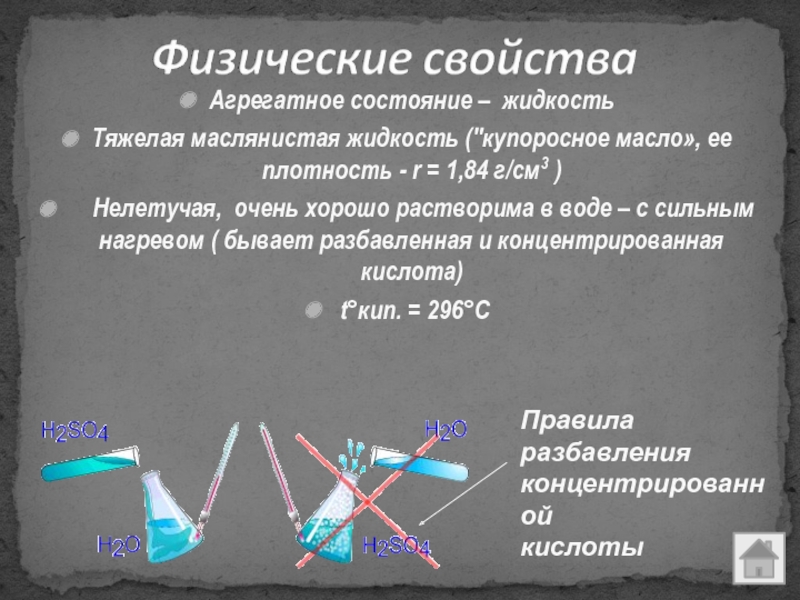
Слайд 5Агрегатное состояние – жидкость
Тяжелая маслянистая жидкость ("купоросное масло», ее плотность
- r = 1,84 г/см3 )
Нелетучая, очень хорошо
растворима в воде – с сильным нагревом ( бывает разбавленная и концентрированная кислота)t°кип. = 296°С
Правила
разбавления
концентрированной
кислоты
Слайд 6Все, что по серной кислоте узнал –
Запомни – это важно,
Чтоб пользоваться ей
Было бы тебе не страшно!
Если вдруг захочешь
кислоту ты растворить,Надо правило важное повторить:
Слайд 7Химические свойства H2SO4
С металлами (в ряду активности металлов до водорода):
H2SO4+Zn=ZnSO4
+ H2
2. С оксидами металлов:
H2SO4+K2O=K2SO4+H2O
3. С гидроксидами металлов:
H2SO4+2NaOH=Na2SO4+2H2O
4. С солями:
H2SO4+MgCO3=MgSO4+H2O+CO2
Слайд 8ОСОБОЕ СВОЙСТВО КОНЦЕНТРИРОВАННОЙ
СЕРНОЙ КИСЛОТЫ –
ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
При взаимодействии концентрированной
серной кислоты с металлами до водорода возможно образование газа-сероводорода или
серы.Концентрированная серная кислота при нагревании может взаимодействовать с металлами, расположенными в ряду напряжений металлов правее водорода.
При этом продуктом реакции является сернистый газ:
Cu + H2SO4 ----CuSO4 + SO2 + H2O
Zn + H2SO4 ---ZnSO4 + S + H2O
В этих реакциях серная кислота проявляет окислительные свойства, так как сера понижает свою степень окисления.
Слайд 10Соли H2SO4
Они могут быть как растворимыми, так и нерастворимыми
Химические свойства
сульфатов:
1. С металлами (прибавляемый металл должен быть активнее металла в
соли):CuSO4+Fe=FeSO4+Cu
2. С щелочами:
FeSO4+2NaOH=Na2SO4+Fe(OH)2
3. С другими солями:
К2SO4+BaСl2=2КСl+BaSO4
Сульфаты (SO4) – средние соли
Гидросульфаты (НSO4) – кислые соли
Слайд 11В природе встречается 180 минералов сульфатов, и на их долю
приходится ~0,5 % массы земной коры.
Их даже много и в
морской воде, особенно в лагунах по берегам морей. Много сульфатов и в горячих водных растворах, просачивающихся из глубин Земли.
Слайд 12Сульфат кальция
Сульфат бария
В Мексике не так давно обнаружили пещеру
с 15-метровыми кристаллами гипса!
2Н2О)
(CaSO4
Слайд 13Применение H2SO4
1. В производстве минеральных удобрений
2. Как электролит в свинцовых
аккумуляторах
3. Для получения различных минеральных кислот и солей
4. В нефтяной,
металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности5. В пищевой промышленности (пищевая добавка Е513)
Слайд 16
Существуют предположения, что кислотное озеро возникло сравнительно недавно в результате
извержения, произошедшего незаметно для людей.
Тот, кто сумел достичь его
подножия, просто обязан подняться на кромку кратера. Зрелище, которое открывается глазам, незабываемо: двухсотметровый провал кратера, дымящееся зеленое озеро, буйство красок на внутренних стенках.
В ясную ветреную погоду можно спуститься в кратер.
Это обитель «подземных духов»
Это одно из чудес камчатской природы
Слайд 17Озеро шириной 500 м и глубиной
140 м состоит из
прогретого до 40 градусов раствора серной и соляной кислот средней
концентрацииСлайд 18Серная кислота –
очень активная жидкость, особенно
концентрированная,
которая реагирует со
многими
неорганическими веществами,
также она легко действует на
органические соединения:
обугливает
бумагу,сахар, древесину, т.е. соединения,
которые содержат в себе углерод.
Хранят ее в стеклянной таре,
а перевозят в стальных цистернах
ВЫВОД
Слайд 19Нет кислоты, которая была бы нужнее и применялась бы чаще,
чем серная.
Главным образом, ее применяют в качестве полуфабриката; многочисленные
предприятия по производству серной кислоты перерабатывают ее далее в различных процессах.
Не случайно, перспективные планы развития химической промышленности каждой страны предусматривают увеличение производства серной кислоты и числа требующихся для этого многочисленных установок.
Слайд 20Ссылки на источники:
1.http://www.sigmatec.ru/main/prod/sernaya_kislota/nature
2. http://dobavkam.net/dobavki/e513
3. Учебник для общеобразовательных учреждений – 9
класс, О.С.Габриелян
4. Википедия (электронная энциклопедия)
Слайд 21Автоцистерна для перевозки
http://www.avtomash.ru/pred/graz/ack5612.htm
Цистерна на слайде 2: http://www.othodov.ru/kislota.php
Серная
кислота в стеклянной банке http://www.hayinfo.ru/ru/news/policy/87948.html
Формула серной кислоты http://www.million-deals.ru/sell/product-details/sernaja-kislota-10349.html
Серная кислота на последнем слайде
http://sc.karelia.ru/catalog/rubr/8f5d7210-86a6-11da-a72b-0800200c9a66/20882/?&sort=
Озеро на Камчатке: http://fotki.yandex.ru/search/%D0%BE%D0%B7%D0%B5%D1%80%D0%BE%20%D1%81%20%D1%81%D0%B5%D1%80%D0%BD%D0%BE%D0%B9%20%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%BE%D0%B9/users/kiril70/view/95617?page=0&how=week&type=image
Производство серной кислотыhttp://www.newchemistry.ru/fold.php?cat_id=24&cat_parent=&page=1
Ссылки на рисунки:
http://razdelpricepi.biz-market.ru/number8089363.html
Минералы сульфаты
http://pptcloud.ru/fotografii/khimija/Mineraly/024-Fosfaty.html
http://commons.wikimedia.org/wiki/Category:Chalcanthite?uselang=ru
Применение серной кислоты
http://him.1september.ru/articlef.php?ID=200601801