Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Первоначальные химические понятия
Содержание
- 1. Первоначальные химические понятия
- 2. обобщить первоначальные химические понятия; уметь составлять химические
- 3. Конкурс №1 «Разминка»Что изучает наука химия?Что называется
- 4. Конкурс №2 «Отгадай ребус»Команда №1.
- 5. Конкурс №3 «Определи явление»Определить тип явления, выписать букву, соответствующую правильному ответу.Команда 1 I команда
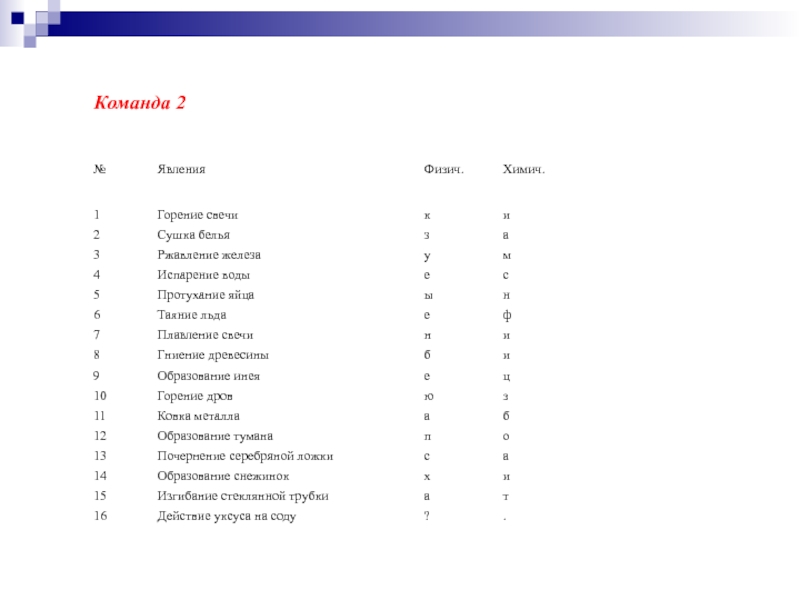
- 6. Команда 2
- 7. ФизкультминуткаH2ONO2CuOCaSO4H2CO3H3PO4H2SO4Mn(OH)2HNO3HNO2NaClHClHBrKNO3Fe2O3H2SiO3Ca3(PO4)2
- 8. Конкурс №4«Признаки химических явлений»Прочитайте отрывок из книги.
- 9. Конкурс №5 «Химик-эрудит»1-ая команда, «Знаешь ли
- 10. Конкурс №5 «Химик-эрудит»Команда 1Задание №2
- 11. Физкультминутка Правил безопасности много есть друзьяМы расскажем
- 12. Химик же, наоборот,Вот как поступаетКислоты чуть-чуть прильет
- 13. Конкурс №6 «Практический»Чтобы Золушка не смогла поехать
- 14. Конкурс №7 «Решение задач»1)Вычислите массовые доли элементов
- 15. Конкурс №8 «Кто он?»Задание: по описанию важнейших
- 16. Конкурс «Кто он?»Это был гениальный учёный, теория
- 17. РефлексияЧемодан, мясорубка, корзинаЧемодан – всё, что пригодится в дальнейшемМясорубка – информацию переработаюКорзина – все выброшу
- 18. Спасибо за урок!
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Подготовила учитель химии
Алимова Э.Н.
МОУ «Вольновская школа»
Республика Крым, П.Вольное
2015 г.
Внеклассное мероприятие
по теме «Первоначальные химические понятия»
Слайд 2обобщить первоначальные химические понятия; уметь составлять химические формулы, проводить расчеты
по формулам веществ, проводить опыты по разделению смесей, умения использования
химической посуды и оборудования. Уметь работать в коллективе и самостоятельно, выделять главное, сравнивать, делать выводы.Цели:
Слайд 3Конкурс №1 «Разминка»
Что изучает наука химия?
Что называется веществом?
Что называется атомом?
Что
такое молекула?
Какие вещества называются сложными?
Что называется формулой?
Что обозначает индекс и
коэффициент?Как вычисляют относительную молекулярную массу?
Как рассчитать массовую долю элемента в соединении?
Озвучьте закон сохранения массы веществ.
Слайд 4Конкурс №2 «Отгадай ребус»
Команда №1
. Mg
B Fe
K C Pt (молекула)1 2 3,4 1 1 2,3
Li S H Hg Ca Fe Cu (Лавуазье)
1 4 1 3 2 5 4, 2
Команда №2
As V C Na He (явление)
5 1 3, 4 1, 5 2
Li Sn Cu Os Na Sn S Os W ) по первым буквам.
Слайд 5Конкурс №3 «Определи явление»
Определить тип явления, выписать букву, соответствующую правильному
ответу.
Команда 1
I команда
Слайд 7Физкультминутка
H2O
NO2
CuO
CaSO4
H2CO3
H3PO4
H2SO4
Mn(OH)2
HNO3
HNO2
NaCl
HCl
HBr
KNO3
Fe2O3
H2SiO3
Ca3(PO4)2
Слайд 8Конкурс №4«Признаки химических явлений»
Прочитайте отрывок из книги. Подчеркните упоминание химической
реакции. Выпишите признак этой реакции.
« - Я пробью тебя шпагой,
как барана! – закричал купец и схватился за свою шпагу. Но шпага так отсырела на морском воздухе, что покрылась ржавчиной и ни за что не хотела вылезать из ножен». Ф.Рабле «Гаргантюа и Пантагрюэль».«Доктор Окс… попросту разлагал слегка подкисленную воду с помощью изобретенной им батареи… Электрический ток проходил через большие чаны, наполненные водой, которая разлагалась на водород и кислород». Ж.Верн. «Опыт доктора Окса».
Слайд 9Конкурс №5 «Химик-эрудит»
1-ая команда, «Знаешь ли ты валентность?»
Задание №1 а)
Составьте формулы сложных веществ образованных элементом кислородом и следующими элементами: Mn(VII); Cr(VI); Si(IV); P(V); Al(III); Mg; Hg(I).б) Обозначьте римскими цифрами валентность элементов в соединениях с хлором, зная, что в данных соединениях он одновалентен:
KCl; CaCl2; FeCl3; PCl5; ZnCl2; CrCl3; SiCl4.
2-ая команда, «Знаешь ли ты валентность?».
Задание №1 а) Составьте формулы сложных веществ, образованных элементом кислородом и следующими элементами: Сl(VII); S(VI); As(V); Pb(IV); B(III); Zn; Cu(I).
б) Обозначьте римскими цифрами валентность элементов в соединениях с серой, зная, что в данных соединениях она двухвалентна:
Al2S3; Na2S; MgS; CS2; Ag2S; ZnS; H2S.
Слайд 10Конкурс №5 «Химик-эрудит»
Команда 1
Задание №2
“Учись уравнивать.»
Расставьте коэффициенты в уравнениях химических реакций, укажите типы
химических реакции.a) P+O2P2O5; б) NaNO3 → NaNO2 + O2
в) Al+CuCl2AlCl3+Cu. г) H2SO4 + KOH = K2SO4 + H2O
Команда 2
a) Fe+Cl2FeCl3; б) Zn+HCl→ZnCl2+H2
в) CH4C+H2. г) CuSO4+NaOH→NaSO4+Cu(OH)2
Слайд 11Физкультминутка
Правил безопасности много есть друзья
Мы расскажем главные –
Ведь
без них нельзя!
Опыт можно проводить только с разрешенья
Так как могут
не проститьВаши прегрешенья. (Наклоны головой вперед и назад)
К носу совершай рукой
Легкие движенья
Вот тогда нюхач такой
Просто загляденье! (Движения кистями рук поочередно к носу)
Чтоб разбавить кислоту
Лил в нее водицу?
Плохо! Видно за версту –
Это не годится! (Круговые движения рук в локтевом суставе)
Слайд 12Химик же, наоборот,
Вот как поступает
Кислоты чуть-чуть прильет
В воду и
мешает. (Сжимания и разжимания кистей рук в кулак)
К пламени нельзя
никакНизко наклоняться,
Только, скажем так, чудак
Станет обжигаться. (Наклоны туловища вперед)
Из-под крана воду пить –
Все - равно, что «Ваниш».
Жажду можно утолить,
Но козленком станешь! (Поднимания и опускания на цыпочках).
Навсегда запомните:
Правила важны,
Зная их, вы с химией
Будете дружны! (Повороты туловища влево, вправо, руки на поясе).
Слайд 13Конкурс №6 «Практический»
Чтобы Золушка не смогла поехать на бал, мачеха
придумала ей работу: она смешала древесные стружки с мелкими железными
гвоздями, сахар и речным песком и велела Золушке очистить сахар, а гвозди сложить в отдельную коробку. Золушка быстро справилась с заданием и успела поехать на бал. Объясните , как можно быстро справиться с заданием мачехи.Слайд 14Конкурс №7 «Решение задач»
1)Вычислите массовые доли элементов Н3РО4, H2CO3
2) Определите
простейшую формулу соединения, содержащим по данным анализа, 40% меди, 20%
серы и 40% кислорода.Определите простейшую формулу соединения, содержащим по данным анализа, 24,7% калия, 35% марганца, 41% кислорода.
Слайд 15Конкурс №8 «Кто он?»
Задание: по описанию важнейших событий жизни и
деятельности учёного назвать его имя. За правильный ответ после первой
подсказки – 15 баллов, после второй – 10 баллов, после третьей – 5 баллов.Он – гордость русской науки – воплотил в себе народный гений, широту и силу русского характера. На все века он оставил своей Родине пример того, как наука может и должна служить народу.
Подсказка 1. Его исследования известны в области химии, физики, математики, астрономии, это был учёный – энциклопедист.
Подсказка 2. Он был первым физико-химиком, создал первую химическую лабораторию и первый университет. «Он, лучше сказать, сам был первым нашим университетом»(А.С.Пушкин)
Подсказка 3. Этот учёный сформулировал в своих трудах основные положения атомно – молекулярного учения
Слайд 16Конкурс «Кто он?»
Это был гениальный учёный, теория и практика всегда
неразрывно сочетались в его деятельности. Он был страстным патриотом и
смелым защитником прогрессивных идей.Подсказка 1. Этот учёный был избран почётным членом различных российских учебных заведений и научных обществ, многих иностранных академий наук.
Подсказка 2. Известны его труды по физике, минералогии, метеорологии, экономике. Исследования свойств растворов привели учёного к выводу о химической природе процессов растворения
Подсказка 3. Этот учёный смог объединить разрозненные химические знания в определённую систему и смог найти свойство, объединяющее все химические элементы.