Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Серная кислота
Содержание
- 1. Серная кислота
- 2. Цель урокаИзучить химические свойства и стадии получения серной кислоты
- 3. Химические свойства С основаниями (реакция нейтрализации) H2SO4
- 4. Химические свойства С металлами (стоящие в ряду
- 5. Химические свойства С солями BaCl2
- 6. Концентрированная серная кислотаCu + 2H2SO4 -> CuSO4 + SO2 + 2H2O
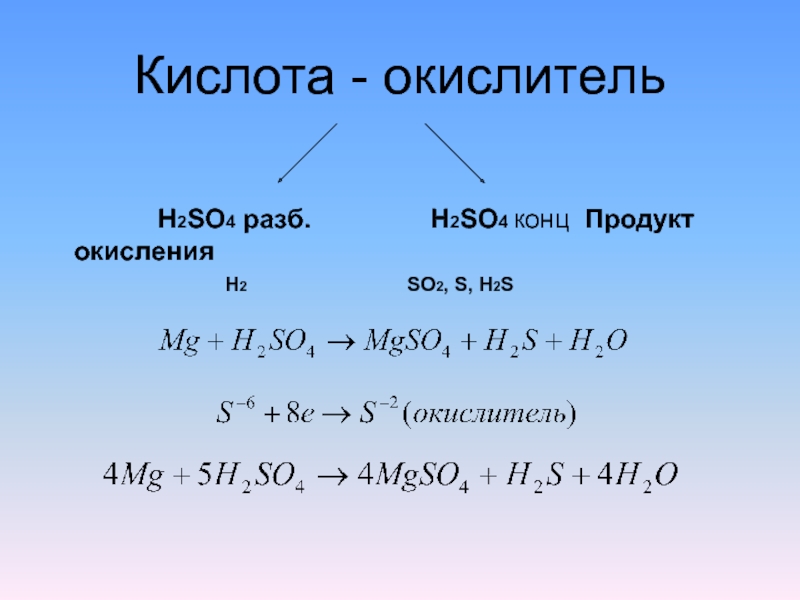
- 7. Кислота - окислитель H2SO4 разб.
- 8. Производство серной кислотыI стадия – получение сернистого газа SO2Получение из пирита
- 9. Производство серной кислотыII стадия – получение SO32-я стадия
- 10. Производство серной кислотыIII стадия – получение H2SO43-я стадия
- 11. Выводы Серная кислота может являться реагентом для
- 12. Проверь себяВариант I
- 13. УРОК ОКОНЧЕН
- 14. Скачать презентанцию
Цель урокаИзучить химические свойства и стадии получения серной кислоты
Слайды и текст этой презентации
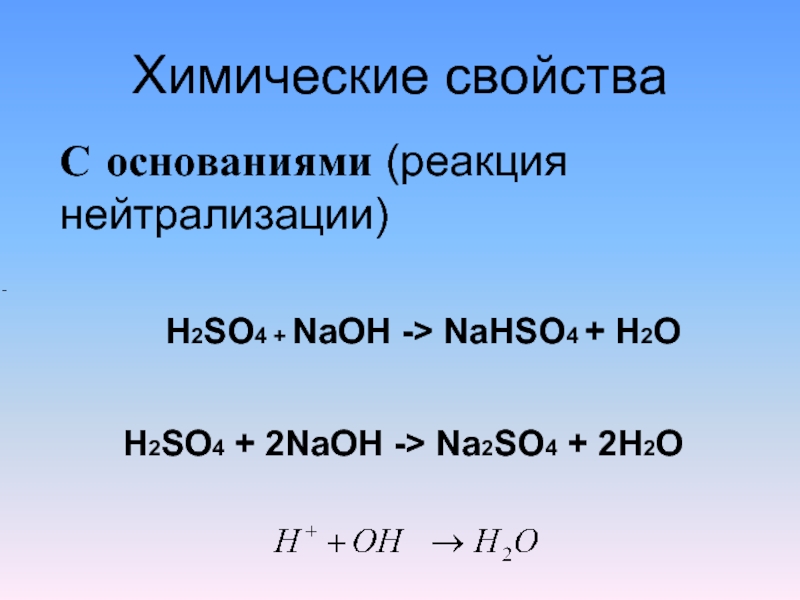
Слайд 3Химические свойства
С основаниями (реакция нейтрализации)
H2SO4 + NaOH ->
NaHSO4 + H2O
H2SO4 + 2NaOH -> Na2SO4 + 2H2O
Слайд 4Химические свойства
С металлами (стоящие в ряду напряжения до водорода)
Zn + H2SO4 -> ZnSO4 + H2
Слайд 5Химические свойства
С солями
BaCl2 + H2SO4 ->
BaSO4 + 2HCl
Хлорид бария является качественным реактивом на H2SO4
Слайд 11Выводы
Серная кислота может являться реагентом для получения водорода
Серная кислота
является сильным окислителем
Серная кислота взаимодействует не только с металлами стоящие
в ряду напряжений до водорода, но и со стоящими после него.Хлорид бария может являться качественным реагентом на сульфат-анион
Производство серной кислоты является сложным многостадийным химическим процессом
Теги