Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Признаки химических реакций
Содержание
- 1. Признаки химических реакций
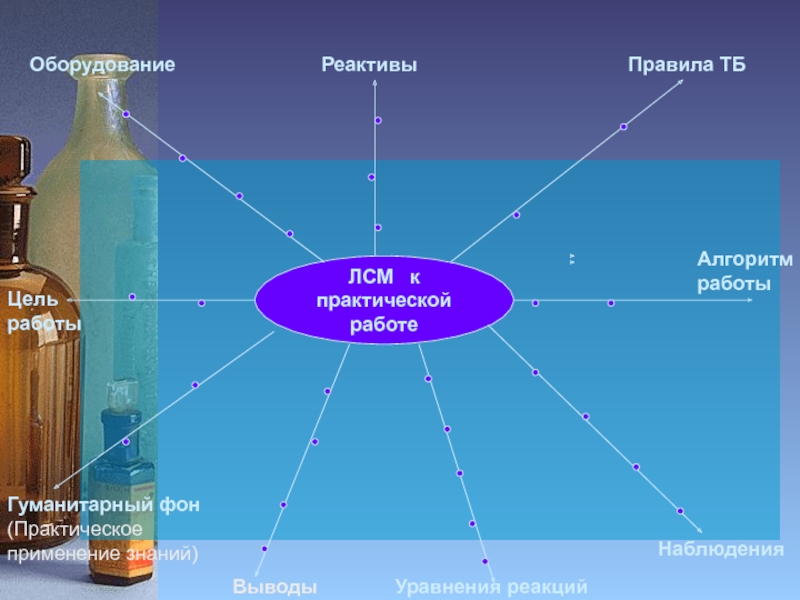
- 2. ЛСМ к практической работеЦель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение знаний)Уравнения реакцийНаблюденияВыводыАлгоритмработы
- 3. Инструкция к практической работе №1Цель работыОборудованиеРеактивыПравила ТБГуманитарный
- 4. Практическая работа №1Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение
- 5. Практическая работа №2Получение водорода и определение его свойств
- 6. Инструкция кпрактической работе №2Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое
- 7. Практическая работа №2Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение
- 8. Практическая работа №3Получение и свойствакислорода
- 9. Инструкция к практической работе №3Цель работыОборудованиеРеактивыПравила ТБГуманитарный
- 10. Практическая работа №3Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение
- 11. Практическая работа №4Условия протекания химических реакций
- 12. Инструкция к практической работе №4Цель работыОборудованиеРеактивыПравила ТБГуманитарный
- 13. Практическая работа №4Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение
- 14. Практическая работа №5Свойства кислот, оснований, оксидов
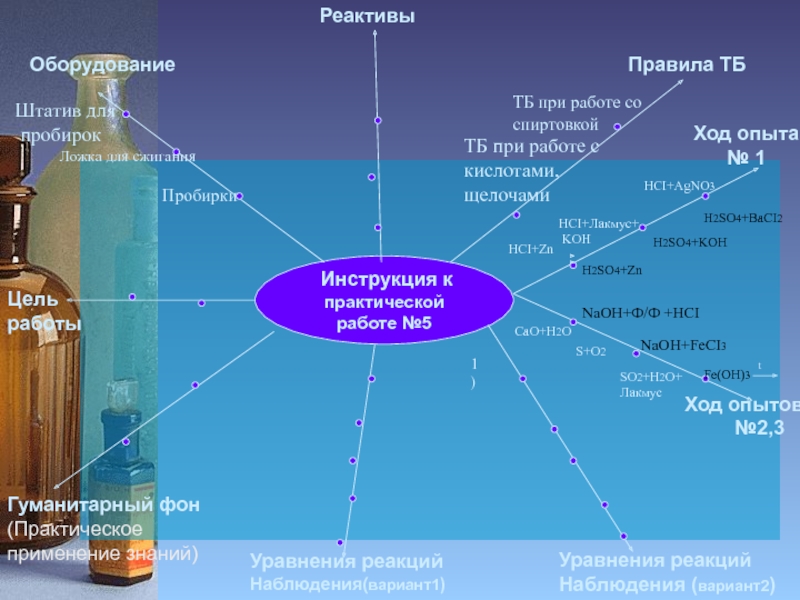
- 15. Инструкция к практической работе №5Цель работыОборудованиеРеактивыПравила
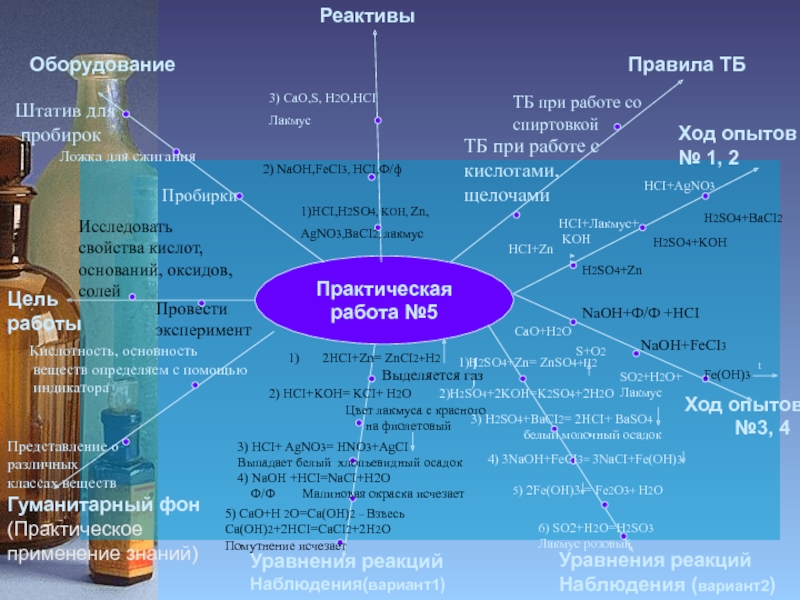
- 16. Практическая работа №5Цель работыОборудованиеРеактивыПравила ТБГуманитарный фон(Практическое применение
- 17. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2ЛСМ к
практической работе
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения
реакций
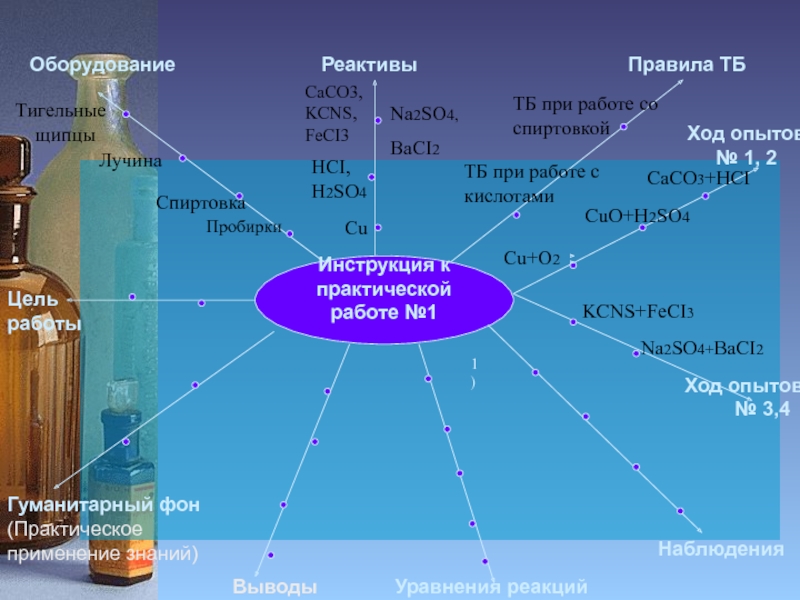
Слайд 3Инструкция к
практической работе №1
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения
реакций
Наблюдения
Ход опытов № 1, 2
Пробирки
Спиртовка
Лучина
Тигельные
щипцы
Cu
HCI,
H2SO4
CaCO3,
KCNS,
FeCI3
Na2SO4,
BaCI2
ТБ при работе со спиртовкой
ТБ при работе с
кислотами
Выводы
Ход опытов
№ 3,4
Cu+O2
CaCO3+HCI
CuO+H2SO4
KCNS+FeCI3
Na2SO4+BaCI2
1)
Слайд 4Практическая работа №1
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения
Ход опытов
№ 1, 2
Исследовать признаки
химических реакций
Пробирки
Спиртовка
Провести
экспериментЛучина
Тигельные
щипцы
Cu
HCI,
H2SO4
CaCO3,
KCNS,
FeCI3
Na2SO4,
BaCI2
ТБ при работе со спиртовкой
ТБ при работе с
кислотами
Выводы
Ход опытов
№3, 4
Cu+O2
CaCO3+HCI
CuO+H2SO4
KCNS+FeCI3
Na2SO4+BaCI2
1)
1)Проволока чернеет, при t образуется голубой раствор
2) Выделяется газ,
лучина тухнет
3)Образуется красно-бурый раствор
4)Выпадает белый
осадок
2Cu+O2=2CuO соединение
CuO+H2SO4=CuSO4+H2O
обмен
CaCO3+2HCI=CaCI2+CO2 +H2O
обмен
3KCNS+FeCI3=3KCI+Fe(CNS)3
обмен
Na2SO4+BaCI2=2NaCI+BaSO4
Изменение цвета
Выделение
газа
Выпадение осадка
Наблюдали признаки
химических реакций
1)CO2 –газ, не поддерживает
горение
2) О химическом явлении можно судить по признакам реакции
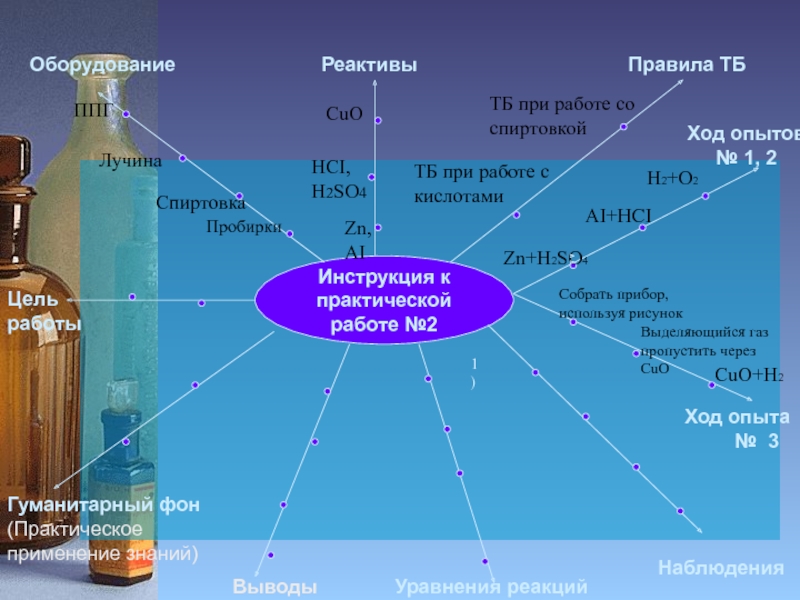
Слайд 6Инструкция к
практической работе №2
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения
Ход
опытов № 1, 2
Пробирки
Спиртовка
Лучина
ППГ
Zn, АI
HCI,
H2SO4
CuO
ТБ
при работе со спиртовкойТБ при работе с
кислотами
Выводы
Ход опыта
№ 3
Zn+H2SO4
H2+O2
AI+HCI
Собрать прибор,
используя рисунок
Выделяющийся газ пропустить через CuO
1)
CuO+H2
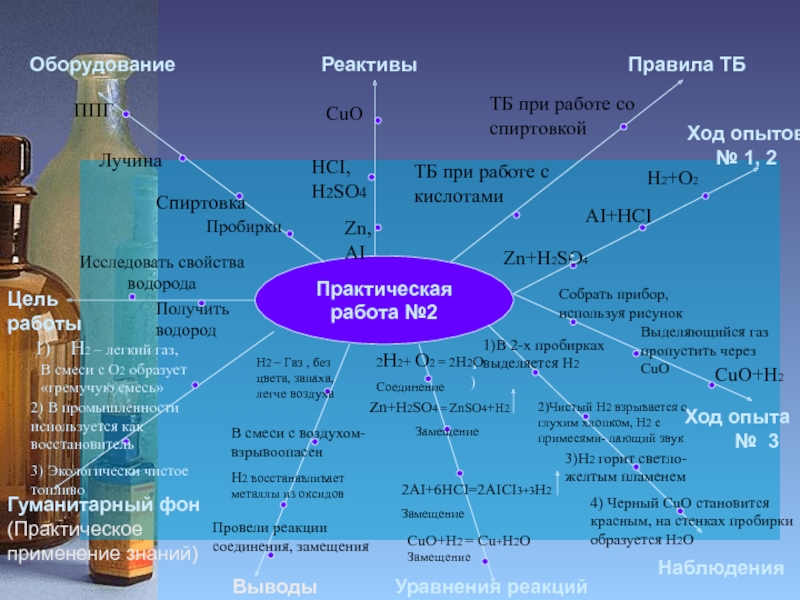
Слайд 7Практическая работа №2
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения
Ход опытов
№ 1, 2
Исследовать свойства
водорода
Пробирки
Спиртовка
Получить водород
Лучина
ППГ
Zn,
АIHCI,
H2SO4
CuO
ТБ при работе со спиртовкой
ТБ при работе с
кислотами
Выводы
Ход опыта
№ 3
Zn+H2SO4
H2+O2
AI+HCI
Собрать прибор,
используя рисунок
Выделяющийся газ пропустить через CuO
1)
1)В 2-х пробирках выделяется Н2
2)Чистый Н2 взрывается с глухим хлопком, Н2 с примесями- лающий звук
3)Н2 горит светло-желтым пламенем
4) Черный CuO становится
красным, на стенках пробирки
образуется H2O
Zn+H2SO4 = ZnSO4+H2
Замещение
CuO+H2 = Cu+H2O
Замещение
2AI+6HCI=2AICI3+3H2
Замещение
Н2 – Газ , без цвета, запаха,
легче воздуха
В смеси с воздухом-
взрывоопасен
Н2 восстанавливает металлы из оксидов
Провели реакции соединения, замещения
H2 – легкий газ,
В смеси с О2 образует
«гремучую смесь»
2) В промышленности используется как восстановитель
3) Экологически чистое топливо
CuO+H2
2H2+ O2 = 2H2O
Соединение
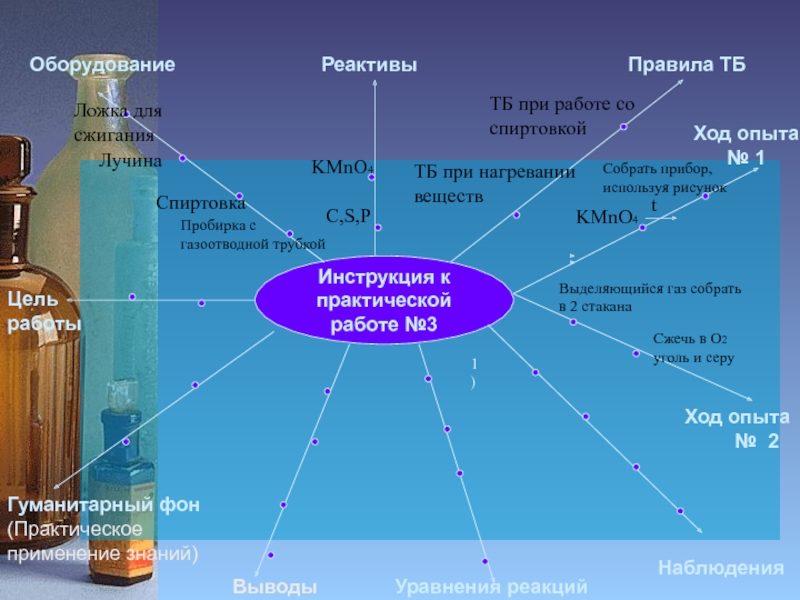
Слайд 9Инструкция к
практической работе №3
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения
реакций
Наблюдения
Ход опыта №
1Пробирка с
газоотводной трубкой
Спиртовка
Лучина
Ложка для сжигания
C,S,P
KMnO4
ТБ при работе со спиртовкой
ТБ при нагревании
веществ
Выводы
Ход опыта
№ 2
Собрать прибор,
используя рисунок
Выделяющийся газ собрать в 2 стакана
1)
KMnO4
t
Сжечь в О2
уголь и серу
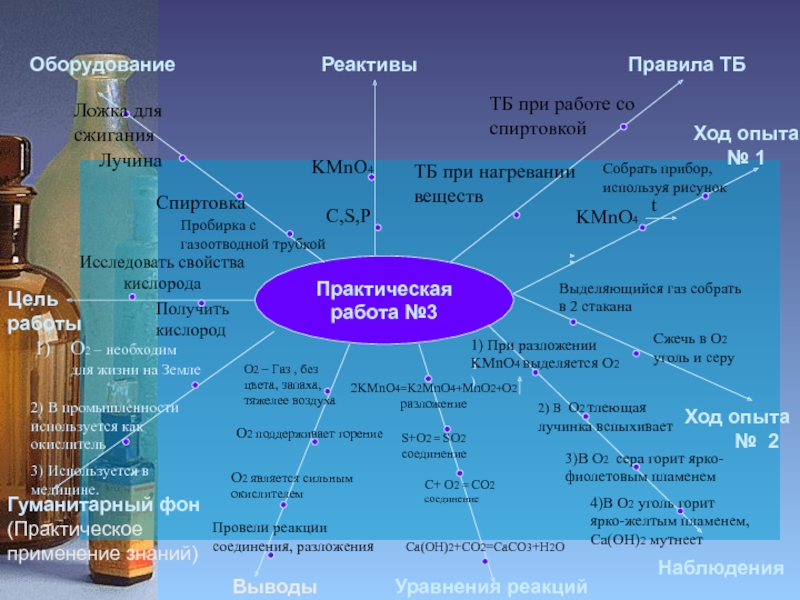
Слайд 10Практическая работа №3
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения
Ход опыта
№ 1
Исследовать свойства
кислорода
Пробирка с
газоотводной трубкой
Спиртовка
Получить кислород
Лучина
Ложка для сжигания
C,S,P
KMnO4
ТБ при работе со спиртовкой
ТБ при нагревании
веществ
Выводы
Ход опыта
№ 2
Собрать прибор,
используя рисунок
Выделяющийся газ собрать в 2 стакана
1)
1) При разложении KMnO4 выделяется O2
2) В O2 тлеющая лучинка вспыхивает
3)В О2 сера горит ярко-фиолетовым пламенем
4)В О2 уголь горит
ярко-желтым пламенем,
Ca(OH)2 мутнеет
O2 – Газ , без цвета, запаха, тяжелее воздуха
О2 поддерживает горение
О2 является сильным окислителем
Провели реакции соединения, разложения
О2 – необходим для жизни на Земле
2) В промышленности используется как окислитель
3) Используется в медицине.
KMnO4
t
Сжечь в О2
уголь и серу
2KMnO4=K2MnO4+MnO2+O2 разложение
S+O2 = SO2
соединение
С+ O2 = CO2
соединение
Сa(OH)2+CO2=CaCO3+H2O
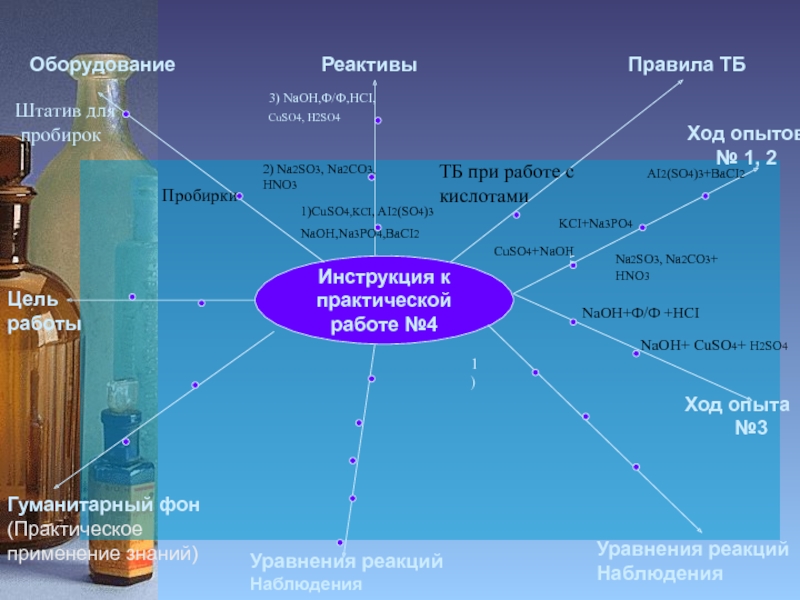
Слайд 12Инструкция к
практической работе №4
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения
реакций
Наблюдения
Уравнения реакций
Наблюдения
Ход опытов № 1,
2Пробирки
Штатив для
пробирок
1)CuSO4,KCI, AI2(SO4)3
NaOH,Na3PO4,BaCI2
2) Na2SO3, Na2CO3,
HNO3
ТБ при работе с кислотами
Ход опыта
№3
AI2(SO4)3+BaCI2
KCI+Na3PO4
NaOH+Ф/Ф +HCI
NaOH+ CuSO4+ H2SO4
1)
3) NaOH,Ф/Ф,HCI,
CuSO4, H2SO4
CuSO4+NaOH
Na2SO3, Na2CO3+
HNO3
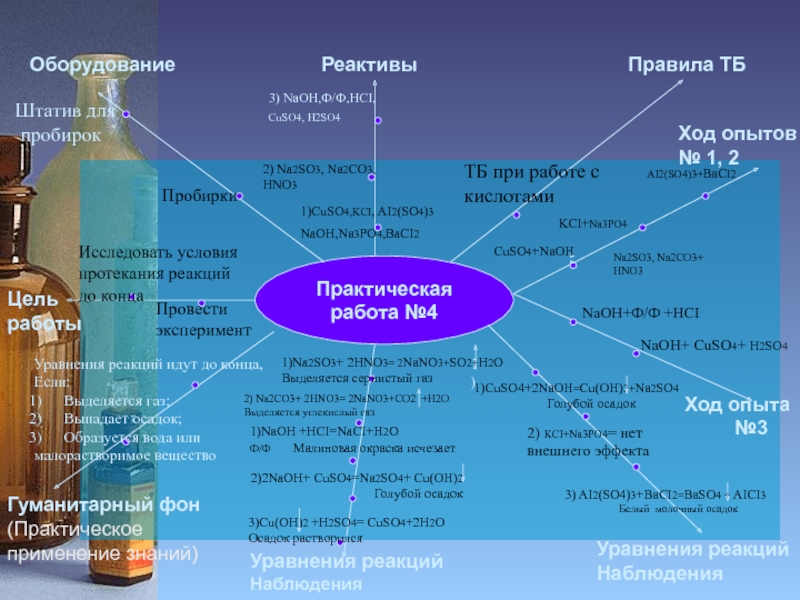
Слайд 13Практическая работа №4
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения
Уравнения реакций
Наблюдения
Ход
опытов № 1, 2
Исследовать условия
протекания
реакций до конца
Пробирки
Провести эксперимент
Штатив для
пробирок
1)CuSO4,KCI, AI2(SO4)3
NaOH,Na3PO4,BaCI2
2) Na2SO3, Na2CO3,
HNO3
ТБ при работе с
кислотами
Ход опыта
№3
AI2(SO4)3+BaCI2
KCI+Na3PO4
NaOH+Ф/Ф +HCI
NaOH+ CuSO4+ H2SO4
1)
1)CuSO4+2NaOH=Cu(OH)2+Na2SO4 Голубой осадок
2) KCI+Na3PO4= нет внешнего эффекта
3) AI2(SO4)3+BaCI2=BaSO4 + AICI3
Белый молочный осадок
2) Na2СO3+ 2HNO3= 2NaNO3+СO2 +H2O Выделяется углекислый газ
3) NaOH,Ф/Ф,HCI,
CuSO4, H2SO4
CuSO4+NaOH
Na2SO3, Na2CO3+
HNO3
1)Na2SO3+ 2HNO3= 2NaNO3+SO2+H2O Выделяется сернистый газ
1)NaOH +HCI=NaCI+H2O Ф/Ф Малиновая окраска исчезает
2)2NaOH+ CuSO4=Na2SO4+ Cu(OH)2
Голубой осадок
3)Cu(OH)2 +H2SO4= CuSO4+2H2O
Осадок растворился
Уравнения реакций идут до конца,
Если:
Выделяется газ;
Выпадает осадок;
Образуется вода или
малорастворимое вещество
Слайд 15 Инструкция к
практической работе №5
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение
знаний)
Уравнения реакций
Наблюдения(вариант1)
Уравнения реакций
Наблюдения (вариант2)
Ход опыта
№ 1Пробирки
Штатив для
пробирок
ТБ при работе со спиртовкой
ТБ при работе с
кислотами,
щелочами
Ход опытов
№2,3
HCI+AgNO3
HCI+Лакмус+
KOH
NaOH+Ф/Ф +HCI
NaOH+FeCI3
1)
Ложка для сжигания
HCI+Zn
H2SO4+Zn
H2SO4+KOH
H2SO4+BaCI2
Fe(OH)3
t
CaO+H2O
S+O2
SO2+H2O+
Лакмус
Слайд 16Практическая работа №5
Цель работы
Оборудование
Реактивы
Правила ТБ
Гуманитарный фон
(Практическое применение знаний)
Уравнения реакций
Наблюдения(вариант1)
Уравнения реакций
Наблюдения
(вариант2)
Ход опытов № 1, 2
Исследовать
свойства кислот, оснований, оксидов, солейПробирки
Провести эксперимент
Штатив для
пробирок
1)HCI,H2SO4, KOH, Zn,
AgNO3,BaCI2, лакмус
2) NaOH,FeCI3, HCI,Ф/ф
ТБ при работе со спиртовкой
ТБ при работе с
кислотами,
щелочами
Ход опытов
№3, 4
HCI+AgNO3
HCI+Лакмус+
KOH
NaOH+Ф/Ф +HCI
NaOH+FeCI3
1)
3) CaO,S, H2O,HCI
Лакмус
Ложка для сжигания
HCI+Zn
H2SO4+Zn
H2SO4+KOH
H2SO4+BaCI2
Fe(OH)3
t
CaO+H2O
S+O2
SO2+H2O+
Лакмус
2HCI+Zn= ZnCI2+H2
Выделяется газ
2) HCI+KOH= KCI+ H2O
Цвет лакмуса с красного
на фиолетовый
3) HCI+ AgNO3= HNO3+AgCI
Выпадает белый хлопьевидный осадок
4) NaOH +HCI=NaCI+H2O
Ф/Ф Малиновая окраска исчезает
5) CaO+H 2O=Ca(OH)2 – Взвесь
Ca(OH)2+2HCI=CaCI2+2H2O
Помутнение исчезает
1)H2SO4+Zn= ZnSO4+H2
2)H2SO4+2KOH=K2SO4+2H2O
3) H2SO4+BaCI2= 2HCI+ BaSO4
белый молочный осадок
4) 3NaOH+FeCI3= 3NaCI+Fe(OH)3
5) 2Fe(OH)3 = Fe2O3+ H2O
6) SO2+H2O=H2SO3
Лакмус розовый
Кислотность, основность
веществ определяем с помощью
индикатора
Представление о различных классах веществ