Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соединения серы.
Содержание
- 1. Соединения серы.
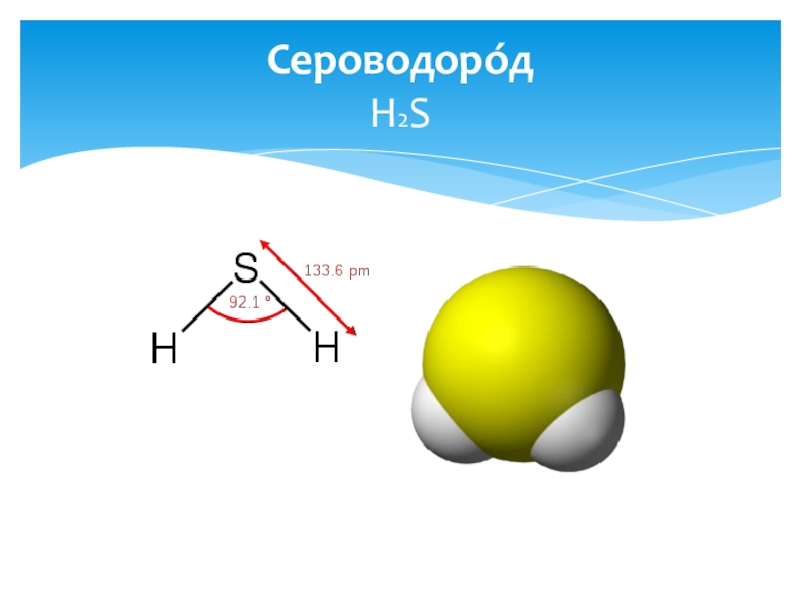
- 2. Сероводоро́д Н2S
- 3. Физические свойства: бесцветный газ, плохо растворим в
- 4. Бесцветный газБесцветный газ с неприятным запахом (тухлого
- 5. Термически неустойчив (при температурах больше
- 6. В воде сероводород мало растворим, водный раствор
- 7. СульфидыСоли сероводородной кислоты называют сульфидами. В
- 8. Сероводород из-за своей токсичности находит ограниченное применение.В
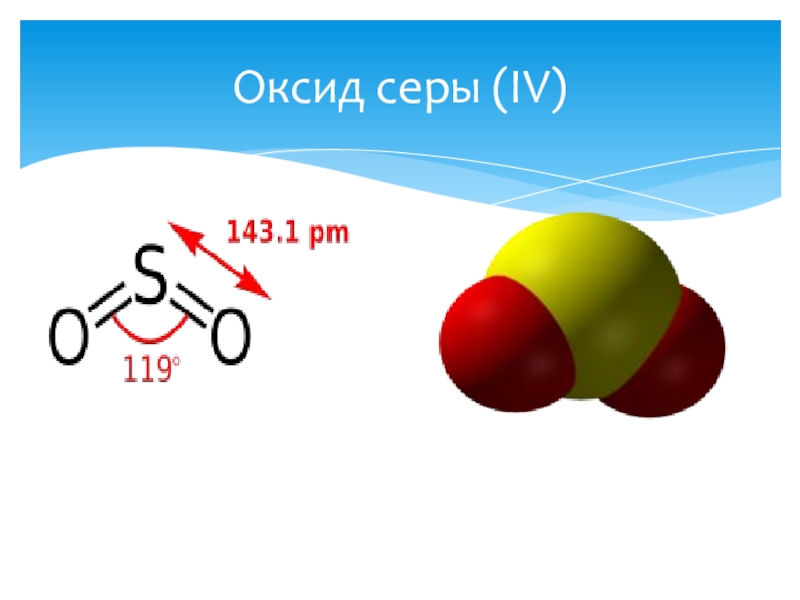
- 9. Оксид серы (IV)
- 10. Общие свойстваСистематическое наименование Оксид серы(IV) Химическая формула
- 11. Относится к кислотным оксидам. Растворяется в воде
- 12. Данная реакция является качественной реакцией на сульфит-ион
- 13. Неустойчивая двухосновная кислотаНеустойчивая двухосновная кислота средней силы,
- 14. Кислота средней силы:H2SO3 H+ + HSO3-, KI
- 15. Сернистая кислота и её соли применяют как
- 16. Оксид серы (VI)
- 17. Общие свойстваСистематическое наименование Оксид серы(VI)Химическая формула SO3Отн.
- 18. Окси́д се́ры(VI) (се́рный ангидри́д, трео́кись се́ры, се́рный
- 19. При переходе в жидкое и кристаллическое
- 20. Получают, окисляя оксид серы(IV)Получают, окисляя оксид серы(IV)
- 21. 1. Кислотно-основные: SO3 — типичный кислотный оксид
- 22. 2. Окислительно-восстановительные: SO3 характеризуется сильными окислительными свойствами,
- 23. Серная кислота Н2 SO4
- 24. Общие свойстваСистематическое наименование серная кислотаХимическая формула H2SO4Отн.
- 25. Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая
- 26. Серная кислота - сильная двухосновная кислота, диссоциация
- 27. Серная кислота проявляет все свойства сильных кислот:а)
- 28. Железо, алюминий, хром концентрированной серной кислотой пассивируются,
- 29. Серная кислота как двухосновная кислота образует два
- 30. В производстве минеральных удобрений; как электролит в
- 31. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Физические свойства: бесцветный газ, плохо растворим в воде. Плотность 5392г/л г/см³,температура
плавления -82.30 °C
Слайд 4Бесцветный газБесцветный газ с неприятным запахом (тухлого яйца) и сладковатым
вкусом. Плохо растворим в воде, хорошо — в этаноле. При
больших концентрациях разъедает металл. Взрывчатая смесь с воздухом 4,5 - 45%.В природе встречается очень редко в виде смешанных веществ нефти и газа. Имеет очень неприятный запах, вреден для лёгких и всего организма. Сейчас сероводород используют в лечебных целях, например, в сероводородных ваннах
Сероводоро́д,
сернистый водород Н2S
Слайд 5 Термически неустойчив (при температурах больше 400 °C разлагается на
простые вещества Термически неустойчив (при температурах больше 400 °C разлагается
на простые вещества — S Термически неустойчив (при температурах больше 400 °C разлагается на простые вещества — S и H2), ядовитый (вдыхание воздуха с его примесью вызывает головокружение, головную боль, тошноту, а со значительным содержанием приводит к коме, судорогам, отёку лёгких и даже к летальному исходу), газ, тяжелее воздуха с неприятным запахом тухлых яиц.Молекула Молекула сероводорода имеет угловую форму, поэтому она полярна (μ = 0,34·10-29 Кл·м). В отличие от молекул воды, молекулы сероводорода не образуют прочных водородных связей, поэтому H2S — газ. Насыщенный водныйS — газ. Насыщенный водный растворS — газ. Насыщенный водный раствор (сероводородная вода) H2S является очень слабой сероводородной кислотой.
Сероводоро́д Н2S
Физические свойства
Слайд 6В воде сероводород мало растворим, водный раствор H2S является очень
слабой кислотой:
H2S → HS− + H+
Ka = 6.9×10−7 моль/л;
pKa = 6.89. С основаниями реагирует:
H2S + 2NaOH = Na2S + 2H2O (обычная соль, при избытке NaOH)
H2S + NaOH = NaHS + H2O (кислая соль, при отношении 1:1)
Сероводород — сильный восстановитель. На воздухе он горит синим пламенем:
2H2S + ЗО2 = 2Н2О + 2SO2
при недостатке кислорода:
2H2S + O2 = 2S + 2H2O
(на этой реакции основан промышленный способ получения серы).
Сероводород реагирует также со многими другими окислителями, при его окислении в растворах образуется свободная сера или SO42-, например:
3H2S + 4HClO3 = 3H2SO4 + 4HCl
2H2S + SO2 = 2Н2О + 3S
H2S + I2 = 2HI + S
Сероводоро́д Н2S
Химические свойства
Слайд 7 Сульфиды
Соли сероводородной кислоты называют сульфидами. В воде хорошо растворимы
только сульфиды щелочных металлов, бария и аммония. Сульфиды остальных металлов
практически не растворимы в воде, они выпадают в осадок при введении в растворы солей металлов раствора сульфида аммония (NH4)2S. Многие сульфиды ярко окрашены.Для щелочных и щелочноземельных металлов известны также гидросульфиды M+HS и M2+(HS)². Гидросульфиды Са²+ и Sr2+ очень нестойки. Являясь солями слабой кислоты, растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих металлы в высоких степенях окисления (Al2S3, Cr2S3 и др.) часто проходит необратимо.
Многие природные сульфиды в виде минералов являются ценными рудами (пиритМногие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопиритМногие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопирит, киноварь).
Получение
Взаимодействие разбавленных кислот на сульфиды:
Взаимодействие сульфида алюминияВзаимодействие сульфида алюминия с водой (эта реакция отличается чистотой полученного сероводорода):
Сероводоро́д Н2S
Химические свойства
Слайд 8Сероводород из-за своей токсичности находит ограниченное применение.
В аналитической химииВ аналитической
химии сероводород и сероводородная водаВ аналитической химии сероводород и сероводородная
вода используются как реагенты для осаждения тяжёлых металловВ аналитической химии сероводород и сероводородная вода используются как реагенты для осаждения тяжёлых металлов, сульфиды которых очень слабо растворимыВ медицине — в составе природных и искусственных сероводородных ванн, а также в составе некоторых минеральных вод
Сероводород применяют для получения серной кислоты, элементной серы, сульфидов
Используют в органическом синтезеИспользуют в органическом синтезе для получения тиофенаИспользуют в органическом синтезе для получения тиофена и меркаптанов
В последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моряВ последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моря, в качестве энергетического (сероводородная энергетика) и химического сырья.
Применеие сероводорода Н2S
Слайд 10Общие свойства
Систематическое наименование Оксид серы(IV)
Химическая формула SO2
Относительная молекулярная массаОтносительная
молекулярная масса 64.054 а. е. м.
Молярная массаМолярная масса 64.054 г/моль
Физические свойства
Состояние (норм. условия )бесцветный газ,
Плотность 2,927 г/л (г/см³)Термические свойства
Температура плавления−75,5 °C
Температура кипения−10,01 °C
Химические свойства
Растворимость в воде11,5 г/100 мл
Классификация Рег. номер CAS[7446-09-5]
Оксид серы (IV)
Слайд 11Относится к кислотным оксидам. Растворяется в воде с образованием сернистой
кислоты (при обычных условиях реакция обратима):
SO2 + H2O ↔ H2SO3.
Со
щелочами образует сульфиты:SO2 + 2NaOH → Na2SO3 + H2O.
Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается:
SO2 + Br2 + 2H2O → H2SO4 + 2HBr,
2SO2 + O2 → 2SO3 (требуется катализатор V2O5 и температура 450°С),
Химические свойства
оксида серы (IV)
Слайд 12Данная реакция является качественной реакцией на сульфит-ион SO32- и на
SO2 (обесцвечивание фиолетового раствора).
5SO2 + 2KMnO4 + 2H2O → 2H2SO4
+ 2MnSO4 + K2SO4.В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства. Например, для извлечения серы их отходящих газов металлургической промышленности используют восстановление SO2 оксидом углерода(II):
SO2 + 2CO → 2CO2 + S↓.
Или для получения фосфорноватистой кислоты:
PH3 + SO2 → H(PH2O2) + S↓
Химические свойства
оксида серы (IV)
Слайд 13Неустойчивая двухосновная кислотаНеустойчивая двухосновная кислота средней силы, существует лишь в
разбавленных водных растворах (в свободном состоянии не выделена):
SO2 + H2O
⇆ H2SO3 ⇆ H+ + HSO3- ⇆ 2H+ + SO32-.Сернистая кислота
H2SO3
Слайд 14Кислота средней силы:
H2SO3 H+ + HSO3-, KI = 2·10-2
HSO3- H+ + SO32-, KII = 6·10-8
Растворы H2SO3
всегда имеют резкий специфический запах (похожий на запах зажигающейся спичкивсегда имеют резкий специфический запах (похожий на запах зажигающейся спички), обусловленный наличием химически не связанного водой SO2.Двухосновная кислотаДвухосновная кислота, образует два ряда солей: кислые — гидросульфитыДвухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи):
и средние — сульфитыи средние — сульфиты (в избытке щёлочи):
Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями:
При взаимодействии с ещё более сильными восстановителями может играть роль окислителя:
Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:
Химические свойства
Сернистой кислоты H2SO3
Слайд 15Сернистая кислота и её соли применяют как восстановители, для беления
шерстиСернистая кислота и её соли применяют как восстановители, для беления
шерсти, шелкаСернистая кислота и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора).Сернистую кислоту применяют при консервировании плодов и овощей.
Гидросульфит кальция Са(HSO3)2 (сульфитный щелок) используют для переработки древесины в так называемую сульфитную целлюлозуГидросульфит кальция Са(HSO3)2 (сульфитный щелок) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнинГидросульфит кальция Са(HSO3)2 (сульфитный щелок) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги).
Применение
Сернистой кислоты H2SO3
Слайд 17Общие свойства
Систематическое наименование Оксид серы(VI)
Химическая формула SO3
Отн. молек. МассаОтн. молек.
Масса 80.06 а. е. м.
Молярная массаМолярная масса 80.06 г/моль
Физические свойства
СостояниеСостояние (ст. усл.) бесцветный газ
Плотность1.92 г/см³
Термические
свойстваТемпература плавления16,9 °C
Температура кипения45 °C
Энтальпия образованияЭнтальпия образования (ст. усл.)−397.77 кДж/моль Классификация Рег. номер CAS[7446-11-9]
Оксид серы (VI)
Слайд 18Окси́д се́ры(VI) (се́рный ангидри́д, трео́кись се́ры, се́рный га́з)
SO3 —
высший оксид серы,
тип химической связи: ковалентная полярная
В
обычных условиях легколетучая бесцветная жидкость с удушающим запахом. При температурах ниже 16,9 °C застывает с образованием смеси различных кристаллических модификаций твёрдого SO3.
Оксид серы (VI)
Физические свойства
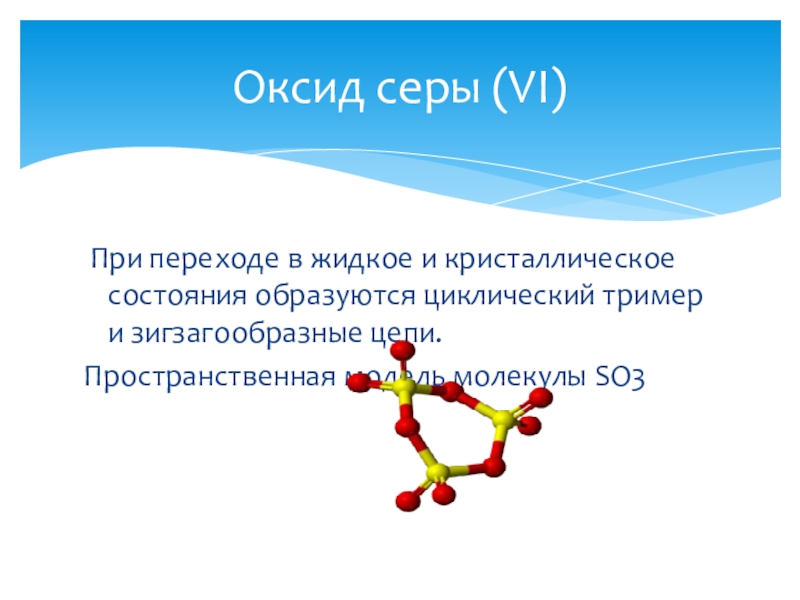
Слайд 19 При переходе в жидкое и кристаллическое состояния образуются циклический
тример и зигзагообразные цепи.
Пространственная модель молекулы SO3
Оксид серы (VI)
Слайд 20Получают, окисляя оксид серы(IV)Получают, окисляя оксид серы(IV) кислородомПолучают, окисляя оксид
серы(IV) кислородом воздуха при нагревании, в присутствии катализатораПолучают, окисляя оксид
серы(IV) кислородом воздуха при нагревании, в присутствии катализатора (V2O5, Pt, Pt или Na2VO3):2SO2 + O2 → 2SO3 + Q.
Можно получить термическим разложением сульфатов:
Fe2(SO4)3 → Fe2O3 + 3SO3,
или взаимодействием SO2 с озоном:
SO2 + O3 → SO3 + O2↑.
Для окисления SO2 используют также NO2:
SO2 + NO2 → SO3 + NO↑.
Эта реакция лежит в основе исторически первого, нитрозного способа получения серной кислоты.
Получение оксида серы (VI)
Слайд 211. Кислотно-основные: SO3 — типичный кислотный оксид — типичный кислотный
оксид, ангидрид — типичный кислотный оксид, ангидрид серной кислоты. Его
химическая активность достаточно велика.При взаимодействии с водой образует серную кислоту:
SO3 + H2OO → H2SO4.
Взаимодействует с основаниями:
2KOH + SO3 → K2SO4 + H2O,
основными оксидами:
CaO + SO3 → CaSO4,
c амфотерными оксидами:
3SO3 + Al2O3 → Al2(SO4)3.
SO3 растворяется в 100%-й серной кислоте, образуя олеум:
H2SO4 (100 %) + SO3 → H2S2O7.
Оксид серы (VI)
Химические свойства
Слайд 222. Окислительно-восстановительные: SO3 характеризуется сильными окислительными свойствами, восстанавливается, обычно, до
сернистого ангидрида:
5SO3 + 2P + 2P→ P2O5 + 5SO2
3SO3
+ H2SS → 4SO2 + H2O 2SO3 + 2KI + 2KI → SO2 + I2 + K2SO4.
3. При взаимодействии с хлороводородом образуется хлорсульфоновая кислота:
SO3 + HCl + HCl → HSO3Cl
Также присоединяет хлор, образуя тионилхлорид:
SO3 + Cl2 + 2SCl2 → 3SOCl2
Оксид серы (VI)
Химические свойства
Слайд 24Общие свойства
Систематическое наименование серная кислота
Химическая формула H2SO4
Отн. молек. МассаОтн. молек.
Масса 62.03 а. е. м.
Молярная массаМолярная масса98.078 г/моль
Физические свойства
СостояниеСостояние (ст. усл.)бесцветная маслянистая жидкость без запаха
Плотность1,8356 г/см³
Термические
свойстваТемпература плавления10,38 °C
Температура кипения279,6 °C
Химические свойства
Растворимость в водесмешивается во всех соотношениях г/100 мл
Классификация
Рег. номер CAS7664-93-
Серная кислота Н2 SO4
Слайд 25Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления
серы (+6).
При обычных условиях концентрированная серная кислота — тяжёлая маслянистая
жидкость При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3.
Если молярное отношение SO3:H2O < 1, то это водный раствор серной кислоты, если > 1, — раствор SO3 в серной кислоте (олеум).
Физические свойства
серной кислоты Н2 SO4
Слайд 26Серная кислота - сильная двухосновная кислота, диссоциация ее протекает по
двум ступеням:
H2SO4 = H+ + HSO4- - первая ступень
HSO4-
=H+ + SO42- - вторая ступеньВ концентрированных растворах диссоциация серной кислоты по второй ступени незначительна.
Серная кислота - сильнейшее дегидратирующее (водоотнимающее) вещество. Она поглощает влагу из воздуха (гигроскопична), отнимает воду
1. от кристаллогидратов:
CuSO4*5H2O голубой ------------------------> CuSO4 белый + 5H2O
2. углеводов (обугливает дерево и бумагу):
C12H22O11 --------------------------> 12C + 11H2O
3. спиртов:
C2H5OH -----------------------------> CH2=CH2 + H2O
В окислительно-восстановительных реакциях разбавленная серная кислота проявляет свойства обычной кислоты (неокислитель) - при этом восстанавливаются ионы Н+, например:
Fe + H2SO4 разб.= FeSO4 + H2
Разбавленная H2SO4 не взаимодействует с металлами, стоящими в ряду напряжений правее водорода.
Концентрированная серная кислота - кислота-окислитель, при этом восстанавливается сера (+6).
Она окисляет металлы, стоящие в ряду напряжений правее водорода:
Cu + 2H2SO4конц. = CuSO4 + SO2 + 2H2O
Химические свойства
серной кислоты Н2 SO4
Слайд 27Серная кислота проявляет все свойства сильных кислот:
а) взаимодействует с основными
оксидами:
CuO + H2SO4 = CuSO4 + H2O
б) с основаниями:
2NaOH +
H2SO4= Na2SO4 + 2H2Oв) вытесняет другие кислоты из их солей, например те, которые слабее нее:
CaCO3 + H2SO4 = CaSO4 + CO2 + H2O
или более летучие (обладающие температурами кипения ниже, чем у серной кислоты):
NaNO3твердый + H2SO4 конц.= NaHSO4 + HNO3- при нагревании
и металлы,стоящие левее водорода, при этом сера восстанавливается до степени окисления +4, 0 и -2:
Zn + 2H2SO4 = ZnSO4 + SO2 + 2H2O
3Zn + 4H2SO4 = 3ZnSO4 + S + 4H2O
4Zn + 5H2SO4 = 4ZnSO4 + H2S + 4H2O
Химические свойства
серной кислоты Н2 SO4
Слайд 28Железо, алюминий, хром концентрированной серной кислотой пассивируются, однако при сильном
нагревании реакция начинается, например:
2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2
+ 6H2OКонцентрированная серная кислота окисляет неметаллы, например:
C + 2H2SO4 = CO2 + 2SO2 + 2H2O
S +2H2SO4 = 3SO2 + 2H2O
Концентрированная серная кислота окисляет также сложные вещества, например HI и HBr:
2HBr + H2SO4 = Br2 + SO2 + 2H2O
8HI + H2SO4 = 4I2 + H2S + 4H2O
соли железа (2):
2FeSO4 + 2H2SO4 = Fe2(SO4)3 + 2H2O + SO2
Химические свойства
серной кислоты Н2 SO4
Слайд 29Серная кислота как двухосновная кислота образует два ряда солей -
кислые - гидросульфаты и средние - сульфаты. В безводном состоянии
выделены только гидросульфаты щелочных металлов. Средние сульфаты (безводные) - как правило, бесцветные кристаллические вещества, склонные к образованию кристаллогидратов (часто окрашеных), например:Na2SO4*10H2O - глауберова соль (мирабилит) - бесцветная
MgSO4*7H2O - горькая (английская) соль - бесцветная
CuSO4*5H2O - медный купорос - голубой
FeSO4*7H2O - железный купорос - голубовато-зеленый
CaSO4*2H2O - гипс - белый
Сульфаты при нагревании разлагаются (кроме сульфатов щелочных металлов, которые термически устойчивы), например CaSO4 - при 1400oС:
2CaSO4 = 2CaO + 2SO2 + O2
Сульфаты переходных металлов разлагаются при более низких температурах, например Fe2(SO4)3 - при 700-800oС:
Fe2(SO4)3 = Fe2O3 + 3SO3
Соли серной кислоты
Слайд 30В производстве минеральных удобрений;
как электролит в свинцовых аккумуляторах;
для
получения различных минеральных кислот и солей;
в производстве химических волокон,
красителей, дымообразующих веществ и взрывчатых веществ; в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности;
в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513(эмульгатор);
в промышленном органическом синтезе в реакциях:
дегидратации (получение диэтилового эфира, сложных эфиров);
гидратации (этанолгидратации (этанол из этилена);
сульфирования (синтетические моющие средства и промежуточные продукты в производстве красителей);
алкилирования (получение изооктанаалкилирования (получение изооктана, полиэтиленгликоля, капролактама) и др.
Самый крупный потребитель серной кислоты — производство минеральных удобрений.
Применение серной кислоты