Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Степень окисления. Составление формул веществ 8 класс
Содержание
- 1. Степень окисления. Составление формул веществ 8 класс
- 2. Автор:Лобанова Ольга Васильевнаучитель химии Степень окисления. Составление
- 3. Степень окисления – это условный заряд атома,
- 4. Слайд 4
- 5. У свободных атомов и у простых веществ
- 6. Неметаллы могут иметьВысшую положительную С.О. = N
- 7. Ме, H, Si, As, P, Se,
- 8. ЭF- - фторидЭCl-_ хлоридЭBr- - бромидЭI- -
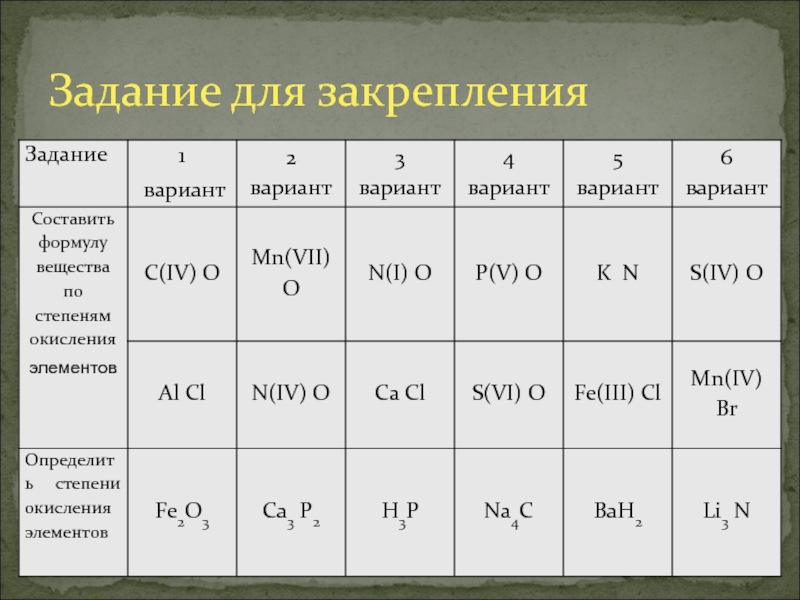
- 9. Задание для закрепления
- 10. ОтветыКритерии выставления отметки: Если выполнены правильно все
- 11. § 17 читать, повторить определения и правила.Задания
- 12. Учебник Химия.8 класс: учеб. для общеобразоват. учреждений
- 13. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Из атомов мир создавала природа
Два атома легких взяла водорода
Прибавила атом
один кислорода
H2OСлайд 2Автор:
Лобанова Ольга Васильевна
учитель химии
Степень окисления. Составление формул веществ.
Муниципальное бюджетное
общеобразовательное учреждение
города Иркутска средняя общеобразовательная школа № 57
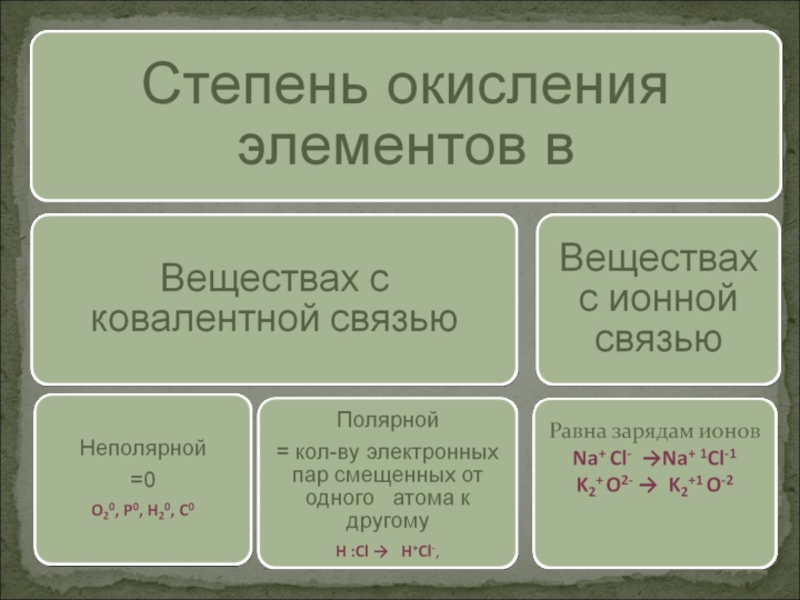
Слайд 3Степень окисления – это условный заряд атома, характеризующий число смещенных
электронов (электронных пар) от одного атома к другому в химических
соединениях.С.О.- величина постоянная и переменная.
Понятие о степени окисления
Слайд 5У свободных атомов и у простых веществ СТЕПЕНЬ ОКИСЛЕНИЯ равна
0
Металлы во всех соединениях имеют ПОЛОЖИТЕЛЬНУЮ С.О.
Металлы IА группы С.О.
+1Металлы IIА группы С.О. +2
Металлы IIIА группы С.О. +3
В соединениях кислород имеет С.О.-2
(кроме Н2О-12 , К2О-12, О+2F2 )
В соединениях с неметаллами у водорода С.О.+1, а с металлами С.О. -1
В соединениях фтор имеет С.О. -1
В соединениях сумма всех С.О. равна 0
Если степень окисления переменная – будет указано в скобках !
Правила определения степеней окисления
Слайд 6
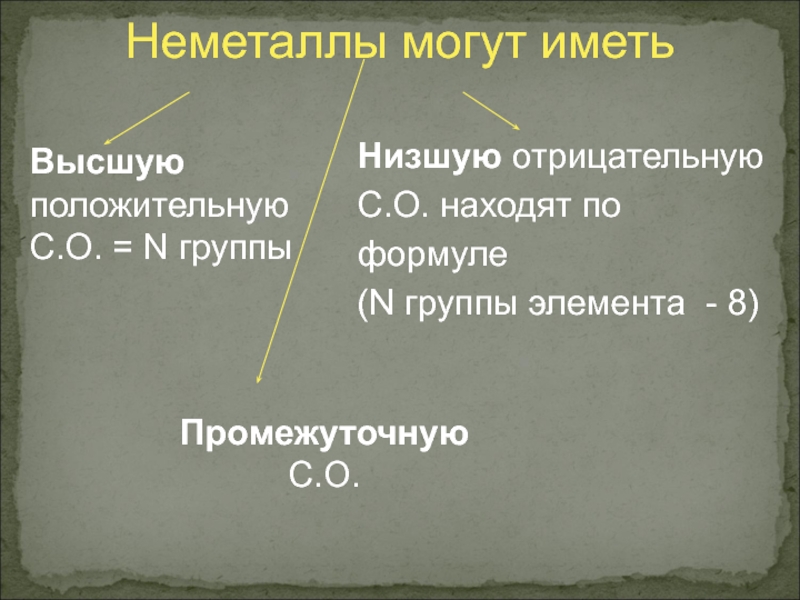
Неметаллы могут иметь
Высшую положительную С.О. = N группы
Низшую отрицательную
С.О. находят по формуле
(N группы элемента - 8)Промежуточную С.О.
Слайд 7 Ме, H, Si, As, P, Se, C, S, I,
Br, Cl, N, O, F
элемент стоящий в ряду правее
проявляет (-) С.О., а левее (+) С.О.На первом месте элемент высшая или переменная с.о.+, а на втором низшая отрицательная
Ряд электроотрицательности
Слайд 8ЭF- - фторид
ЭCl-_ хлорид
ЭBr- - бромид
ЭI- - иодид
ЭH- - гидрид
ЭS-2
-сульфид
ЭN-3 – нитрид
ЭC-4 –карбид
ЭSi-4 -силицид
Бинарные соединения
Слайд 10Ответы
Критерии выставления отметки:
Если выполнены правильно все 3 задания –
оценка «5»,
Если выполнено 2 задания– оценка «4»,
Если выполнено 1
задание – оценка «3». Слайд 11§ 17 читать, повторить определения и правила.
Задания по карточкам (по
желанию): 16 чел.
Остальные-
с.90 в.№ 1+сообщение «Применение бинарного соединения» на
выбор CaO, H2O, NH3, CO2 .Домашнее задание
Слайд 12Учебник Химия.8 класс: учеб. для общеобразоват. учреждений / О.С. Габриелян.
– 15-е изд., стереотип.- М.: Дрофа, 2012.- 270 с.;
Аликберова
Л.Ю. «Занимательная химия», М, «АСТ – Пресс», 2002г.; http://www.alhimik.ru/
Литература