Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводороды ароматического ряда
Содержание
- 1. Углеводороды ароматического ряда
- 2. Какие углеводороды называются ароматическими? Ароматические углеводороды
- 3. Виды ароматических углеводородов
- 4. Майкл Фарадей (1791 - 1867) Английский
- 5. Фридрих Август Кекуле 1829 - 1896
- 6. Строение молекулы бензола
- 7. Строение молекулы бензола
- 8. Модель молекулы бензола
- 9. Образование σ-связей в молекуле бензола
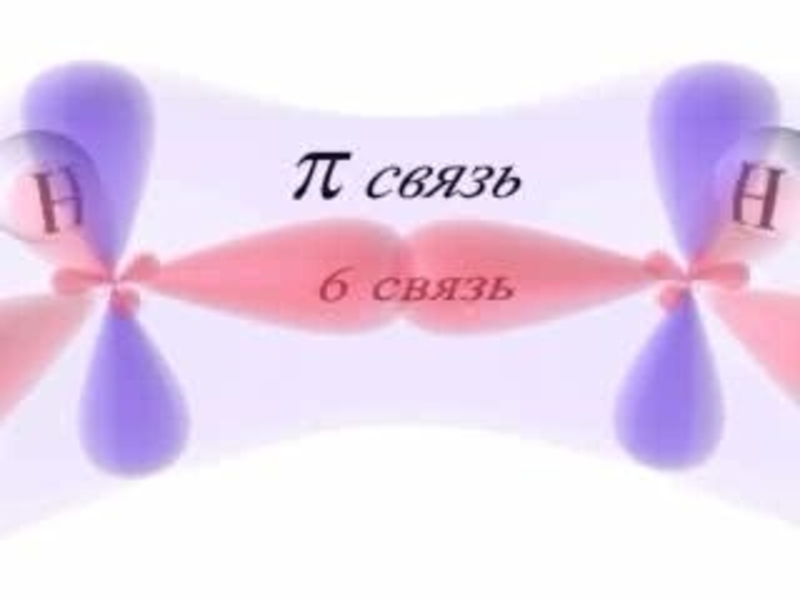
- 10. Образование π-системы в молекуле бензола
- 11. Слайд 11
- 12. Изомерия и номенклатура
- 13. Номенклатура аренов
- 14. Гомологи бензола
- 15. Способы получения аренов
- 16. Арены получают главным образом при
- 17. Дегидрирование циклоалканов
- 18. Дегидрирование циклоалканов
- 19. Циклоароматизация алканов
- 20. Тримеризация ацетилена
- 21. Николай Дмитриевич Зелинский 1861 – 1953 гг.
- 22. Алкилирование аренов
- 23. Физические свойства аренов В обычных
- 24. Слайд 24
- 25. Растворимость бензола
- 26. Слайд 26
- 27. Бензол как растворитель
- 28. Слайд 28
- 29. Химические свойства аренов
- 30. Общая характеристика реакционной способности аренов Для
- 31. Галогенирование аренов
- 32. Слайд 32
- 33. Нитрование бензола
- 34. Сульфирование аренов
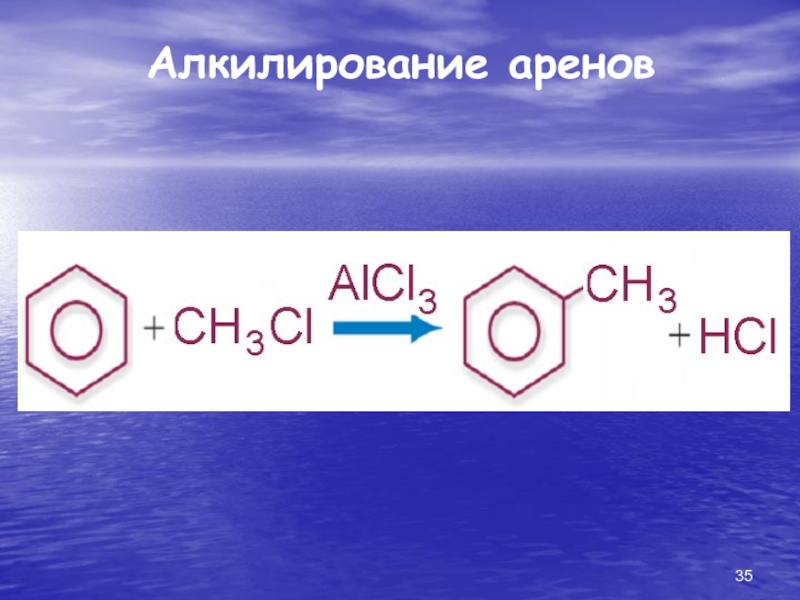
- 35. Алкилирование аренов
- 36. Правила ориентации в бензольном кольцеЗаместители I рода
- 37. Правила ориентации в бензольном кольцеЗаместители II рода
- 38. Гидрироване бензола
- 39. Хлорирование бензола
- 40. Реакции окисления
- 41. Слайд 41
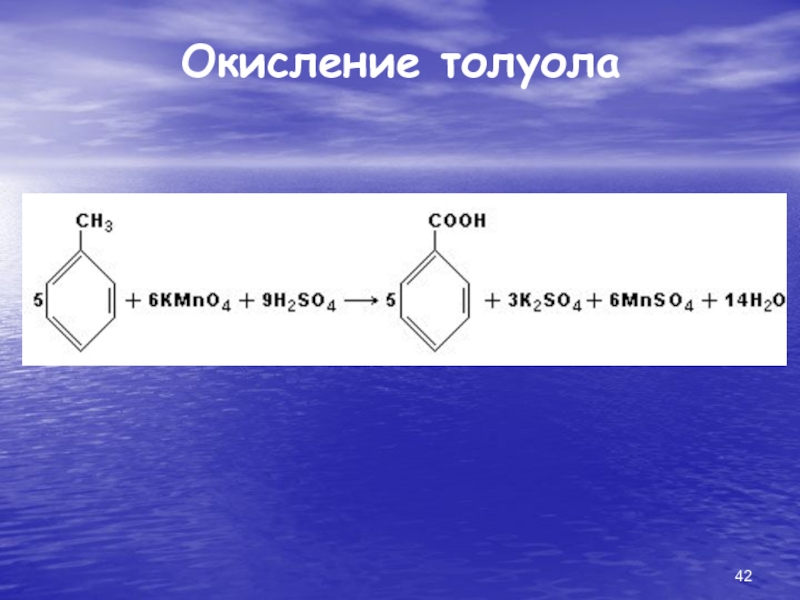
- 42. Окисление толуола
- 43. Слайд 43
- 44. Горение аренов
- 45. Применение аренов
- 46. Скачать презентанцию
Какие углеводороды называются ароматическими? Ароматические углеводороды (арены) – это углеводороды с общей формулой СnH2n-6, в молекулах которых имеется хотя бы одно бензольное кольцо.
Слайды и текст этой презентации
Слайд 4Майкл Фарадей
(1791 - 1867)
Английский физик и химик, член
Лондонского королевского общества. Один из основателей количественной электрохимии. В 1823
г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). В 1825 г. открыл бензол, изучил его физические и некоторые химические свойства. Положил начало исследованиям каучука. В 1833 - 1836 гг. установил количественные законы электролиза.Слайд 5Фридрих Август Кекуле
1829 - 1896
Немецкий химик-органик. Предложил структурную
формулу молекулы бензола. С целью проверки гипотезы о равноценности всех
шести атомов водорода в молекуле бензола получил его галоген-, нитро-, амино-, и карбоксипроизводные. Открыл перегруппировку диазоамино- в азоаминобензол, синтезировал трифенилметан и антрахинол.Слайд 16 Арены получают главным образом при сухой перегонке каменного
угля. При нагревании каменного угля в ретортах или коксовальных печах
без доступа воздуха при 1000 – 1300 0С происходит разложение органических веществ каменного угля с образованием твердых, жидких и газообразных продуктов.Альтернативным источником получения аренов служит древесина. В самой древесине аренов нет, однако при ее пиролизе они образуются и могут быть выделены.
В странах богатых нефтью арены получают при ее переработке. Нефтяные продукты нагревают при температуре 700 0С, в результате чего из продуктов разложения нефти удается получить 15-18% аренов.