Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку химии "Фенолы", 10 класс
Содержание
- 1. Презентация к уроку химии "Фенолы", 10 класс
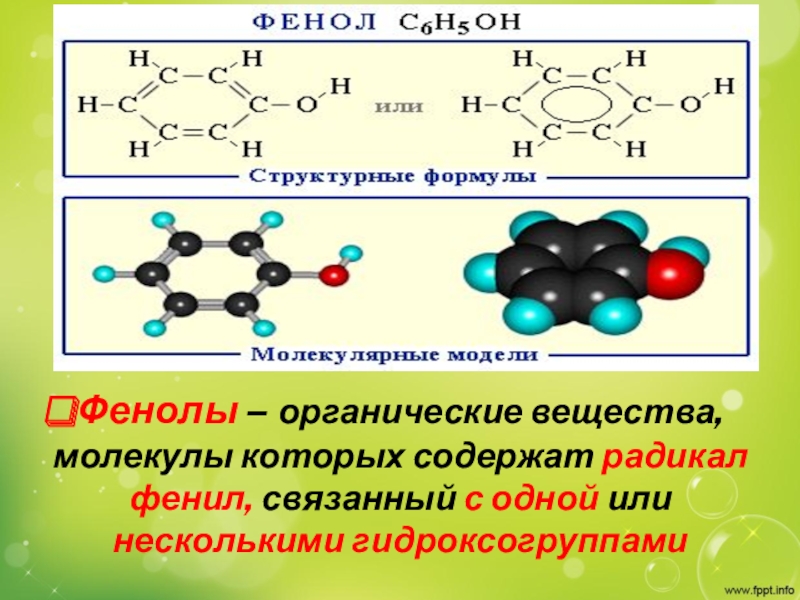
- 2. Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами
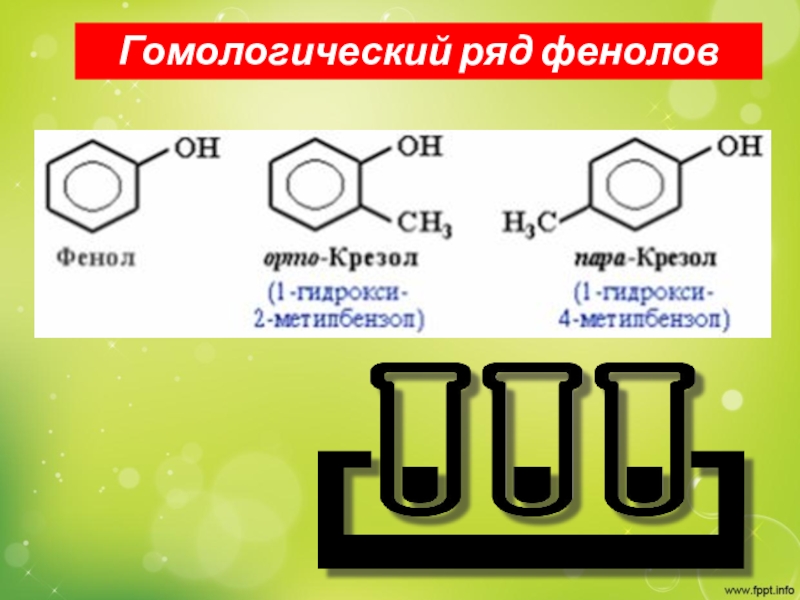
- 3. Гомологический ряд фенолов
- 4. Классификация феноловФенолы классифицируют по атомности, т.е. по
- 5. По количеству бензольных колец фенолы бывают моноядерные и многоядерныеНа план урокаКлассификация фенолов
- 6. НоменклатураПри составлении названия фенолов нумерация атомов углерода
- 7. Строение молекулы фенолаГидроксогруппа и бензольное кольцо оказывают
- 8. Строение молекулы фенолаОНδ-δ-δ-Гидроксильная группа влияет на бензольное
- 9. Физические свойства фенолаФенол - твёрдое бесцветное кристаллическое
- 10. Химические свойства фенолаХимические свойства фенола обусловлены наличием в его молекулегидроксильной группыбензольного ядра
- 11. Химические свойства, обусловленные наличием гидроксильной группы1. Диссоциация
- 12. 2.Взаимодействие с натриемФенол, как и спирты, взаимодействует
- 13. 3. Взаимодействие со щелочами Влияние
- 14. Карболовая кислота в
- 15. Химические свойства, обусловленные наличием бензольного ядра
- 16. 2. Реакции замещения. А. Галогенирование –
- 17. Б. Нитрование фенола Нитрование фенола
- 18. В результате полного нитрования фенола
- 19. 3. Реакции гидрирования При нагревании в
- 20. 4.Реакции поликонденсации с альдегидамиПоликонденсация фенола с альдегидами,
- 21. Качественные реакции на фенола) Бромирование фенола
- 22. ПОЛУЧЕНИЕКумольный способ получения фенола В настоящее время кумольный способ используется как основной в мировом производстве фенола.
- 23. ПОЛУЧЕНИЕ2). Из каменноугольной смолы (как побочный продукт – выход
- 24. ПОЛУЧЕНИЕ4). Сплавлением солей ароматических сульфокислот с твёрдыми щелочами:
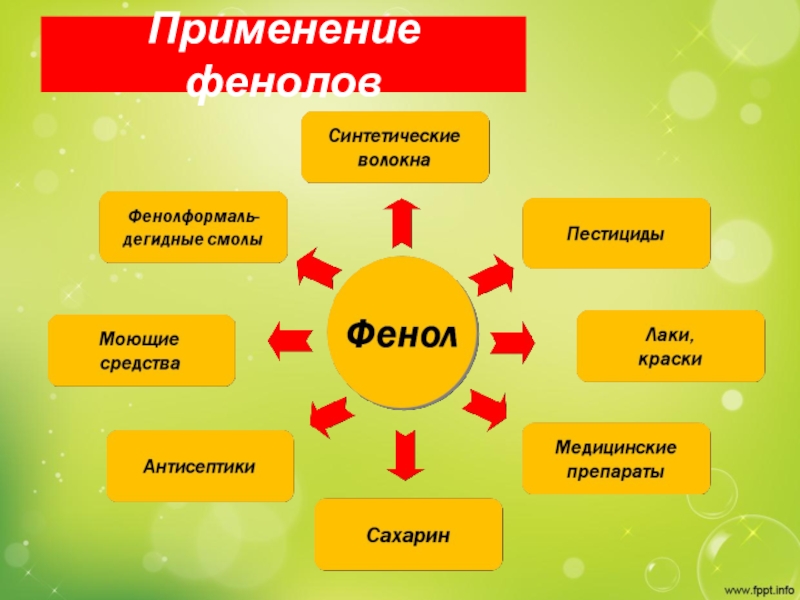
- 25. Применение фенолов
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный
с одной или несколькими гидроксогруппами
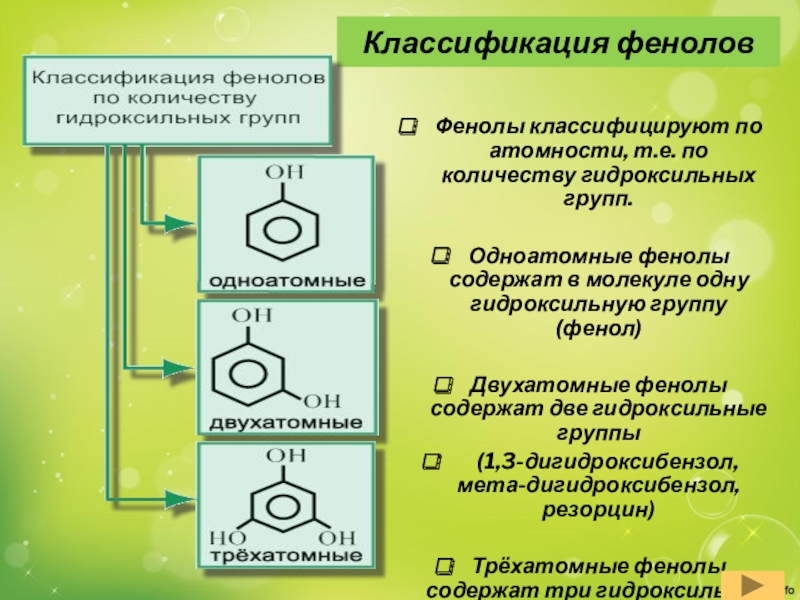
Слайд 4Классификация фенолов
Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп.
Одноатомные фенолы содержат в молекуле одну гидроксильную группу (фенол)
Двухатомные фенолы
содержат две гидроксильные группы (1,3-дигидроксибензол, мета-дигидроксибензол, резорцин)
Трёхатомные фенолы содержат три гидроксильные группы
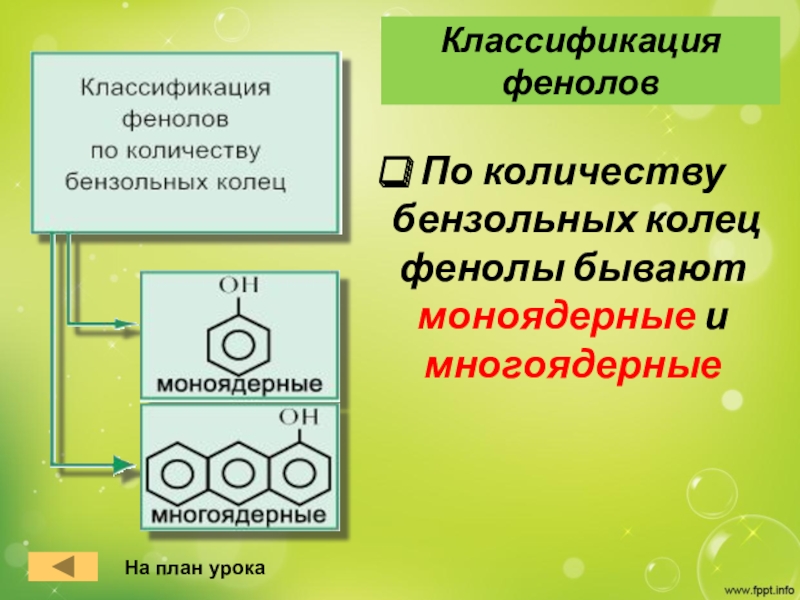
Слайд 5По количеству бензольных колец фенолы бывают моноядерные и многоядерные
На план
урока
Классификация фенолов
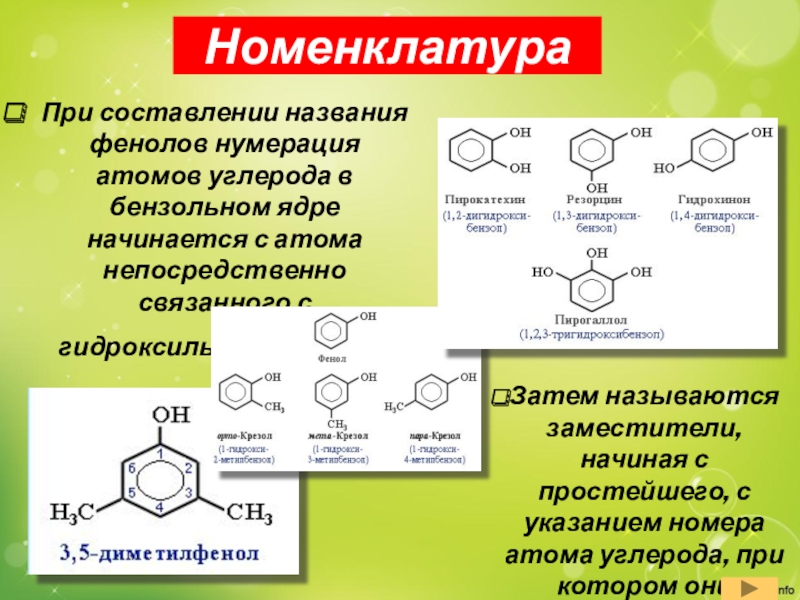
Слайд 6Номенклатура
При составлении названия фенолов нумерация атомов углерода в бензольном ядре
начинается с атома непосредственно связанного с гидроксильной группой .
Затем
называются заместители, начиная с простейшего, с указанием номера атома углерода, при котором они находятся.
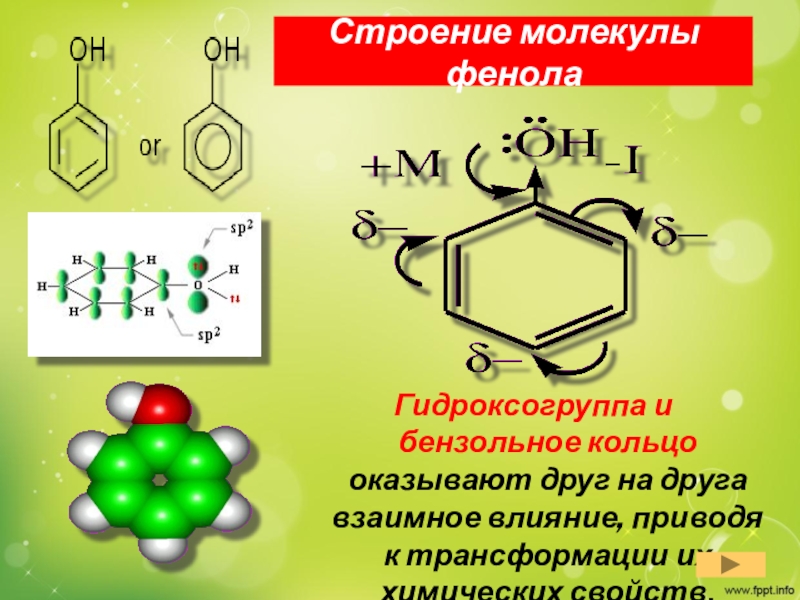
Слайд 7Строение молекулы фенола
Гидроксогруппа и бензольное кольцо оказывают друг на друга
взаимное влияние, приводя к трансформации их химических свойств.
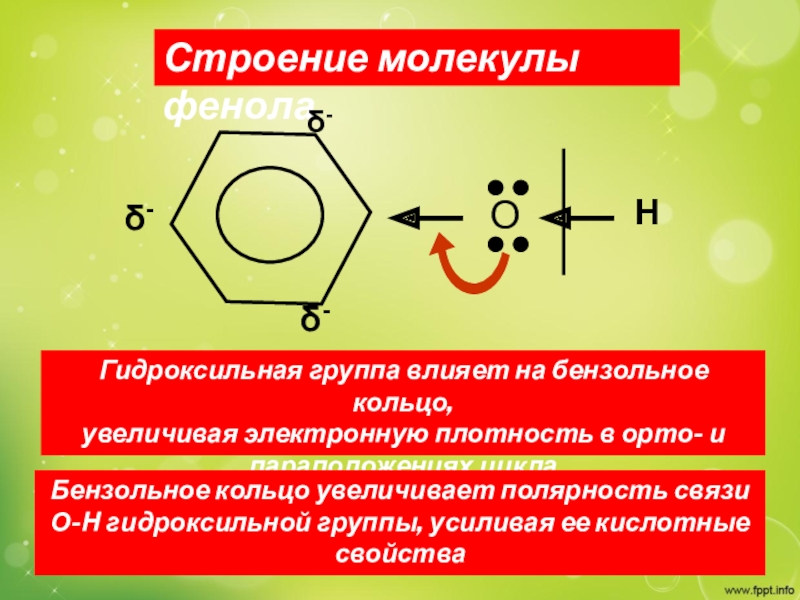
Слайд 8Строение молекулы фенола
О
Н
δ-
δ-
δ-
Гидроксильная группа влияет на бензольное кольцо,
увеличивая электронную
плотность в орто- и
параположениях цикла
Бензольное кольцо увеличивает полярность связи
О-Н
гидроксильной группы, усиливая ее кислотные свойства
Слайд 9Физические свойства фенола
Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного
окисления на воздухе он бывает окрашен в розовый цвет. Его
температура плавления +42ºС, температура кипения +181ºС. Фенол обладает резким характерным запахом. В холодной воде он мало растворим, но уже при 70 ºС растворяется в любых отношениях.Фенол ядовит! При попадании на кожу вызывает ожоги поэтому с фенолом необходимо обращаться осторожно!
Слайд 10Химические свойства фенола
Химические свойства фенола обусловлены наличием в его молекуле
гидроксильной
группы
бензольного ядра
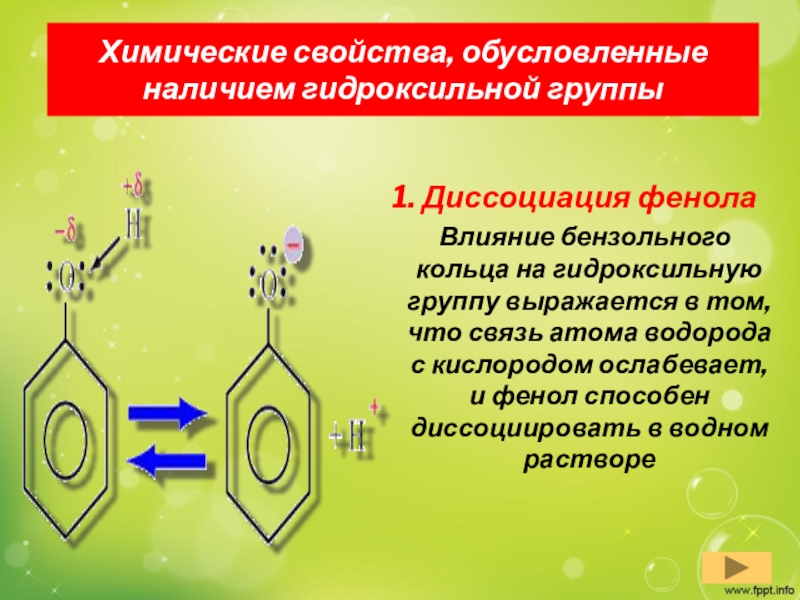
Слайд 11Химические свойства, обусловленные наличием гидроксильной группы
1. Диссоциация фенола
Влияние
бензольного кольца на гидроксильную группу выражается в том, что связь
атома водорода с кислородом ослабевает, и фенол способен диссоциировать в водном растворе
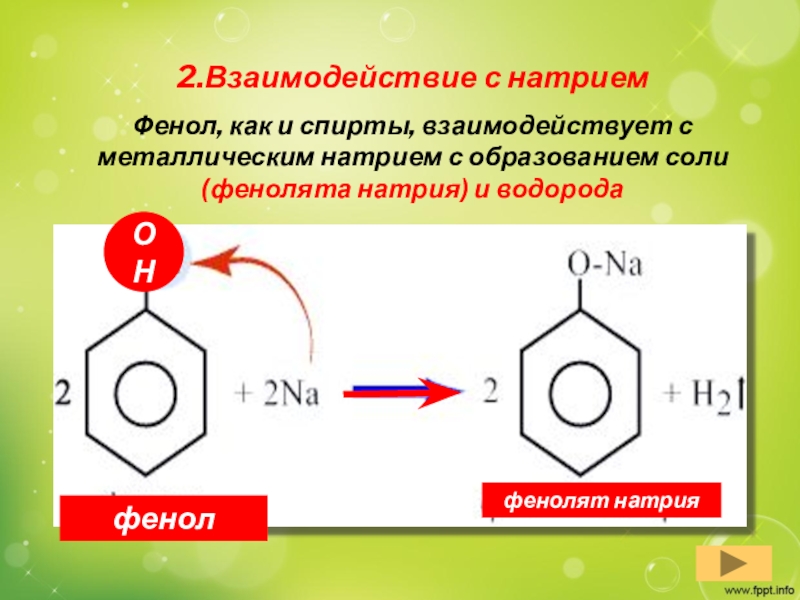
Слайд 122.Взаимодействие с натрием
Фенол, как и спирты, взаимодействует с металлическим натрием
с образованием соли (фенолята натрия) и водорода
фенолят натрия
фенол
ОН
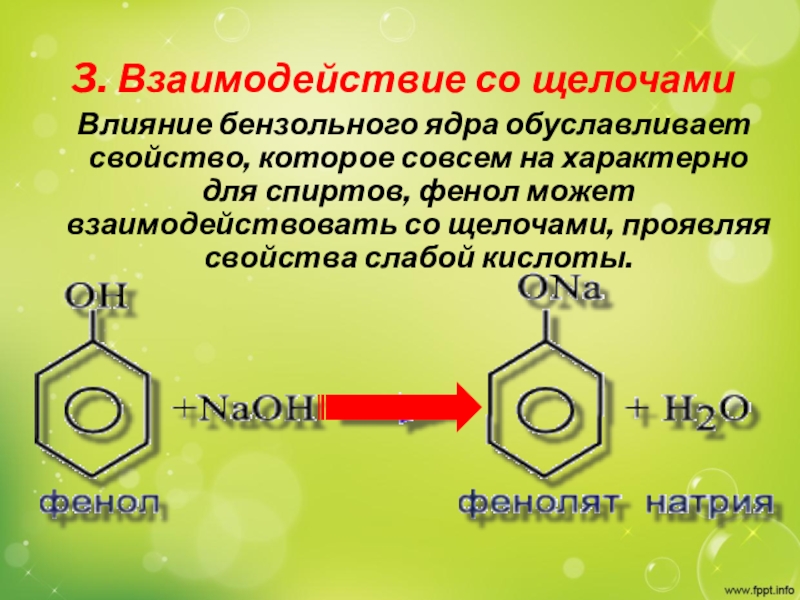
Слайд 133. Взаимодействие со щелочами
Влияние бензольного ядра обуславливает
свойство, которое совсем на характерно для спиртов, фенол может взаимодействовать
со щелочами, проявляя свойства слабой кислоты.
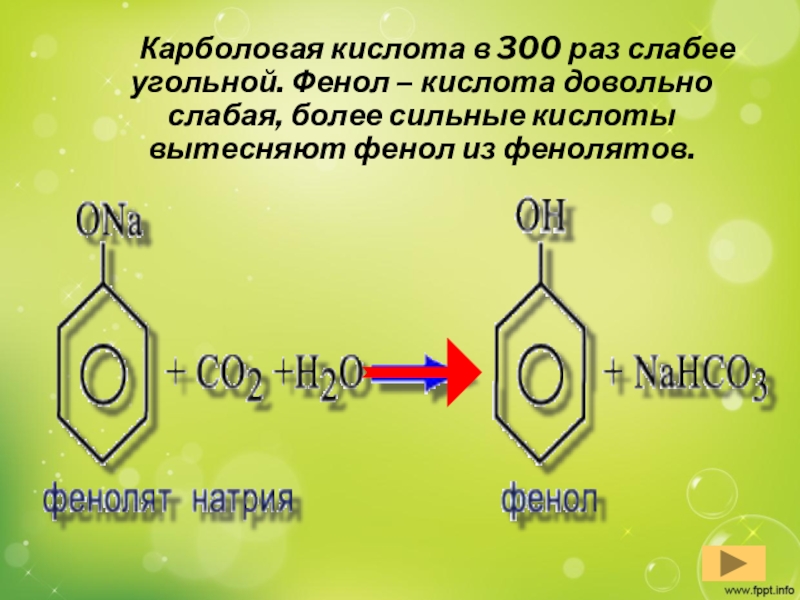
Слайд 14 Карболовая кислота в 300 раз слабее
угольной. Фенол – кислота довольно слабая, более сильные кислоты вытесняют
фенол из фенолятов.
Слайд 15Химические свойства, обусловленные наличием бензольного ядра
Отличия от
ароматических углеводородов:
1. Реакции окисления
Фенол окисляется кислородом воздуха, приобретая фиолетовую
окраску.
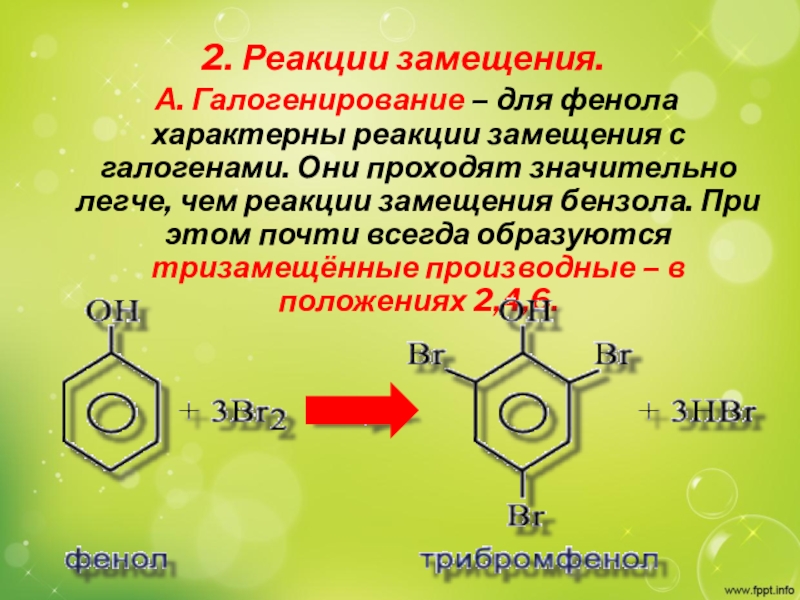
Слайд 162. Реакции замещения.
А. Галогенирование – для фенола характерны
реакции замещения с галогенами. Они проходят значительно легче, чем реакции
замещения бензола. При этом почти всегда образуются тризамещённые производные – в положениях 2,4,6.
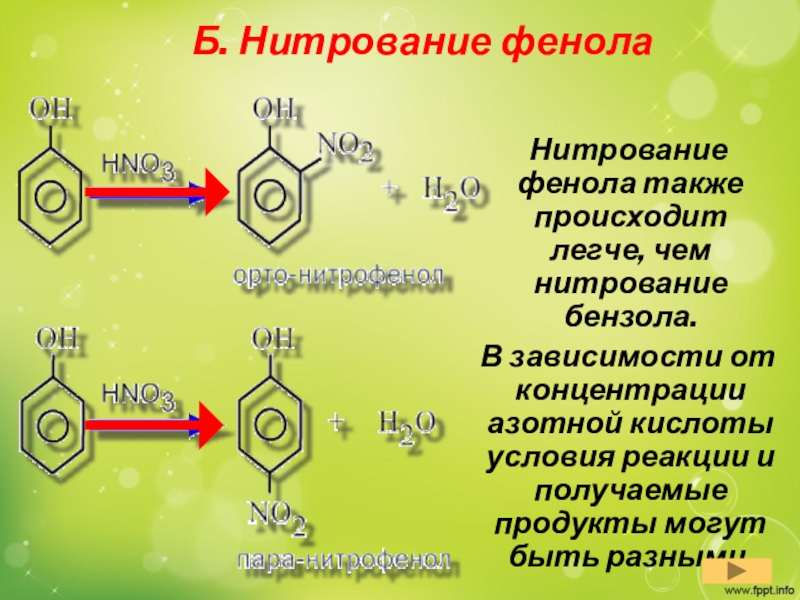
Слайд 17Б. Нитрование фенола
Нитрование фенола также происходит легче, чем
нитрование бензола.
В зависимости от концентрации азотной кислоты условия
реакции и получаемые продукты могут быть разными.
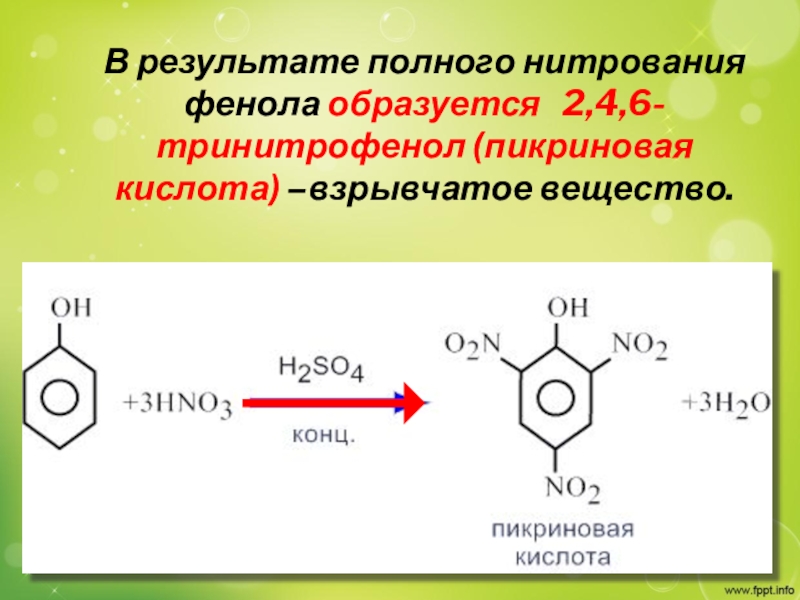
Слайд 18 В результате полного нитрования фенола образуется 2,4,6-тринитрофенол
(пикриновая кислота) –взрывчатое вещество.
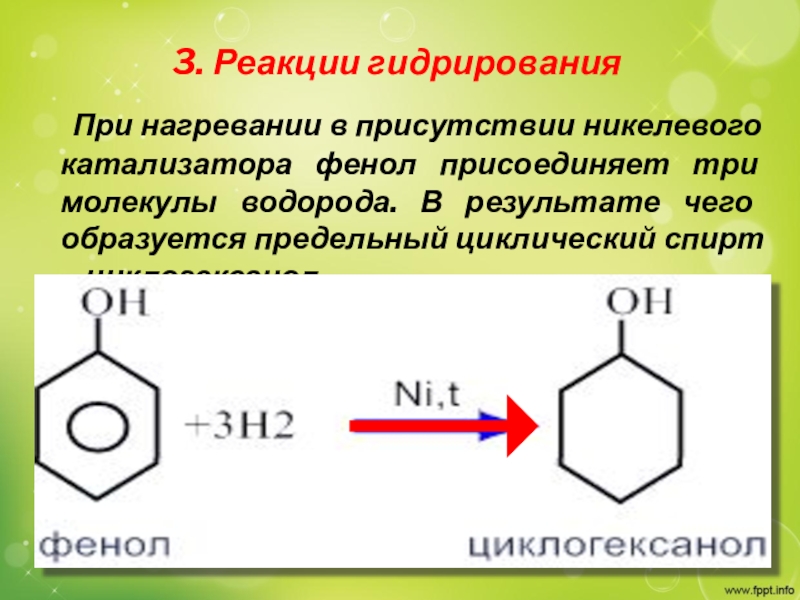
Слайд 193. Реакции гидрирования
При нагревании в присутствии никелевого катализатора
фенол присоединяет три молекулы водорода. В результате чего образуется предельный
циклический спирт – циклогексанол.
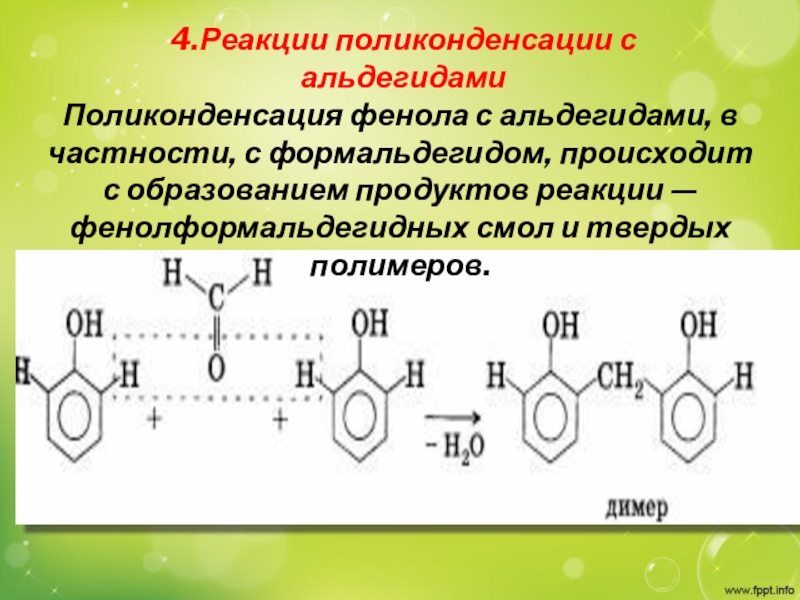
Слайд 204.Реакции поликонденсации с альдегидами
Поликонденсация фенола с альдегидами, в частности, с
формальдегидом, происходит с образованием продуктов реакции — фенолформальдегидных смол и
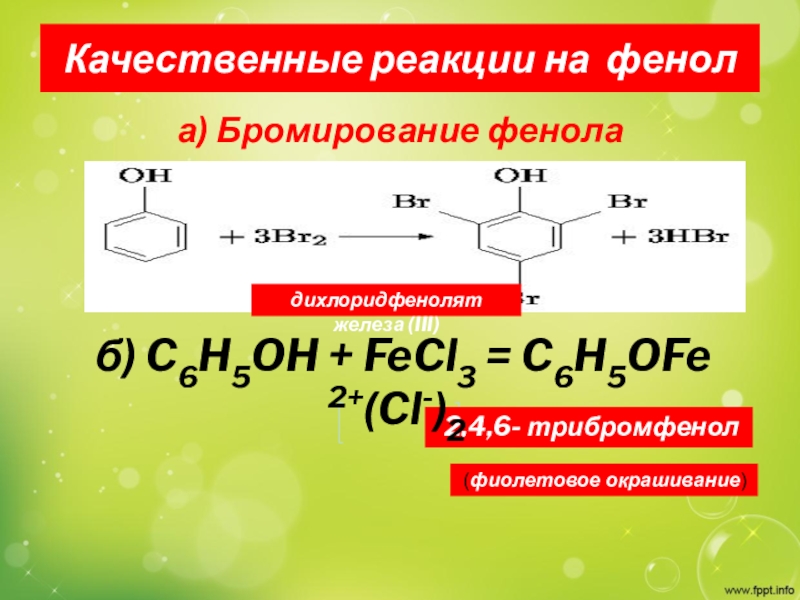
твердых полимеров.Слайд 21Качественные реакции на фенол
а) Бромирование фенола
2,4,6- трибромфенол
дихлоридфенолят железа (III)
(фиолетовое окрашивание)
б) C6H5OH + FeCl3 = C6H5OFe 2+(Cl-)2
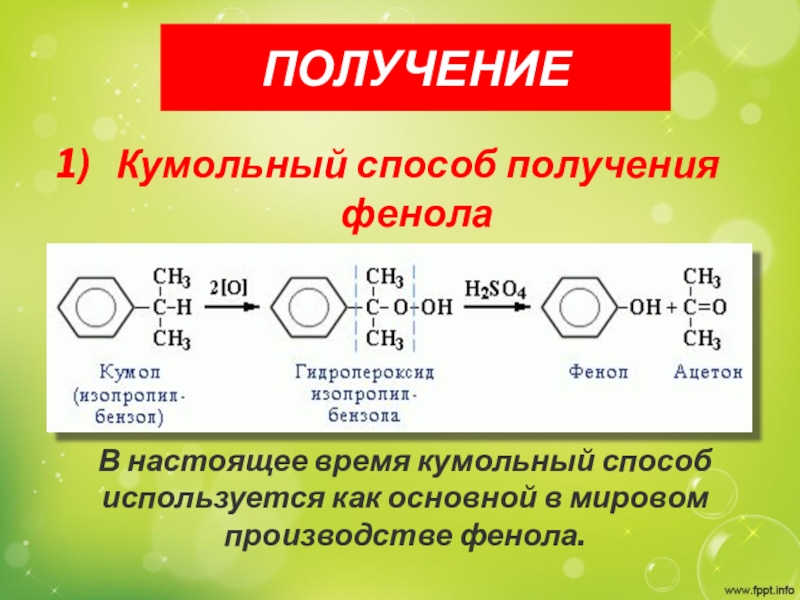
Слайд 22ПОЛУЧЕНИЕ
Кумольный способ получения фенола
В настоящее время кумольный способ используется как
основной в мировом производстве фенола.
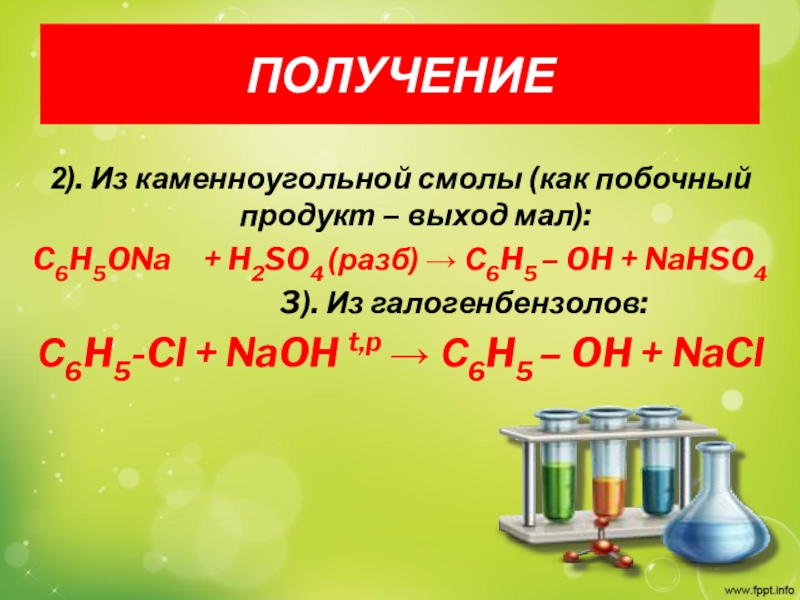
Слайд 23ПОЛУЧЕНИЕ
2). Из каменноугольной смолы (как побочный продукт – выход мал):
C6H5ONa + H2SO4 (разб)
→ С6H5 – OH + NaHSO4
3). Из галогенбензолов: С6H5-Cl + NaOH t,p → С6H5 – OH + NaCl