Слайд 1
УГЛЕВОДЫ –
моносахариды(глюкоза)
План урока:
Единство химической организации живых организмов на Земле.
Историческая справка.
( сообщение учащейся)(8б -15б)
Проблемный вопрос ( что же значат углеводы
для жизни?)
Что такое углеводы?
Классификация углеводов.
Получение глюкозы.(эксперимент Фотосинтез)
Физические свойства и нахождение в природе глюкозы. (опыт _ растворение глюкозы)
Химические свойства глюкозы. (видео опыт, опыт – консультанты по 6б)
Биологическое значение и применение глюкозы (презентация учащейся)( 15б-25б)
Слайд 2«Что же значат углеводы для жизни?»
Слайд 3Углеводы.
Историческая справка.
Углеводы используются с глубокой древности – самым первым углеводом
(точнее смесью углеводов), с которым познакомился человек, был мед.
Слайд 4
Европейцы познакомились с тростниковым сахаром благодаря походам Александра Македонского в
327г. До н.э.
Родиной сахарного тростника является северо-западная Индия-Бенгалия.
Свекловичный сахар
в чистом виде был открыт лишь в 1747 г. Немецким химиком А. Марггафом.
Крахмал был известен еще древним грекам.
Целлюлоза, как составная часть древесины, используется с глубокой древности.
Слайд 5
Термин слова «сладкий» и окончание –оза- для сахаристых веществ было
предложено французским химиком Ж. Дюла в 1838г.
сторически сладость была главным
признаком, по которому то или иное вещество относится к углеводам.
В 1811г. Русский химик Кирхгоф впервые получил глюкозу гидролизом крахмала, а впервые правильную эмпирическую формулу глюкозы предложил шведский химик Я.Берцелиус в 1837 г. C6H12O6
Синтез углеводов из формальдегидов в присутствии Ca(OH)2 был произведён А.М.Бутлеровым в 1864 г.
Слайд 6Сn(Н2 О)m
Углеводы – органические соединения, состоящие из углерода,
водорода и кислорода, причем водород и кислород входят в соотношении
(2:1) как в воде, отсюда и название. На основе этой аналогии русский химик К. Шмидт в 1844 г. предложил термин углевода (углерод и вода), а общая формула углеводов Сn(Н2 О)m
Слайд 8ПОЛУЧЕНИЕ ГЛЮКОЗЫ
1) Реакция фотосинтеза
6СО2 + 6H2O → С6Н12 О6 +
6О2 +Q
2) Реакция полимеризации
О
6 Н – С → С6Н12 О6
Н
Слайд 9
В промышленности глюкозу получают гидролизом крахмала:
(С6H10O5)n + nH20 = nC6H12O6
Слайд 10Физические свойства глюкозы
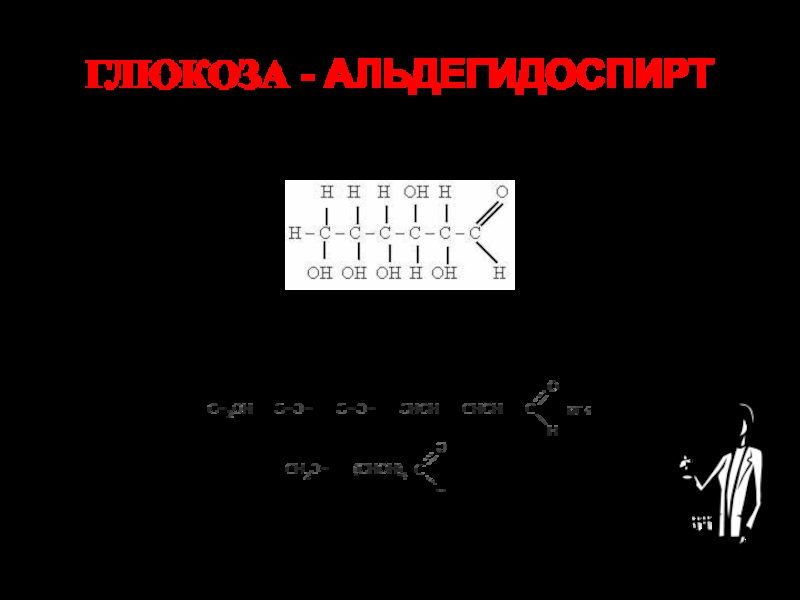
ГЛЮКОЗА -
бесцветное кристаллическое вещество,
хорошо растворимо в воде,
сладкое на вкус,
температура плавления 146 С.
Если сладость раствора сахарозы принять
за 100 %,
то сладость фруктозы – 173 %,
глюкозы – 81 %,
мальтозы и галактозы – 32 %,
лактозы – 16 %.
Слайд 11ПРАВИЛА ВЫЖИВАНИЯ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ
Если в руках у вас жидкое
– не разлейте, порошкообразное – не рассыпьте, газообразное – не
выпустите наружу.
Если включили – выключите.
Если открыли – закройте.
Если разобрали – соберите.
Если вы не можете собрать – позовите на помощь умельца.
Если вы не разбирали, не вздумайте собирать.
Если вы одолжили что-нибудь – верните.
Если вы пользуетесь чем-либо, держите в чистоте и порядке.
Если вы привели что-либо в беспорядок – восстановите статус кво.
Если вы сдвинули что-нибудь – верните на место.
Если вы не знаете, как это действует, ради бога, не трогайте.
Если вас это не касается – не вмешивайтесь.
Если вы не знаете, как это делается – сразу спросите.
Если вы не можете что-либо понять – почешите в затылке.
Если все же не поймете – то и не пытайтесь.
Если вы "горите" на уроке – постарайтесь чтобы, у вас ничего не загорелось.
Если у вас что-либо взорвалось – проверьте, остались ли живы.
Если вы не усвоили этих правил – не входите в лабораторию.
Слайд 13В особом виде глюкоза содержится почти во всех органах зеленых
растений.
Особенно ее много в виноградном соке, поэтому глюкозу иногда
называют виноградным сахаром,
Мед в основном состоит из смеси глюкозы с фруктозой.
Нахождение глюкозы
в природе
Слайд 15Таблица 2.
Содержание углеводов на 100 г. продуктов
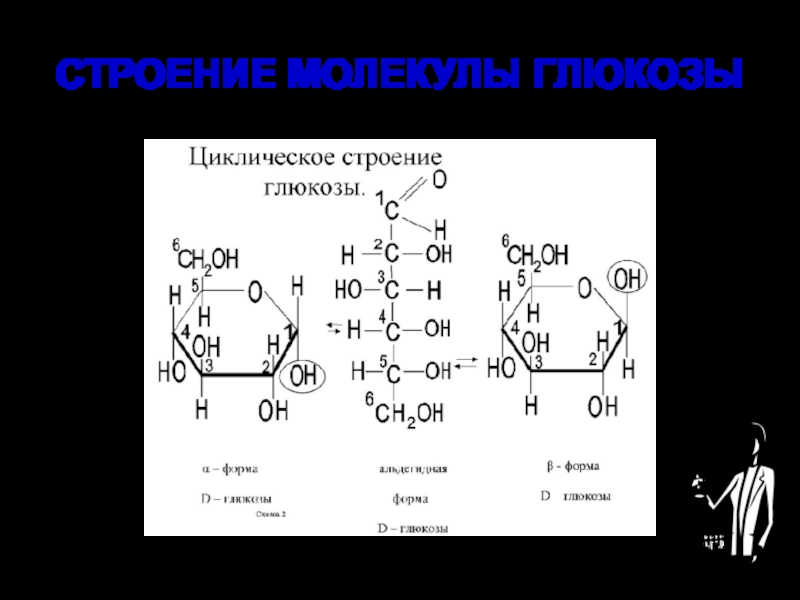
Слайд 18Изомерия глюкозы
Глюкоза является альдегидоспиртом, а фруктоза - кетоноспиртом
Слайд 20ХИМИЧЕСКИЕ СВОЙСТВА
Реакция “серебряного зеркала”
СН2ОН – (СНОН)4 – СОН + Ag2O
→
СН2ОН – (СНОН)4 – СООН + 2Ag↓
2) Взаимодействие с
гидроксидом меди (II)
СН2ОН – (СНОН)4 – СОН + 2Сu(ОН)2 →
СН2ОН – (СНОН)4 – СООН + Сu2О + 2Н2 О
Слайд 21ХИМИЧЕСКИЕ СВОЙСТВА
3) Гидрирование глюкозы
СН2ОН – (СНОН)4 – СОН + Н2
→
СН2ОН – (СНОН)4 – СН2 ОН
сорбит
Продукт реакции – сорбит – является заменителем сахара для людей, страдающих сахарным диабетом
Продук
Слайд 22СПЕЦИФИЧЕСКИЕ СВОЙСТВА
а) Спиртовое брожение (под действием дрожжей)
С6Н12 О6
→ 2 С2 Н5 ОН + 2СО2
б) Молочнокислое брожение (под
действием молочнокислых бактерий)
Слайд 23СПЕЦИФИЧЕСКИЕ СВОЙСТВА
в) Маслянокислое брожение
С6 Н12 О6 → С3 Н7 СООН
+ 2 Н2↑ +2 СО2↑
масляная кислота
Слайд 24
Упомянутые виды брожения, вызываемые
микроорганизмами, имеют широкое практическое
значение. Например,
спиртовое – для получения
этилового спирта, в виноделии, пивоварении и
т.д.,
а молочнокислое – для получения молочной
кислоты и кисломолочных продуктов, лимоннокислое
- для получения лимонной кислоты.
Слайд 25МОНОСАХАРИДЫ — углеводы, которые не гидролизуются. В зависимости от числа
атомов углерода подразделяются на триозы, тетрозы, пентозы, гексозы.
Слайд 26ДИСАХАРИДЫ – углеводы, которые гидролизуются с образованием двух молекул моносахаридов.
Слайд 27ПОЛИСАХАРИДЫ — высокомолекулярные соединения — углеводы, которые гидролизуются с образованием
множества молекул моносахаридов.