Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Виды химических связей 11 класс
Содержание
- 1. Виды химических связей 11 класс
- 2. Под химической связью понимаются электрические силы притяжения,
- 3. Причина образования химической связи — стремление атомов
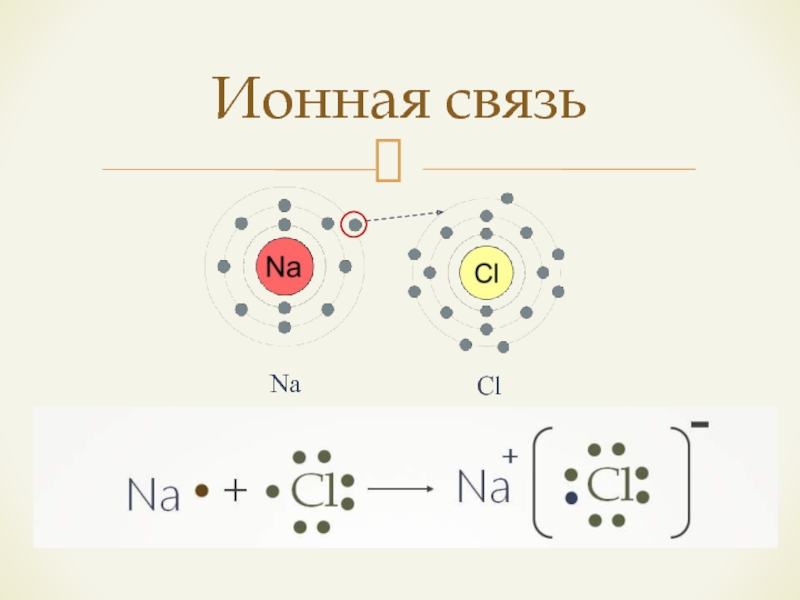
- 4. Ионная связьNaCl
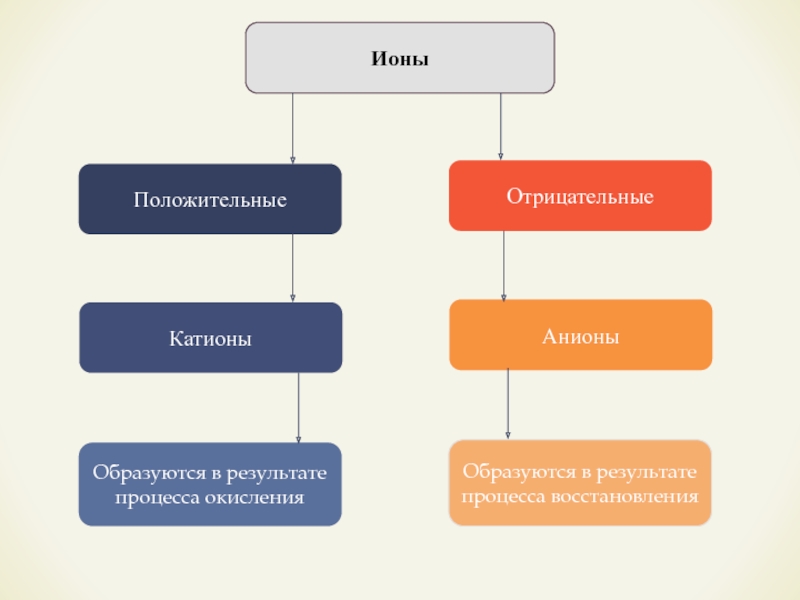
- 5. ИоныПоложительныеОтрицательныеКатионыОбразуются в результате процесса окисленияАнионыОбразуются в результате процесса восстановления
- 6. Как правило, ионная связь возникает между атомами типичных металлов и типичных неметаллов.
- 7. Ковалентная связьНеполярнаяПолярная H2, O2, N2, Cl2 H2S, NH3, HCl
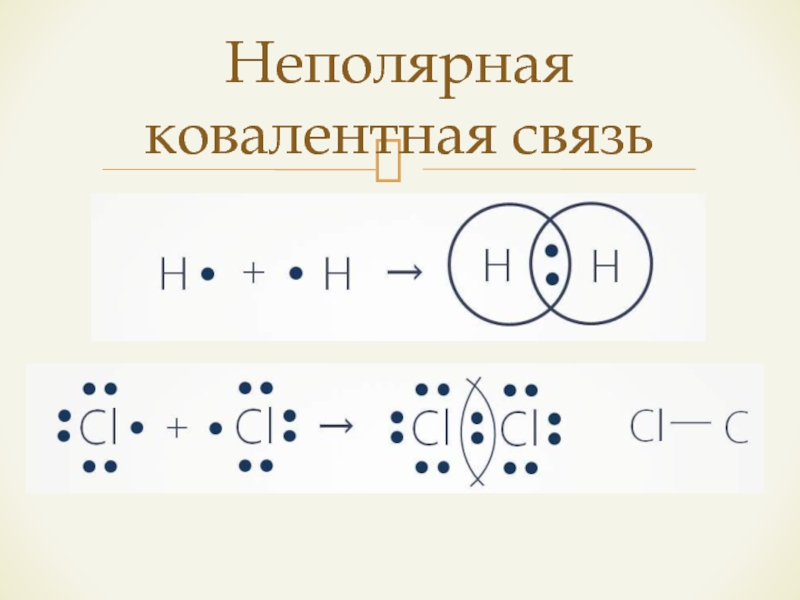
- 8. Неполярная ковалентная связь
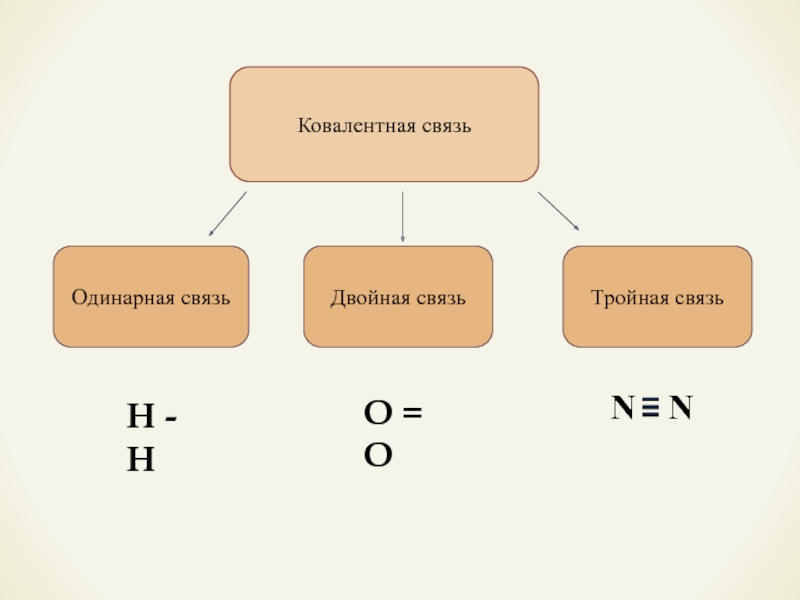
- 9. Ковалентная связьОдинарная связьДвойная связьТройная связьО = ОН - Н
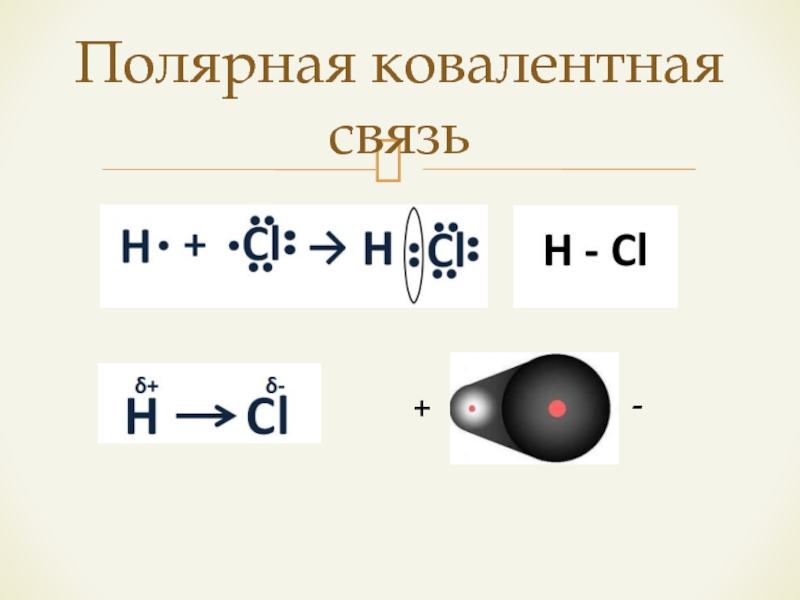
- 10. Полярная ковалентная связь+-
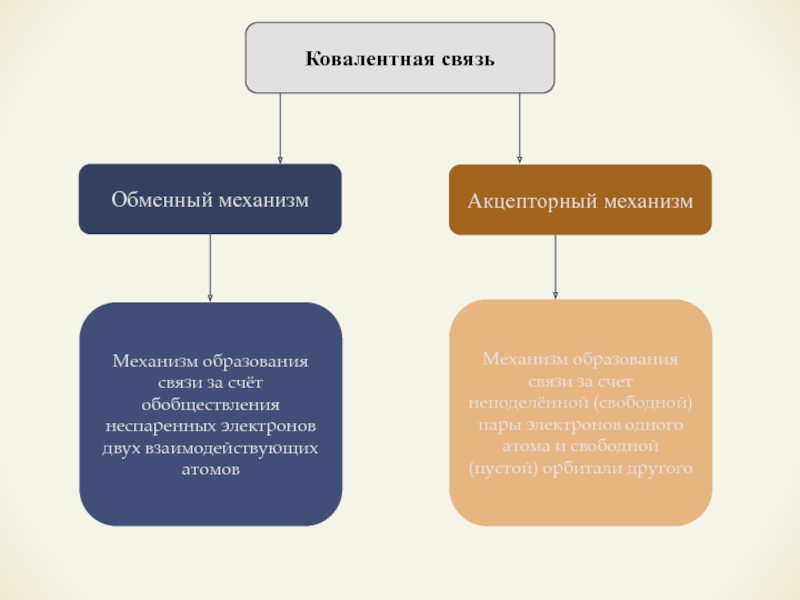
- 11. Ковалентная связьОбменный механизмАкцепторный механизмМеханизм образования связи за
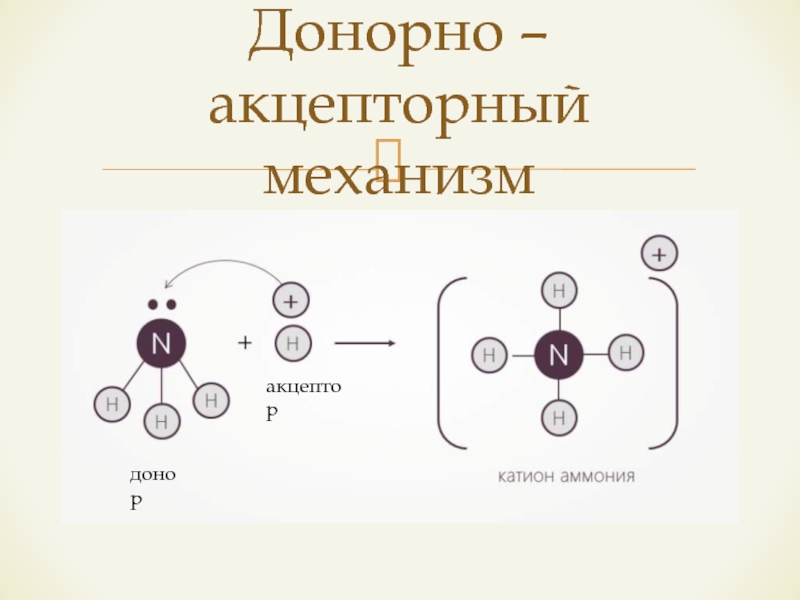
- 12. Донорно – акцепторный механизмдоноракцептор
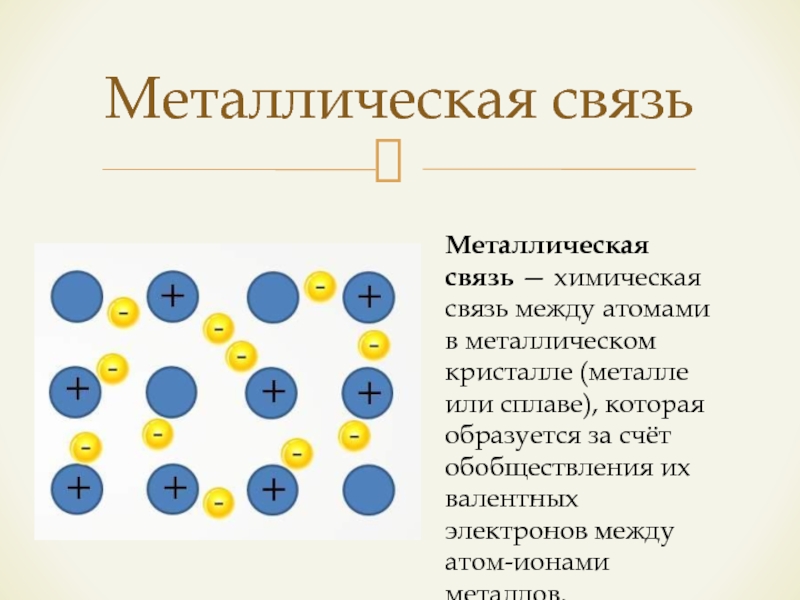
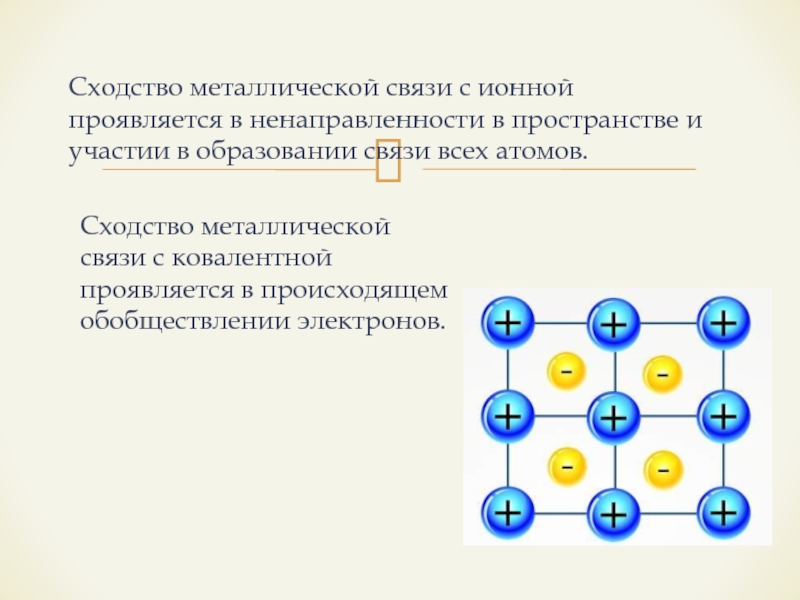
- 13. Металлическая связьМеталлическая связь — химическая связь между
- 14. Сходство металлической связи с ионной проявляется в
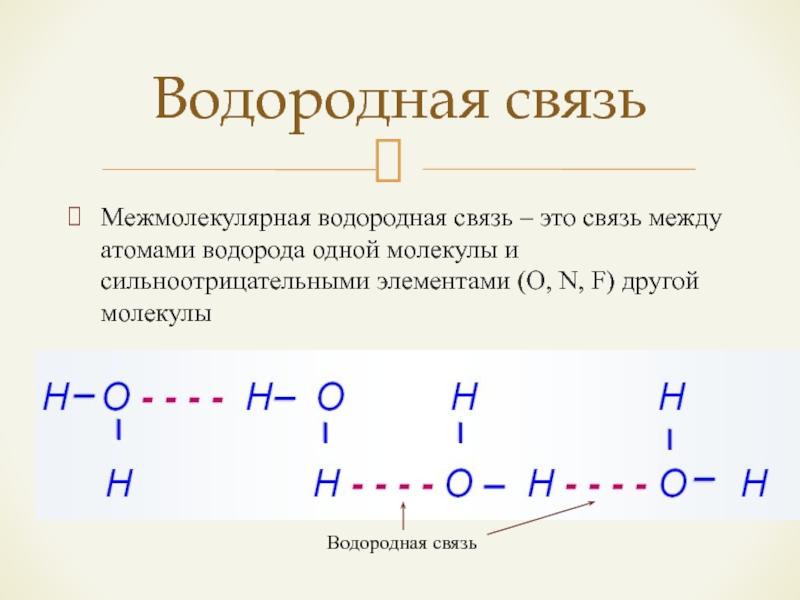
- 15. Межмолекулярная водородная связь – это связь между
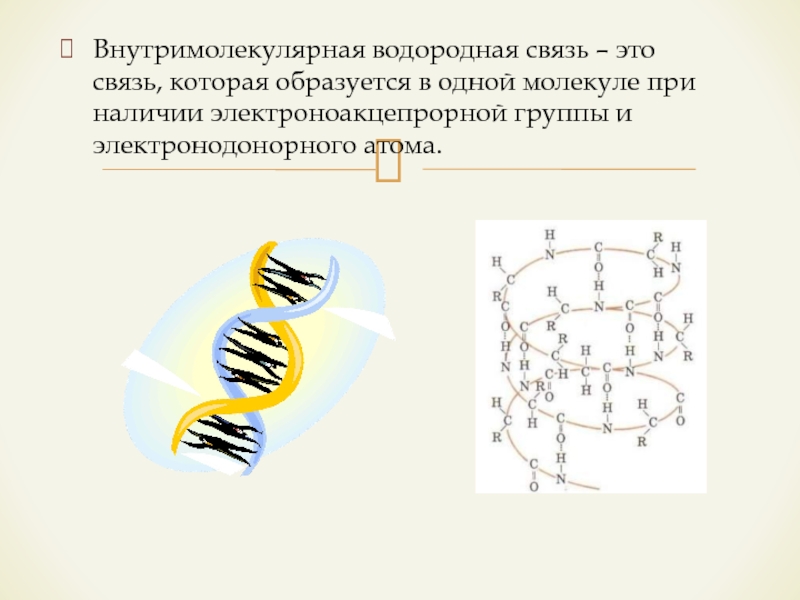
- 16. Внутримолекулярная водородная связь – это связь, которая
- 17. Скачать презентанцию
Под химической связью понимаются электрические силы притяжения, удерживающие частицы друг около друга. Частицами могут быть атомы, ионы, молекулы.
Слайды и текст этой презентации
Слайд 2Под химической связью понимаются электрические силы притяжения, удерживающие частицы друг
около друга. Частицами могут быть атомы, ионы, молекулы.
Слайд 3Причина образования химической связи — стремление атомов посредством взаимодействия с
другими атомами достичь более устойчивого состояния.
Электроотрицательность (ЭО) – способность притягивать
электроны.Если атомы обладают одинаковой ЭО, возникает ковалентная неполярная связь;
Если атомы обладают ЭО разной, но не резко отличаются, разность в ЭО < 1,7 – возникает ковалентная полярная связь;
Если атомы обладают ЭО разной, резко отличаются, разность в ЭО > 1,7 – возникает ионная связь.