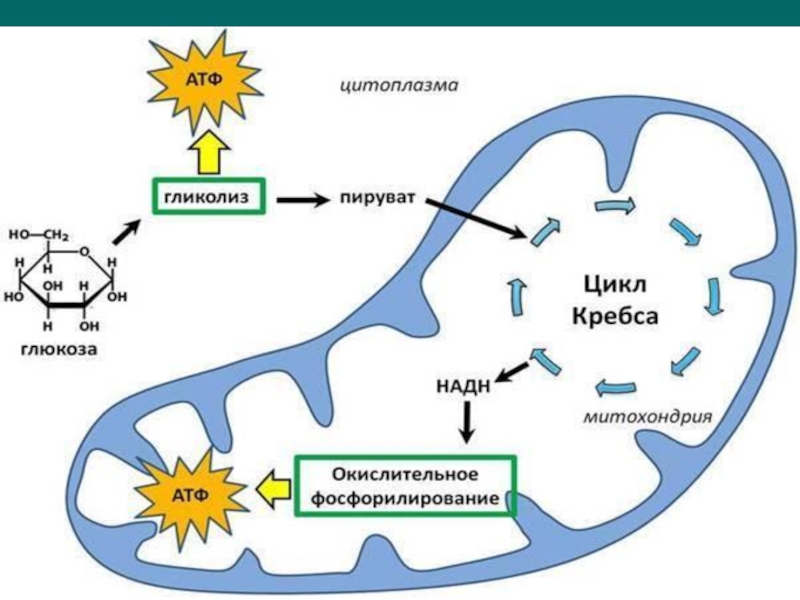
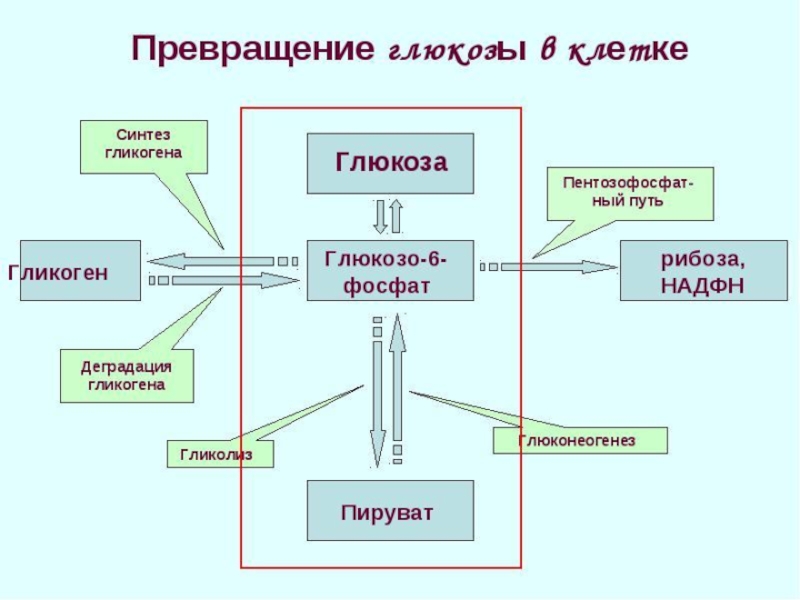
Слайд 2Промежуточный обмен углеводов в организме.
1. Поступление глюкозы в клетки тканей.
2.Биосинтез
гликогена в печени и мышцах
3.Распад гликогена в печени и мышцах
4.Дихотомический
путь распада глюкозы – гликолиз
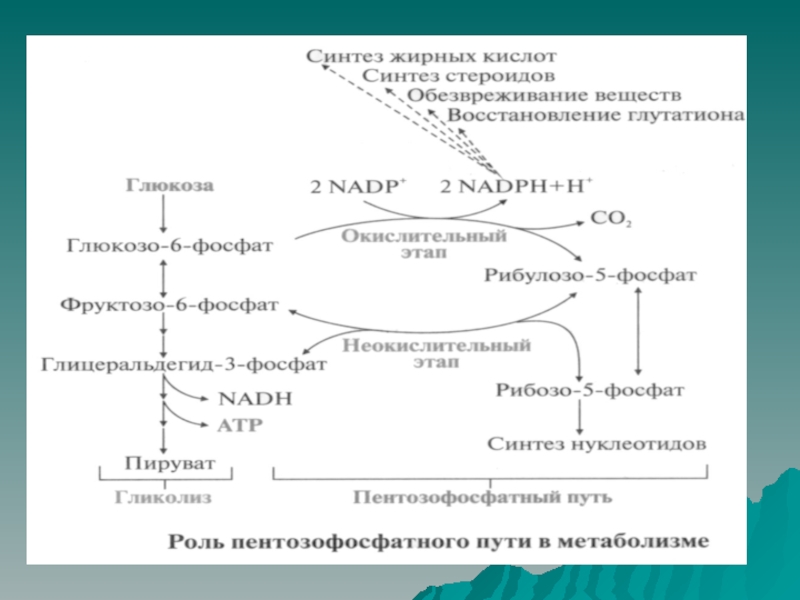
5.Апотомический путь распада глюкозы – пентозофосфатный путь
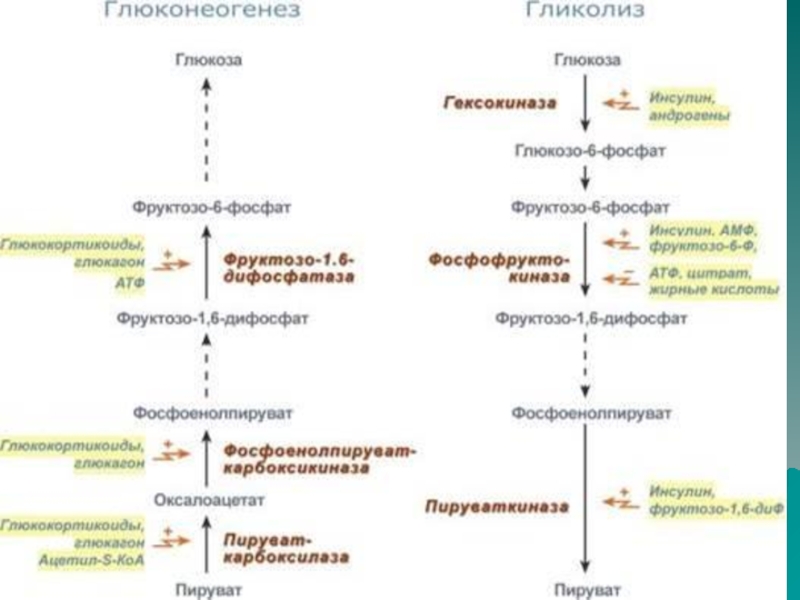
6.Биосинтез глюкозы из неуглеводных компонентов-глюконеогенез
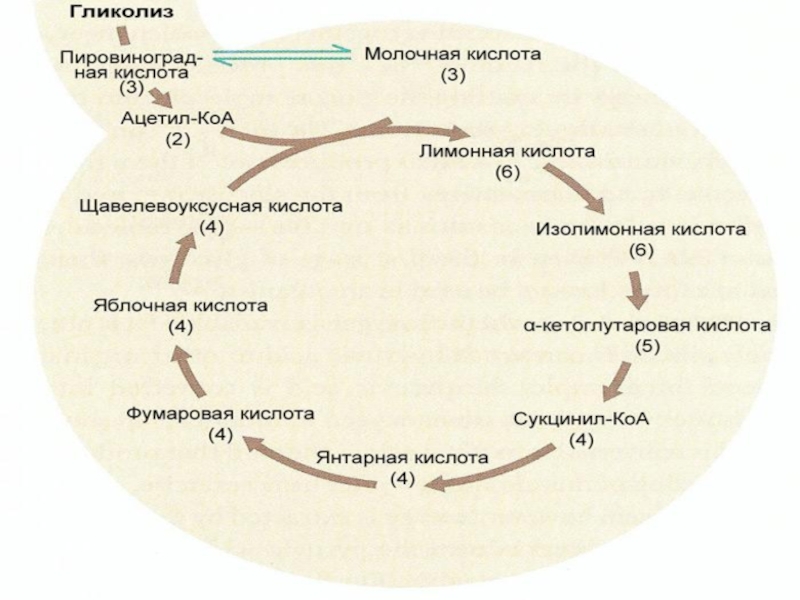
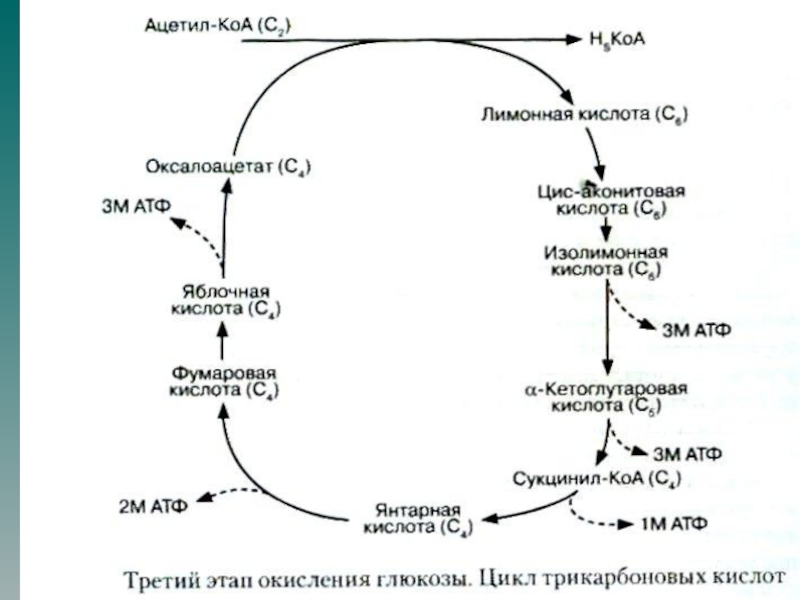
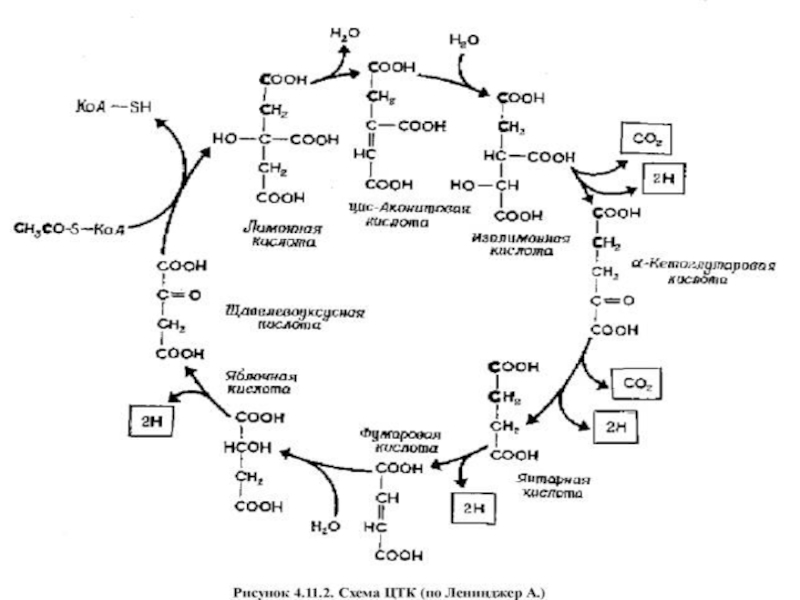
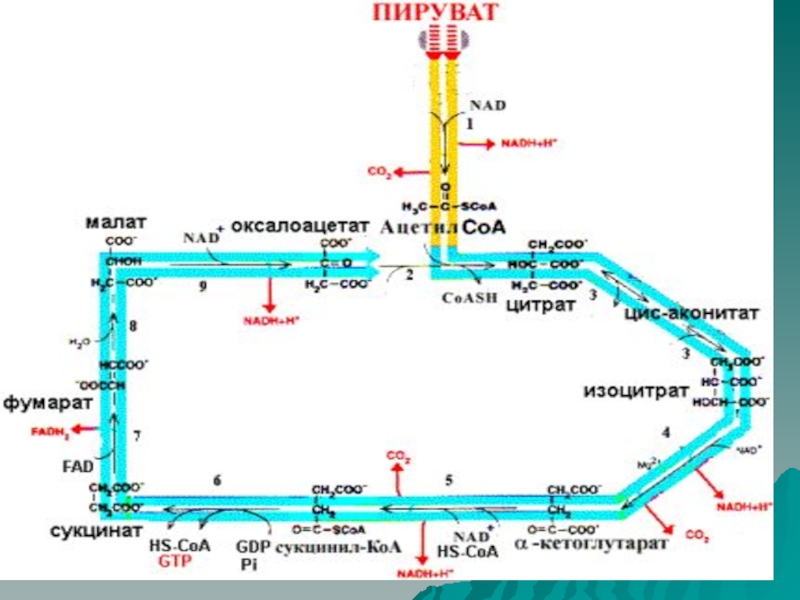
7.Цикл трикарбоновых кислот
8.Окислительное фосфорилирование
С 1 по 6 пункт – специфические пути обмена глюкозы
С 7 по 8 пункт – общий путь терминального окисления
Слайд 3
Существует 3 метаболических пути, в которых может окисляться глюкоза.
Аэробный
гликолиз
Анаэробный гликолиз
Аэробный распад глюкозы до СО2 и Н2О
Гликолиз
- основной процесс образования энергии путем окисления глюкозы
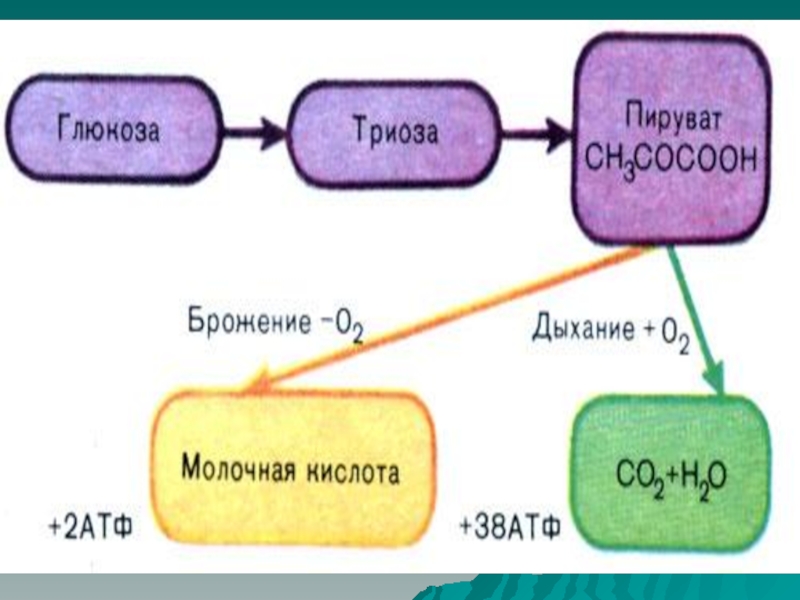
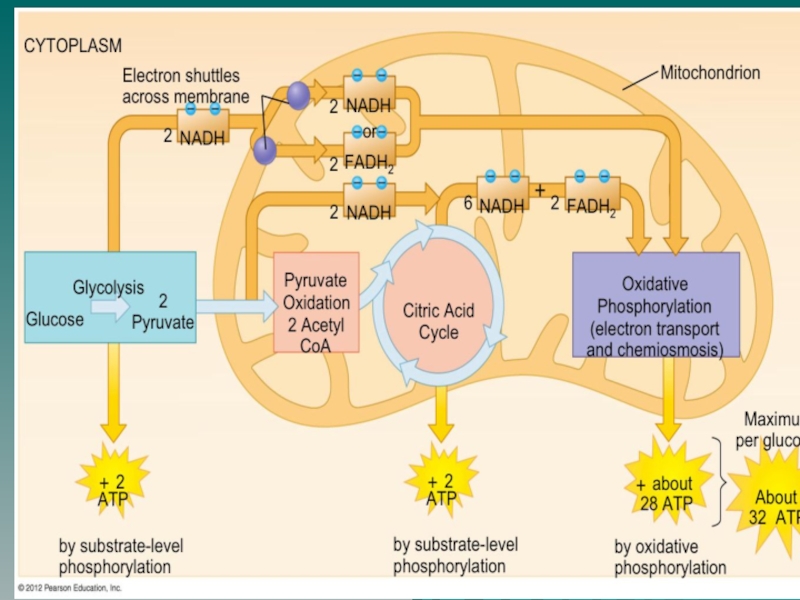
Слайд 4Аэробный гликолиз – превращение глюкозы в 2 молекулы пирувата, которое
происходит в аэробных условиях и сопровождается синтезом 8 молекул АТФ.
Анаэробный
гликолиз – образование из глюкозы 2 молекул лактата без участия кислорода и митохондриальной ЦПЭ. Энергетический выход процесса составляет 2 молекулы АТФ.
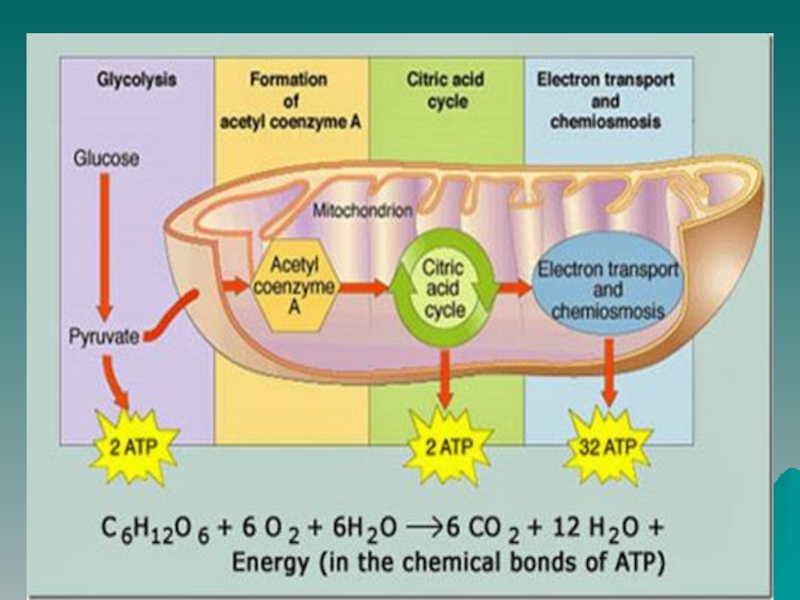
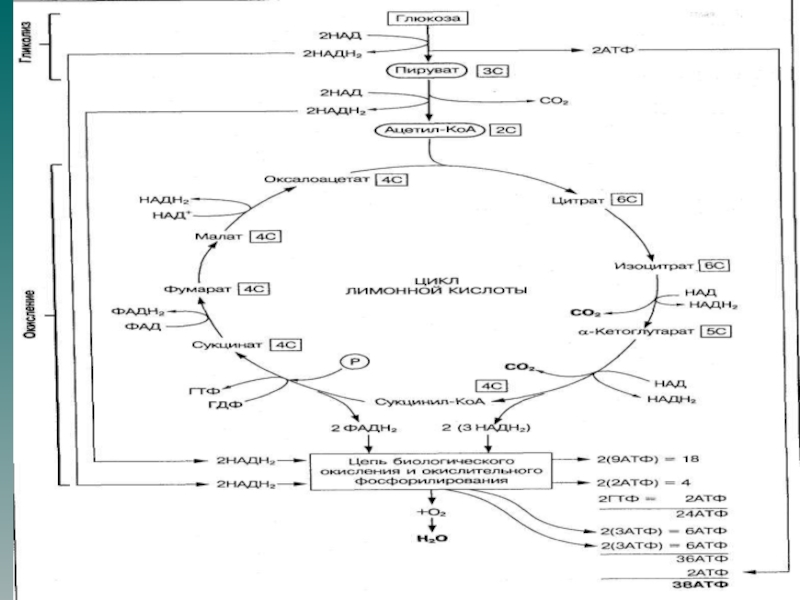
Аэробный распад глюкозы до СО2 и Н2О включает аэробный гликолиз и последующее окисление 2 молекул пирувата в общем пути катаболизма. При аэробном распаде глюкозы синтезируются 38 молекул АТФ.
Слайд 7Аэробный и анаэробный гликолиз имеет не только энергетическое, но и
анаболическое значение, т.к. промежуточные и конечные продукты этих процессов могут
использоваться для синтеза многих соединений.
В жировой ткани и печени гликолиз обеспечивает образование субстратов, необходимых для синтеза жиров.
В печени из лактата синтезируется глюкоза, а из пирувата – аминокислоты.
В эритроцитах при анаэробном гликолизе образуется 2,3-бисфосфоглицерат – аллостерический регулятор сродства гемоглобина к кислороду.
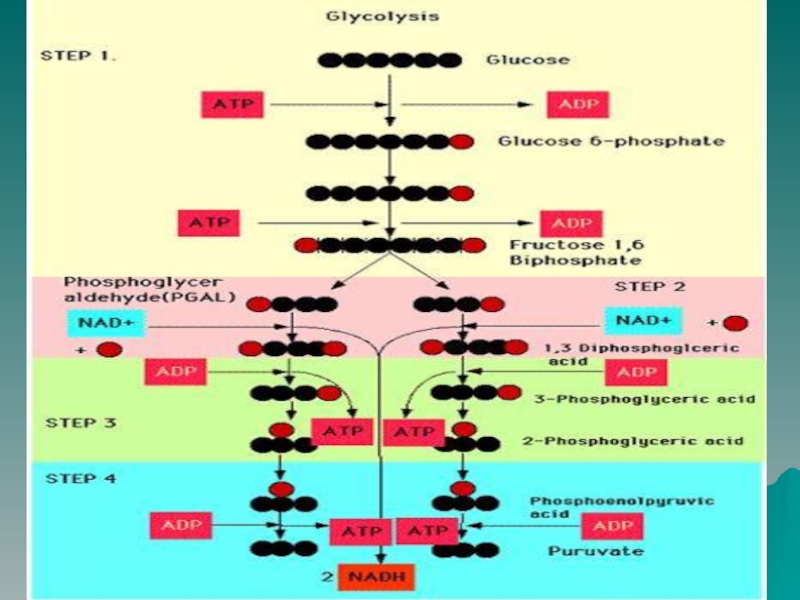
Слайд 8АЭРОБНЫЙ ГЛИКОЛИЗ
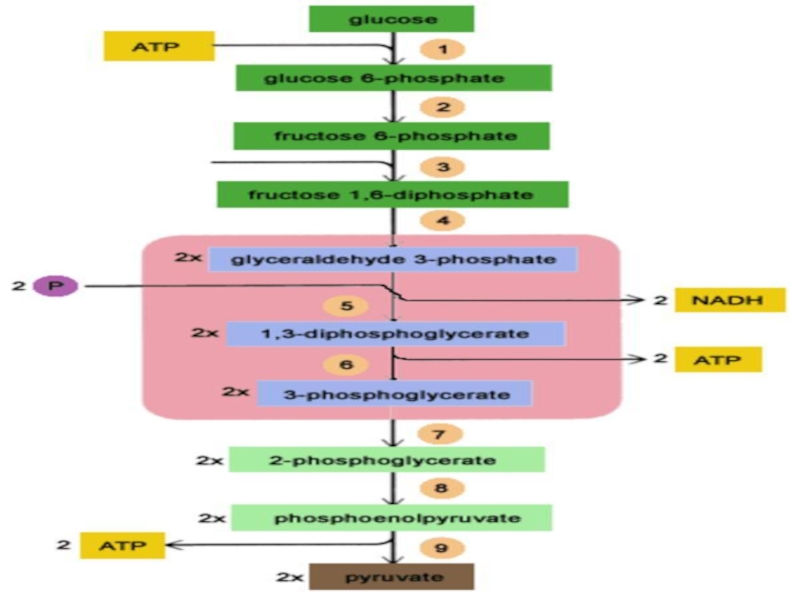
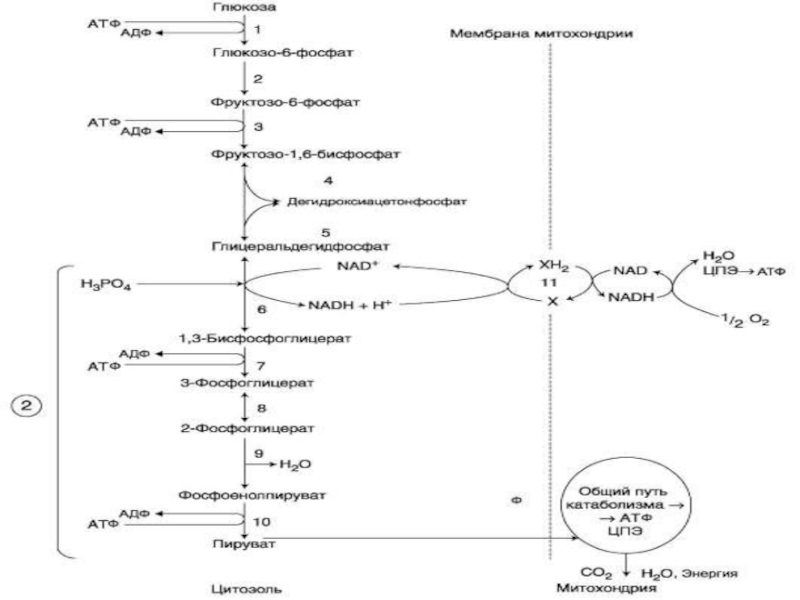
В последовательности реакций аэробного гликолиза можно выделить 2 этапа.
На первом этапе из молекулы глюкозы образуются две триозы –
глицеральдегид-3-фосфат (ГАФ) и дигидроксиацетонфосфат (ДАФ).
Первый этап гликолиза требует затраты 2 молекул АТФ и приводит к образованию 2 молекул ГАФ.
Включает 5 реакций.
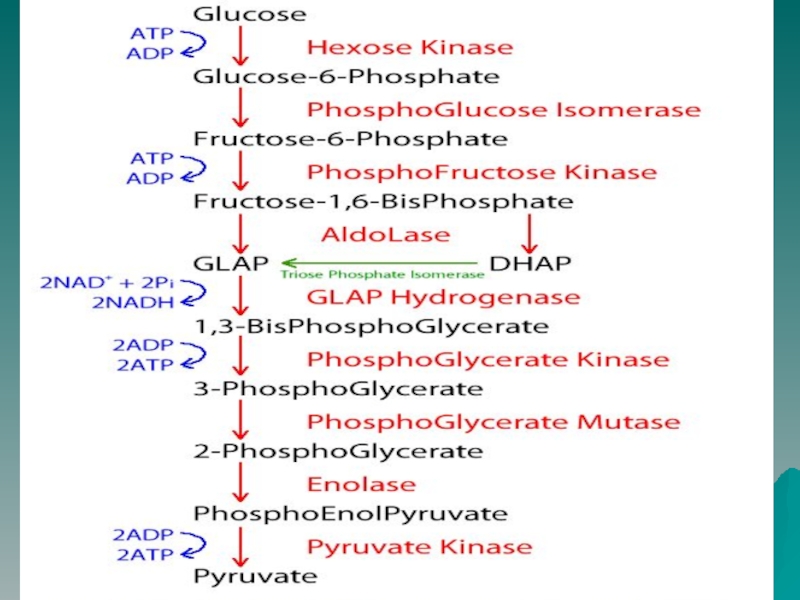
Слайд 9фосфорилирование глюкозы гексокиназой или глюкокиназой с образованием глюкозо-6-фосфата, которое идет
с затратой молекулы АТФ
2. изомеризация глюкозо-6-фосфата во фруктозо-6- фосфат при
участии фосфофглюкоизомеразы
3. фосфорилирование фруктозо-6-фосфат фосфофруктокиназой с использованием молекулы АТФ и с образованием фруктозо-1,6-дисфосфата
4. альдольное расщепление фруктозо-1,6-дисфосфата, катализируемое альдолазой, с образованием двух триоз - глицеральдегид-3-фосфата (ГАФ) и дигидроксиацетонфосфата (ДАФ)
5. изомеризацию ДАФ и ГАФ под действием триозофосфатизомеразы
Слайд 11Второй этап этого метаболического пути обеспечивает синтез АТФ.
В него
вступают 2 молекулы глицеральдегид-3-фосфат (ГАФ), поэтому стехиометрический коэффициент для всех
последующих реакций гликолиза равен 2.
Слайд 126. окисление ГАФ NAD+-зависимой глицеральдегидфосфат-дегидрогеназой при участии Н3РО4, которое приводит
к образованию 1,3-дисфосфоглицерата, содержащего макроэргическую связь
7. превращение 1,3-дисфосфоглицерата в 3-фосфоглицерат
под действием фосфоглицераткиназы, сопровождающееся субстратным фосфорилированием АДФ.
8. изомеризация 3-фосфоглицерата в 2-фосфоглицерат, катализируемая фосфоглицеромутазой
9. дегидратация 2-фосфоглицерата ферментом енолазой с образованием фосфоенолпирувата, содержащего макроэргическую связь
10. образование пирувата из фосфоенолпирувата под действием пируваткиназы, сопряженное с субстратным фосфорилированием АДФ.
Слайд 15В аэробном гликолизе есть 3 необратимые реакции, которые катализируют ферменты
гексокиназа (глюкокиназа), фосфофруктокиназа, пируваткиназа.
Единственная ОВР аэробного гликолиза – дегидрирование
глицеральдегид-3-фосфат (ГАФ) – идет под действием NAD+-зависимой глицеральдегидфосфатдегидрогеназы.
Акцептором 2 е и Н+ в этой реакции является NAD+, который восстанавливается в NADН.
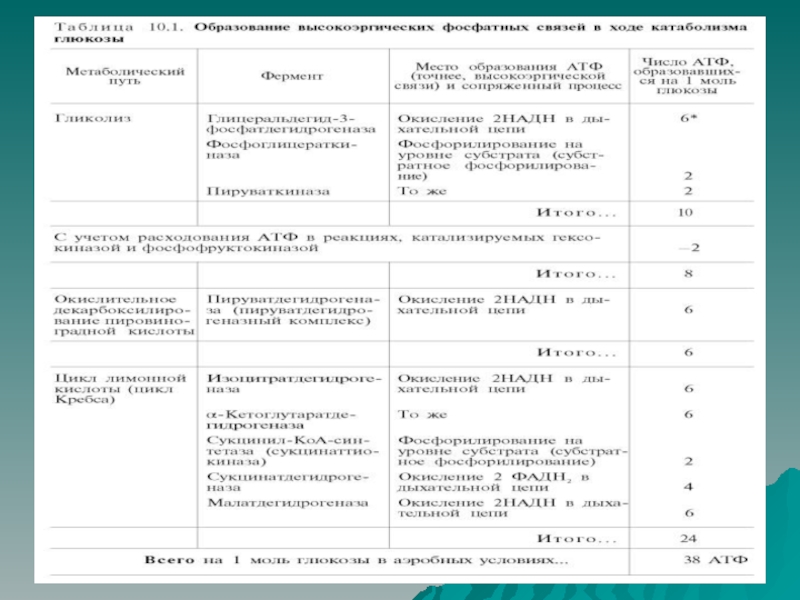
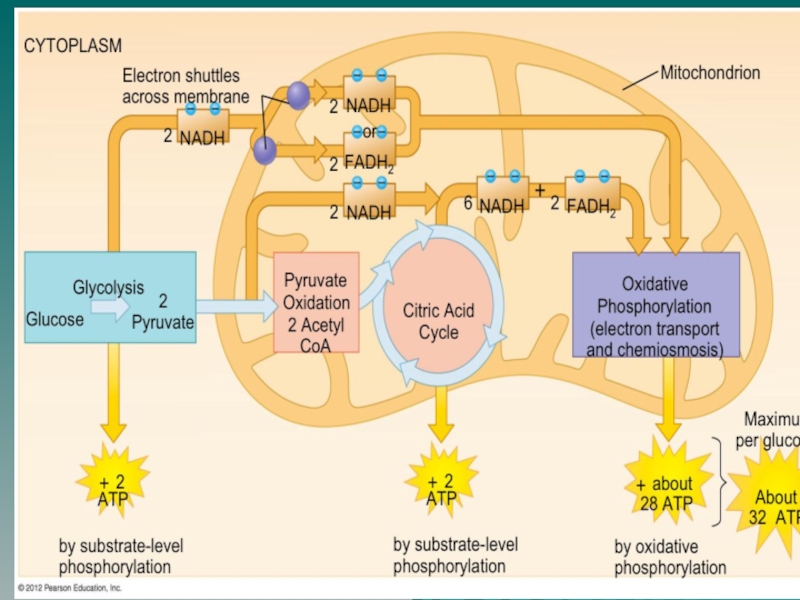
Слайд 16Выход АТФ при аэробном гликолизе
При аэробном гликолизе образуются 10
молекул АТФ, причем 6 из них – в результате окислительного
фосфорилирования, 4 АТФ – при субстратном.
2 АТФ используются на первом этапе гликолиза в реакциях фосфорилирования глюкозы и фруктозо-6-фосфата.
Следовательно суммарный энергетический выход АТФ при аэробном гликолизе составляет (6+4) - 2 = 8 АТФ.
Слайд 17Все реакции гликолиза идут в цитоплазме клеток, но мембрана митохондрий
непроницаема для NADН, поэтому транспорт водорода через митохондриальную мембрану осуществляется
с помощью особых челночных механизмов.
Слайд 18Малат-аспартатная челночная система
Эта система, в которой участвуют малат, цитозольная
и митохондриальная малатдегидрогеназы, является наиболее универсальной.
В цитоплазме NADH восстанавливает
оксалоацетат в малат, который при участии переносчика проходит в митохондрии, где окисляется в оксалоацетат NAD-зависимой малатдегидрогеназой.
Слайд 19Восстановленный в ходе этой реакции NAD отдаёт водород в митохондриальную
ЦПЭ.
Однако образованный из малата оксалоацетат выйти самостоятельно из митохондрий
в цитозоль не может, так как мембрана митохондрий для него непроницаема.
Поэтому оксалоацетат превращается в аспартат, который и транспортируется в цитозоль, где снова превращается в оксалоацетат.
В результате происходит регенерация цитоплазматического NAD+ из NADH.
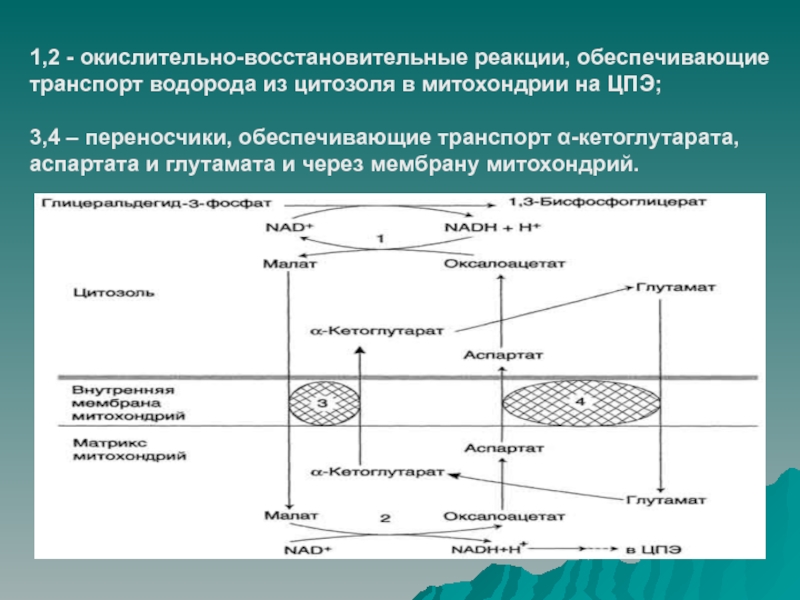
Слайд 201,2 - окислительно-восстановительные реакции, обеспечивающие транспорт водорода из цитозоля в
митохондрии на ЦПЭ;
3,4 – переносчики, обеспечивающие транспорт α-кетоглутарата, аспартата
и глутамата и через мембрану митохондрий.
Слайд 22Транспорт водорода в митохондрии с помощью малат-аспартатной системы позволяет получить
3
молекулы АТФ путем окислительного фосфорилирования.
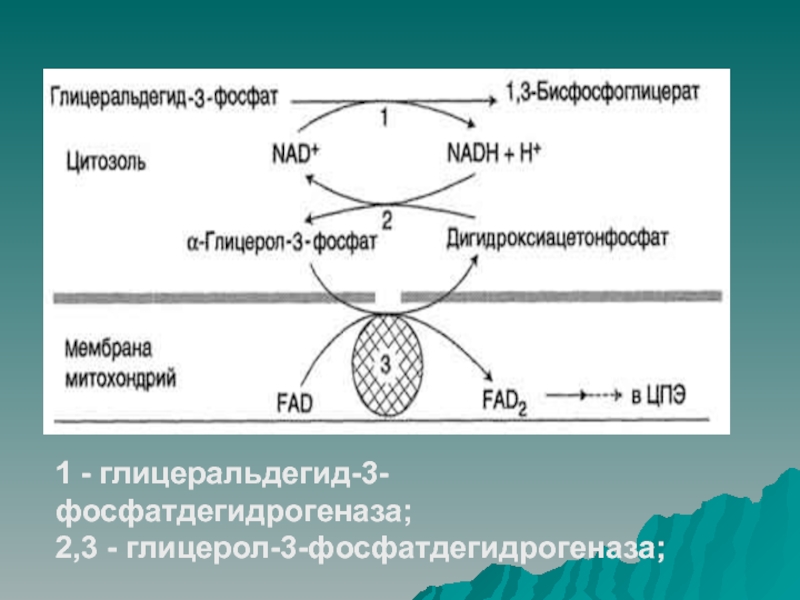
Слайд 23Глицерофосфатная челночная система
Глицерол-3-фосфат поступает в митохондрии и окисляется глицерол-3-фосфатдегидрогеназой
(FAD-зависимым ферментом). NADH является донором водорода для восстановления ДАФ в
глицерол-3-фосфат.
Транспорт водорода в ЦПЭ с помощью этого механизма позволяет синтезировать 2 АТФ путем окислительного фосфорилирования.
Слайд 241 - глицеральдегид-3-фосфатдегидрогеназа;
2,3 - глицерол-3-фосфатдегидрогеназа;
Слайд 25Аэробный распад глюкозы включает реакции аэробного гликолиза, заканчивающиеся образованием 2
молекул пирувата, которые далее превращаются в СО2 и Н2О в
общем пути катаболизма (ОПК) и митохондриальной ЦПЭ. Эти реакции идут в цитоплазме и митохондриях.
Аэробный распад глюкозы – это основной путь катаболизма глюкозы в тканях. Для мозга глюкоза – основной энергетический субстрат.
Слайд 29Анаэробный гликолиз позволяет синтезировать АТФ при недостатке кислорода в тканях,
например, в мышцах в первые минуты мышечных сокращений и в
эритроцитах.
Первые 10 реакций анаэробного и аэробного гликолиза одинаковы, но в отличие от аэробного гликолиза, в анаэробном гликолизе при снижении поступления кислорода в митохондрии NADH, образующийся в результате дегидрирования ГАФ, не может использоваться в ЦПЭ.
Слайд 30NADH окисляется в цитоплазме в реакции, которую катализирует лактатдегидрогеназа (ЛДГ).
Акцептором водорода в этой реакции является пируват, который превращается в
лактат.
Слайд 32
Следовательно, последняя реакция анаэробного гликолиза, катализируемая ЛДГ, обеспечивает регенерацию NAD+,
который необходим для работы глицеральдегидфосфатдегидрогеназы.
АТФ при анаэробном распаде глюкозы
образуется только в двух реакциях субстратного фосфорилирования.
Слайд 33
Образующийся в мышцах и эритроцитах лактат поступает в кровь и
транспортируется в печень, где может превращаться в глюкозу или окисляться
в пируват, который далее включается в ОПК.
Лактат всегда присутствует в крови, но его концентрация может повышаться при снижении поступления кислорода в клетки.
Слайд 35Основное физиологическое назначение катаболизма глюкозы - использование энергии, освобождающейся в
этом процессе для синтеза АТФ.
Аэробный распад глюкозы происходит во
всех органах и тканях и служит основным источником энергии для процессов жизнедеятельности.
Некоторые ткани находятся в наибольшей зависимости от катаболизма глюкозы как источника энергии.
Например, клетки мозга расходуют до 100 г глюкозы в сутки, окисляя её аэробным путём.
!!! Поэтому недостаточное снабжение мозга глюкозой или гипоксия проявляются симптомами, свидетельствующими о нарушении функций мозга (головокружения, судороги, потеря сознания).
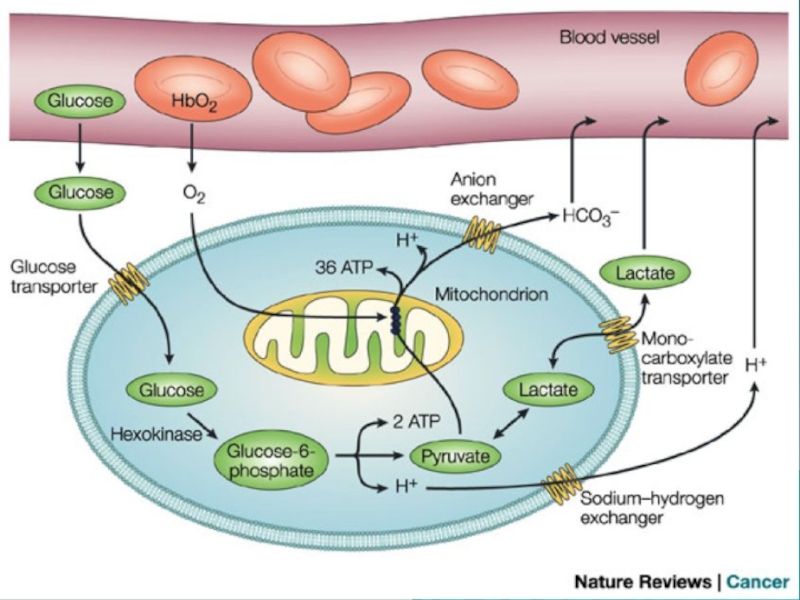
Слайд 36Анаэробный распад глюкозы происходит в мышцах, в эритроцитах, а также
в разных органах в условиях ограниченного снабжении их кислородом, в
том числе и в клетках опухолей.
Для метаболизма клеток опухолей характерно ускорение как аэробного, так и анаэробного гликолиза.
!!! Анаэробный гликолиз и увеличение синтеза лактата служит показателем повышенной скорости деления клеток при недостаточной обеспеченности их системой кровеносных сосудов.
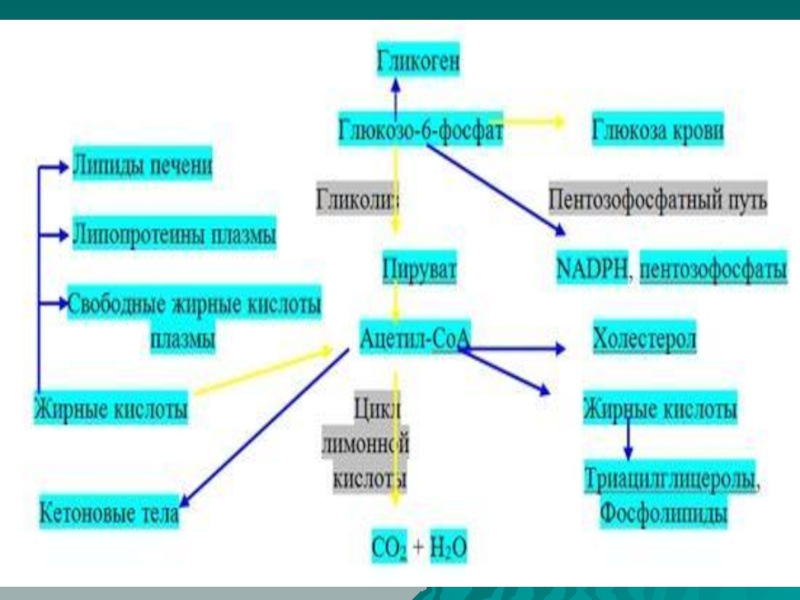
Слайд 37Катаболизм глюкозы может выполнять и анаболические функции. Метаболиты гликолиза используются
для синтеза новых соединений.
Фруктозо-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата
- структурного компонента нуклеотидов;
3-фосфоглицерат может включаться в синтез аминокислот (серин, глицин, цистеин).
В печени и жировой ткани ацетил-КоА, образующийся из пирувата, используется как субстрат при биосинтезе жирных кислот, холестерина, а ДАФ (дигидроксиацетонфосфат) как субстрат для синтеза глицерол-3-фосфата.
Слайд 39Скорость гликолиза коррелирует с затратами энергии в организме.
Большинство реакций
гликолиза обратимы, за исключением трёх, катализируемых гексокиназой (или глюкокиназой), фосфофруктокиназой
и пируваткиназой.
Регуляторные факторы, изменяющие скорость гликолиза, направлены на необратимые реакции.
Показателем потребления АТФ является накопление АДФ и АМФ.
Последний образуется в реакции, катализируемой аденилаткиназой:
2 АДФ ↔ АМФ + АТФ
Скорость гликолиза коррелирует с затратами энергии в организме.
Большинство реакций гликолиза обратимы, за исключением трёх, катализируемых гексокиназой (или глюкокиназой), фосфофруктокиназой и пируваткиназой.
Регуляторные факторы, изменяющие скорость гликолиза, направлены на необратимые реакции.
Показателем потребления АТФ является накопление АДФ и АМФ.
Последний образуется в реакции, катализируемой аденилаткиназой:
2 АДФ ↔ АМФ + АТФ
Скорость гликолиза коррелирует с затратами энергии в организме.
Большинство реакций гликолиза обратимы, за исключением трёх, катализируемых гексокиназой (или глюкокиназой), фосфофруктокиназой и пируваткиназой.
Регуляторные факторы, изменяющие скорость гликолиза, направлены на необратимые реакции.
Показателем потребления АТФ является накопление АДФ и АМФ.
Последний образуется в реакции, катализируемой аденилаткиназой:
2 АДФ ↔ АМФ + АТФ
Скорость гликолиза коррелирует с затратами энергии в организме.
Большинство реакций гликолиза обратимы, за исключением трёх, катализируемых гексокиназой (или глюкокиназой), фосфофруктокиназой и пируваткиназой.
Регуляторные факторы, изменяющие скорость гликолиза, направлены на необратимые реакции.
Показателем потребления АТФ является накопление АДФ и АМФ.
Последний образуется в реакции, катализируемой аденилаткиназой:
2 АДФ ↔ АМФ + АТФ

Слайд 40Отношение уровня АТФ к АДФ и АМФ характеризует энергетический статус
клетки,
а его составляющие служат аллостерическими регуляторами скорости как общего
пути катаболизма, так и гликолиза.
Слайд 41Существенное значение для регуляции гликолиза имеет изменение активности фосфофруктокиназы как
фермента самой медленной реакции.
Фосфофруктокиназа активируется АМФ, но ингибируется АТФ.
АМФ,
связываясь с аллостерическим центром фосфофруктокиназы, увеличивает сродство фермента к фруктозо-6-фосфату и повышает скорость его фосфорилирования. АТФ может взаимодействовать как с аллостерическим, так и с активным центром фермента, в последнем случае как субстрат.
Слайд 42При физиологических значениях АТФ активный центр фосфофруктокиназы всегда насыщен субстратами
(в том числе АТФ).
Повышение уровня АТФ относительно АДФ снижает
скорость реакции, поскольку АТФ в этих условиях действует как ингибитор: связывается с аллостерическим центром фермента, вызывает конформационные изменения и уменьшает сродство к его субстратам.
Слайд 43Изменение активности фосфофруктокиназы способствует регуляции скорости фосфорилирования глюкозы гексокиназой.
Снижение
активности фосфофруктокиназы при высоком уровне АТФ ведёт к накоплению как
фруктозо-6-фосфата, так и глюкозо-6-фосфата, а последний ингибирует гексокиназу.
Гексокиназа во многих тканях (за исключением печени и β-клеток поджелудочной железы) ингибируется глюкозо-6-фосфатом.
Слайд 44При высоком уровне АТФ снижается скорость цикла лимонной кислоты и
дыхательной цепи.
В этих условиях процесс гликолиза также замедляется.
Аллостерическая
регуляция ферментов ОПК и дыхательной цепи также связана с изменением концентрации NADH, АТФ и некоторых других метаболитов.
Слайд 45NADH если не успевает окислиться в дыхательной цепи ингибирует аллостерические
ферменты цитратного цикла.
В печени и жировой ткани гликолиз в
период пищеварения функционирует в основном как источник субстратов для синтеза жиров.
Слайд 46В процессе гликолиза может протекать реакция превращения 1,3-бисфосфоглицерата в 2,3-бисфосфоглицерат
(2,3-БФГ) под действием бисфосфоглицератмутазы. 2,3-БФГпри участии 2,3-бисфосфоглицератфосфатазы превращаться в -фосфоглицерат.
Слайд 47В большинстве тканей 2,3-БФГ образуется в небольших количествах.
Но в
эритроцитах этот метаболит образуется в значительных количествах и выполняет роль
аллостерического регулятора функции гемоглобина.
2,3-БФГ, связываясь с гемоглобином, понижает его сродство к кислороду, способствует диссоциации кислорода и переходу его в ткани.
Слайд 48ПЕНТОЗОФОСФАТНЫЙ
ПУТЬ ПРЕВРАЩЕНИЯ
ГЛЮКОЗЫ
Слайд 49Глюкозо-6-фосфат может включаться в реакции пентозофосфатного пути.
В этом процессе
образуется рибозо-5-фосфат, необходимый для синтеза нуклеотидов, и восстанавливается кофермент NADP+.
NADPН является донором водорода в реакциях восстановления при синтезе жирных кислот, холестерола, стероидных гормонов, инактивации чужеродных веществ и обезвреживании активных форм кислорода.
Слайд 50Реакции этого метаболического пути идут в большинстве тканей, но наиболее
активно в печени, жировой ткани, эритроцитах.
Все реакции этого метаболического
пути идут в цитоплазме клеток и их можно разделить на два этапа:
окислительный
неокислительный
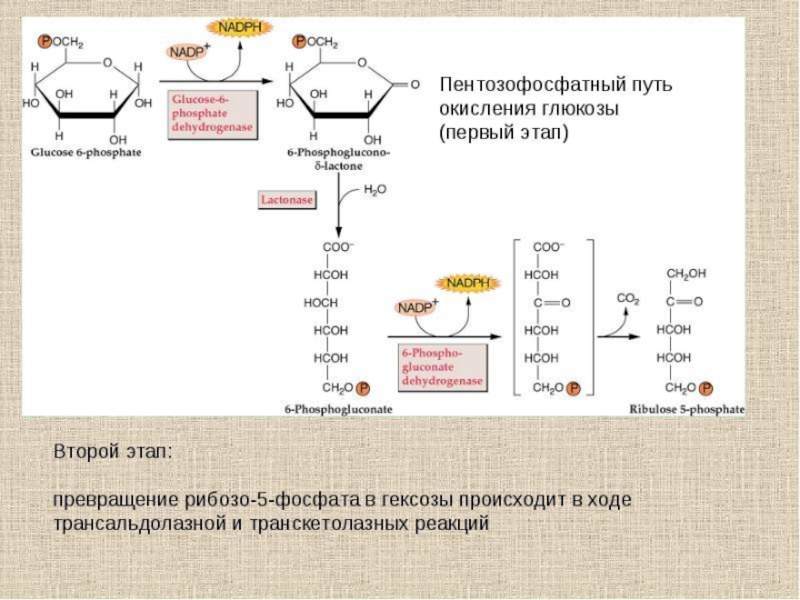
Слайд 51превращение глюкозо-6-фосфата в 6-фосфоглюконолактон, катализируется NADP+-
зависимой глюкозо-6-фосфатдегидрогеназой и сопровождается окислением
альдегидной группы у первого атома углерода и образованием NADPН.
2. превращение
6-фосфоглюконолактона в 6-фосфоглюконат под действием фермента глюконолактонгидратазы.
3. окислительное декарбоксилирование 6-фосфоглюконата с образованием пентозы рибулозо-5-фосфата и NADPН. Реакцию катализирует NADP+-зависимая 6-фосфоглюконат дегидрогеназа.
Слайд 52Окислительный этап включает три реакции,
две из которых являются ОВР
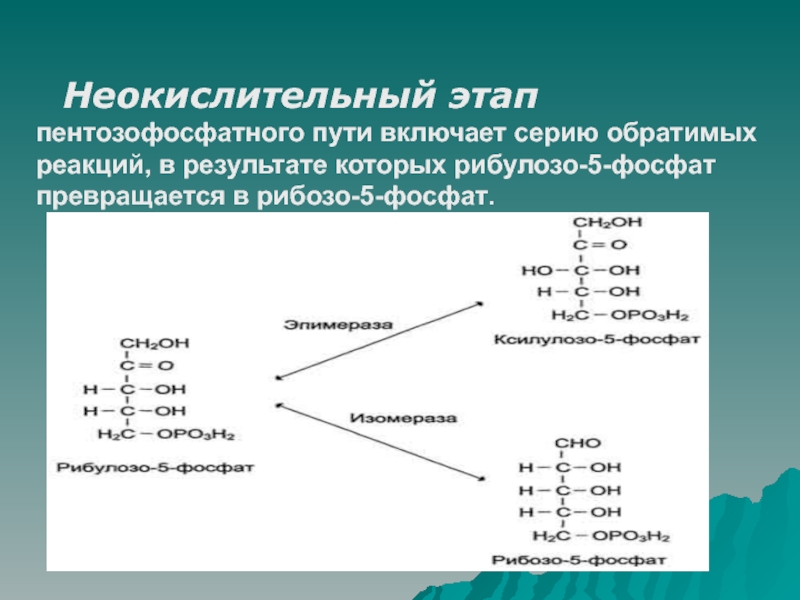
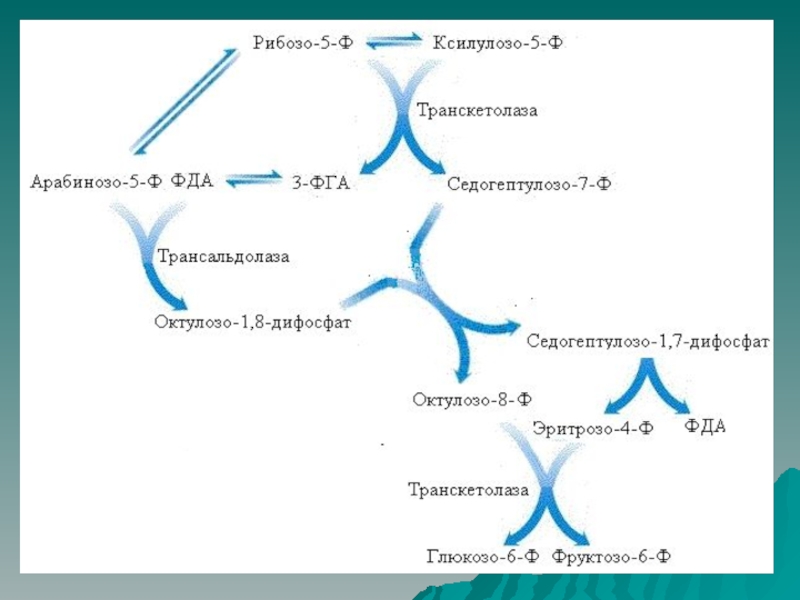
Слайд 53Неокислительный этап пентозофосфатного пути включает серию обратимых реакций, в результате
которых рибулозо-5-фосфат превращается в рибозо-5-фосфат.
Слайд 54Промежуточные метаболиты гликолиза фруктозо-6-фосфат и глицеральдегид-3-фосфат, включаясь в реакции неокислительного
пути, могут служить субстратами для синтеза рибозо-5-фосфата.
Вследствие обратимости реакций
пентозофосфатного пути молекулы рибозо-5-фосфата могут превращаться в глицеральдегид-3-фосфат и фруктозо-6-фосфат, дальнейший катаболизм которых происходит в гликолизе и ОПК.
Слайд 55Если в реакции пентозофосфатного пути вступают 6 молекул глюкозо-6-фосфата, то
на окислительном этапе образуются 6 молекул рибулозо-5-фосфата и 6 молекул
СО2.
Дальнейшее превращение 6 молекул рибулозо-5-фосфата на неокислительном этапе заканчивается образованием 5 молекул фруктозо-6-фосфата, которые под действием фосфоглюкоизомеразы могут превращаться в 5 молекул глюкозо-6-фосфата.
6 Глюкозо-6-фосфат + 12 NADP+ + 2 Н2О →
5 Глюкозо-6-фосфат + 12 NADPH +Н+ + 6 СO2