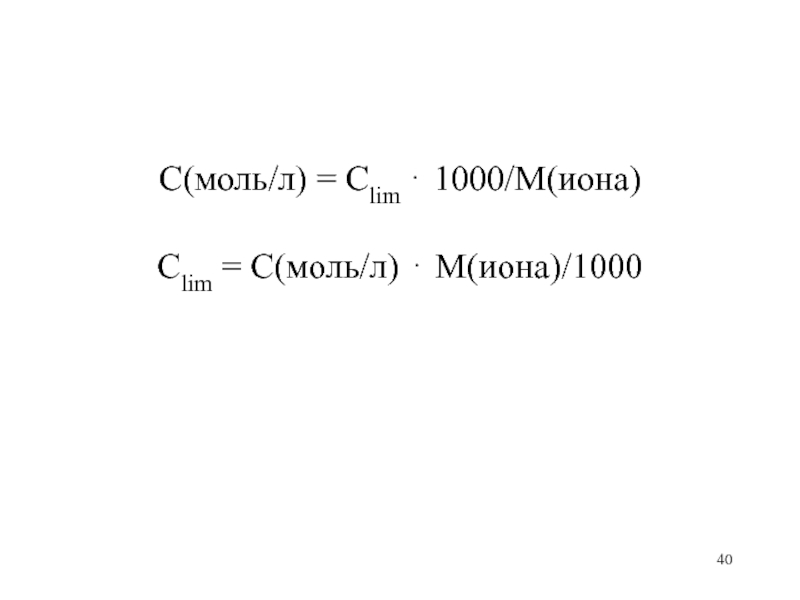Слайд 3Аналитическая химия. Аналитика 1. Общие теоретические основы. Качественный анализ [Электронный ресурс]
/ Харитонов Ю.Я. - М. : ГЭОТАР-Медиа, 2014. - http://www.studmedlib.ru/book/ISBN9785970429341.html
Аналитическая химия. Аналитика 2. Количественный анализ. Физико-химические (инструментальные) методы анализа [Электронный ресурс] / Ю.Я. Харитонов - М. : ГЭОТАР-Медиа, 2014. - http://www.studmedlib.ru/book/ISBN9785970429419.html
Слайд 5Консультант студента
Аналитическая химия. Практикум [Электронный ресурс] / Харитонов Ю.Я., Григорьева В.Ю.
- М. : ГЭОТАР-Медиа, 2009. http://www.studmedlib.ru/book/ISBN9785970413852.html
Аналитическая химия. Качественный анализ. Титриметрия.
Сборник упражнений [Электронный ресурс] : учебное пособие / Ю.Я. Харитонов, Д.Н. Джабаров - М. : ГЭОТАР-Медиа, 2015. http://www.studmedlib.ru/book/ISBN9785970432723.html
Аналитическая химия. Количественный анализ. Физико-химические методы анализа: практикум [Электронный ресурс] : учебное пособие / Харитонов Ю.Я., Джабаров Д.Н., Григорьева В.Ю. - М. : ГЭОТАР-Медиа, 2012. - http://www.studmedlib.ru/book/ISBN9785970421994.html
Слайд 6
Аналитическая служба это сервисная система, обеспечивающая конкретный анализ определенного
объекта с исполь-зованием методов, рекомендуемых анали-тической химией.
Слайд 7 Аналитическая химия это наука об определении химического состава веществ
и отчасти их химического строения.
Методы аналитической химии позволяют отвечать
на вопрос о том, из чего состоит вещество, какие компоненты входят в его состав и в каком количестве. Иногда можно оценить пространственное расположение этих компонентов.
Слайд 8
Про аналитическую химию говорят, что это наука о методах и
средствах химического анализа и в известной мере установления химического строения.
Под средствами подразумеваются приборы, реактивы, стандартные образцы, компьютерные программы и т.д.
Слайд 9
Под химическим анализом понимается совокупность действий, имеющих своей целью получение
информации о химическом составе объекта. В зависимости от поставленной задачи,
выделяют элементный, фазовый, молекулярный анализ и т.д.
Слайд 10
Под методом анализа понимается достаточно универсальный и теоретически обоснованный способ
определения состава безотносительно к определяемому компо-ненту и к анализируемому объекту.
Слайд 11
Когда говорят о методе анализа, то имеют в виду принцип,
положенный в его основу, количественное выражение связи между составом и
каким-либо измеряемым свойством, отработанные приемы осу-ществления, устройства для практической реализации и способы обработки резуль-татов измерений.
Слайд 12
Методика анализа подробное описание анализа данного объекта с использованием
выбранного метода.
Слайд 13
«Методика спектрофотометрического определения левомицетина в таблетках левомицетина»
Метод - спектрофотометрия
Объект – таблетки левомицетина
Анализируемый компонент - левомицетин
Слайд 14 «Гравиметрический метод анализа»
В основу гравиметрического метода анализа положено определение
массы соединения, содержащего определяемый компонент.
В методику гравиметрического опреде-ления компонента
входят: описание условий осаждения этого малорастворимого соеди-нения, способ отделения осадка от раствора, перевод осажденного вещества в удобную для взвешивания форму и т.д.
Слайд 15
В методику вводят также описание операций отбора пробы и подготовки
ее к анализу, например, растворение образца в подходящем растворителе и
устранение влияния веществ, мешающих опреде-лению.
Слайд 16Классификации методов аналитической химии
* Классификация по видам анализа
* Классификация, основанная
на масштабе работы, объеме или массе пробы
* Классификация, основанная на
природе обнаруживаемых частиц.
Слайд 17Классификация по видам анализа:
- Качественный анализ и количественный анализ
- Деструктивный
анализ и недеструктивный анализ
- Валовый анализ и локальный анализ
- Контактный
анализ и дистанционный анализ
Слайд 18
Качественный и количественный анализ
Качественный анализ неорганических веществ основан на обнаружении
катионов и анионов, путем проведения дробного или систематического анализа.
Слайд 19 В дробном анализе катионы и анионы обнаруживаются специфическими реаген-тами в
присутствии всех остальных компо-нентов анализируемой пробы.
Систематический анализ предусматривает разделение
смеси анализируемых ионов на аналитические группы с последующим обнаружением каждого иона внутри выде-ленной группы.
Слайд 20Классификации катионов по группам:
- сульфидная (сероводородная)
- аммиачно-фосфатная
-
кислотно-основная.
Классификация анионов по группам основана:
- на способности к
образованию малораство-
римых соединений
- на окислительно-восстановительных свой-
ствах.
Слайд 21 Качественный анализ органических соединений основан на обнаружении функциональных групп (-COOH,
-OH, -NH2 и т.д.) соответствующими аналитическими реагентами и реакциями.
Количественный
анализ включает гравиметрический и титриметрические методы анализа.
Слайд 22
Отдельной позицией выделены инструментальные методы анализа (оптические, хроматографические, электро-химические и
т.д.).
Инструментальные методы анализа позволяют проводить как качественный, так и
количественный анализ.
Слайд 23Классификация, основанная на масштабе работы, объеме или массе пробы
Вид анализа
Масса пробы, г
Объем раствора, мл
Макроанализ 0,1 10 – 103
Полумикроанализ 0,01 – 0,1 101 10
Микроанализ 0,01 102 1
Субмикроанализ 104 103 102
Ультрамикроанализ 104 103
Слайд 24Классификация, основанная на природе обнаруживаемых частиц
- Элементный анализ
-
Изотопный анализ
- Функциональный анализ
- Вещественный анализ
- Молекулярный анализ
- Фазовый анализ
Слайд 25 Фармацевтический анализ определение качества лекарственных средств, выпускаемых фармацевтической промышленностью
и аптечными учреждениями.
Фармакопейные методы - методы, описанные в фармакопейных
статьях или включенные в Государственную Фармакопею сборник обязательных общегосударственных стандартов и положений, нормирующих качество лекарственных средств.
Разные страны имеют свои собственные Фармакопеи.
Слайд 27
Аналитические признаки веществ
и
аналитические реакции
Слайд 28Аналитические признаки свойства анализируемого вещества, которые позволяют судить о
наличии в нем тех или иных компонентов (цвет, запах, угол
вращения плоскости поляризации света, способность к взаимодействию с элек-тромагнитным излучением, в результате чего появляются полосы поглощения в ультрафиолетовой, инфракрасной и видимой областях спектра).
Слайд 29Аналитическая реакция реакция, в результате которой образуется вещество с
аналитическими признаками (реакции образования осадка, окрашенного раство-ра, выделения пузырьков газа,
окраши-вания бесцветного пламени газовой горелки, образования соединений, люминисцирующих в растворе).
Протекание аналитической реакции зависит от температуры, концентрации растворов, рН среды, присутствия веществ, мешающих, маскирующих или катализирующих протека-ние реакции.
Слайд 30
Чувствительность
аналитических реакций
Слайд 31 Предельное разбавление Vlim –максимальный объем раствора, в котором данной аналитической
реакцией может быть обнаружен 1 г вещества, мл/г.
Предельная концентрация Clim
– наименьшая концентрация вещества, которая может быть обнаружена данной аналитической реакцией, г/мл.
Слайд 32
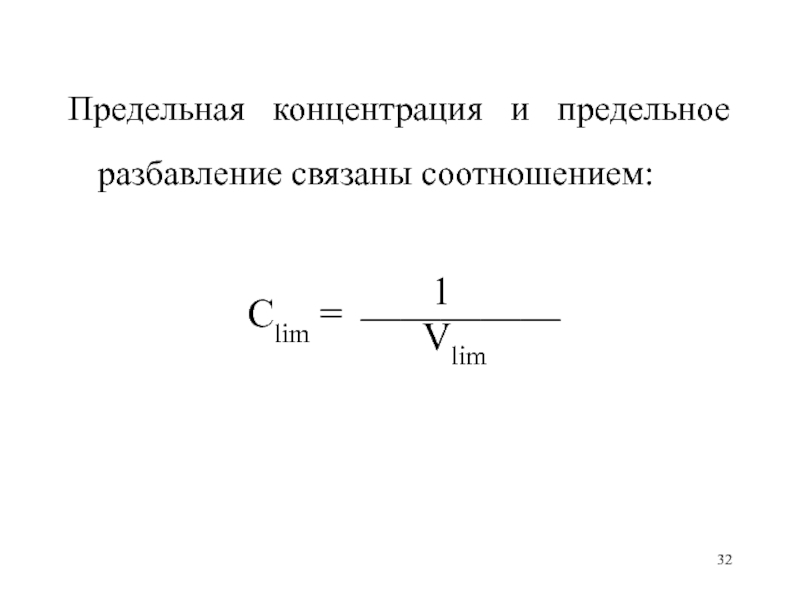
Предельная концентрация и предельное разбавление связаны соотношением:
1
Clim =
Vlim
Слайд 33 Минимальный объем предельно раз-бавленного раствора Vmin – наименьший объем раствора,
необходимый для обнаружения вещества данной аналити-ческой реакцией, мл.
Открываемый минимум (предел
обнаружения) m – наименьшая масса вещества, которую можно открыть в минимальном объеме предельно разбав-ленного раствора, мкг
(1мкг = 10-6 г).
Слайд 34 Предел обнаружения связан с предельной концентрацией и минималь-ным объемом предельно
разбавленного раствора соотношениями:
m = Clim Vmin
или
Vmin
m =
Vlim
Слайд 35 Аналитическая реакция тем чувствительнее, чем меньше ее откры-ваемый минимум, минимальный
объем предельно разбавленного раствора и чем больше предельное разбавление.
Чувствительность
аналитических реакций зависит от природы откры-ваемого вещества и аналитического реагента, температуры, рН среды, присутствия других веществ.
Слайд 36Задача 1.
Предел обнаружения катионов калия тетрафенилборатом натрия равен 1 мкг,
предельное разбавление - 5104 мл/г. Рассчитайте предельную концентрацию катионов калия
и минимальный объем предельно разбавленного раствора.
Слайд 37Дано: m = 1 мкг = 1·10–6
г
Vlim
= 5·104 мл/г
Сlim = ? Vmin = ?
Решение:
Clim = 1/ Vlim = 1/5·104 = 210-5 (г/мл)
m = Vmin / Vlim
Vmin = m Vlim = 1·10–6 · 5·104 = 0,05 (мл)
Ответ: 210-5г/мл; 0,05 мл.
Слайд 38 Задача 2.
При обнаружении катионов кальция оксалат-ионами, минимальный объем предельно разбавленного
раствора равен 0,01 мл, предел обнаружения 0,04 мкг. Рассчитайте минимальную
молярную концентрацию катионов кальция.
Слайд 39Дано: Vmin = 0,01 мл
m = 0,04 мкг = 0,04·10–6 г
С(моль/л) = ?
Решение:
m = Clim Vmin
Clim = m/Vmin = 0,04·10–6/0,01 = 4·10–6 г
С(моль/л) = Clim 1000/М(иона)
С(моль/л) = 4·10–6 1000/40 = 1·10–4
Ответ: 1·10–4 моль/л.
Слайд 40
С(моль/л) = Clim 1000/М(иона)
Clim = С(моль/л) М(иона)/1000


![1
Аналитическая химия Аналитическая химия. Аналитика 1. Общие теоретические основы. Качественный анализ [Электронный ресурс] / Аналитическая химия. Аналитика 1. Общие теоретические основы. Качественный анализ [Электронный ресурс] / Харитонов Ю.Я. - М. : ГЭОТАР-Медиа,](/img/tmb/4/326495/b78b941a77d0abbf9522edfb6563ae0c-800x.jpg)

![1
Аналитическая химия Консультант студентаАналитическая химия. Практикум [Электронный ресурс] / Харитонов Ю.Я., Григорьева В.Ю. - Консультант студентаАналитическая химия. Практикум [Электронный ресурс] / Харитонов Ю.Я., Григорьева В.Ю. - М. : ГЭОТАР-Медиа, 2009. http://www.studmedlib.ru/book/ISBN9785970413852.html Аналитическая химия.](/img/thumbs/e7ffef589b7711c9123256562abd1137-800x.jpg)