Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
8 лекция МНС, ИД.ppt
Содержание
- 1. 8 лекция МНС, ИД.ppt
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
- 5. Слайд 5
- 6. Слайд 6
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
- 17. МНС-сем. Генов, кодирующих молекулы 3 классов.
- 18. HLA антигены I класса представлены на
- 19. Гены II класса - на клетках
- 20. Слайд 20
- 21. Слайд 21
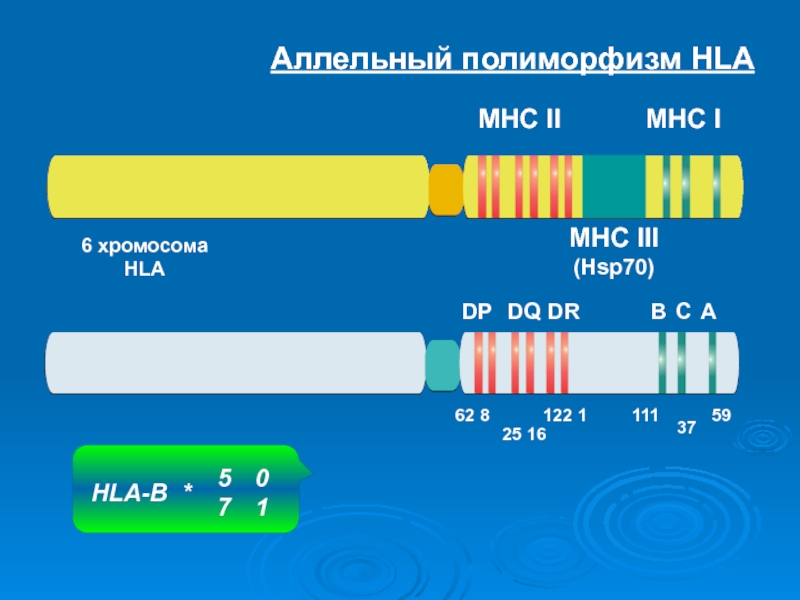
- 22. Расположение комплекса генов HLA на 6 хромосоме человека
- 23. Слайд 23
- 24. Слайд 24
- 25. astronaut
- 26. Презентация антигеновЭкзогенные белки попадают в клетку извне
- 27. MHC II MHC IМолекулы гистосовместимости (MHC)
- 28. Презентация антигенов с участием MHC IНаличие костимулирующих
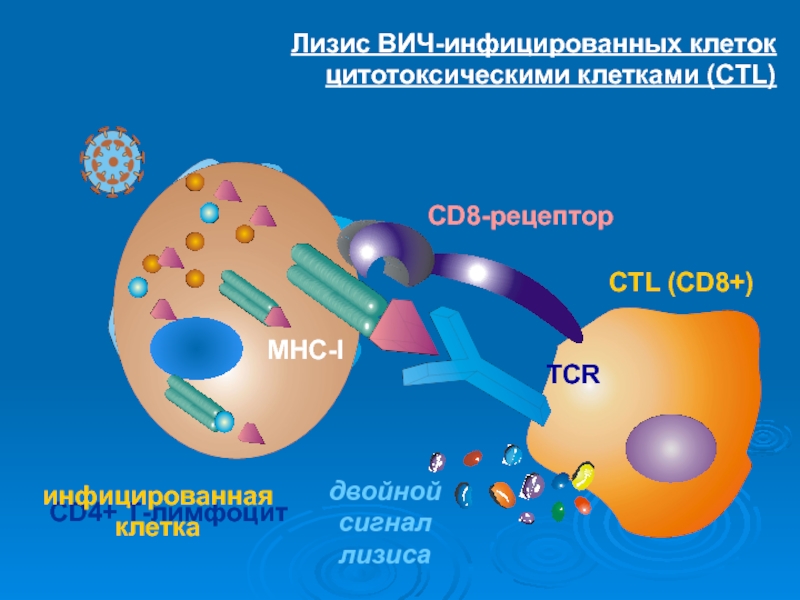
- 29. Лизис ВИЧ-инфицированных клеток цитотоксическими клетками (CTL)MHC-Iдвойной сигнал лизиса
- 30. Активация CD4+ Т-клетокдвойной сигнал активацииMHC-II
- 31. Установлена
- 32. Определение
- 33. Аллельный полиморфизм HLA6 хромосомаHLAMHC IIMHC IHLA-B*5701
- 34. «вредные» аллели HLA-B*27- анкилозирующий спондилит и синдром
- 35. Иммуногенетика ВИЧ-инфекции: «полезные» и «вредные» аллелиIL10-5*-592AKIR2DS2 KIR3DS1
- 36. Слайд 36
- 37. ИД
- 38. Лица с
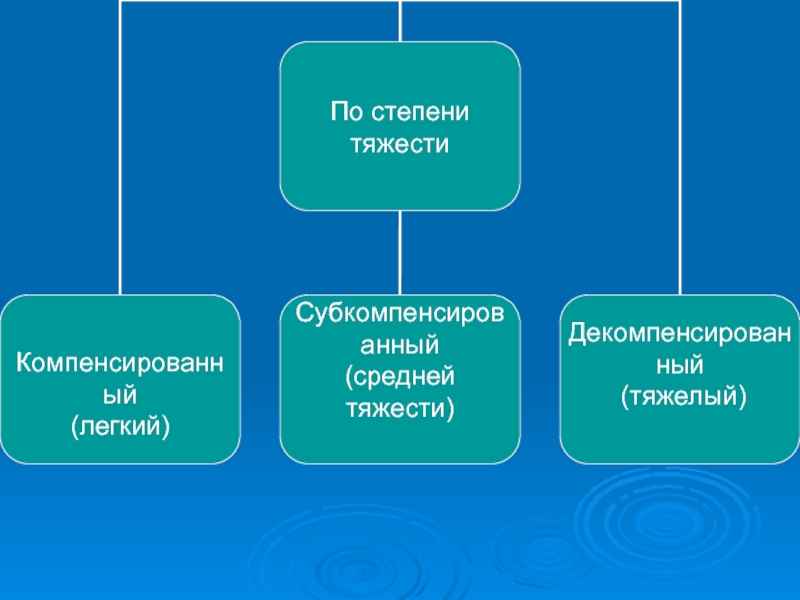
- 39. Классификация ИД
- 40. Первичные
- 41. Первичные иммунодефициты проявляются на ранних этапах постнатального периода, наследуются по аутосомно-рецессивному
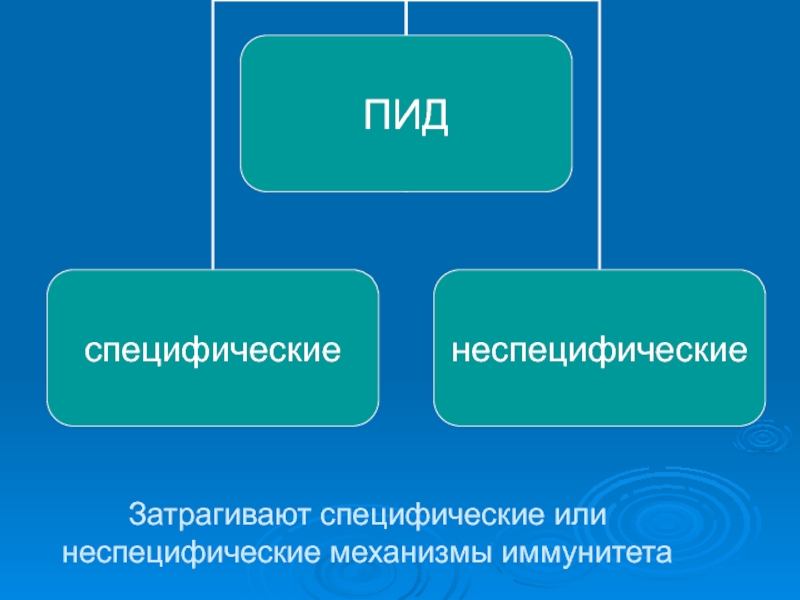
- 42. Затрагивают специфические или неспецифические механизмы иммунитета
- 43. Причины
- 44. Основные
- 45. Недостаточность
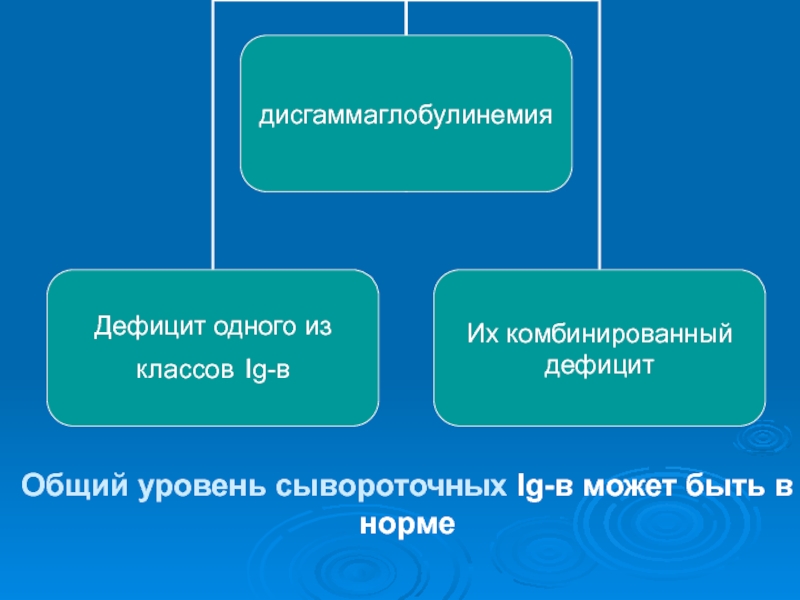
- 46. Общий уровень сывороточных Ig-в может быть в норме
- 47. Слайд 47
- 48. Слайд 48
- 49. Нарушен иммунитет: - противовирусный - противогрибковый - противоопухолевый - трансплантационный
- 50. Комбинированные
- 51. дефицит системы
- 52. Недостаточность
- 53. Слайд 53
- 54. Слайд 54
- 55. Вторичный иммунодефицит - нарушение
- 56. особенности ВИД Нарушения в ИС вторичны, возникают
- 57. Классификация ВИД (Мешкова Р.Я. С соавт.)
- 58. Слайд 58
- 59. Слайд 59
- 60. Слайд 60
- 61. Причины развития ВИДПротозойные инвазии и гельминтозы (малярия,
- 62. Причины развития ВИДСостояния с потерей ИК клеток
- 63. Признаки ИДРецидивирующие бактериально-вирусные инфекции, характеризующиеся- хроническим течениемНеполным
- 64. Признаки ИДКандидоз слизистой полости рта- Врожденные пороки
- 65. Первичные клеточные мишени ВИЧ-1 - клетки
- 66. 050100150Время полужизни (дни) Свободные вирусные частицыИнфицированные макрофагиПродуктивно
- 67. Слайд 67
- 68. Слайд 68
- 69. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
ГБОУ ВПО «ТИХООКЕАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ» МЗ РФ
Кафедра микробиологии
и вирусологии
д.м.н., проф. Шаркова В. А.Слайд 2
Главный комплекс
гистосовмесгимости - ГКГС (Major Histocompatibility Complex) - участок
хромосомы, образованный генетическими локусами, ответственными за отторжение чужеродных (т.е. отличных от своих) тканейСлайд 3
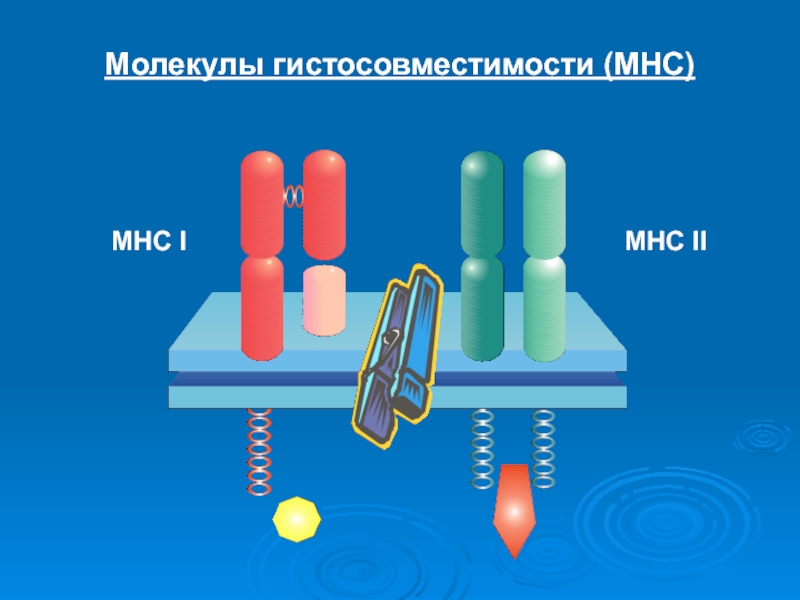
МНС составляют гликопротеины
– мембранные гликопротеиновые рецепторы, присутствующие на поверхности всех клеток организма. Они
обеспечивают распознавание «своего и чужого»Слайд 4
Несовпадение этих гликопротеинов
между трансплантатами и клетками реципиента
приводит к развитию иммунного ответа
Слайд 5
Молекулы МНС проявляют
свойства антигенов, поэтому их называют антигенами гистосовместимости, а кодирующие их
гены – генами гистосовместимостиСлайд 6
Human Leukocyti Antigens
(HLA): – антигены лейкоцитов человека - МНС человека - данный комплекс генов
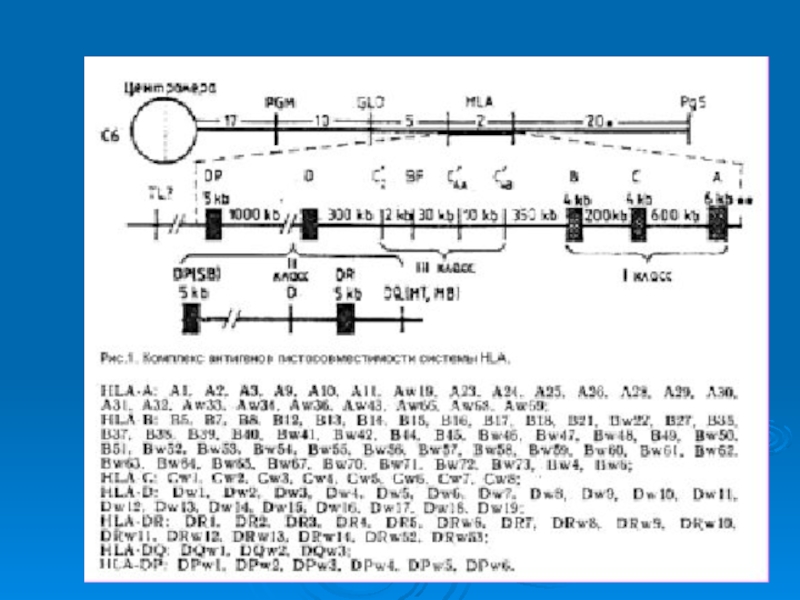
локализован в 6 хромосомеСлайд 7
Размеры комплекса HLA
позволяют разместить 105-106 генов, что составляет 1/1000 часть всего генофонда
человека. HLA антигены I класса занимают не более 1% клеточной поверхностиСлайд 8
Эти молекулы проявляют
антигенность когда распознаются иммунной системой не собственного, а генетически иного
организма (напр., при аллотрансплантации органов)Слайд 9
В естественной природе
нет процессов трансплантации тканей отдельных особей во внутреннюю среду других
особейСлайд 10
Зачем нужны эти
гены и продукты, ими кодируемые, организмам, которым не пересаживают и
никогда не будут пересаживать чужие органы?Слайд 11
Р. Цинкернагель и
П. Дохерти открыли природные функции белков МНС (1973-1974гг.): - представлять для
распознавания пептидные антигены для Т-лимфоцитовСлайд 12
Важнейшие биологические функции
системы ГКГС (или системы HLA): участвует - в распознавании бактерий и
вирусов - в реакции на трансплантационные антигены - во взаимодействии иммунокомпетентных клеток в ходе развития клеточного и гуморального ИО - в генетическом контроле активности системы С′ - осуществляет генетический контроль за уровнем некоторых гормонов - осуществляет генетический контроль за процессом размножения и развития - осуществляет генетический контроль за взаимодействием между любыми, а не только иммунокомпетентными клеткамиСлайд 13
Гены HLA системы
контролируют образование трансплантационных антигенов Наибольшее их количество представлено на лимфоцитах, в
коже, меньше – в легких, печени, кишечнике, сердце, еще меньше – в мозге. Они обнаружены на поверхности ядросодержащих клеток, тромбоцитовСлайд 15
Интенсивность, продолжительность и
исход иммунологического конфликта (реакции отторжения) определяются: - системой антигенных различий между
донором и реципиентом - уровнем иммунной реактивности реципиента – характером трансплантата - наличием в нем лимфоидной ткани - удельным содержанием антигенов гистосовместимостиСлайд 17
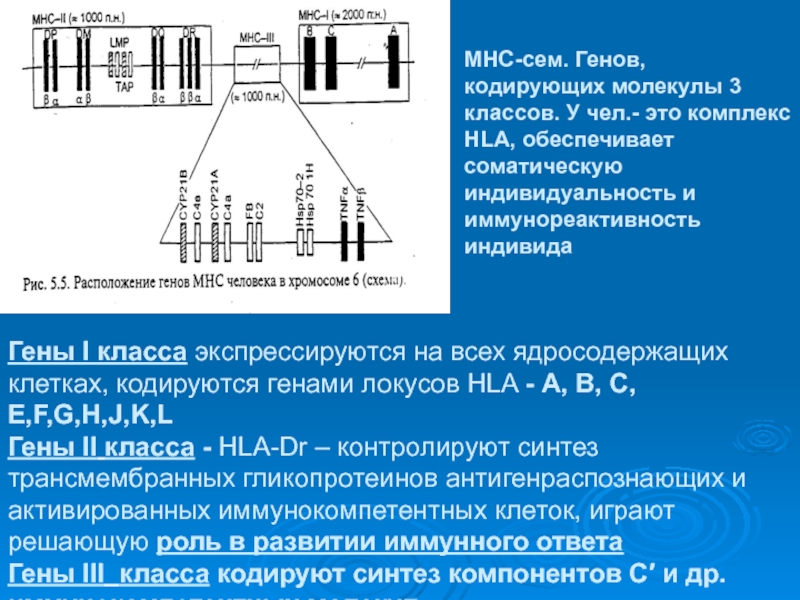
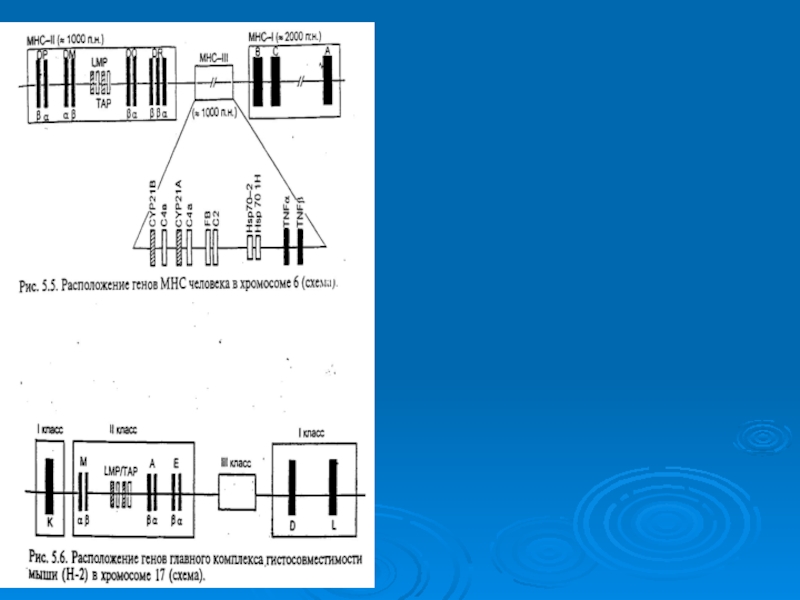
МНС-сем. Генов, кодирующих молекулы 3 классов. У чел.- это
комплекс HLA, обеспечивает соматическую индивидуальность и иммунореактивность индивида
Гены I класса
экспрессируются на всех ядросодержащих клетках, кодируются генами локусов HLA - А, В, С, E,F,G,H,J,K,LГены II класса - HLA-Dr – контролируют синтез трансмембранных гликопротеинов антигенраспознающих и активированных иммунокомпетентных клеток, играют решающую роль в развитии иммунного ответа
Гены III класса кодируют синтез компонентов С′ и др. иммунокомпетентных молекул
Слайд 18
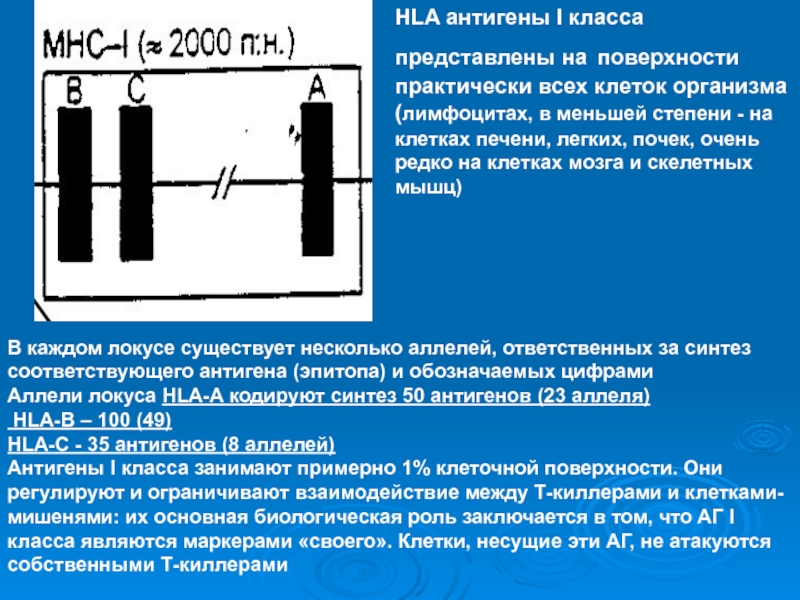
HLA антигены I класса представлены на поверхности практически всех
клеток организма (лимфоцитах, в меньшей степени - на клетках печени,
легких, почек, очень редко на клетках мозга и скелетных мышц)В каждом локусе существует несколько аллелей, ответственных за синтез соответствующего антигена (эпитопа) и обозначаемых цифрами
Аллели локуса HLA-A кодируют синтез 50 антигенов (23 аллеля)
HLA-B – 100 (49)
HLA-C - 35 антигенов (8 аллелей)
Антигены I класса занимают примерно 1% клеточной поверхности. Они регулируют и ограничивают взаимодействие между Т-киллерами и клетками-мишенями: их основная биологическая роль заключается в том, что АГ I класса являются маркерами «своего». Клетки, несущие эти АГ, не атакуются собственными Т-киллерами
Слайд 19
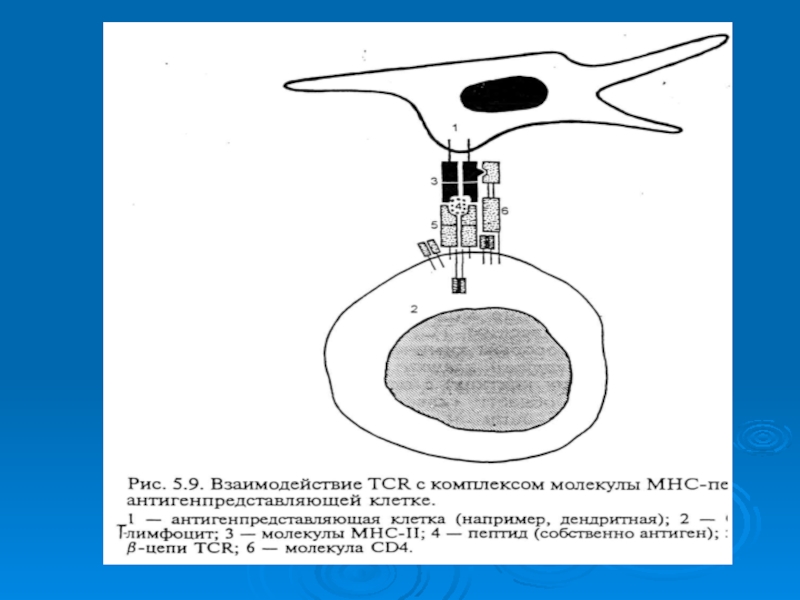
Гены II класса - на клетках иммунной системы, макрофагах,
эпителиальных клетках (презентация)
HLA-Dr экспрессированы на В-лимфоцитах, макрофагах, активированных клетках после
стимуляции их g-интерферономГены, контролирующие антигены II класса, представлены локусами: HLA-DR, HLA-DQ, HLA-DP, -DМ, ТАР (процессинг)
Локус DR α, β состоит из 2-137 генов (16 ал), локус DQ – 16-25 (3), локус DP – 8-66 (6). HLA-АГ II класса участвуют в распознавании чужеродных антигенов, в межклеточных взаимодействиях В-лимфоцитов и макрофагов с Т-хелперами
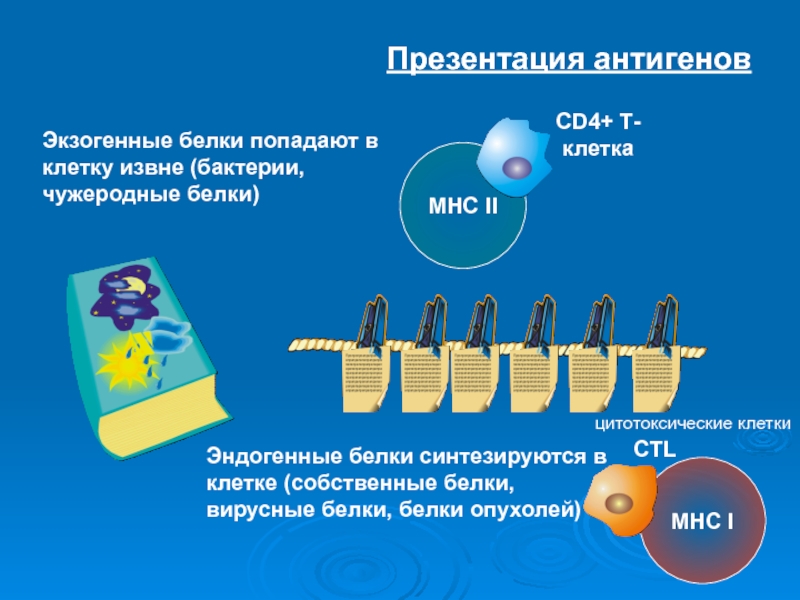
Слайд 26Презентация антигенов
Экзогенные белки попадают в клетку извне (бактерии, чужеродные белки)
Эндогенные
белки синтезируются в клетке (собственные белки, вирусные белки, белки опухолей)
MHC
IICD4+ Т-клетка
цитотоксические клетки
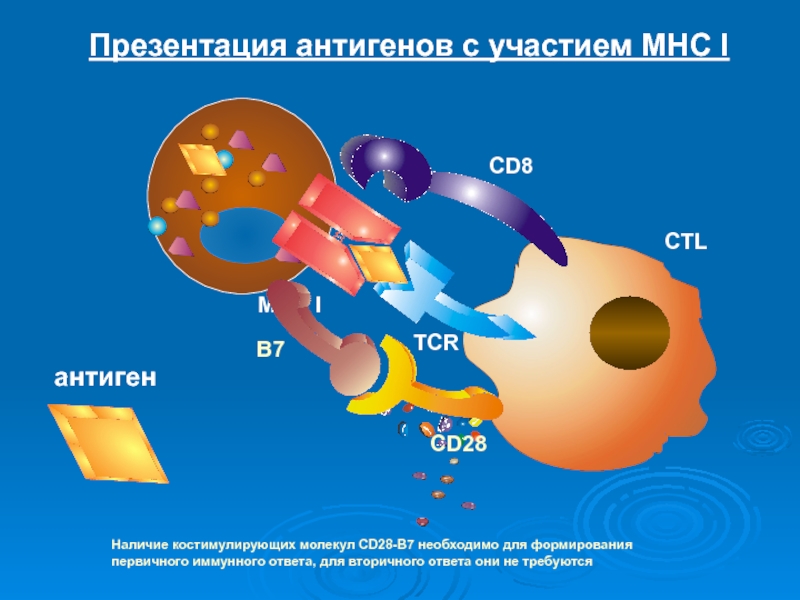
Слайд 28Презентация антигенов с участием MHC I
Наличие костимулирующих молекул CD28-B7 необходимо
для формирования первичного иммунного ответа, для вторичного ответа они не
требуютсяСлайд 31
Установлена зависимость:
- силы ИО на различные АГ от
HLA фенотипа - связей иммунологических показателей с генетическими маркерами от рас,
национальностей и др. - определенные HLA –антигены ассоциируются с некоторыми болезнями - тяжесть течения заболевания от антигенов гистосовместимостиСлайд 32
Определение HLA-антигенов необходимо:
- при типировании тканей с целью подбора
донора реципиенту имеет значение совместимость по антигенам локуса HLA-DR; для
установления связи экспрессии определенных антигенов и предрасположенности к тому или иному заболеванию - при оценке иммунного статуса, когда используется выявление активированных Т-клеток, несущих HLA-DR антигены, и определение HLA-DR экспрессирующих мононуклеаров, участвующих в распознавании антигеновСлайд 34«вредные» аллели
HLA-B*27- анкилозирующий спондилит и синдром Рейтера
HLA DR3, DR4
- инсулинозависимый сахарный диабет
HLA-В7, Bw22, В40- повышенное образование анти-IgE-антител
Слайд 37
ИД состояния обычно не имеют каких-либо характерных клинических симптомов
и проявляются в виде: - инфекционных осложнений - гематологических нарушений - желудочно-кишечных расстройств -
аутоиммунных процессов - образования опухолей - аллергических реакций - врожденных пороков развитияСлайд 38
Лица с ИДС подвержены заболеваниям:
- аллергической
- аутоиммунной природы
- злокачественным
новообразованиям
Слайд 40
Первичные иммунодефициты - иммунодефицитные состояния, в основе которых лежит
генетически обусловленная неспособность организма реализовать какие-либо звенья иммунного ответа
Слайд 41
Первичные иммунодефициты
проявляются на ранних этапах постнатального периода, наследуются
по аутосомно-рецессивному
Слайд 43
Причины врожденных иммунодефицитных синдромов и болезней:
- удвоение хромосом
- точечные
мутации - дефект ферментов обмена нуклеинов кислот - генетически обусловленные нарушения мембран
иммунокомпетентных клеток - повреждение генома в эмбриональном периоде, др.Слайд 44
Основные типы нарушений иммунитета:
- комбинированные поражения клеточного и гуморального
иммунитета, при которых имеется выраженный дефицит Т- и В-системы иммунитета -
поражение В-системы иммунитета - поражение Т-системы иммунитета - нарушения системы комплемента - нарушения функции нейтрофиловСлайд 45
Недостаточность гуморального звена
- дисгаммаглобулинемия-
избирательный дефицит иммуноглобулинов
- агамма(гипогамма)глобулинемия (нарушение
синтеза иммуноглобулинов или их ускоренный распад). В крови больных Ig
отсутствуют или их количество резко снижено: сцепленная с Х-хромосомой, транзиторная, общая вариабельнаяСлайд 47
Недостаточность клеточного иммунитета
обусловлена нарушением функциональной активности Т-клеток :
-
алимфоцитоз (синдром Нозелофа) - врожденная гипо-, аплазия тимуса и паращитовидных желез
(с-м Ди Джорджи) - хронический слизисто-кожный кандидоз - ИД при болезни Дауна - ИД при карликовом ростеСлайд 48
Недостаточность клеточного иммунитета
обусловлена нарушением функциональной активности Т-клеток :
-
алимфоцитоз (синдром Нозелофа) - врожденная гипо-, аплазия тимуса и паращитовидных желез
(с-м Ди Джорджи) - хронический слизисто-кожный кандидоз - ИД при болезни Дауна - ИД при карликовом ростеСлайд 49
Нарушен иммунитет:
- противовирусный
- противогрибковый
- противоопухолевый
- трансплантационный
Слайд 50
Комбинированные ИД---
развиваются при сочетании нарушений Т- и В-звеньев ИС
– наиболее тяжело протекающие ИД. Связаны с нарушением функций центральных органов
ИС - атаксия-телеангиэктазия (синдром Луи-Бар) - синдром Вискотта Олдрича - тяжелый комбинированный ИД: Х-сцепленный, аутосомно-рецессивный - ИД с карликовостьюСлайд 51
дефицит системы фагоцитов--
- хронический гранулематоз
- синдром Чедиака-Стейнбринка-Хигаси
- синдром Джоба
-
дефицит экспресс молекул адгезии
дефицит системы комплемента
- врожденный ангионевротический отек
Слайд 52
Недостаточность фагоцитоза обусловлена:
- уменьшением числа фагоцитов
– их функциональной
неполноценностью
Проявляется:
- нарушении распознавания антигена
- расстройствах кооперации с иммунокомпетентными клетками
Слайд 53
Лечение 1. замещение дефектных тканей, клеток, молекул: переливание
крови (пересадка ткани, клеток – проблема тканевой несовместимости) 2. антибиотикотерапия 3. стерильные условияСлайд 54
генотерапия – введение аутологичных клеток костного
мозга, в которые предварительно трасфецируется недостающий генСлайд 55
Вторичный иммунодефицит - нарушение иммунитета, возникающие в результате соматических
и других болезней, прочих факторов (МКБ) ВИД – это клинико-иммунологический синдром: -
развившийся на фоне ранее нормально функционировавшей ИМ - характеризующийся устойчивым выраженным снижением количественных и функциональных показателей факторов иммунорезистентности - являющийся зоной риска развития хронических инфекций, аутоиммунной патологии, аллергических болезней и опухолевого ростаСлайд 56
особенности ВИД
Нарушения в ИС вторичны, возникают на фоне здоровья
Нарушения в
ИС носят устойчивый и выраженный характер
Нарушения в ИС носят
количественный и функциональный характерЗатрагивают показатели как специфического иммунитета, так и неспецифической резистентности
М.б. косвенные клинические признаки (напр., хр.усталость)- «зона риска» развития патологии
Слайд 57
Классификация ВИД (Мешкова Р.Я. С соавт.)
обусловлен травмой, острым
инф. заболеванием
- на фоне хронических гн-воспалит, аутоим забол, опухолей
Слайд 61Причины развития ВИД
Протозойные инвазии и гельминтозы (малярия, токсоплазмоз, аскаридоз)
Бактериальные
инфекции (стафилококковые, туберкулез)
Вирусные инфекции – острые (корь, грипп), персистирующие (СПИД,
хронический гепатит В), врожденные (краснуха)Нарушение питания (дефицит белка, витаминов, микроэлементов, кахексия, ожирение)
Злокачественные новообразования
Аутоиммунные заболевания
Слайд 62Причины развития ВИД
Состояния с потерей ИК клеток (кровотечения, ожоги)
Экзо- и
эндогенные интоксикации (тиреотоксикоз, отравления)
При воздействиях: физических (СВЧ, ионизирующее излучение), химических
(химиотерапия, иммуносупрессоры, наркотики)Нарушение нейрогормональной регуляции: стрессовые воздействия (операции, травма, спортивные перегрузки, психические травмы)
- «естественные» - детский, геронтологический возраст, беременность
Слайд 63Признаки ИД
Рецидивирующие бактериально-вирусные инфекции, характеризующиеся
- хроническим течением
Неполным выздоровлением
Рефрактерностью к традиционному
течению
Необычным возбудителем (МЛУ,УПМ, оппортунистическая инфекция)
Возраст, наличие родственников с ИД
Необычные р-ции
на живые вакциныДанные физического обследования
- Недостаточность, задержка развития
- ↓ массы тела
- Хроническая диарея
- Органомегалия
- Субфебрилитет
- Увеличение, отсутствие лимфатически узлов,миндалин, тимуса
- дерматиты, кожные абсцессы
-
Слайд 64Признаки ИД
Кандидоз слизистой полости рта
- Врожденные пороки сердца
- Карликовость
- Повышенная
утомляемость
Мед. вмешательства
- Химиотерапия
- Спленомегалия
- Облучение
Длительный стресс физический, психоэмоциональный
Аллергия
Аутоиммунные заболевания
опухоль
При
наличии клинических признаков ИД проводится исследование иммунного статуса-
Слайд 65 Первичные клеточные мишени ВИЧ-1 - клетки иммунной системы, имеющие
CD4- рецептор ----
дендритные клетки (клетки Лангерганса эпителия, фолликулярные клетки лимфоузлов)
микроглиальные клетки мозга
естественные киллеры
стволовые клетки крови
эндотелиальные клетки
эпителиальные клетки ЖКТ
Слайд 66
0
50
100
150
Время полужизни (дни)
Свободные вирусные частицы
Инфицированные макрофаги
Продуктивно инфицированные CD4+ клетки
Вирионы, фиксированные дендритными клетками
Покоящиеся CD4+ клетки (неинтегрированный вирус)
Резервуары ВИЧ-инфекции
Покоящиеся
CD4+ клетки (интегрированный провирус)на сайте: www.ebi.ac.uk/imgt/hla [11]. Аллельный полиморфизм некоторых генов системы HLA класса II.