Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
алюминий
Содержание
- 1. алюминий
- 2. Характеристика1. Электронное строение27Аl+1302e8e3e1s22s22p63s23p1Краткая электронная запись1s22s22p63s23p1Порядок заполнения
- 3. Характеристика Находится в III группе, в главной
- 4. Физические свойстваСеребристо-белый, легкий металл, механически прочный, обладает
- 5. Нахождение в природеВ природе встречается только в виде соединений.АлюмосиликатыNa[AlSi3O8]БокситAl2O3 • nH2OНефелинNa[AlSiO4]
- 6. Химические свойстваВзаимодействие с простыми веществами1. с кислородом:
- 7. Химические свойстваII. Взаимодействие со сложными веществами1. с
- 8. Химические свойства4. С оксидами менее активных металлов
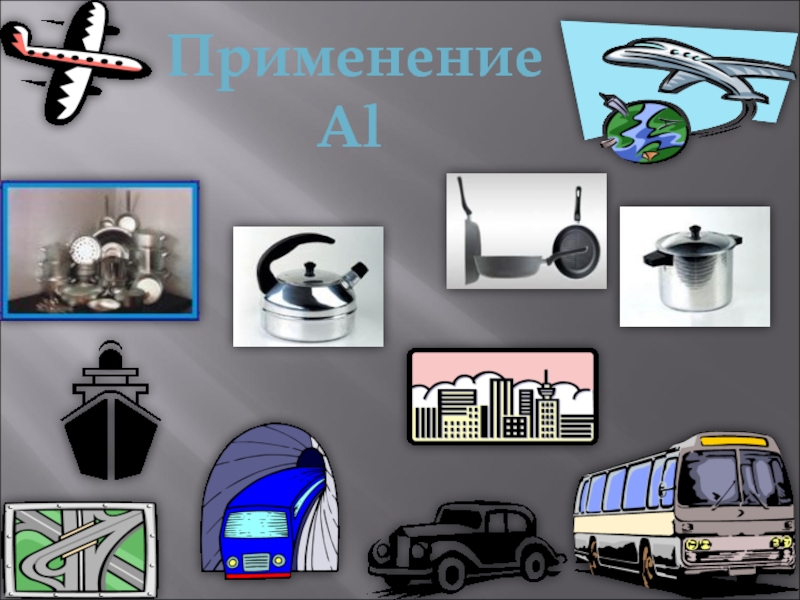
- 9. Применение Al
- 10. Алюминий и его сплавы широко применяют как конструкционный материал
- 11. Из алюминия делают линии электропередач, ёмкости, цистерны, «серебряную» краску.
- 12. Алюминий - крылатый металл
- 13. Скачать презентанцию
Характеристика1. Электронное строение27Аl+1302e8e3e1s22s22p63s23p1Краткая электронная запись1s22s22p63s23p1Порядок заполнения
Слайды и текст этой презентации
Слайд 2Характеристика
1. Электронное строение
27
Аl
+13
0
2e
8e
3e
1s2
2s2
2p6
3s2
3p1
Краткая электронная запись
1s2
2s2
2p6
3s2
3p1
Порядок заполнения
Слайд 3Характеристика
Находится в III группе, в главной подгруппе
На наружном слое
3 электрона: 3s23p6
Слайд 4Физические свойства
Серебристо-белый, легкий металл, механически прочный, обладает хорошей электро- и
теплопроводностью, пластичен, tплавл = 6600С, ρ = 2,7 г/см3
Поверхность алюминия
всегда покрыта оченьпрочной оксидной пленкой оксида алюминия Аl2O3
Слайд 5Нахождение в природе
В природе встречается только в виде соединений.
Алюмосиликаты
Na[AlSi3O8]
Боксит
Al2O3 •
nH2O
Нефелин
Na[AlSiO4]
Слайд 6Химические свойства
Взаимодействие с простыми веществами
1. с кислородом:
4Al + 3O2 =
2Al2O3Алюминий горит
2. с галогенами:
2Al + 3Br2 = 2AlBr3 + Q
2Al + 3I2 = 2Al I3 + Q
3. с серой:
2Al + 3S = Al2S3
t
Слайд 7Химические свойства
II. Взаимодействие со сложными веществами
1. с водой:
2Al + 6H2O = 2Al(OH)3 + 3H2
2.
с кислотами: 2Al + 6HCl = 2AlCl3 + 3H2
3. со щелочами:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Если NaOH в твердом состоянии:
2Al + 2NaOH + 6H2O = 2NaAlO2 + 3H2
Слайд 8Химические свойства
4. С оксидами менее активных металлов
8Al + 3Fe3O4 = 4Al2O3 + 9Fe + Q
5. С
солями менее активных металлов2Al + 3CuSO4 = Al2(SO4)3 + 3Cu




![алюминий Нахождение в природеВ природе встречается только в виде соединений.АлюмосиликатыNa[AlSi3O8]БокситAl2O3 • nH2OНефелинNa[AlSiO4] Нахождение в природеВ природе встречается только в виде соединений.АлюмосиликатыNa[AlSi3O8]БокситAl2O3 • nH2OНефелинNa[AlSiO4]](/img/thumbs/c116ff5e050b934df9465cb939435bad-800x.jpg)