Слайд 1Будова атому
Історичні моделі будови атому
1) 1901 р. Жан Перрен
висунув припущення про ядерно-планетарну будову атома
2) 1902 р. У.
Томсон (лорд Кельвін) висунув припущення, що атом є згустком позитивно зарядженої матерії, всередині якої рівномірно розподілені електрони (кекс з ізюмом).
3) 1903 р. Дж. Дж. Томсон детально розвиває цю модель. Він вважає, що електрони всередині позитивно зарядженої кулі містяться у одній площині та утворюють концентричні кільця.
4)1903 р. Філіп фон
Лєнард створив
модель, у якій
протилежні
заряди у
атомі не
існують
окремо
5)1904р. Хантаро Нагаока запропонував модель, в якій атом подібний
до
планети
Сатурн;
Слайд 2Ернест РЕЗЕРФОРД,
Барон Резерфорд Нельсонський I
1871-1937
під його керівництвом Ганс Гейгер
винайшов свій знаменитий лічильник Гейгера. Саме там у 1911 році
відкрив існування атомного ядра. В роки Першої світової війни займався розробкою сонарів. У 1919 році став професором фізики і директором Кавендишської лабораторії Кембріджського університету і у тому самому році відкрив розпад ядра в результаті бомбардування важкими частинками високих енергій. На цій посаді Резерфорд залишався до кінця життя. Одночасно був президентом Королівського наукового товариства. Похований у Вестмінстерському абатстві поруч з Ньютоном, Дарвіном і Фарадеєм.
Новозеландський фізик. Народився в Нельсоні, у родині фермера-ремісника. Виграв стипендію для одержання освіти у Кембріджському університеті в Англії. Після його закінчення дістав призначення в канадський університет Мак-Гілл, де разом із Фредеріком Содді встановив основні закономірності явища радіоактивності, за що в 1908 році отримав Нобелівську премію з хімії. Незабаром учений перебрався в Манчестерський університет, де
Слайд 4Дослід Резерфорда з дослідження будови атома
Слайд 6Планетарна модель атома Резерфорда
Нестабільність атома Резерфорда
Слайд 7Спектр ( лат. spectrum від лат. Spectare дивитися) - сукупність
значень та їх розподіл за певним параметром, значення якого може
набувати спостережувана величина. Оскільки першими було отримано оптичні спектри, то найчастіше термін спектр використовується згідно з „історичним” значенням - розподіл потоку випромінювання або частинок за довжинами хвиль або енергії.
Розрізняють наступні оптичні спектри
Суцільні, лінійчасті, смугасті.
спектральний аналіз
Слайд 8Лінійчасті спектри дають речовини в атомарному стані
Інфрачервона область спектру
Видиме світло
Ультра
фіолет
Спектр
поглинання
Спектр
випромінювання
ЛІНІЙЧАСТИЙ
СПЕКТР АТОМА ВОДНЮ
Слайд 9Смугасті спектри дають речовини в молекулярному стані
СМУГАСТИЙ СПЕКТР
Інфрачервона область
спектру
Видиме світло
Ультра
фіолет
Спектр
поглинання
Спектр
випромінювання
Слайд 10Суцільні спектри дають речовини в твердому стані або в стані
високотемпературної плазми (зірки, Сонце – зірка)
СУЦІЛЬНИЙ СПЕКТР
Інфрачервона частина спектру
Видиме
світло
Ультрафіолет
Спектр
поглинання
Спектр
випромінювання
Уїльям Воластон у 1802 р. спостерігав темні лінії у сонячному спектрі, але знехтував спостереженнями. У 1814 р. ці лінії незалежно виявив та докладно описав Фраунгофер, який вперше застосував для отримання спектра дифракційну решітку.
Слайд 11Спектр атома водню
Серія Бальмера
(n = 3,4,5…∞)
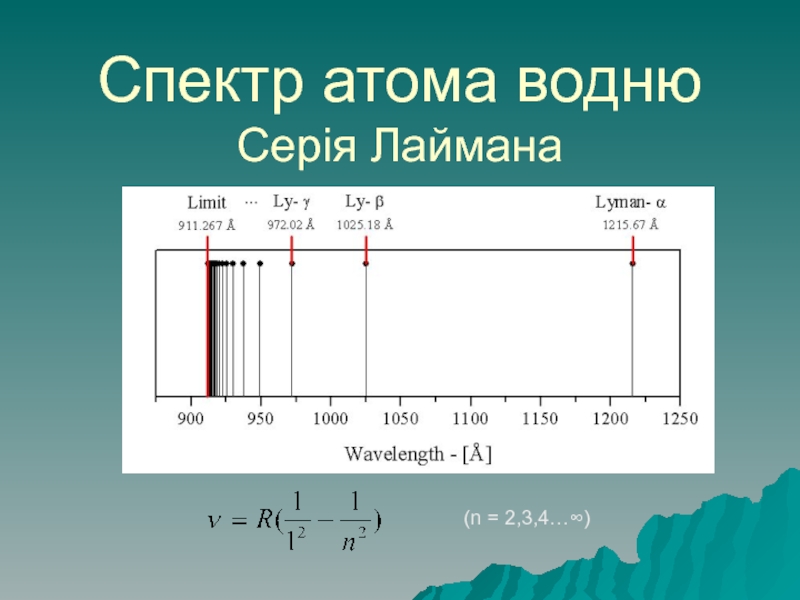
Слайд 12Спектр атома водню
Серія Лаймана
(n = 2,3,4…∞)
Слайд 13Нільс Бор, один з основоположників сучасних уявлень про субатомний світ,
творець першої квантово-механічної моделі будови атома. Фотографія зроблена в 1948
році в Принстонському університеті (США)
Нільс Бор
Слайд 14існують стаціонарні стани атома, знаходячись у яких він не випромінює
і не поглинає енергію.
Цим стаціонарним станам відповідають цілком визначені (стаціонарні)
орбіти, по яким рухаються електрони. Правило квантування орбіт Бора стверджує, що в стаціонарному стані атома електрон, рухаючись по коловій орбіті, повинен мати квантовані значення моменту імпульсу, що задовольняють умові
L= mVr = ħn
де (n=1, 2, 3, …) – головне квантове число, що нумерує орбіти електрона в теорії Бора. Стан з n=1 є основним, не збудженим станом атома. В основному стані атом може знаходитися нескінченно довго. Стани з n>1 - це збуджені стани атома. В таких станах атом може існувати обмежений час.
Квантові постулати Бора
Перший постулат Бора
(постулат стаціонарних станів):
Слайд 15при переході атома з одного стаціонарного стану в інший випромінюється
або поглинається один фотон (квант енергії).
Випромінювання відбувається при переході атома
зі стану з більшою енергією в стан з меншою енергією. Поглинання фотонів супроводжується переходом атомів у стан з більшою енергією. Зміна енергії атома, пов'язана з випромінюванням або поглинанням фотона, пропорційна частоті випромінювання. Якщо - зміна енергії атома в результаті цих процесів, то
ΔE=hv
Квантові постулати Бора
Другий постулат Бора
(правило частот):
Слайд 17Можливості теорії Бора
Електрон в атомі водню утримується силою Кулона:
F=ke2 /r2
Ця сила надає електрону доцентрове прискорення:
F=mV2/r
З іншого боку, принцип квантування
орбіт дає:
mVr = nħ
Тоді: mV2/r = ke2 /r2 або mV2r = ke2
Слайд 18Можливості теорії Бора
З цих рівнянь знайдемо швидкість електрона на стаціонарному
рівні
V = ke2 / nħ
і радіус орбіти електрона
R =
n2ħ2/mke2
Згадаємо, що:
k = 1/4πε0 I ħ = h/2π
Слайд 19Енергія електрона в атомі водню дорівнює сумі кінетичної енергії і
потенціальної енергії його взаємодії з ядром
W = Wk +Wp
Wk
= mV2/2; Wp = - ke2/r
Знак “-” відповідає притяганню між електроном і ядром. Тоді
W = mV2/2 - ke2/r.
Підставимо в це рівняння отримані раніше значення швидкості і радіуса.
Тоді для значення повної енергії електрона в атомі водню отримаємо
W= - mk2e4/2π2ħ2n2.
Енергія Wі = mk2e4/2π2ħ2
Називається енергією іонізації, тоді енергія атома на n–му енергетичному рівні
W = - Wі /n2.
Слайд 20Згідно до другого постулату Бора:
ħv = - Wі (1/n2 -
1/m2).
Таким чином, ми отримали серіальну формулу, яка визначає можливі спектральні
лінії в спектрі атома водню
v= R (1/m2 - 1/n2),
де R= Wі /ħ - стала Рідберга.
Слайд 21Усі лінії спектра випромінювання атомів, які випромінюються при переході електронів
з будь-якої орбіти на певну, називають серією.
Ці серії в спектрі
атома водню отримали свої назви. Для:
m = 1 - серія Лаймана, (n =2,3,4...)вона належить до ультрафіолетової частини спектра;
m = 2 - серія Бальмера, (n =3,4,5...) видима серія. Ця серія вивчається в даній роботі;
m = 3 - серія Пашена, (n =4,5,6...) - в близькій інфрачервоній області,
m = 4 - серія Брэкета, (n =5,6,7...) - в близькій ІЧ області.
m = 5 - серія Пфунда, (n =6,7,8...) - в далекій ІЧ області.
Наведені серіальні закономірності є яскравим проявом квантових властивостей атомних систем.
Як приклад наведемо формулу Бальмера для серії Бальмера
v= R (1/22 - 1/n2),
Слайд 22Спектр атому водню
І – серія Лаймана;
ІІ – серія Бальмера;
ІІІ –
серія Пашена;
ІV – серія Брэкета;
V – серія Пфунда.
Енергетичний спектр атома
водню
ІІ
IV
-13,6
-3,4
-1,5
- 0,85
0
E, еВ
n=1
n=2
n=3
n=4
n=5
I
n=∞
ІІІ
Слайд 23АТОМ ВОДНЮ В КВАНТОВІЙ МЕХАНІЦІ
Потенціальна енергія електрона в цьому атомі
дорівнює:
Слайд 24Ервін Шредінгер - австрійський фізик, один з творців квантової механіки.
Найважливішою заслугою Шредінгера є створення їм хвильової механіки (кінець 1925
— початок 1926): виходячи з гіпотези Л. де Бройля про хвилі матерії, він показав, що стаціонарні стани атомних систем можуть розглядатися як власні коливання хвильового поля, яке відповідає даній системі;
Шредінгер знайшов основне рівняння нерелятивістської квантової механіки (рівняння Шредінгера) та застосував його для вирішення окремих задач. Встановив зв'язок хвильової механіки з «матричною механікою» В. Гейзенберга. Розвинений Шредінгером математичний формалізм й уведена ним хвильова функція y з'явилися найбільш адекватним математичним апаратом квантової механіки і її застосувань. Нобелівська премія (1933). Іноземний член АН СРСР (1934).
(1887 —1961)
Слайд 25Вирішення рівняння Шредінгера дозволяє отримати важливі результати. Виявляється, що стан
атому можна визначити за допомогою набору квантових чисел:
1, n=1,2,3…
- головне квантове число, нумерує енергетичні стани атому за збільшенням енергії, причому стан з n=1 називається основним станом. В основному стані атом може знаходиться необмежений час, це стан з мінімальною потенціальною енергією. Стани з n>1 - збуджені стани, в таких станах атом може знаходитись обмежений час (за звичай), потім атом має перейти на нижчий рівень.
Рівняння Шредінгера має вирішення а) за будь-яких додатних значень енергії (електрон пролітає поблизу ядра і віддаляється у нескінченість); б) за дискретних від’ємних значень енергії (електрон пов’язаний з атомом):
Слайд 284. Спін. У 1921р. Штерном і Герлахом були проведені досліди
по вимірюванню магнітних моментів атомів різних хімічних елементів. Для цього
взяли елементи першої групи таблиці Менделєєва, у яких всі, крім одного, орбітальні механічні (і магнітні) моменти взаємно компенсуються. Вони виявили, що проекція магнітного моменту атома на напрямок поля є кратним магнетону Бора:
Для пояснення цього результату необхідно припустити, що електрон, крім орбітального моменту імпульсу і відповідного йому магнітного моменту має власний механічний момент імпульсу , який називається спіном електрона і відповідний йому власний магнітний момент.
Спін електрона та інших елементарних частинок є особливою властивістю цих частинок: подібно тому, що частинки мають масу, заряд, вони ще мають і спін.
Слайд 29Із загальних висновків квантової механіки випливає, що власний момент імпульсу
електрона квантується:
де s - спінове квантове число (спін). Спінове квантове
число не є цілим, для електрона воно дорівнює:
Припущення про існування спіну було висунуто у 1925р. Гаудсмітом та Уленбеком. Вони надали спіну електрона наочне тлумачення, яке полягає у тому, що спін розглядається як момент імпульсу електрону, пов’язаний з обертанням електрону – зарядженої кульки - навколо своєї вісі. Правда, коли строго підрахувати кутову швидкість такого обертання, виявиться, що швидкість точок на поверхні сфери, радіусом буде у 200 разів більша за швидкість світла у вакуумі!
Слайд 30Отто Штерн
(1888 – 1969)
Німецько-американський фізик.
В
1920 доцент, потім професор університету у Франкфурті-на-Майні, з 1922 професор
університету в Ростоці. В 1923—33 професор и директор Фізико-хімічної лабораторії університету в Гамбурзі. В 1933 емігрував у США, професор Технологічного інституту Карнегі в Пітсбурзі (1933—45). Основні праці з ядерної фізики, квантової фізики, термодинаміки. В 1920 вперше безпосередньо виміряв швидкості молекул (дослід Штерна). Вказав на можливість (1921) експериментальної перевірки просторового квантування магнітного моменту атома і здійснив її спільно з німецьким фізиком В. Герлахом (Дослід Штерна – Герлаха). Спільно з німецьким фізиком Р. Фрішем вперше (1933) визначив магнитний момент протона в молекулі H2. Штерн і його співробітники розвинули метод молекулярних і атомних пучків. Нобелівська премія (1943).
Слайд 31Дослід Штерна – Герлаха
Магнітне поле створюється між двома магнітними
полюсами, один з яких плоский, а інший – дуже гострий.
Внаслідок напруженість магнітного поля зростає біля гострого полюса та зменшується біля плоского. Частинки проходять між магнітними полюсами перпендикулярно до площини рисунка, в місці, відзначеному “хрестиком”.
Z
N
Прилад Штерна - Герлаха
Для самостійного вивчення
Слайд 32АТОМ ВОДНЮ В КВАНТОВІЙ МЕХАНІЦІ
Стан електрону, який має різні
значення орбітального квантового числа, в атомній фізиці позначають наступним способом
s - стан;
p - стан;
d - стан;
f - стан, та т.д.
Слайд 33ОСНОВНИЙ СТАН АТОМУ ВОДНЮ
Розглянемо більш детально s - стан електрону
в атомі водню при n=1. Такий стан називається основним. Хвильова
функція електрону в цьому стані є функцією тільки :r . Це означає, що вірогідність виявити електрон в певній точці атому залежить тільки від r . Вирішення рівняння Шредінгера для воднево подібного атому приводить до енергії атому в основному стані:
як і в теорії Бора. Виявляється, що борівські орбіти електрону є геометричним місцем точок, в яких з найбільшою вірогідністю можна виявити електрон.
Слайд 34ОСНОВНИЙ СТАН АТОМУ ВОДНЮ
На рисунку зображена залежність вірогідності
виявити електрон в стані з n=1 на різних відстанях від
атому. Вона відмінна від нуля в точках
Слайд 35 Вольфганг Ернст Паулі
Австрійсько – швейцарський фізик – теоретик. Його
наукові роботи відносяться до численних розділів сучасної теоретичної фізики. Брав
участь у розвитку квантової механіки, квантової електродинаміки, теорії відносності і т.п. В 1924–25 роках сформулював один з найважливіших принципів сучасної теоретичної фізики – принцип Паулі, за що отримав Нобелевську премію з фізики (1945 р.). У 1931 р. висунув гіпотезу про існування нейтрино.
1900 – 1958
Слайд 36ПРИНЦИП ПАУЛІ
(принцип виключення)
У 1925 р. Паулі встановив квантово-механічний закон
– принцип Паулі (принцип виключення):
В будь-якому атомі не може бути
двох електронів, які б знаходилися в однакових стаціонарних станах, що визначаються набором чотирьох квантових чисел: головного n, орбітального l , магнітного m, спінового s .
Максимальне число електронів, які знаходяться в станах, що визначаються набором трьох квантових чисел n,l,m , тобто відрізняються тільки орієнтацією спінів електронів дорівнює 2, оскільки спін електрону має тільки дві можливі орієнтації
Z(n,l,m)=2
Слайд 37ПРИНЦИП ПАУЛІ
(принцип виключення)
Тепер визначимо максимальне число електронів, що знаходяться
у станах, які відповідають двом квантовим числам n і l
. Вектор моменту імпульсу може мати (2l+1) різних орієнтацій, то
Знайдемо максимальне число електронів, які знаходяться в станах з певним значенням головного квантового числа . Оскільки l при заданому n змінюється від 0 до n-1, то максимальне число електронів можна визначити за формулою:
Слайд 39Періодична система хімічних елементів Д.І.Менделєєва
Слайд 40Теорія періодичної системи базується на наступних положеннях:
1 порядковий
номер хімічного елементу дорівнює загальному числу електронів в атомі даного
елементу;
2 стан електронів в атомі визначається набором їх квантових чисел . Розподіл електронів за енергетичними станами має задовольняти принципу мінімуму потенціальної енергії: із збільшенням числа електронів, кожний наступний електрон має зайняти можливий стан з мінімальною енергією;
3 заповнення електронами енергетичних станів в атомі має відбуватися відповідно до принципу Паулі.