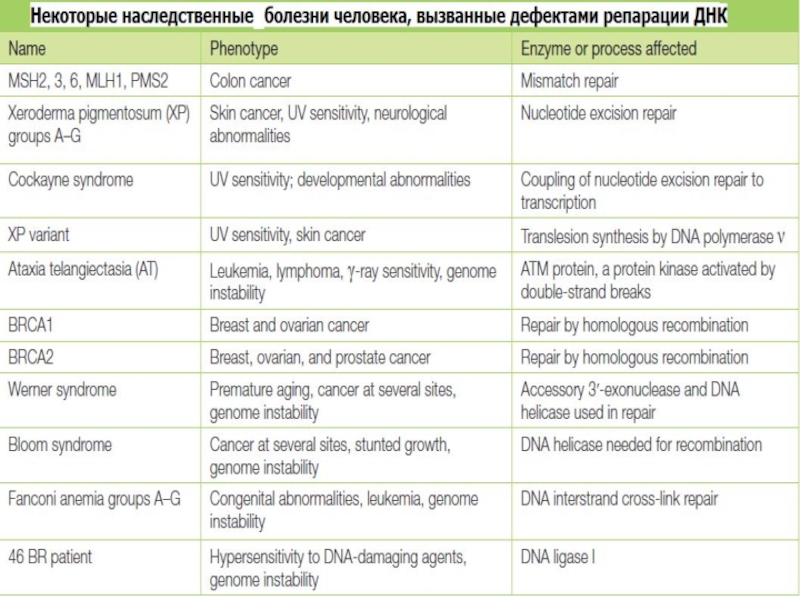
Слайд 3Причины появления повреждений в ДНК
Ошибки репликации
Повреждения ДНК эндогенными агентами:
Гидролиз
(депуринизация,
дезаминирование)
Повреждения ДНК экзогенными агентами
облучение
повреждение химическими агентами (например, алкилирование)
Репликация «через повреждения»
с использованием полимераз, отличающихся низкой точностью копирования
и др.
Для поддержания генетической стабильности организма необходимо не только
точно реплицировать ДНК, но так же и исправлять возникающие в ней повреждения.
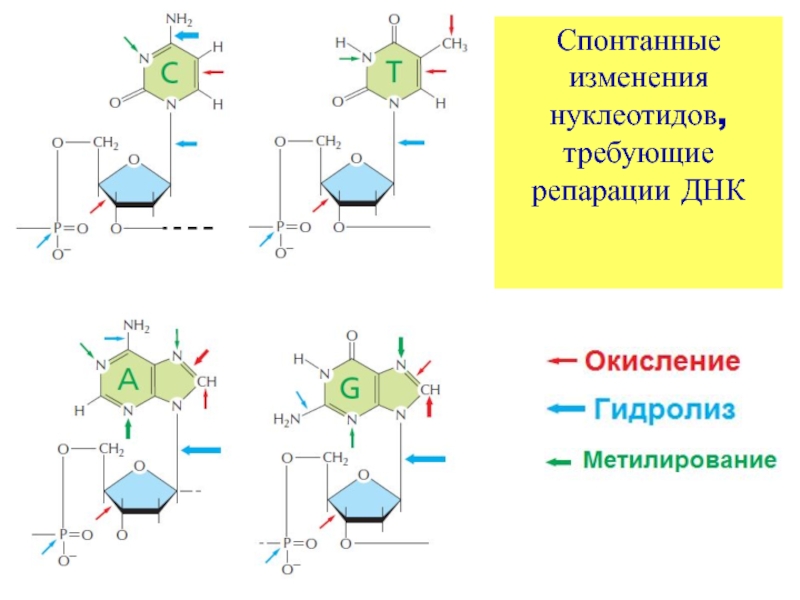
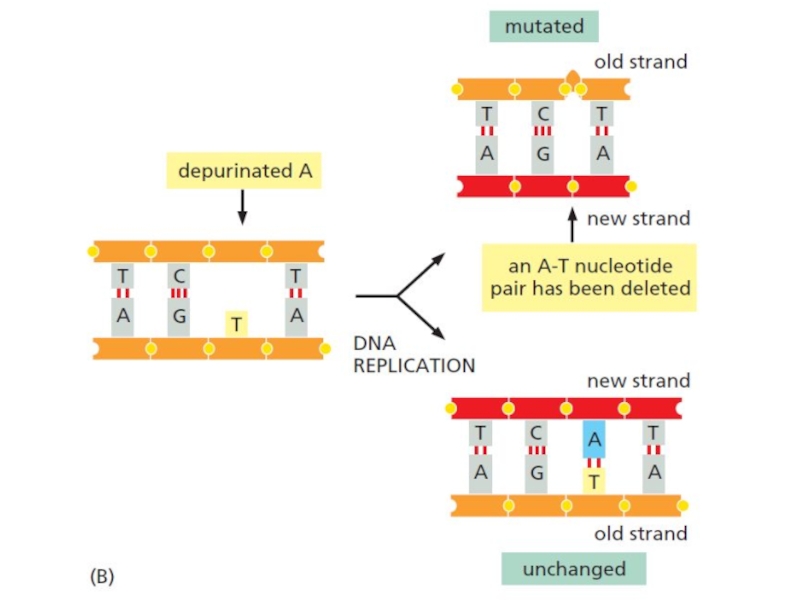
Слайд 4Спонтанные изменения нуклеотидов, требующие репарации ДНК
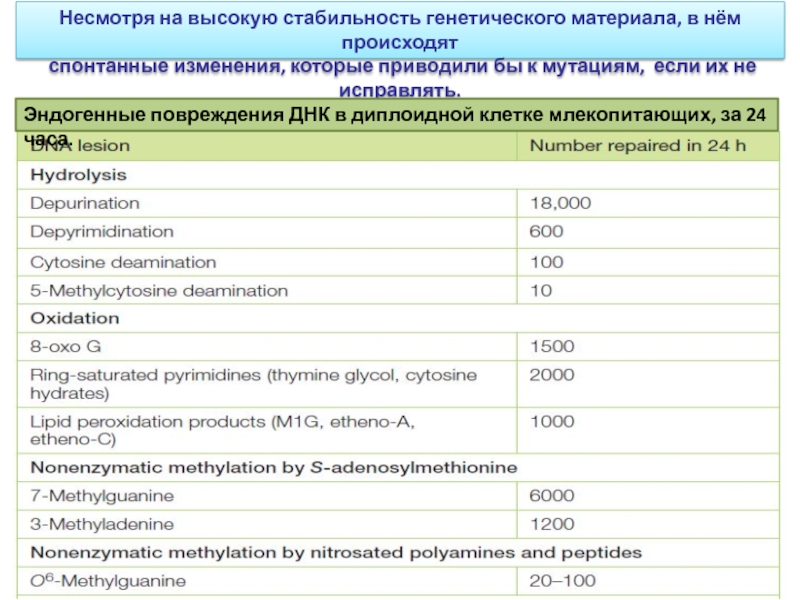
Слайд 5Несмотря на высокую стабильность генетического материала, в нём происходят
спонтанные
изменения, которые приводили бы к мутациям, если их не исправлять.
Эндогенные
повреждения ДНК в диплоидной клетке млекопитающих, за 24 часа.
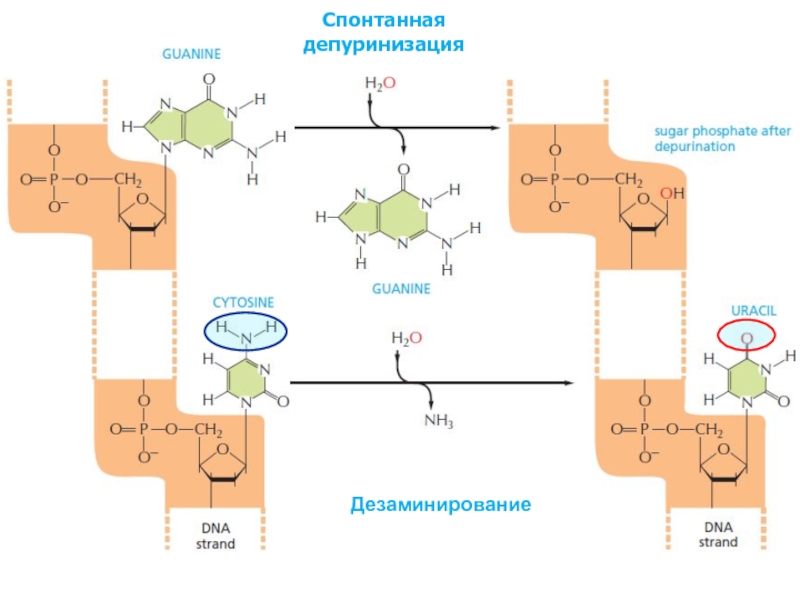
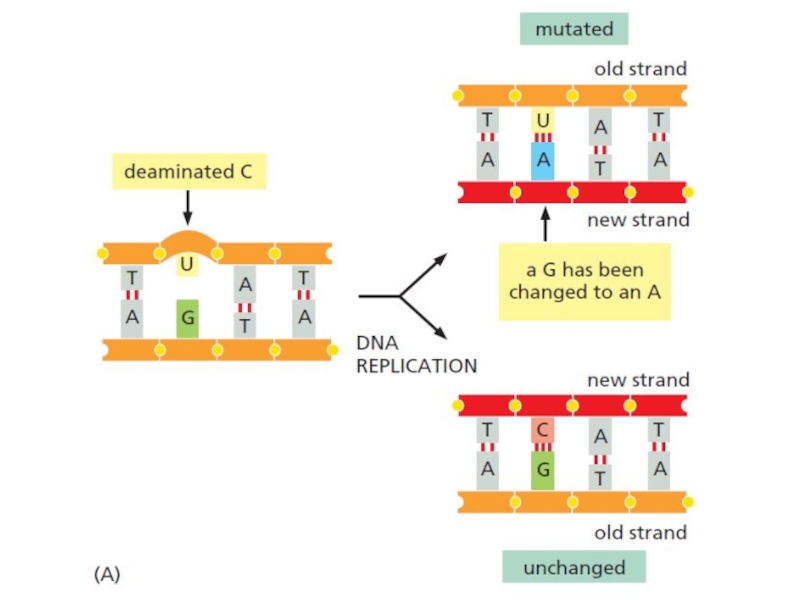
Слайд 6Спонтанная депуринизация
Дезаминирование
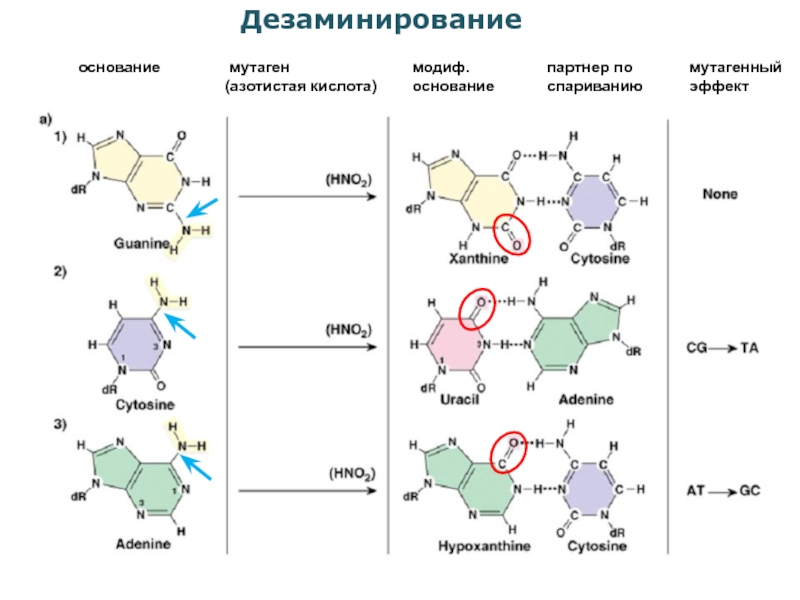
Слайд 7Дезаминирование
основание
мутаген
(азотистая кислота)
модиф.
основание
партнер по
спариванию
мутагенный
эффект
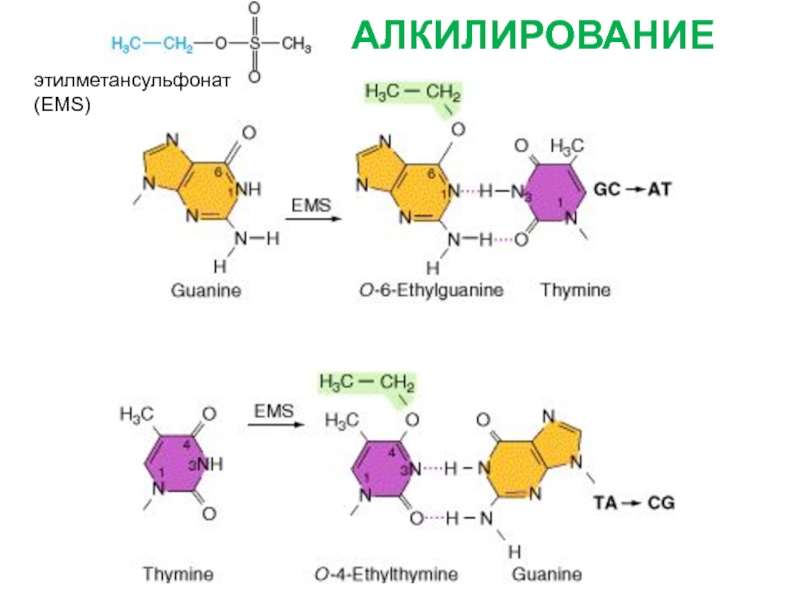
Слайд 8этилметансульфонат
(EMS)
АЛКИЛИРОВАНИЕ
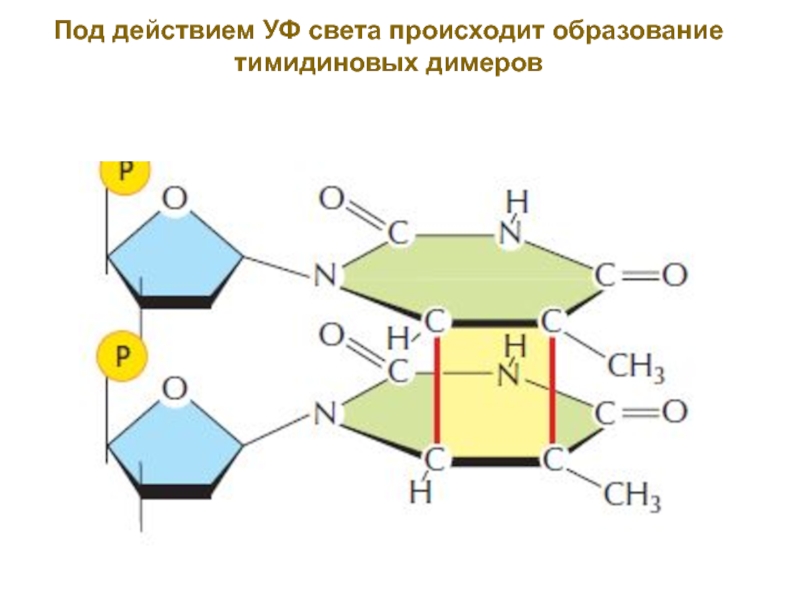
Слайд 9Под действием УФ света происходит образование тимидиновых димеров
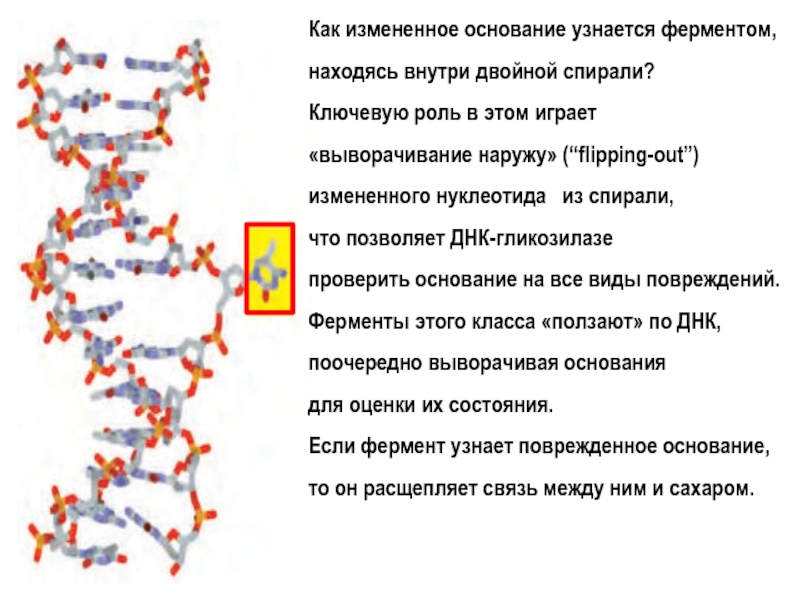
Слайд 13Как измененное основание узнается ферментом,
находясь внутри двойной спирали?
Ключевую роль
в этом играет
«выворачивание наружу» (“flipping-out”)
измененного нуклеотида из
спирали,
что позволяет ДНК-гликозилазе
проверить основание на все виды повреждений.
Ферменты этого класса «ползают» по ДНК,
поочередно выворачивая основания
для оценки их состояния.
Если фермент узнает поврежденное основание,
то он расщепляет связь между ним и сахаром.
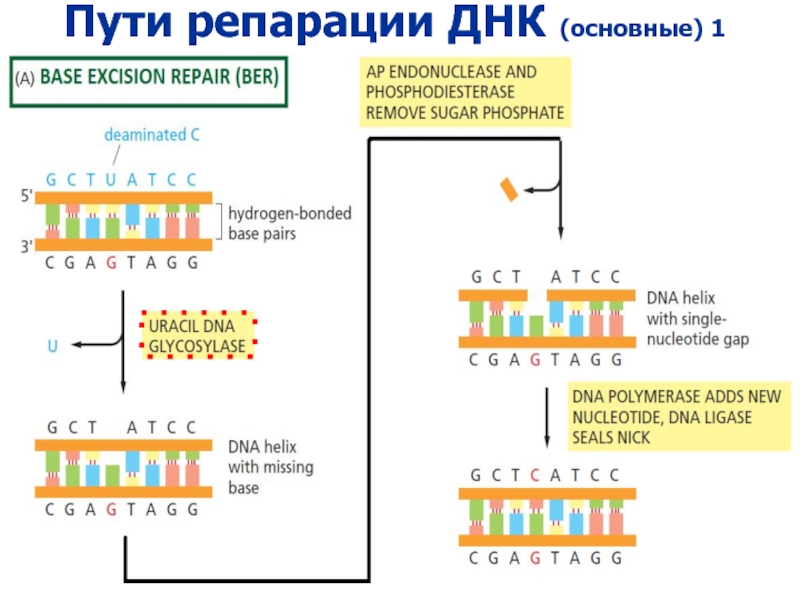
Слайд 14Основные типы повреждений, которые удаляются посредством BER
(большая часть не блокирует
репликацию)
Окисленные основания, в том числе 8-oкси-G, который спаривается с А,
вызывая GC --> TA трансверсии
Дезоксиурацил
Различные продукты алкилирования оснований (например, 3-meA)
Спонтанно возникающие апуриновые сайты
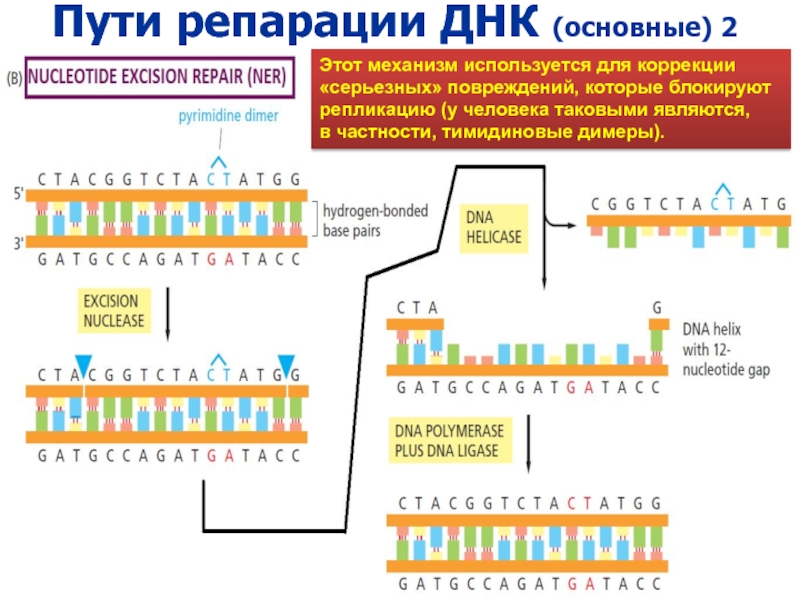
Слайд 15Пути репарации ДНК (основные) 2
Этот механизм используется для коррекции
«серьезных»
повреждений, которые блокируют
репликацию (у человека таковыми являются,
в частности,
тимидиновые димеры).
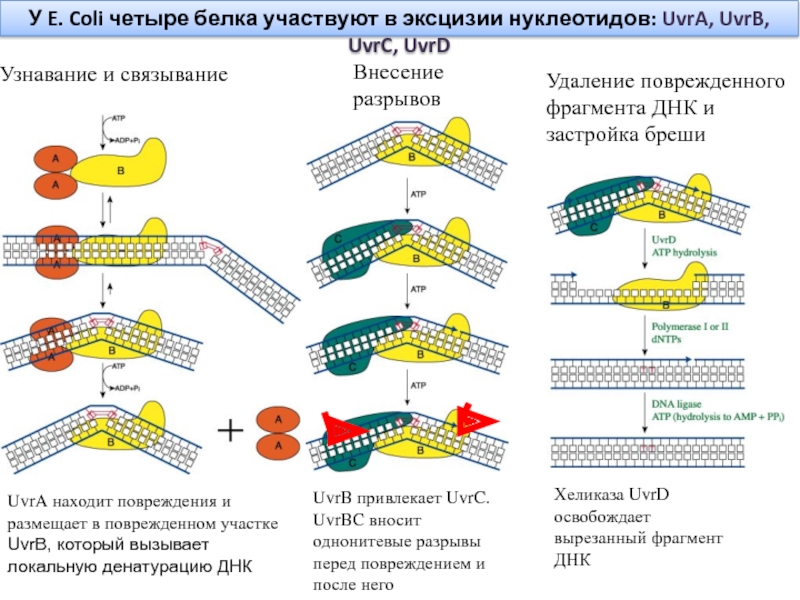
Слайд 16Узнавание и связывание
UvrA находит повреждения и размещает в поврежденном участке
UvrB, который вызывает локальную денатурацию ДНК
У E. Coli четыре белка
участвуют в эксцизии нуклеотидов: UvrA, UvrB, UvrC, UvrD
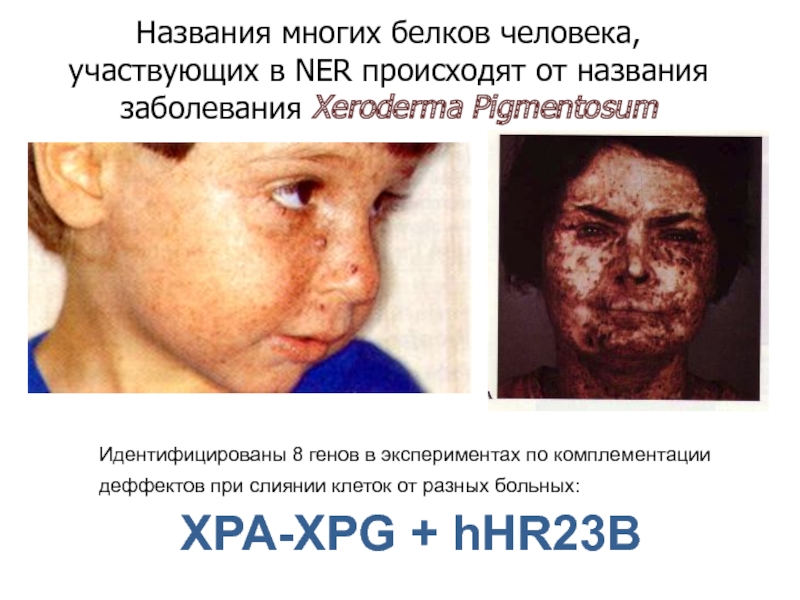
Слайд 17Названия многих белков человека, участвующих в NER происходят от названия
заболевания Xeroderma Pigmentosum
Идентифицированы 8 генов в экспериментах по комплементации
деффектов
при слиянии клеток от разных больных:
XPA-XPG + hHR23B
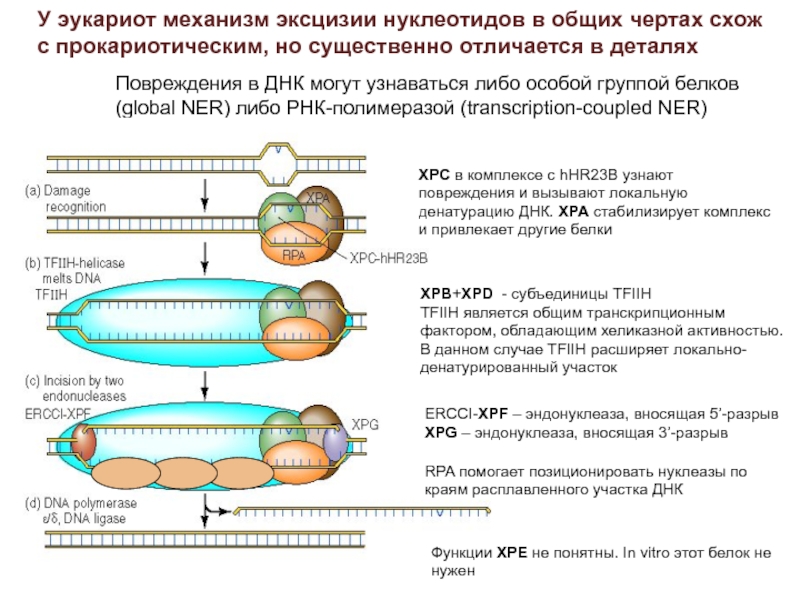
Слайд 18У эукариот механизм эксцизии нуклеотидов в общих чертах схож
с
прокариотическим, но существенно отличается в деталях
Повреждения в ДНК
могут узнаваться либо особой группой белков
(global NER) либо РНК-полимеразой (transcription-coupled NER)
XPC в комплексе с hHR23B узнают
повреждения и вызывают локальную
денатурацию ДНК. XPA стабилизирует комплекс
и привлекает другие белки
XPB+XPD - субъединицы TFIIH
TFIIH является общим транскрипционным
фактором, обладающим хеликазной активностью.
В данном случае TFIIH расширяет локально-
денатурированный участок
ERCCI-XPF – эндонуклеаза, вносящая 5’-разрыв
XPG – эндонуклеаза, вносящая 3’-разрыв
Функции XPE не понятны. In vitro этот белок не
нужен
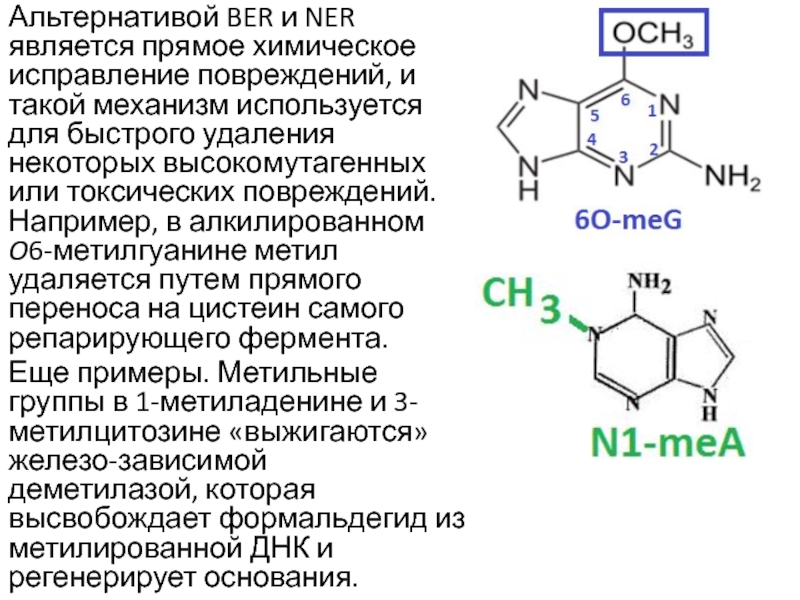
Слайд 19Альтернативой BER и NER является прямое химическое исправление повреждений, и
такой механизм используется для быстрого удаления некоторых высокомутагенных или токсических
повреждений. Например, в алкилированном O6-метилгуанине метил удаляется путем прямого переноса на цистеин самого репарирующего фермента.
Еще примеры. Метильные группы в 1-метиладенине и 3-метилцитозине «выжигаются» железо-зависимой деметилазой, которая высвобождает формальдегид из метилированной ДНК и регенерирует основания.
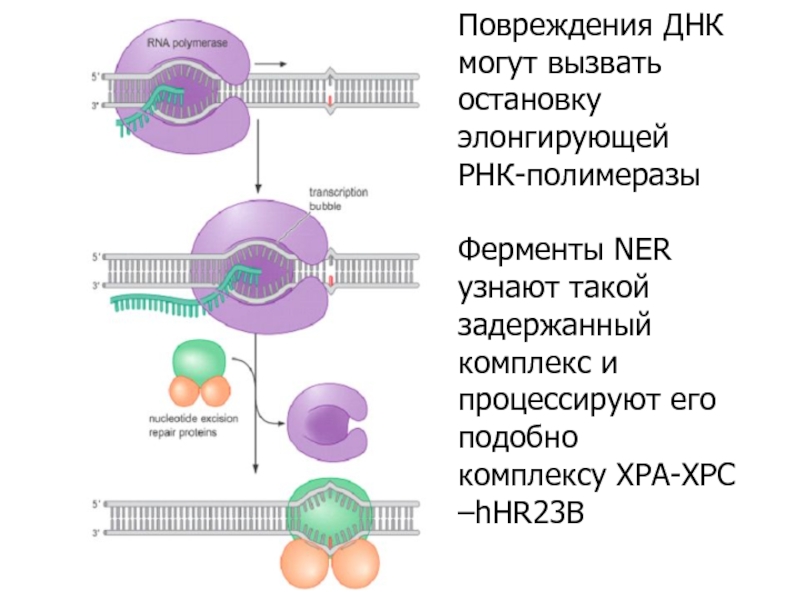
Слайд 20Повреждения ДНК могут вызвать
остановку элонгирующей
РНК-полимеразы
Ферменты NER узнают такой
задержанный
комплекс и
процессируют его подобно
комплексу XPA-XPC –hHR23B
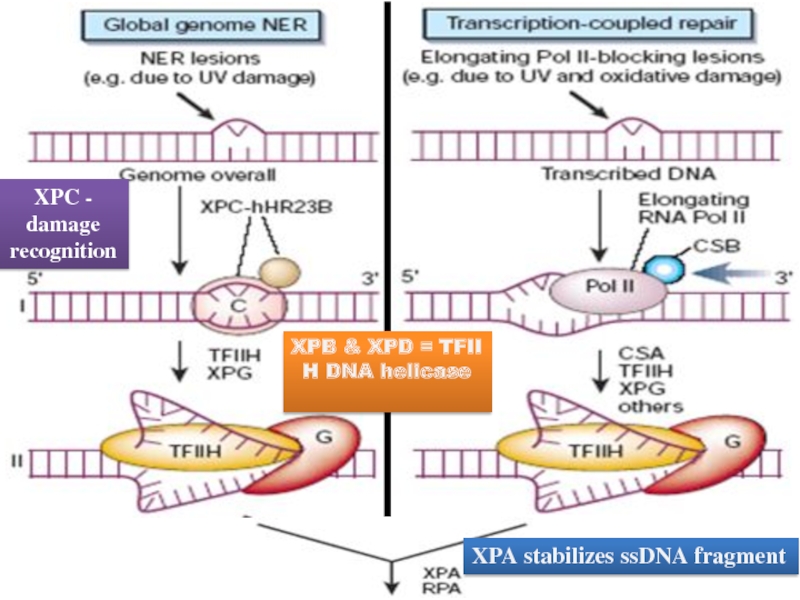
Слайд 21XPC - damage recognition
XPB & XPD = TFII H DNA
helicase
XPA stabilizes ssDNA fragment
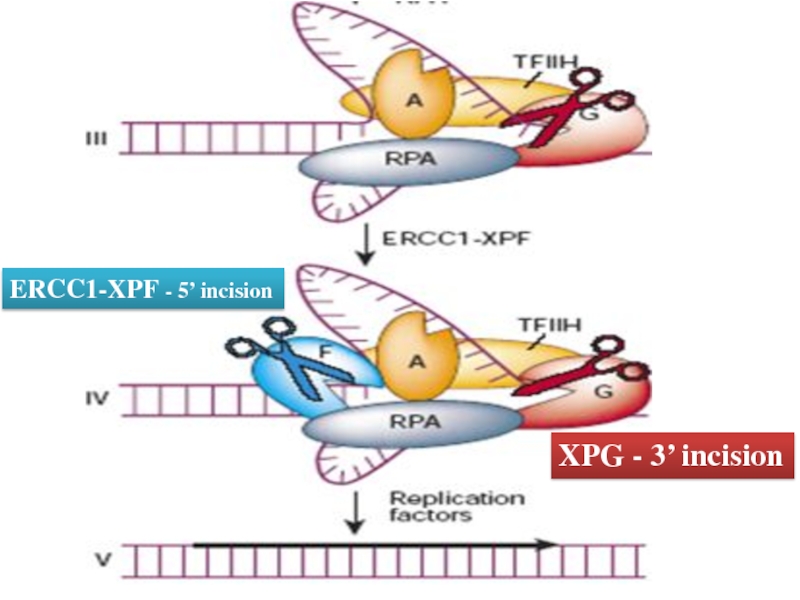
Слайд 22ERCC1-XPF - 5’ incision
XPG - 3’ incision
Слайд 23Исправление ошибок репликации
(Мismatch repair)
ДНК полимеразы (даже те, у которых есть
корректирующая активность) все равно делают ошибки, которые надо исправлять
Система репарации
ошибок репликации должна
1. Быстро находить ошибки
2. Различать родительскую и новосинтезированную
цепь с тем, чтобы в неспаренном участке
заменить ошибочно включенный нуклеотид
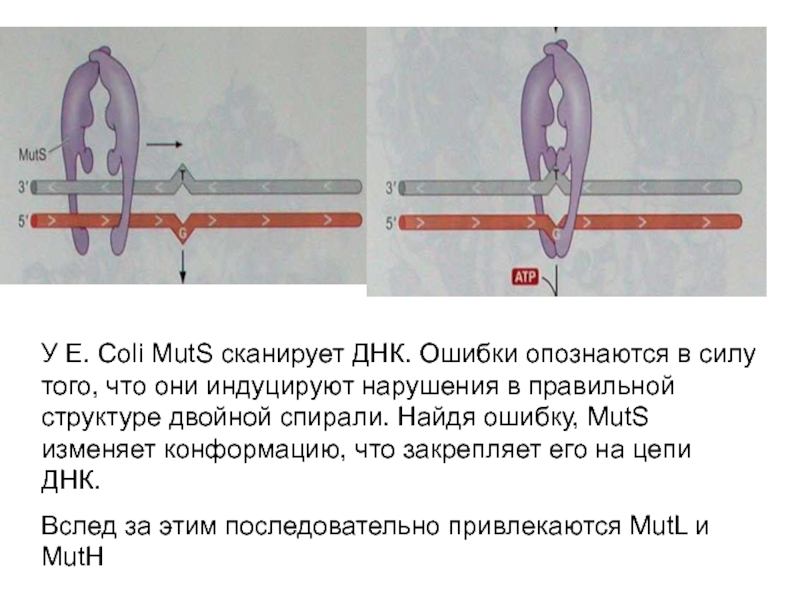
Слайд 24У E. Coli MutS сканирует ДНК. Ошибки опознаются в силу
того, что они индуцируют нарушения в правильной структуре двойной спирали.
Найдя ошибку, MutS изменяет конформацию, что закрепляет его на цепи ДНК.
Вслед за этим последовательно привлекаются MutL и MutH
Слайд 25Что узнается ?
MutS димер (у дрожжей, Msh2/Msh3 или Msh2/Msh6 гетеродимер)
Эксперименты
по связыванию с ДНК in vitro и репарации гетеродуплексов in
vivo показали, что MMR узнает все комбинации неспаренных оснований, кроме C:C, а также короткие <4 п.н. делеции и инсерции («инделы»)
неправильные пары G:T and A:C и инсерции/делеции в 1 п. особенно хорошо узнаются. Эти нарушения являются наиболее частыми ошибками ДНК-полимераз
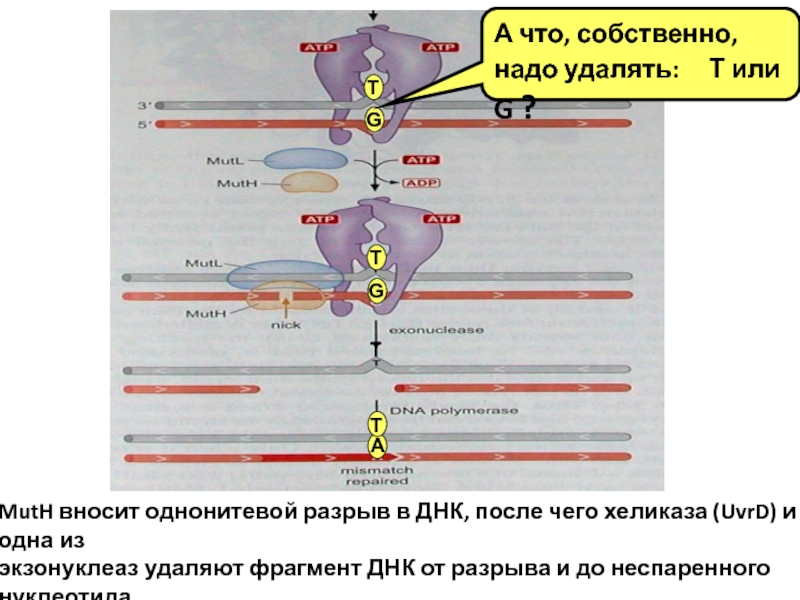
Слайд 26MutH вносит однонитевой разрыв в ДНК, после чего хеликаза (UvrD)
и одна из
экзонуклеаз удаляют фрагмент ДНК от разрыва и до
неспаренного нуклеотида
(включая последний). Брешь застраивается ДНК полимеразой.
T
T
G
G
T
T
A
А что, собственно, надо удалять: T или G ?
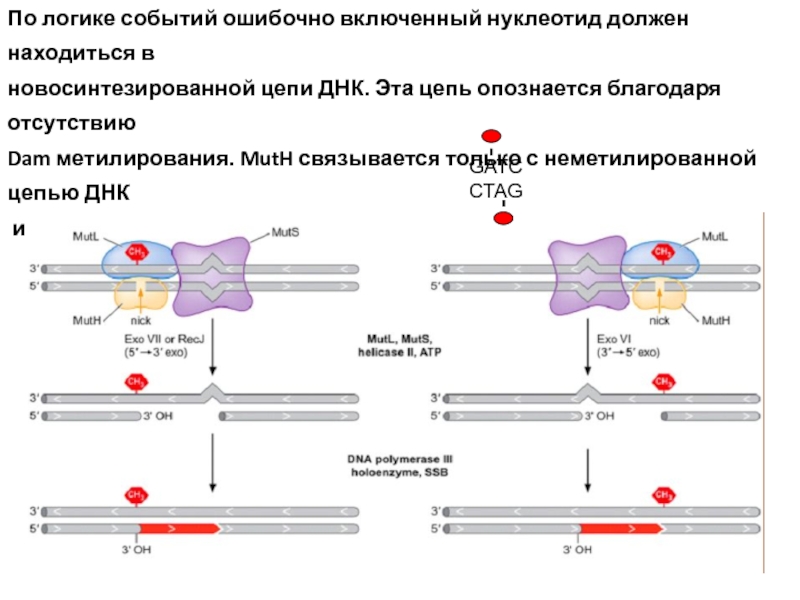
Слайд 27По логике событий ошибочно включенный нуклеотид должен находиться в
новосинтезированной
цепи ДНК. Эта цепь опознается благодаря отсутствию
Dam метилирования. MutH
связывается только с неметилированной цепью ДНК
и вносит разрыв именно в эту цепь
GATC
CTAG
Слайд 28гомологи MutS (MSH — MutS homolog) образуют два
гетеродимерных комплекса:
♣
MSH2-MSH6 (MutSα) узнает неспаренные нуклеотиды
и короткие «инделы»
♣ MSH2-MSH3 (MutSβ)
узнает длинные «инделы»
В эукариотических клетках также существует система
коррекции ошибок репликации
Обнаружены гомологи MutS и MutL;
гомолога MutH не обнаружено
Механизм распознавания новосинтезированной цепи не известен
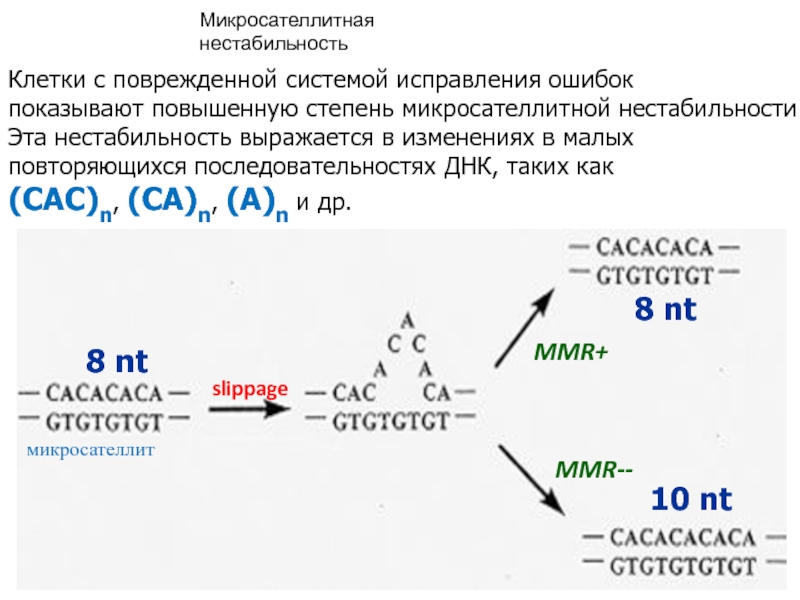
Слайд 29Микросателлитная нестабильность
Клетки с поврежденной системой исправления ошибок
показывают повышенную степень
микросателлитной нестабильности
Эта нестабильность выражается в изменениях в малых
повторяющихся последовательностях
ДНК, таких как
(САС)n, (CA)n, (A)n и др.
микросателлит
slippage
MMR+
MMR--
8 nt
8 nt
10 nt
Слайд 30А если не успели всё починить,
а ДНК уже реплицируется?
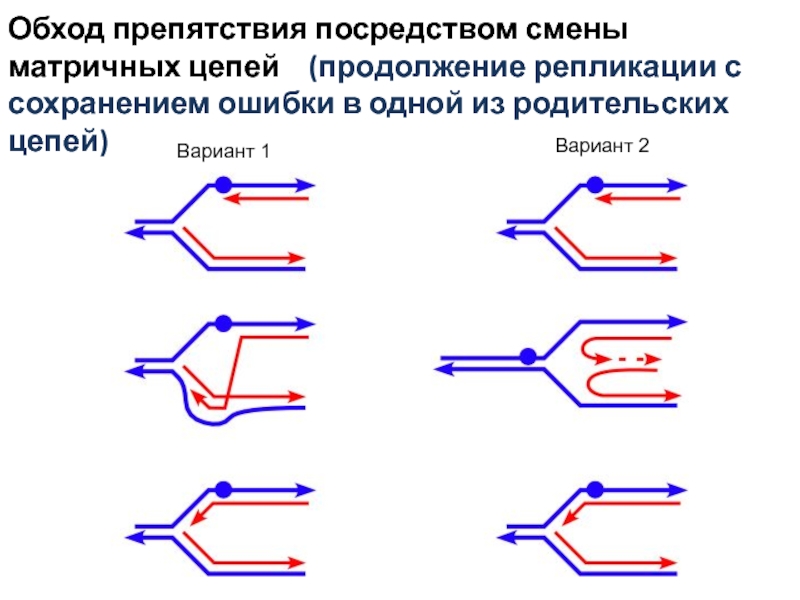
Слайд 31Обход препятствия посредством смены матричных цепей (продолжение репликации с
сохранением ошибки в одной из родительских цепей)
Вариант 1
Вариант 2
Слайд 32существут возможность, что после
остановки вилки репликация начнется
снова после препятствия (с
нового
праймера)
Тогда напротив препятствия будет
брешь. В последствии может
произойти гомологичная рекомбинация,
(обмен участками между
новосинтезированной
и родительской цепями), в результате чего
появится донор гомологии
и брешь будет застроена
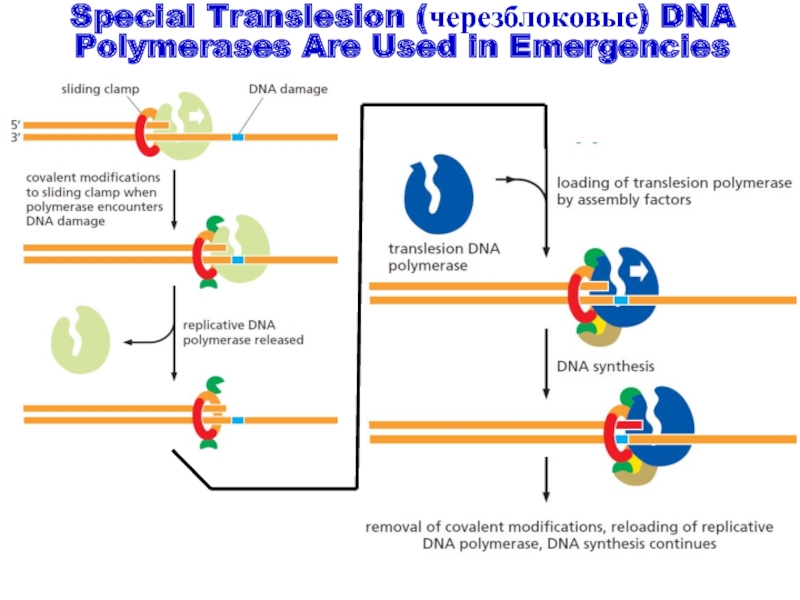
Слайд 33Special Translesion (черезблоковые) DNA Polymerases Are Used in Emergencies
Слайд 34«черезблоковый» синтез катализируемой «мутасомой» (DNA pol V)
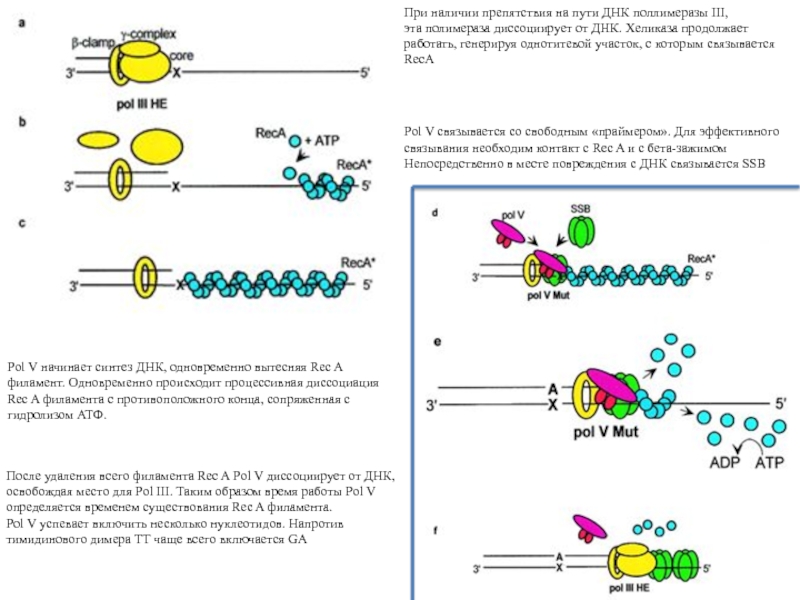
Слайд 35При наличии препятствия на пути ДНК поллимеразы III,
эта полимераза
диссоциирует от ДНК. Хеликаза продолжает
работать, генерируя однотитевой участок, с которым
связывается
RecA
Pol V связывается со свободным «праймером». Для эффективного
связывания необходим контакт с Rec A и с бета-зажимом
Непосредственно в месте повреждения с ДНК связывается SSB
Pol V начинает синтез ДНК, одновременно вытесняя Rec A
филамент. Одновременно происходит процессивная диссоциация
Rec A филамента с противоположного конца, сопряженная с
гидролизом ATФ.
После удаления всего филамента Rec A Pol V диссоциирует от ДНК,
освобождая место для Pol III. Таким образом время работы Pol V
определяется временем существования Rec A филамента.
Pol V успевает включить несколько нуклеотидов. Напротив
тимидинового димера ТТ чаще всего включается GA
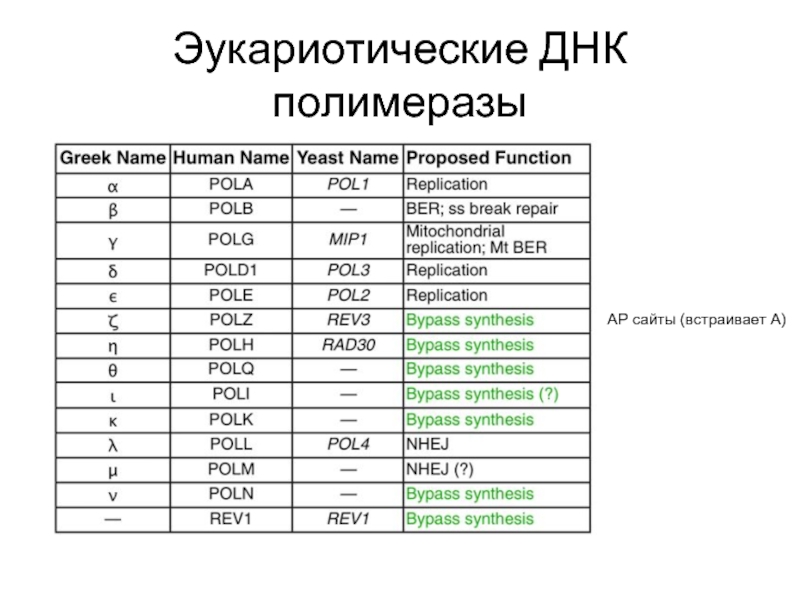
Слайд 36Эукариотические ДНК полимеразы
АР сайты (встраивает А)
Слайд 37Репарация двунитевых разрывов (SOS)
Двунитевые разрывы в ДНК возникают:
под действием
ионизирующего излучения
под действием некоторых химических агентов, в частности, ингибиторов ДНК
топоизомеразы II
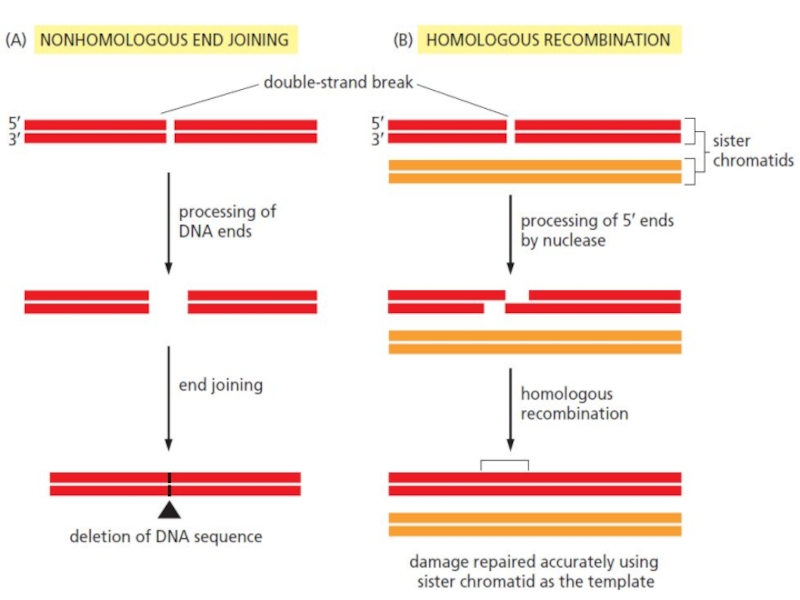
Существует два основных пути репарации
двунитевых разрывов:
гомологичная рекомбинация
негомологичное соединение концов ДНК (NHEJ)
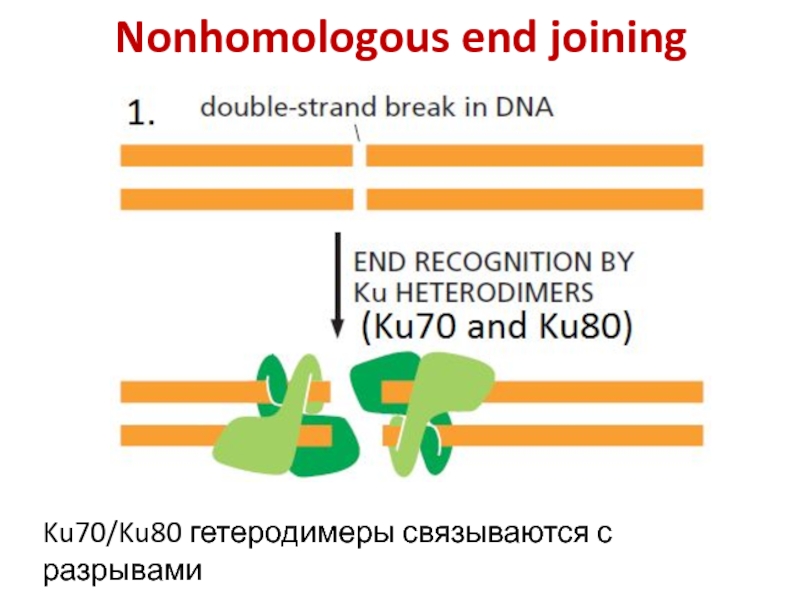
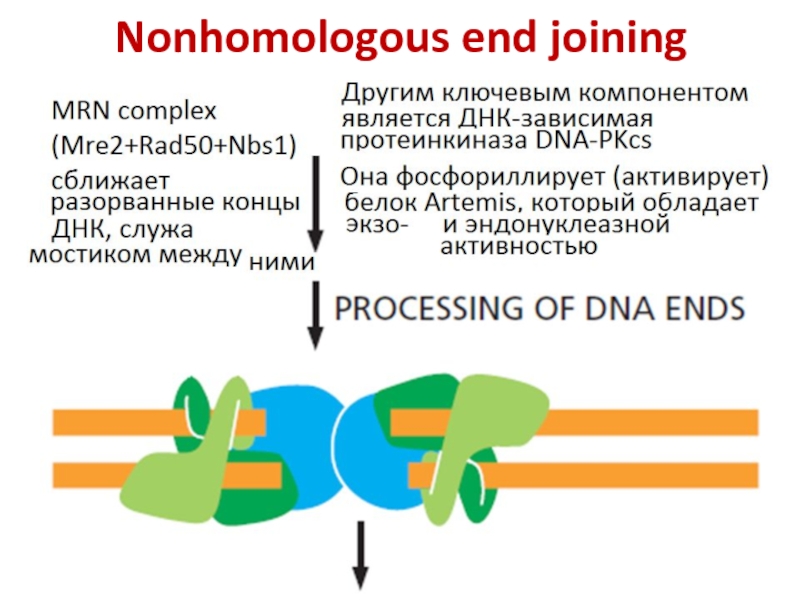
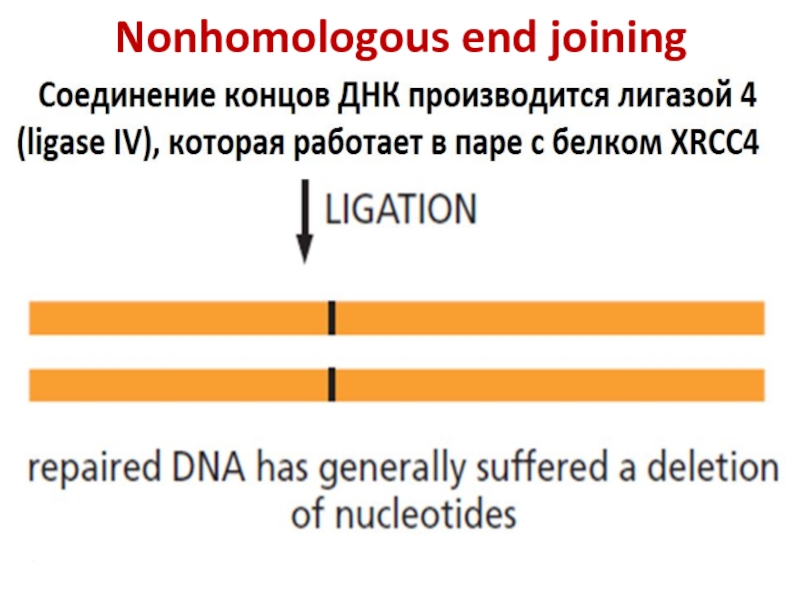
Слайд 39Nonhomologous end joining
Ku70/Ku80 гетеродимеры связываются с разрывами
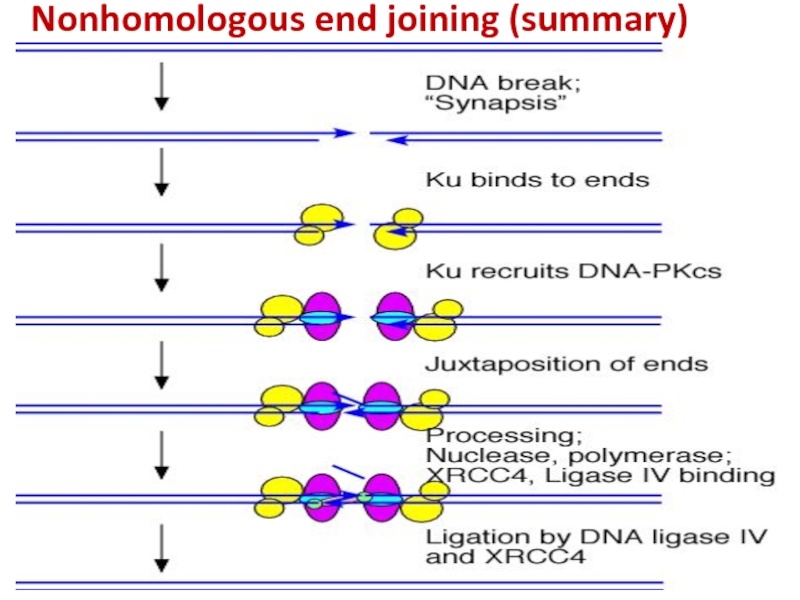
Слайд 42Nonhomologous end joining (summary)
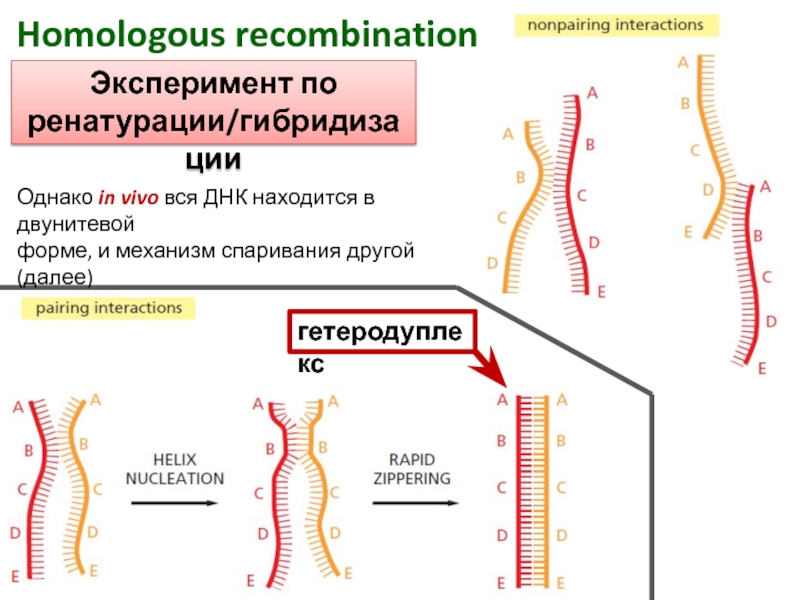
Слайд 43Homologous recombination
Эксперимент по
ренатурации/гибридизации
гетеродуплекс
Однако in vivo вся ДНК находится в
двунитевой
форме, и механизм спаривания другой (далее)
Слайд 44В отличие от NHEJ-механизма, при гомологичной
рекомбинации требуется поврежденную цепь
привести
в соприкосновение с неповрежденной гомологичной
цепью, которая будет служить в
качестве образца.
Поэтому ГР может происходить сразу после репликации
ДНК, когда дочерние цепи лежат близко друг к другу.
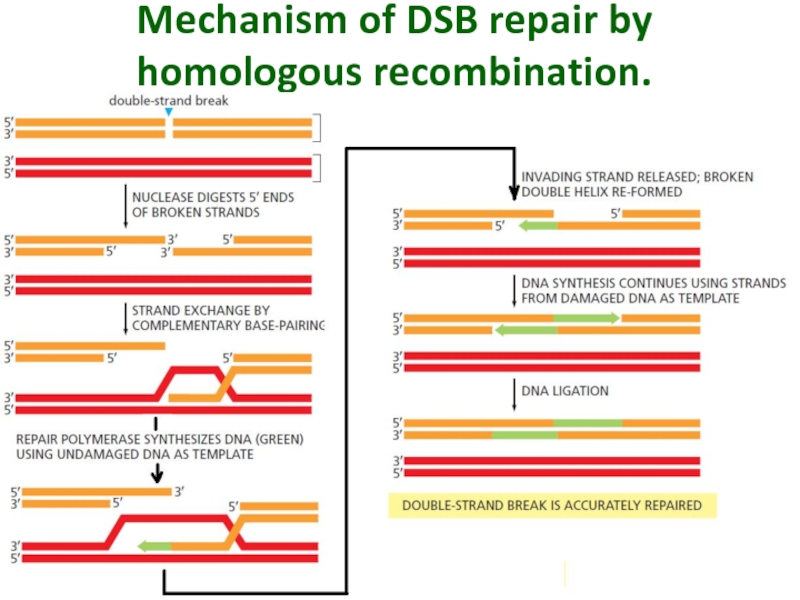
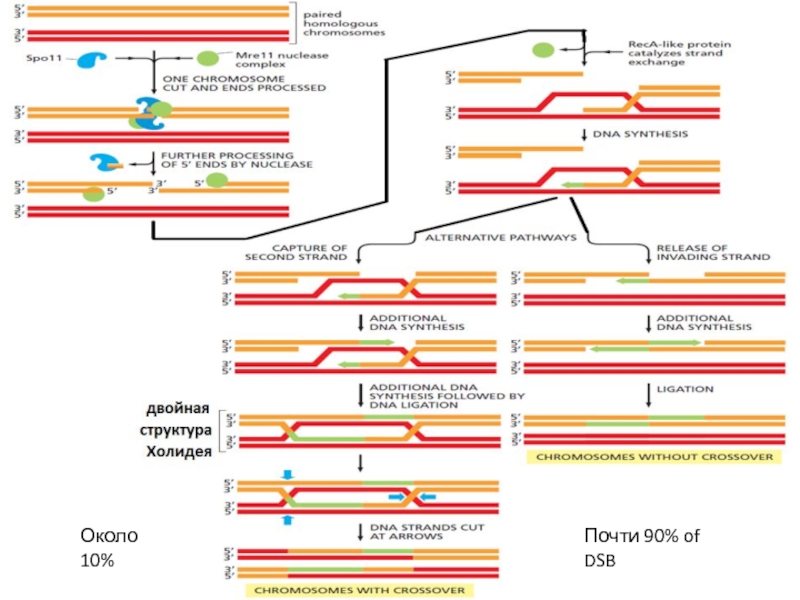
Слайд 45Mechanism of DSB repair by homologous recombination.
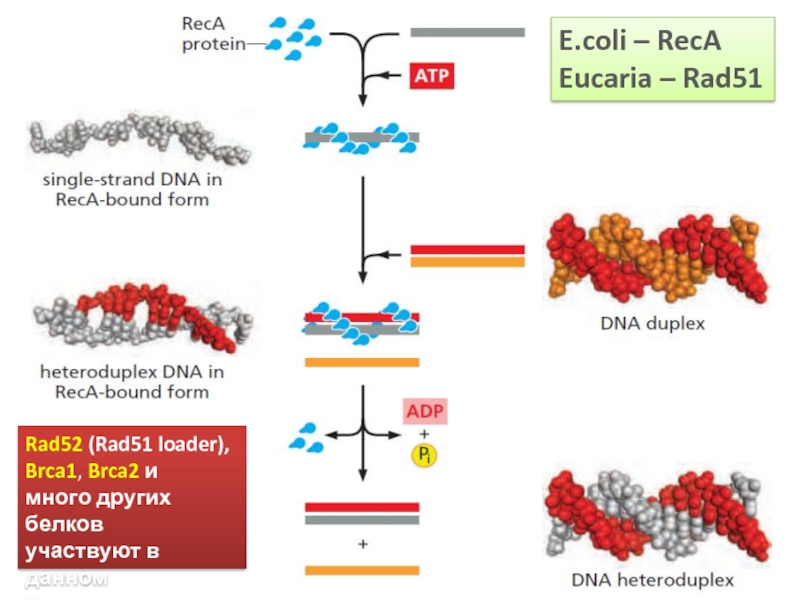
Слайд 46E.coli – RecA
Eucaria – Rad51
Rad52 (Rad51 loader),
Brca1, Brca2 и
много других белков
участвуют в данном
процессе
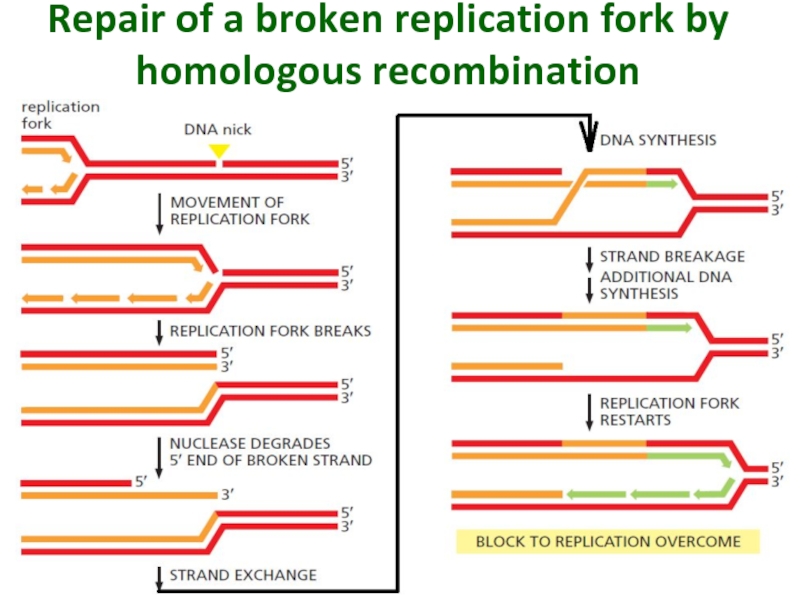
Слайд 47Repair of a broken replication fork by homologous recombination
Слайд 48Потеря гетерозиготности
Иногда при ГР используется не сестринская, а гомологичная копия
(вместо исправления материнской разорванной хромосомы используется не сестринская материнская, а
отцовская гомологичная хромосома и наоборот).
Поскольку последовательности ДНК в гомологах различаются, такой тип исправления может привести к конверсии участка материнской хромосомы в отцовский (и наоборот). Такая конверсия называется потерей гетерозиготности и может в некоторых случаях (если в отцовской хромосоме в данном участке присутствуют онкомутации) приводить к онкозаболеваниям.
Слайд 49BRCA1 и BRCA2 – участники гомологичной рекомбинации. Мутации в них
ведут к наследственным формам рака груди и яичника.
BRCA1 регулирует
ранний процессинг концов в разорванной ДНК, и без него не происходит должной подготовки DSB к ГР, вместо этого такой разрыв репарируется по механизму NHEJ, вносящим мутации.
BRCA2 связывает Rad51 и не дает ему полимеризоваться на ДНК без надобности, поддерживая его в неактивной форме до той поры, пока он не будет нужен. При обнаружении поврежденной ДНК BRCA2 быстро доставляет Rad51 к месту повреждения и позиционирует его на ssDNA активный Rad51.
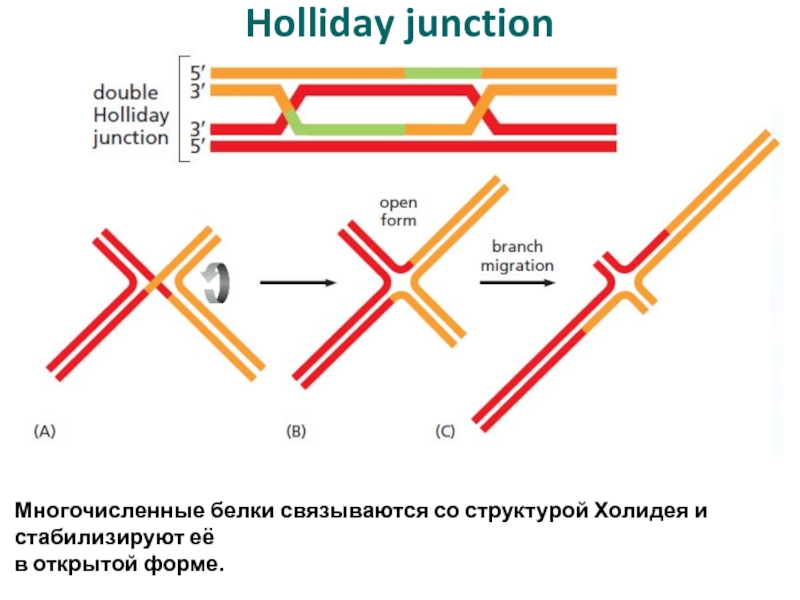
Слайд 51Holliday junction
Многочисленные белки связываются со структурой Холидея и стабилизируют её
в открытой форме.
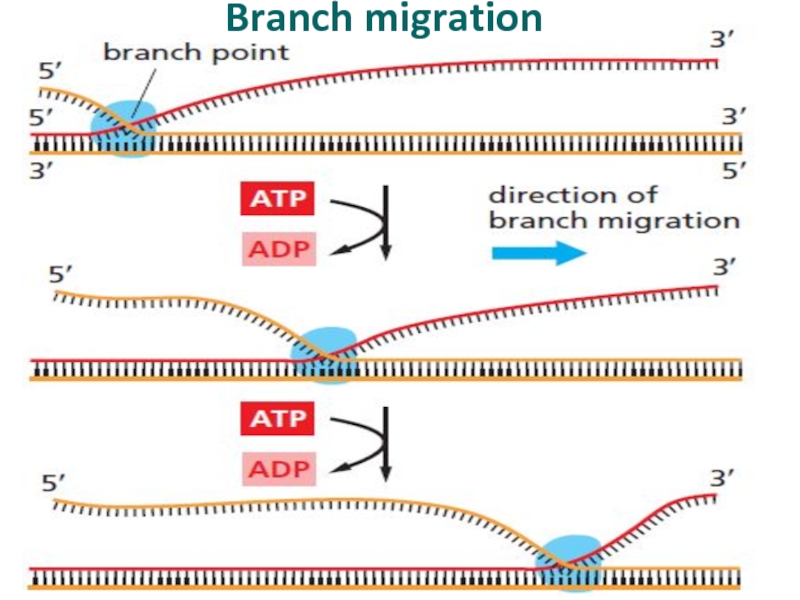
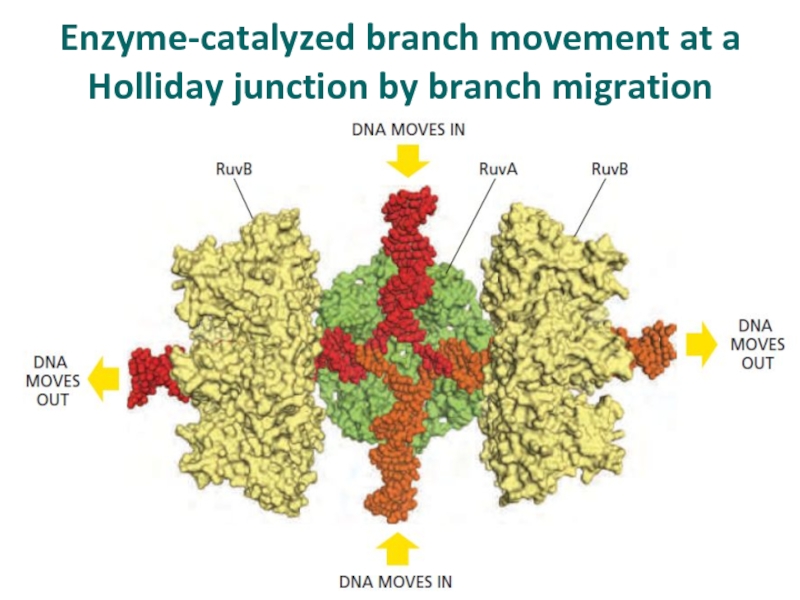
Слайд 53Enzyme-catalyzed branch movement at a Holliday junction by branch migration
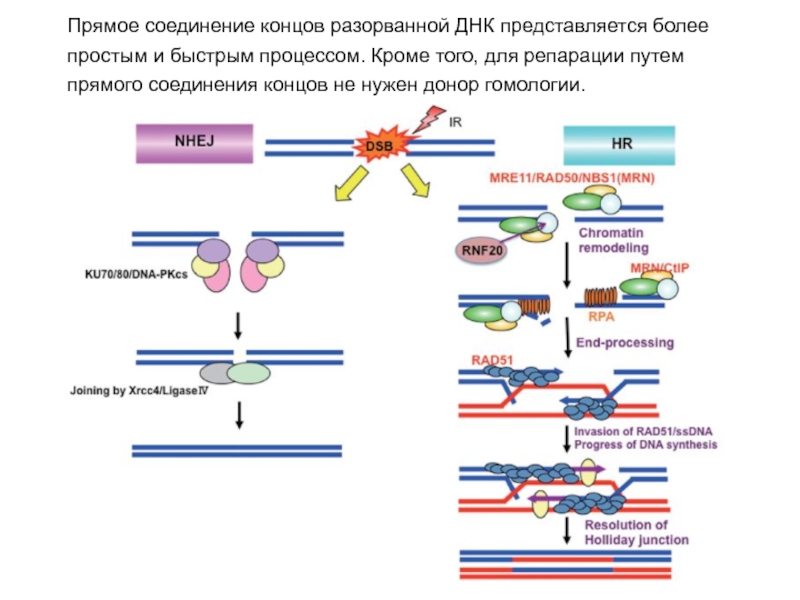
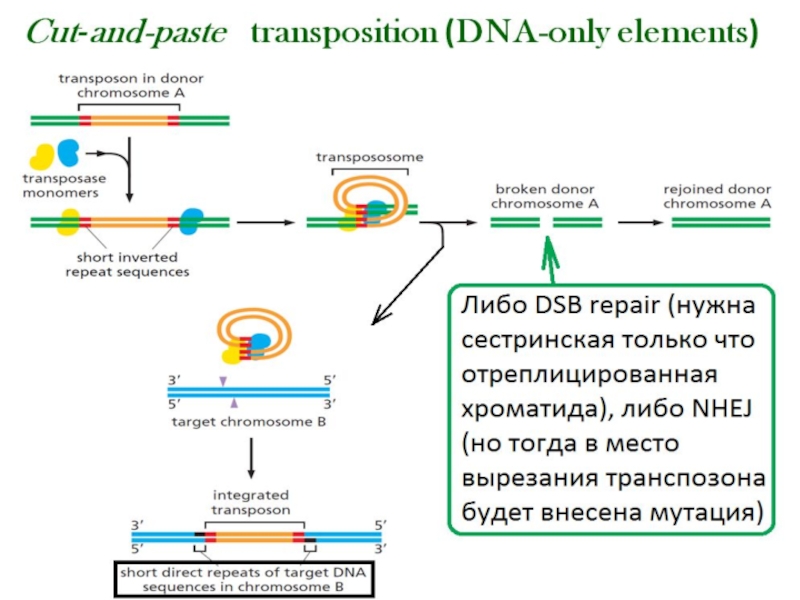
Слайд 54Прямое соединение концов разорванной ДНК представляется более
простым и быстрым процессом.
Кроме того, для репарации путем
прямого соединения концов не нужен донор
гомологии.
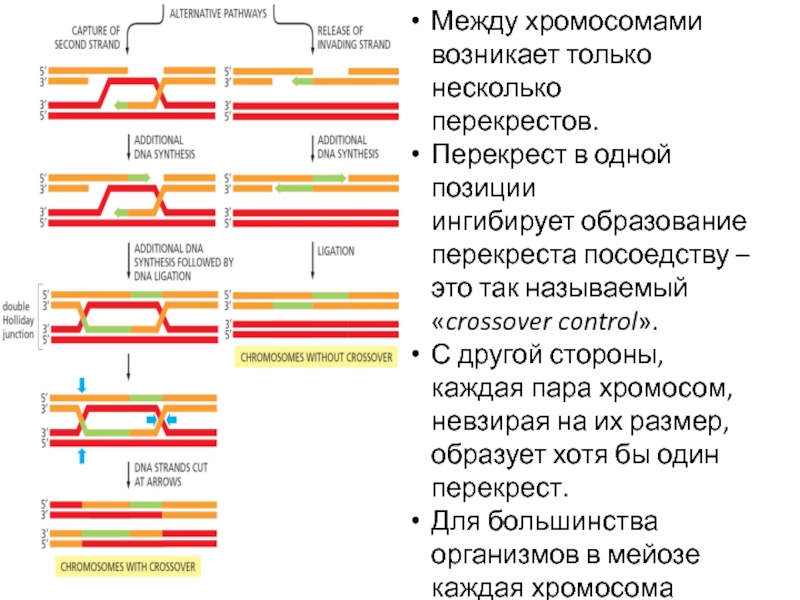
Слайд 55Между хромосомами
возникает только несколько
перекрестов.
Перекрест в одной позиции
ингибирует образование
перекреста посоедству –
это так называемый
«crossover control».
С другой стороны,
каждая пара хромосом,
невзирая на их размер,
образует хотя бы один
перекрест.
Для большинства
организмов в мейозе
каждая хромосома
образует два перекреста –
по одному на каждое плечо.
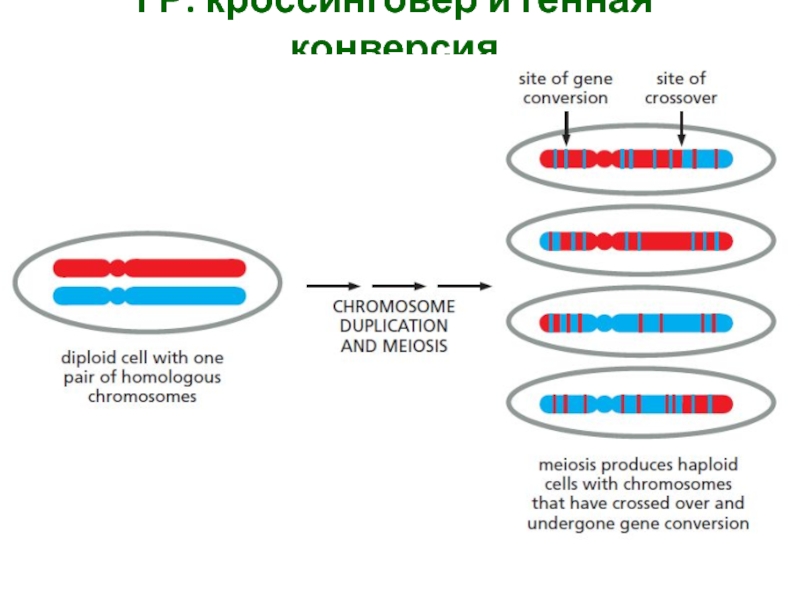
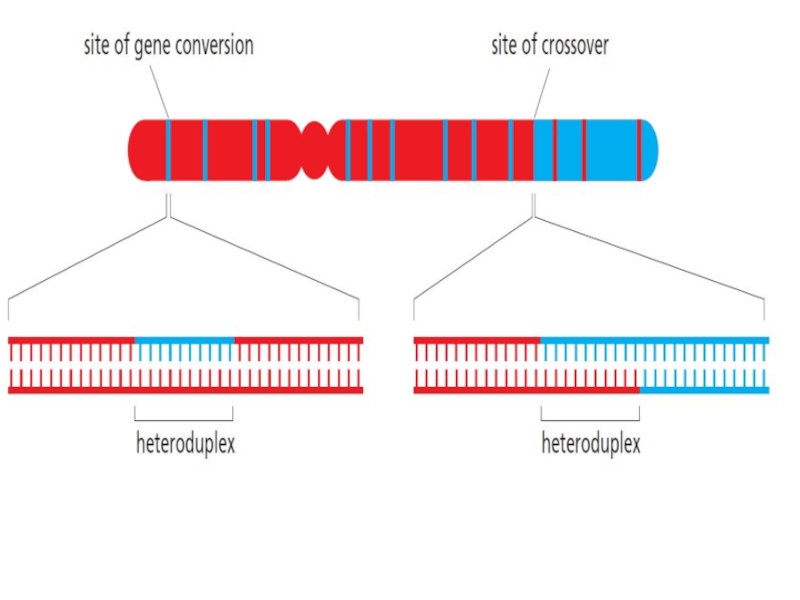
Слайд 56ГР: кроссинговер и генная конверсия
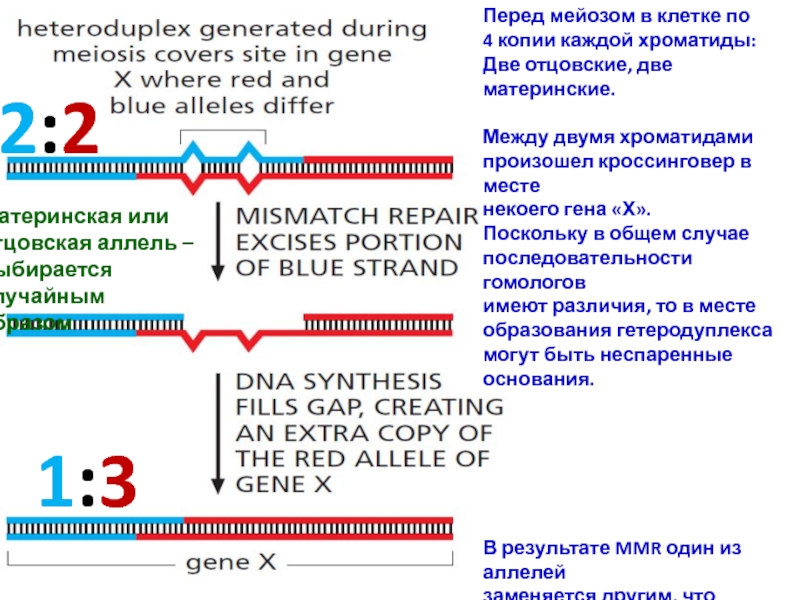
Слайд 582:2
1:3
Перед мейозом в клетке по
4 копии каждой хроматиды:
Две отцовские,
две материнские.
Между двумя хроматидами
произошел кроссинговер в месте
некоего гена
«Х».
Поскольку в общем случае
последовательности гомологов
имеют различия, то в месте
образования гетеродуплекса
могут быть неспаренные
основания.
В результате MMR один из аллелей
заменяется другим, что приводит
к дисбалансу в количестве
материнских и отцовских аллелей –
Генная конверсия.
Материнская или
отцовская аллель –
выбирается случайным
образом
Слайд 59TRANSPOSITION AND CONSERVATIVE SITE-SPECIFIC RECOMBINATION
Слайд 60Мобильные генетические элементы
(транспозоны)
ДНК транспозоны (у прокариот и эукариот)
для перемещения нужна транспозаза
(интеграза)
возможно простое перемещение (без увеличения
числа копий) либо создание новых копий
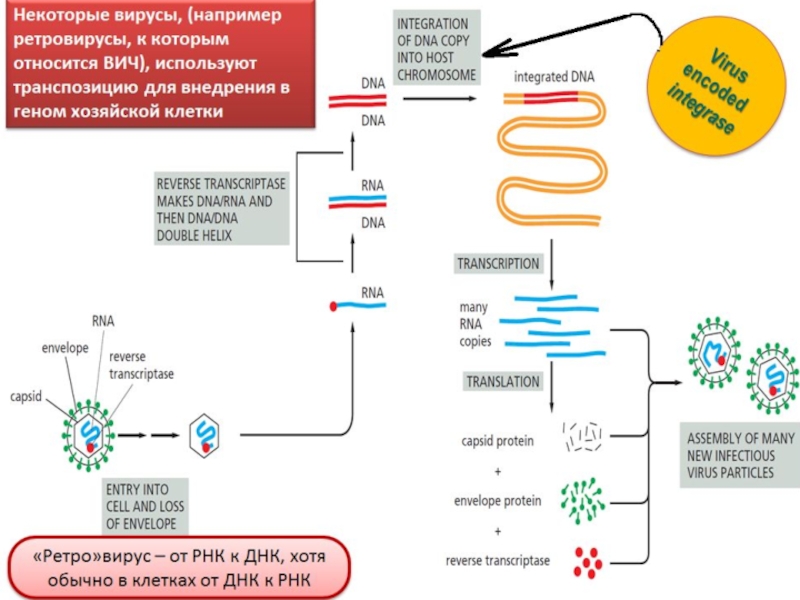
Ретро-транспозоны (у эукариот)
перемещение всегда посредством создания новой
копии
промежуточная РНК-копия
обратная транскриптаза
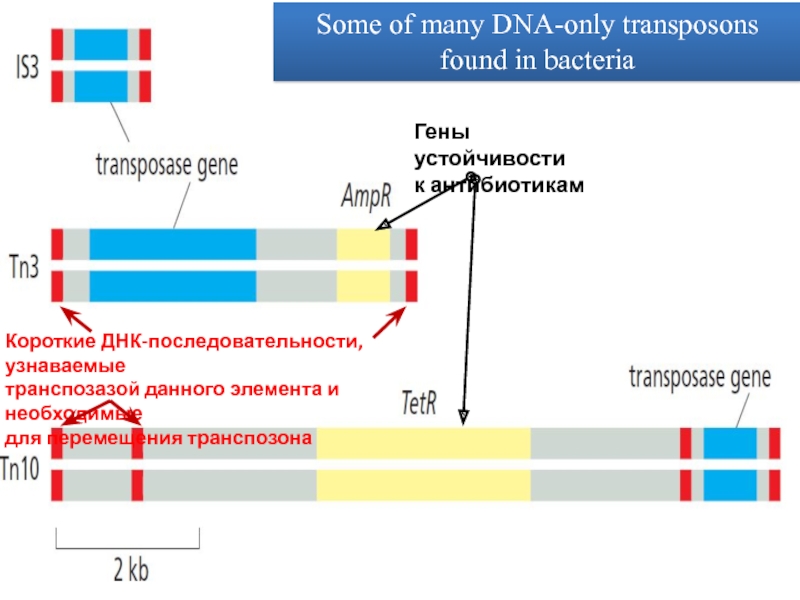
Слайд 61Some of many DNA-only transposons found in bacteria
Гены устойчивости
к антибиотикам
Короткие
ДНК-последовательности, узнаваемые
транспозазой данного элемента и необходимые
для перемещения транспозона
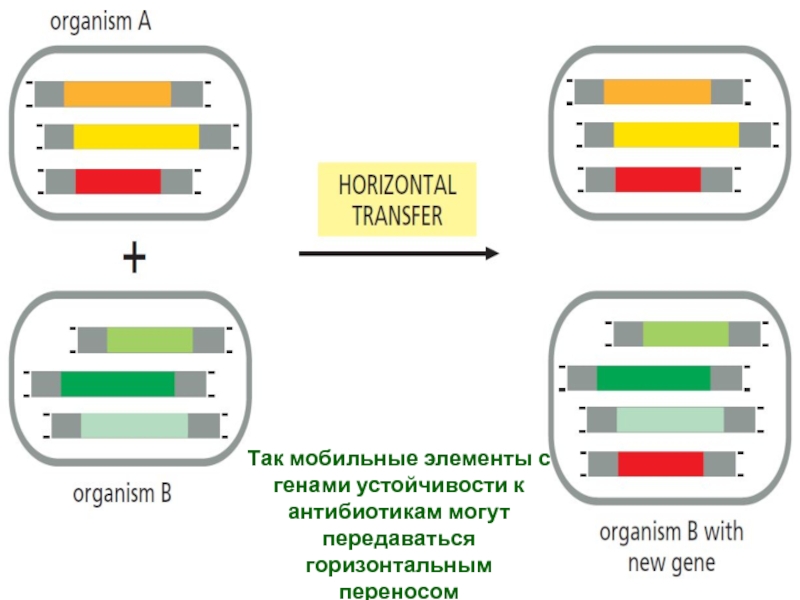
Слайд 62Так мобильные элементы с
генами устойчивости к
антибиотикам могут
передаваться
горизонтальным
переносом
Слайд 65retroviral-like retrotransposons
Сходны с ретровирусами, но сами не могут покидать
хозяйскую
клетку.
Весь ретротранспозон транскрибируется системой
транскрипции хозяйской клетки.
После трансляции с него
синтезируется обратная
транскриптаза, которая синтезирует на dsDNA на
матрице РНК, используя РНК-ДНК гибрид в качестве
интермедиата.
Как и ретровирус, линейная dsDNA теперь интегриру-
ется в геном хозяйской клетки, используя закодирован-
ную в ретротранспозоне интегразу.
Теперь мобильный элемент может передаваться
потомству клетки.
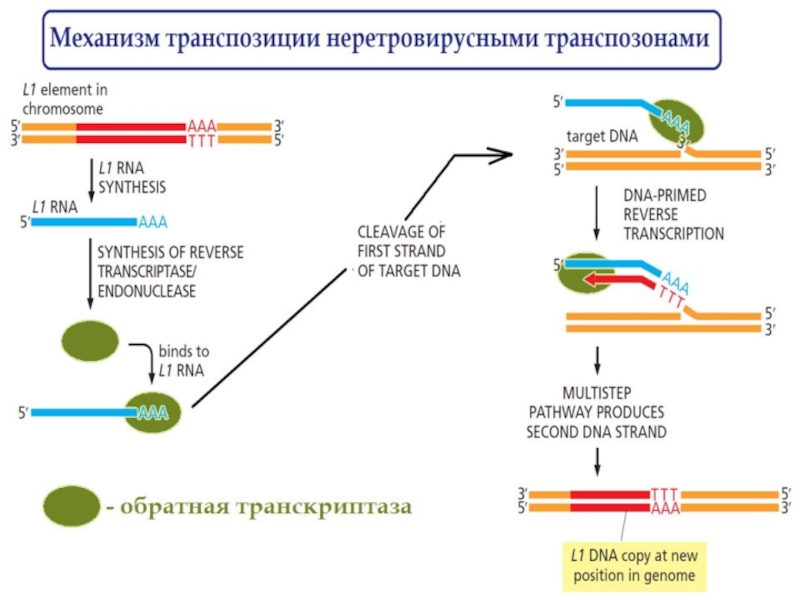
Слайд 66nonretroviral retrotransposons
Третий большой класс мобильных элементов, большинство из
которых в
геноме человека неподвижно, однако некоторые
представители являются подвижными. Например L1-элемент
(от аббревиатуры LINE - Long Interspersed Nuclear Element
(ок. 500 тыс копий)
L1-элемент ответственнен за один из типов гемофилии,
возникающей вследствие встраивания этого элемента
в ген участвующего в свертывании крови белка
Фактор VIII (Антигемофильный глобулин)
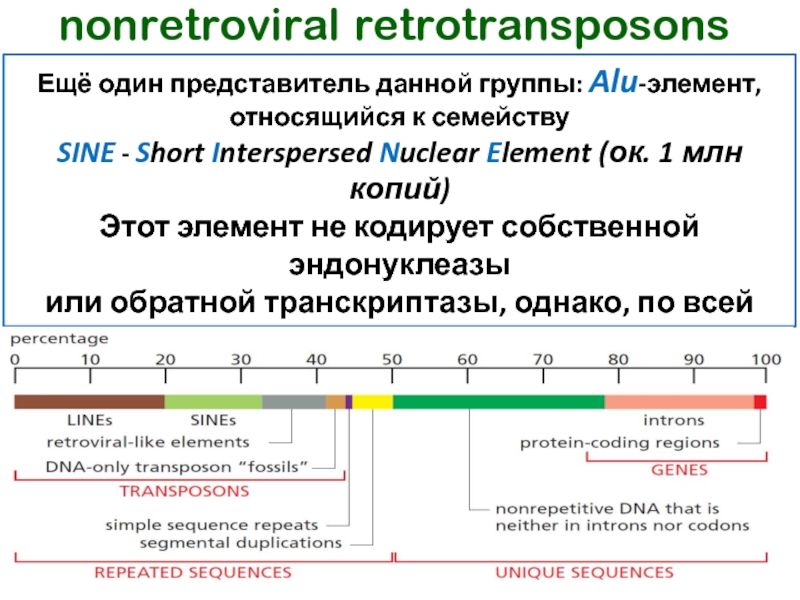
Слайд 68nonretroviral retrotransposons
Ещё один представитель данной группы: Alu-элемент,
относящийся к семейству
SINE - Short Interspersed Nuclear Element (ок. 1 млн копий)
Этот
элемент не кодирует собственной эндонуклеазы
или обратной транскриптазы, однако, по всей види-
мости, он использовал эти ферменты от других
мобильных элементов
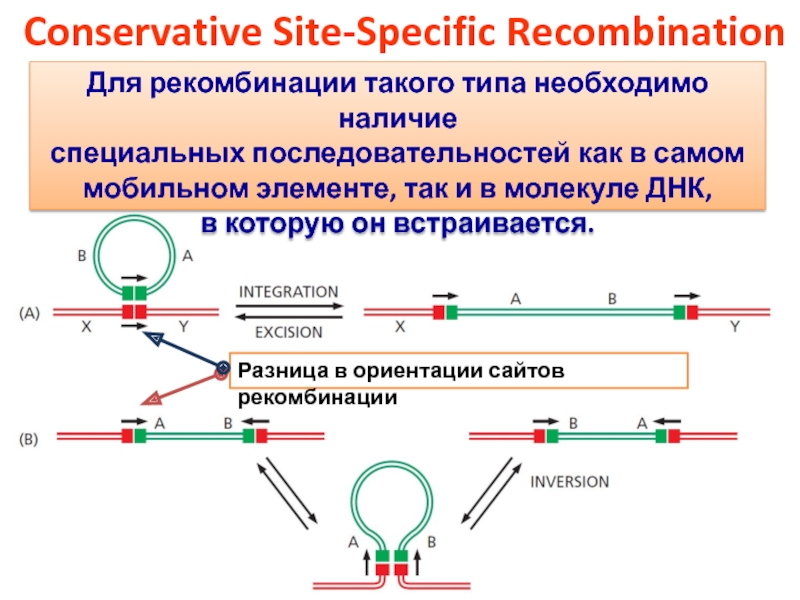
Слайд 69Conservative Site-Specific Recombination
Для рекомбинации такого типа необходимо наличие
специальных последовательностей
как в самом
мобильном элементе, так и в молекуле ДНК,
в которую он встраивается.
Разница в ориентации сайтов рекомбинации
Слайд 70Сайт-специфическая рекомбинация используется некоторыми ДНК-содержащими вирусами
При этом вирус встраивает свою
ДНК в ДНК клетки-хозяина, беспрепятственно реплицируется в ней (как часть
клеточной ДНК) и передается ничего не подозревающей клеткой её потомкам.
Однако при неблагоприятных обстоятельствах ДНК вируса может вырезаться из клеточной и «покидать тонущий корабль» ввиде собравшихся вирусных частиц.
Слайд 71Отличия сайт-специфической рекомбинации от транспозиции
SSR требует наличия специальных сайтов у
обоих участников процесса (сайт-специфичность). Для транспозиции необходимо наличие специальных (узнаваемых
рекомбиназой) лишь у транспозона, последовательность же хозяйской ДНК для большинстватранспозонов может быть любой.
Сами механизмы фундаментально различны.
В SSR рекомбиназа действует подобно топоизомеразам, образовывая транзиентную высокоэнергетичную ковалентную связь с ДНК, используя энергию этой связи для перегруппировки ДНК. При этом все разорванные фосфодиэфирные связи к концу процесса возвращаются на прежнее место (консервативность). Транспозиция не действует по такому механизму и после неё зачастую остаются бреши в ДНК, которые должны быть репарированы ДНК-полимеразами.
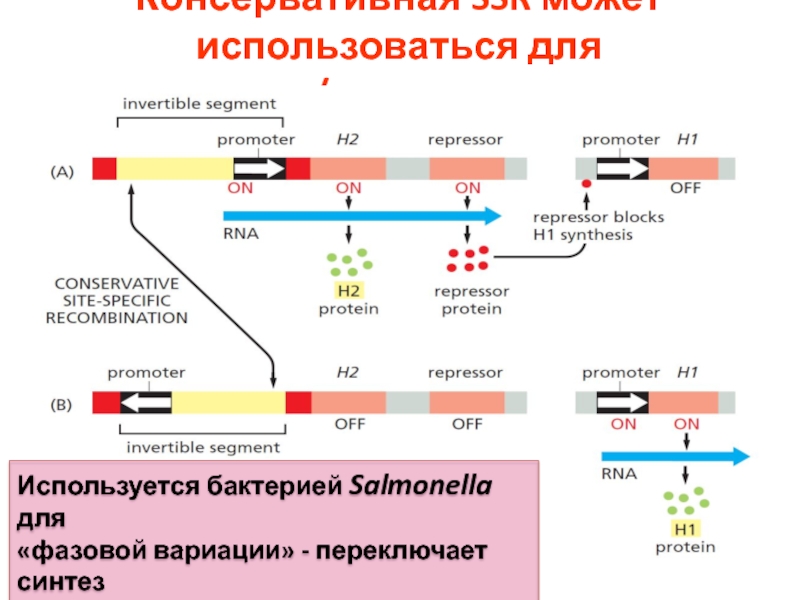
Слайд 72Консервативная SSR может использоваться для включения/выключения генов
Используется бактерией Salmonella для
«фазовой вариации» - переключает синтез
поверхностного антигена – флагеллина –
с одной формы на другую