Слайд 1ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В ПРОИЗВОДНЫХ
БЕНЗОЛА
Слайд 2ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Любая группа, связанная с кольцом, влияет на дальнейшее
течение электрофильного замещения. Это влияние выражается, во-первых, в изменении реакционной
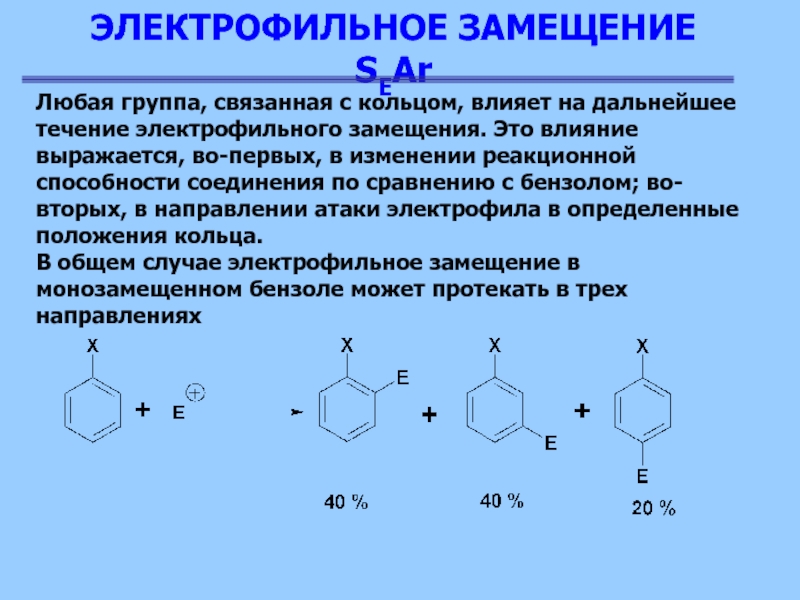
способности соединения по сравнению с бензолом; во-вторых, в направлении атаки электрофила в определенные положения кольца.
В общем случае электрофильное замещение в монозамещенном бензоле может протекать в трех направлениях
Слайд 3ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Если бы заместитель Х не изменял реакционную способность
положений в бензольном кольце, соотношение изомеров определялось бы статистическим фактором
(2- орто, 2-мета и 1-пара- положения).
Рассмотрим экспериментальные данные по нитрованию толуола и нитробензола
Слайд 4ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Как видно из этих данных, учет только статистического
фактора недостаточен для объяснения экспериментальных данных по нитрованию.
Любая группа, связанная
с кольцом, влияет на дальнейшее течение электрофильного замещения. Это влияние выражается, во-первых, в изменении реакционной способности соединения по сравнению с бензолом;
во-вторых, в направлении атаки электрофила в определенные положения кольца
Слайд 5Взаимное влияние атомов в молекуле
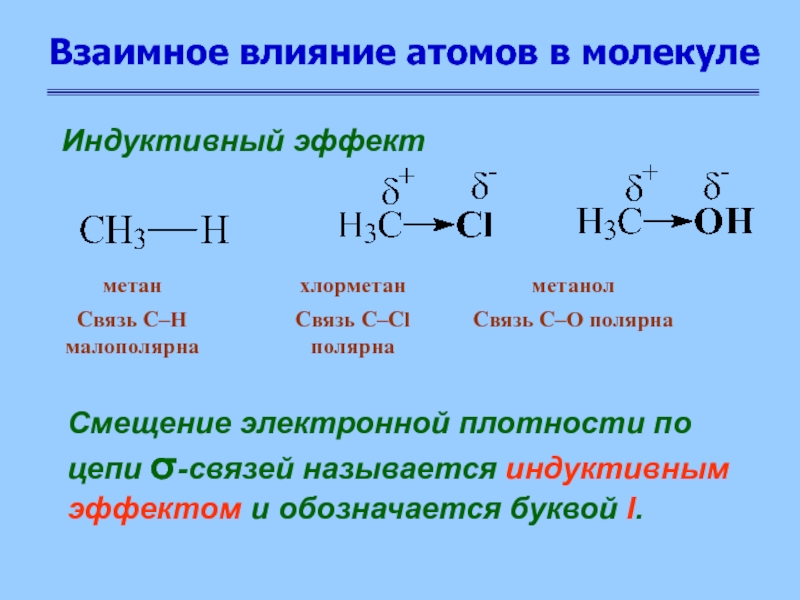
Индуктивный эффект
Смещение электронной плотности
по цепи σ-связей называется индуктивным эффектом и обозначается буквой I.
Слайд 6Взаимное влияние атомов в молекуле
Индуктивный эффект
+I-Эффект проявляют алифатические
углеводородные радикалы, т.е. алкильные радикалы (–CH3, –C2H5 и т. д.).
Большинство
функциональных групп проявляют -I-эффект: –Hal, –NH2, –OH, >С=O, –COOH.
пропен
Слайд 7Взаимное влияние атомов в молекуле
Индуктивный эффект
Электроноакцепторные заместители,
т.е.
атом или группа атомов, смещающие электронную плотность σ-связи от атома
углерода, проявляют отрицательный индуктивный эффект (-I-эффект).
Электронодонорные заместители, т. е. атом или группа атомов, смещающие электронную плотность к атому углерода, проявляют положительный индуктивный эффект
(+I-эффект).
Слайд 8Взаимное влияние атомов в молекуле
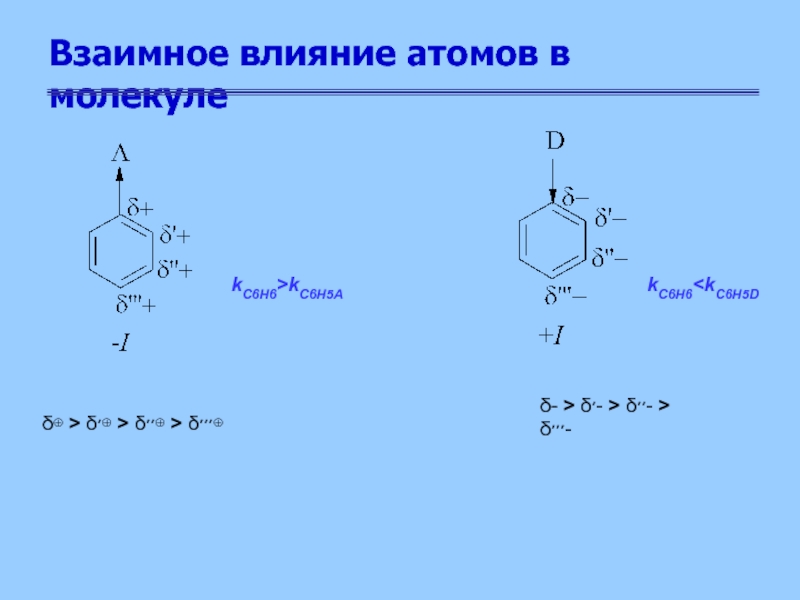
δ⊕ > δ׳⊕ > δ׳׳⊕
> δ׳׳׳⊕
δ- > δ׳- > δ׳׳- > δ׳׳׳-
kC6H6>kC6H5A
kC6H6
Слайд 9Взаимное влияние атомов в молекуле
Мезомерный эффект (эффект сопряжения) возникает
в сопряжённых системах – т.е. в системах, в которых имеет
место чередование простых связей и подвижных пар электронов. Подвижные пары электронов - это электроны кратных связей (π-электроны) или свободные пары электронов (n-электроны). Эти электроны не локализованы между двумя атомами или на одном атоме (n-электроны), а распределены по всей сопряженной системе, т.е. орбитали, на которых находятся электроны, перекрываются между собой и образуют новую орбиталь, охватывающую все атомы сопряженной системы
Слайд 10Взаимное влияние атомов в молекуле
Мезомерным эффектом называется перераспределение π-
и n-электронов в сопряженной системе под влиянием заместителя за счёт
перекрывания орбиталей, на которых находятся делокализующиеся электроны.
Положительным мезомерным эффектом (+ М) обладают электронодонорные группы, способные к частичной или полной передаче пары электронов в общую сопряженную систему
Слайд 11Взаимное влияние атомов в молекуле
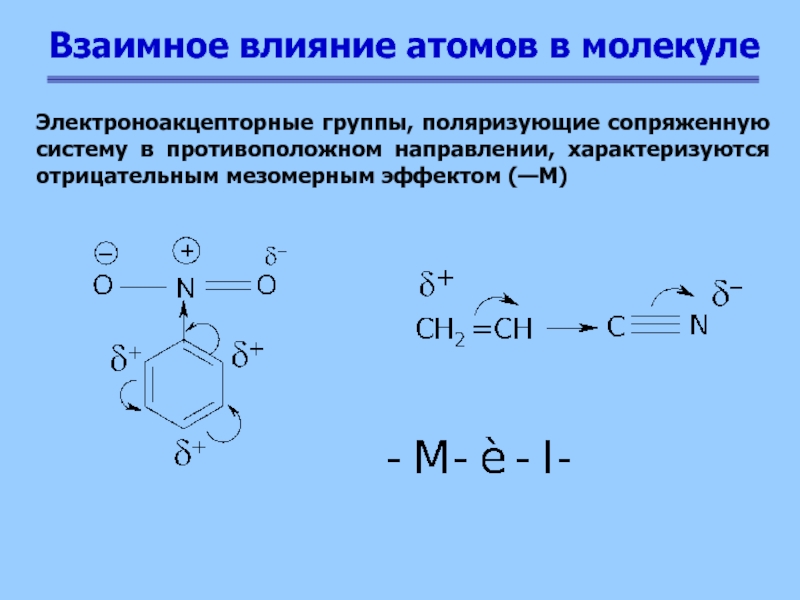
Электроноакцепторные группы, поляризующие сопряженную систему
в противоположном направлении, характеризуются отрицательным мезомерным эффектом (—М)
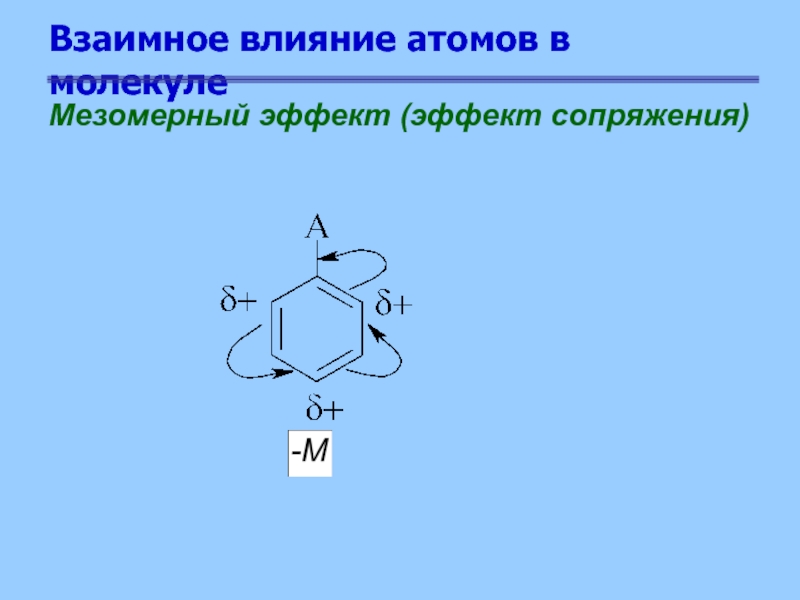
Слайд 12Взаимное влияние атомов в молекуле
Мезомерный эффект (эффект сопряжения)
Слайд 13Взаимное влияние атомов в молекуле
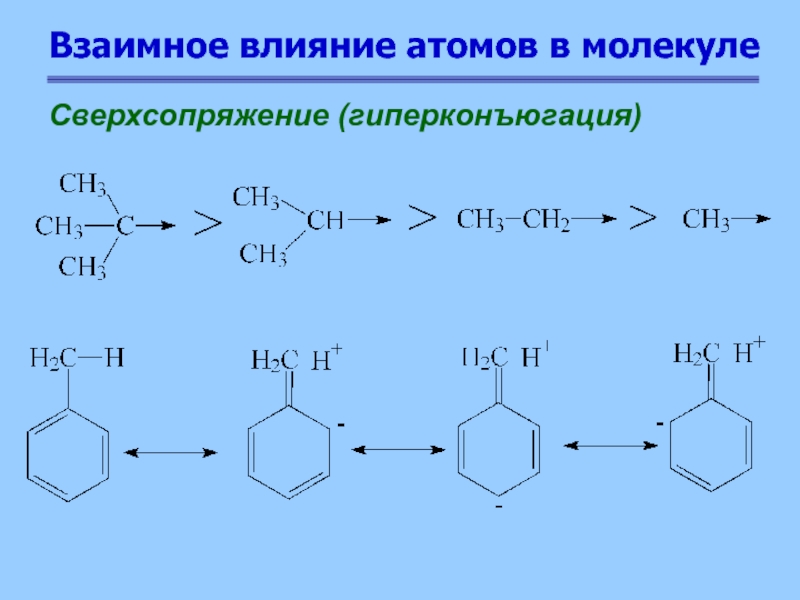
Сверхсопряжение (гиперконъюгация)
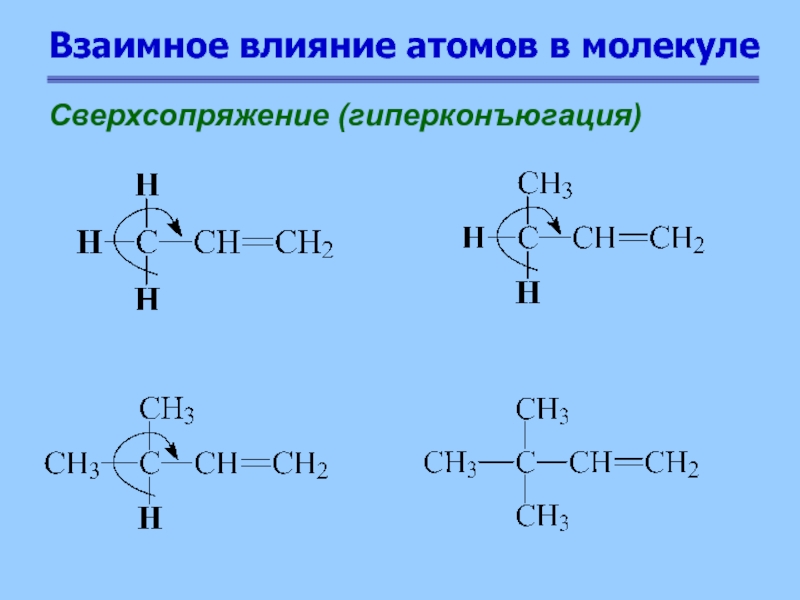
Слайд 14Взаимное влияние атомов в молекуле
Сверхсопряжение (гиперконъюгация)
Слайд 15ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
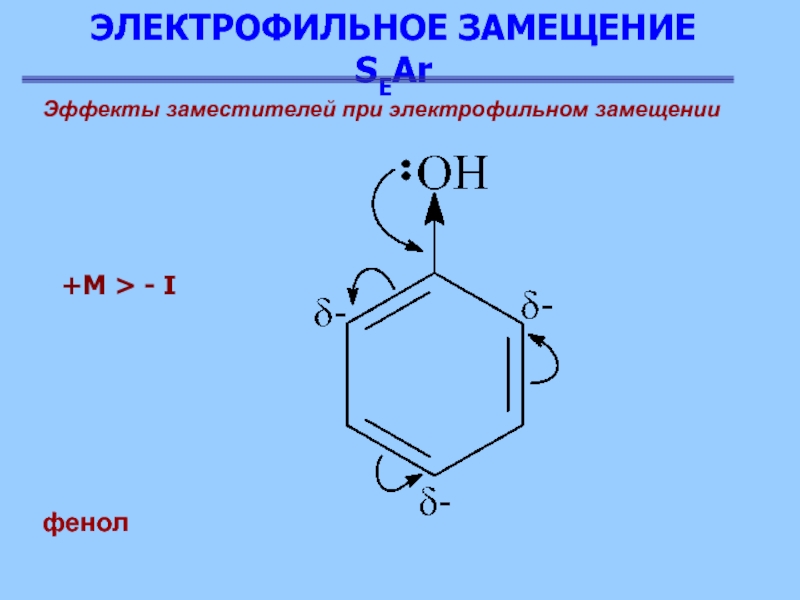
Эффекты заместителей при электрофильном замещении
фенол
+M > - I
Слайд 16ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
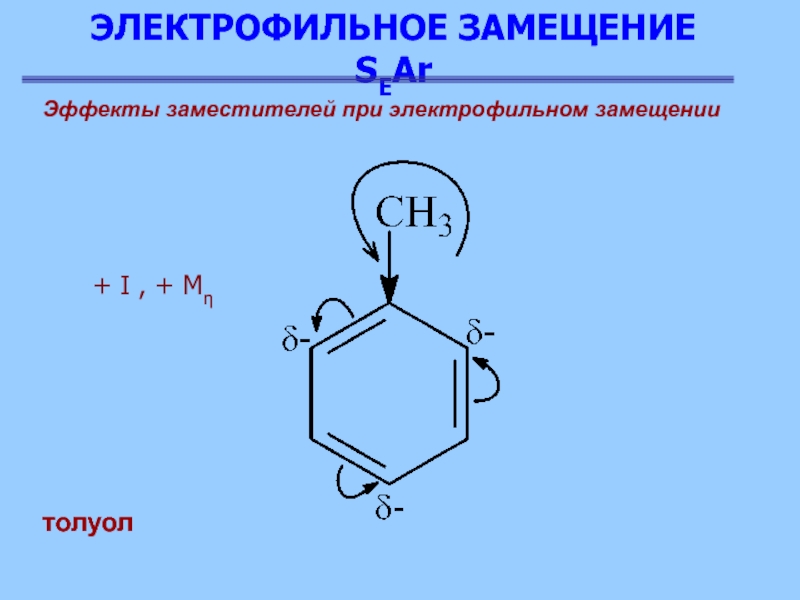
Эффекты заместителей при электрофильном замещении
толуол
+ I , +
Mη
Слайд 17ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
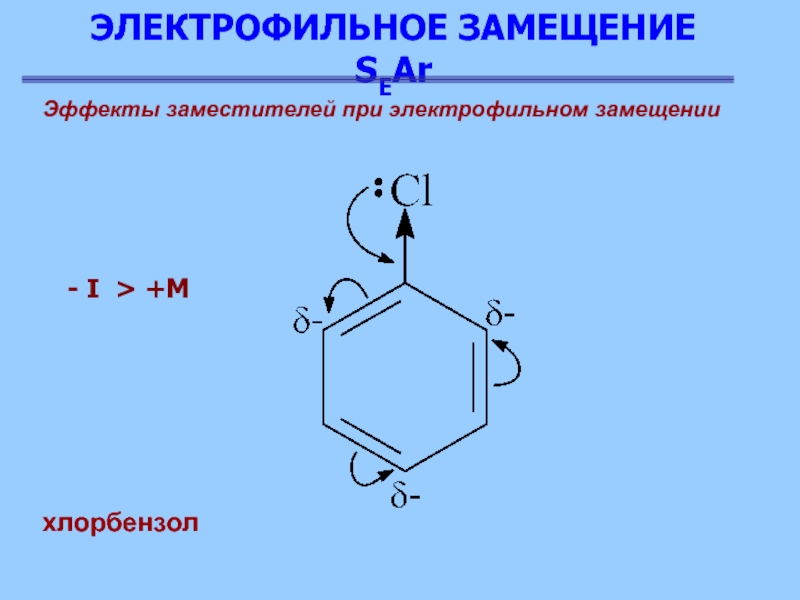
Эффекты заместителей при электрофильном замещении
хлорбензол
- I > +M
Слайд 18ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
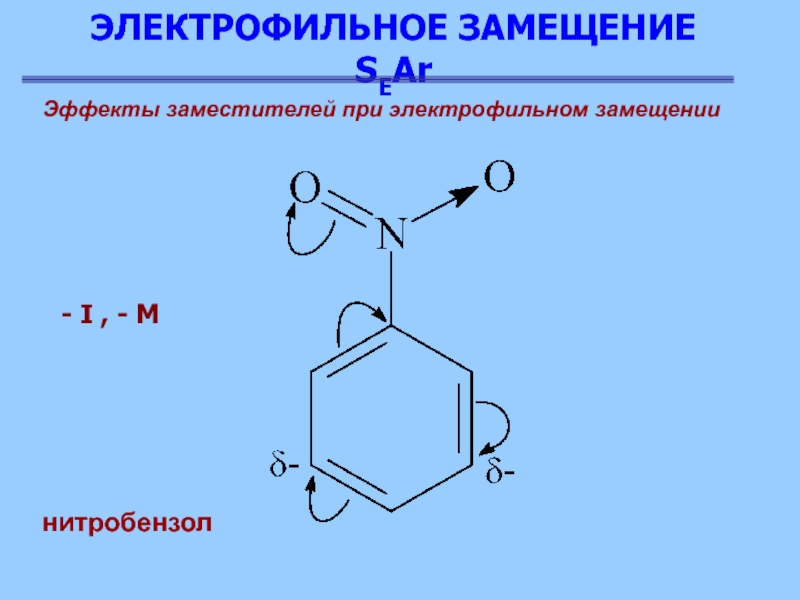
Эффекты заместителей при электрофильном замещении
нитробензол
- I , -
Слайд 19ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
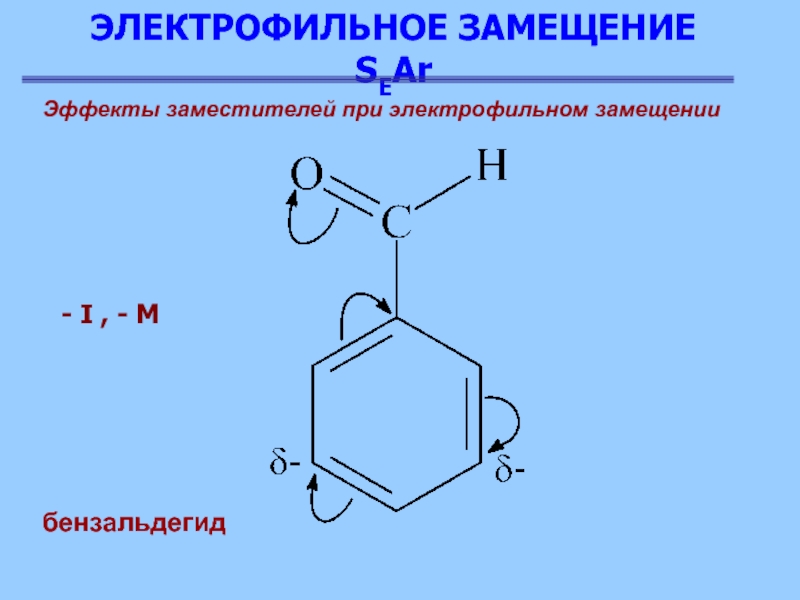
Эффекты заместителей при электрофильном замещении
бензальдегид
- I , -
Слайд 20ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Активирующими называются группы, под влиянием которых повышается реакционная
способность кольца по сравнению с бензолом.
Дезактивирующими являются группы, уменьшающие
реакционную способность кольца по сравнению с бензолом.
В медленной стадии электрофильного замещения образуется карбокатион. Факторы, стабилизирующие карбокатион, должны стабилизировать и активированный комплекс АК1, ведущий к его образованию. Стабилизация активированного комплекса означает уменьшение энергии активации медленной стадии, а, следовательно, увеличение скорости замещения. Факторы, которые дестабилизируют σ-комплекс, должны дестабилизировать и активированный комплекс и уменьшать скорость реакции.
Слайд 21ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Электронодонорные группы активируют все положения кольца, и особенно
сильно они активируют орто- и пара-положения.
Электроноакцепторные группы (кроме галогенов)
дезактивируют все положения кольца, но особенно сильно - орто и пара-положения.
Слайд 22ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
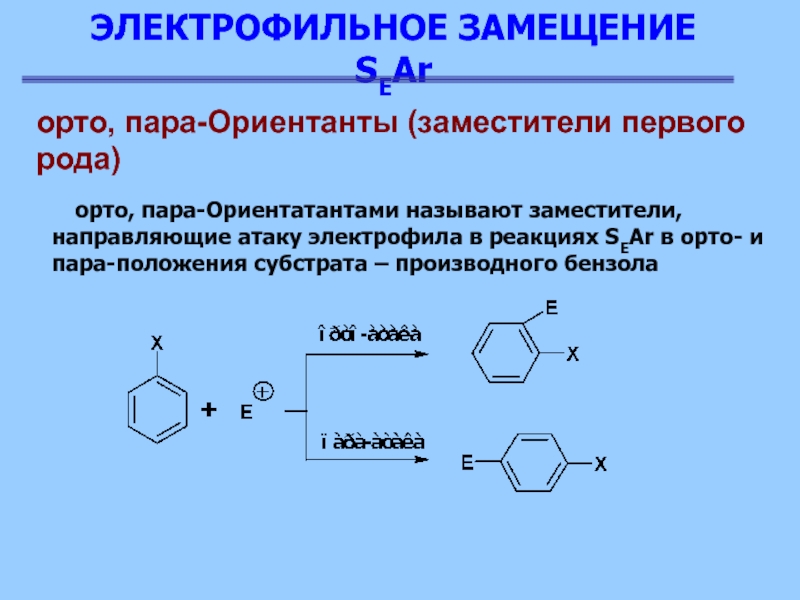
орто, пара-Ориентатантами называют заместители, направляющие атаку электрофила в
реакциях SEAr в орто- и пара-положения субстрата – производного бензола
орто,
пара-Ориентанты (заместители первого
рода)
Слайд 23ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
К орто- , пара-заместителям
относят все электронодонорные заместители и галогены: O-, NH2, NHR, NR2,
OH, NHCOCH3, NHCOR, OCH3, OR, -CH3 и другие алкилы, С6H5-, F, Cl, Br, I.
Слайд 24ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
Электронодонорные группы, сильноактивирующие кольцо:
Для этих групп характерно наличие неподеленной электронной пары у атомов
кислорода или азота, которые вступают в сопряжение с электронами ароматического ядра – электронодонорный эффект p-π-сопряжение (+М-эффект). Электронодонорный эффект p-π-сопряжения этих групп преобладает над электроноакцепторным индукционным эффектом (минус I-эффект), который является следствием большей электроотрицательности азота и кислорода по сравнению с углеродом
Слайд 25ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
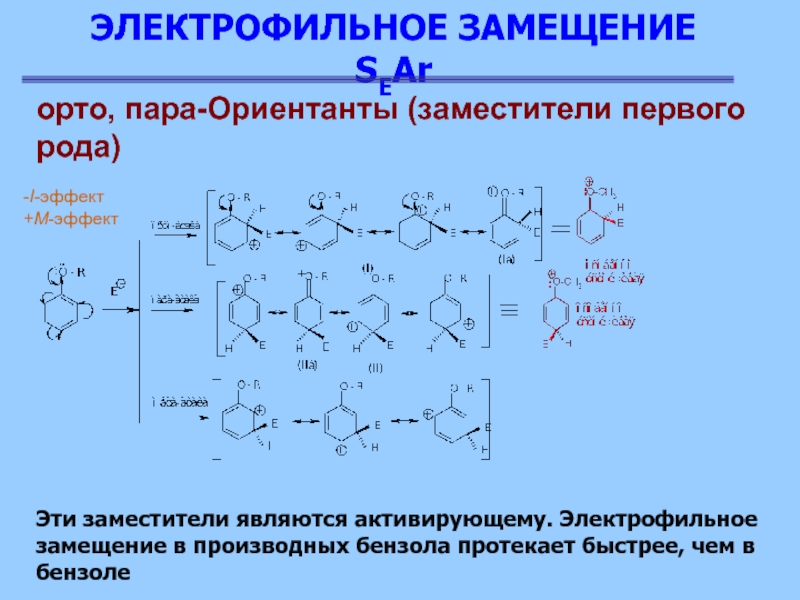
Эти заместители являются активирующему.
Электрофильное замещение в производных бензола протекает быстрее, чем в бензоле
-I-эффект
+М-эффект
Слайд 26АРЕНЫ
Электрофильное замещение в ароматическом ядре
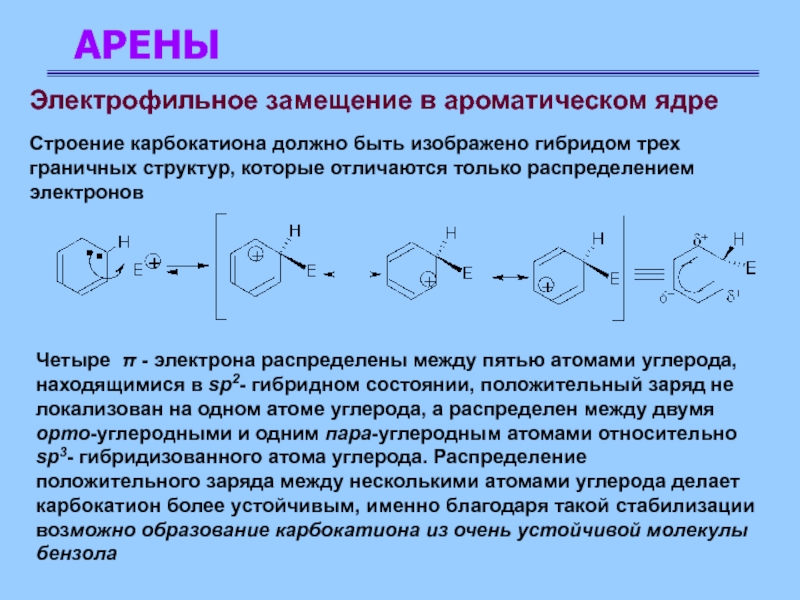
Строение карбокатиона должно быть изображено
гибридом трех граничных структур, которые отличаются только распределением электронов
Четыре
π - электрона распределены между пятью атомами углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизованного атома углерода. Распределение положительного заряда между несколькими атомами углерода делает карбокатион более устойчивым, именно благодаря такой стабилизации возможно образование карбокатиона из очень устойчивой молекулы бензола
Слайд 27ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
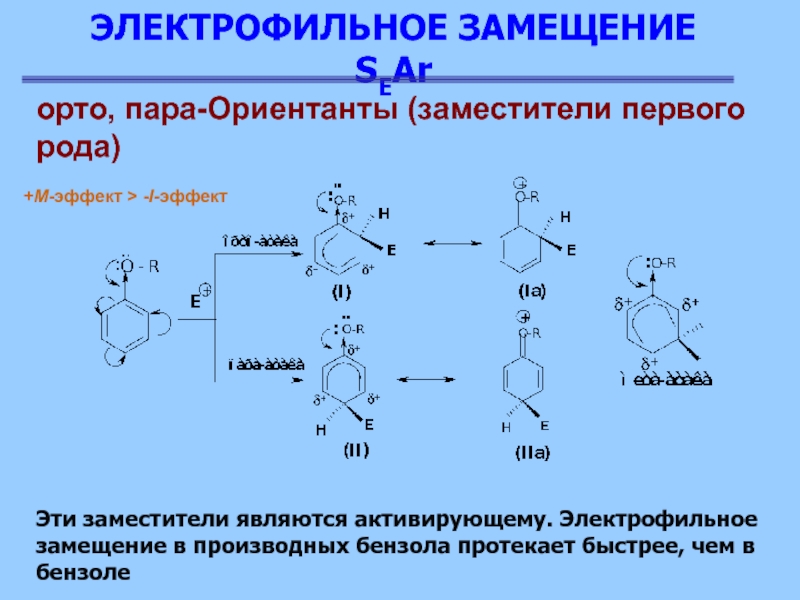
Эти заместители являются активирующему.
Электрофильное замещение в производных бензола протекает быстрее, чем в бензоле
+М-эффект > -I-эффект
Слайд 28ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
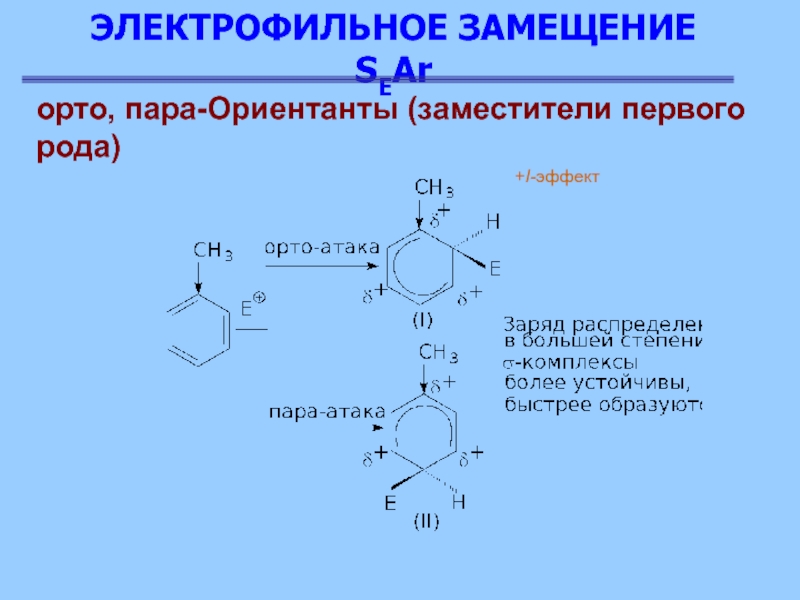
Группа -СН3 подает электроны
ко всем атомам кольца, но наибольшее влияние она оказывает на
тот атом, с которым непосредственно связана. В кабокатионах (I) и (II) метильная группа, подавая электроны на атом углерода, несущий положительный заряд, в некоторой степени погашает на нем заряд и сама приобретает частичный положительный заряд. В результате в кабокатионах (I) и (II) заряд оказывается распределенным в большей степени, чем в карбокатионе (III). Следовательно, о-, п-σ-комплексы (I) и (II) более устойчивы и быстрее образуются, чем м-σ-комплекс (III)
Слайд 29ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
+I-эффект
Слайд 30ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
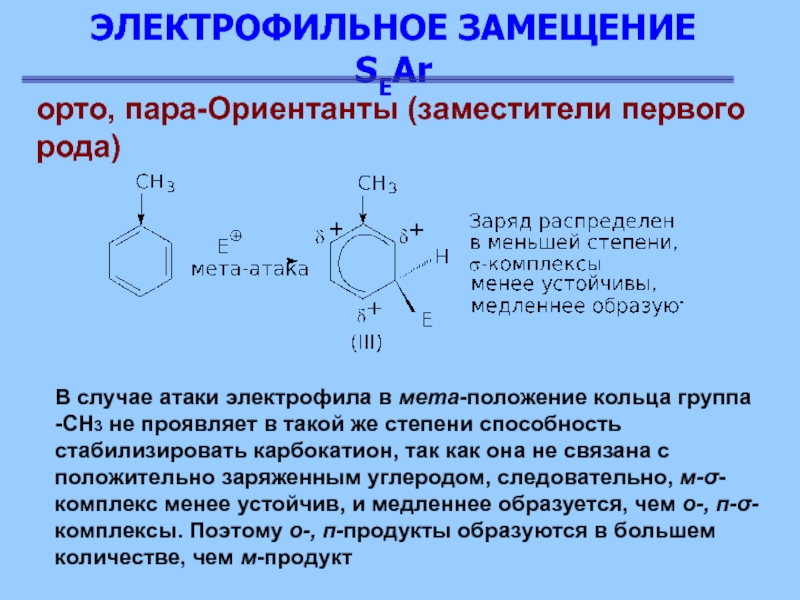
В случае атаки электрофила
в мета-положение кольца группа -СН3 не проявляет
в такой же степени способность стабилизировать карбокатион, так как она не связана с положительно заряженным углеродом, следовательно, м-σ-комплекс менее устойчив, и медленнее образуется, чем о-, п-σ-комплексы. Поэтому о-, п-продукты образуются в большем количестве, чем м-продукт
Слайд 31ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
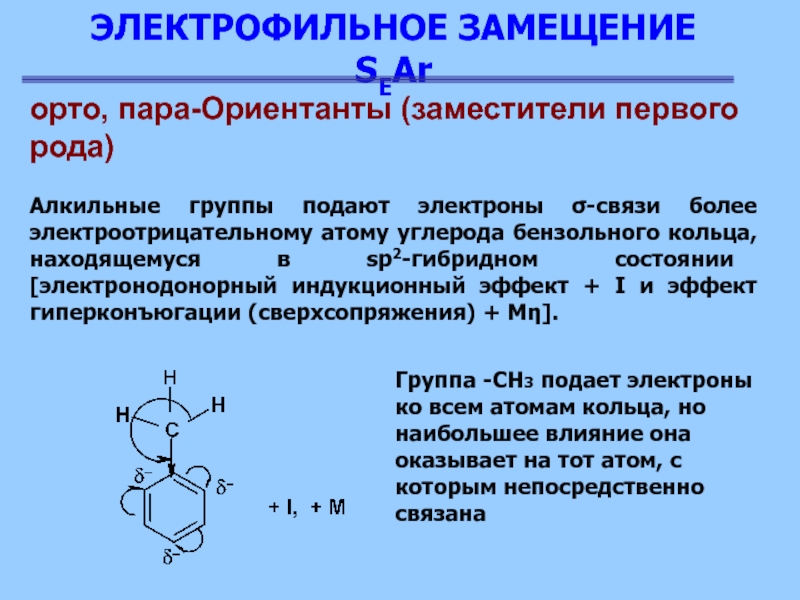
Алкильные группы подают электроны
σ-связи более электроотрицательному атому углерода бензольного кольца, находящемуся в sp2-гибридном
состоянии [электронодонорный индукционный эффект + I и эффект гиперконъюгации (сверхсопряжения) + Mη].
Группа -СН3 подает электроны ко всем атомам кольца, но наибольшее влияние она оказывает на тот атом, с которым непосредственно связана
Слайд 32ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
Ацилоксидные и ациламидные группы
в меньшей степени, чем группы –OH и –NH2, отдают свои
электроны кольцу, так как они частично смещены к карбонильным группам
Слайд 33ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
Галогены также являются орто,
пара-ориентантами, но при этом дезактивируют электрофильное замещение
Эти группы обладают электроноакцепторным
индукционным эффектом (-I), превосходящим электронодонорный эффект сопряжения (+М)
Слайд 34ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
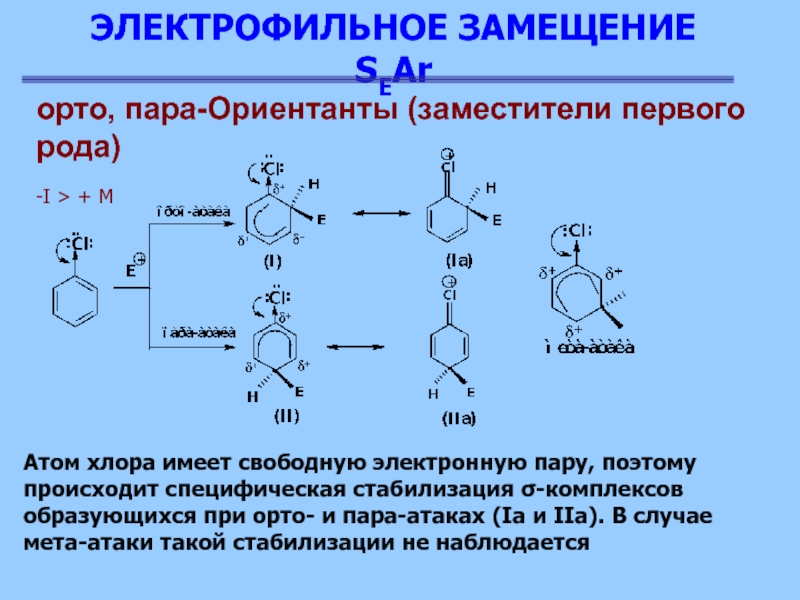
Атом хлора имеет свободную
электронную пару, поэтому происходит специфическая стабилизация σ-комплексов образующихся при орто-
и пара-атаках (Ia и IIa). В случае мета-атаки такой стабилизации не наблюдается
-I > + M
Слайд 35ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
орто, пара-Ориентанты (заместители первого
рода)
Почему галогены ведут себя
необычным образом? Благодаря слабому электронодонорному эффекту сопряжения (+М ) галогены
являются о- и п-ориентантами, как и все группы, содержащие атомы с неподеленной электронной парой (-OH, -NH2 и др.). Однако сильный электроноакцепторный индукционный эффект галогенов (минус I) преобладает над электронодонорным эффектом сопряжения (+M ) и замедляет электрофильное замещение в любом положении кольца, но в орто- и пара-положениях - не слишком сильно из-за стабилизирующего влияния π-р-сопряжения
Слайд 36ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
мета-Ориентанты (заместители второго рода)
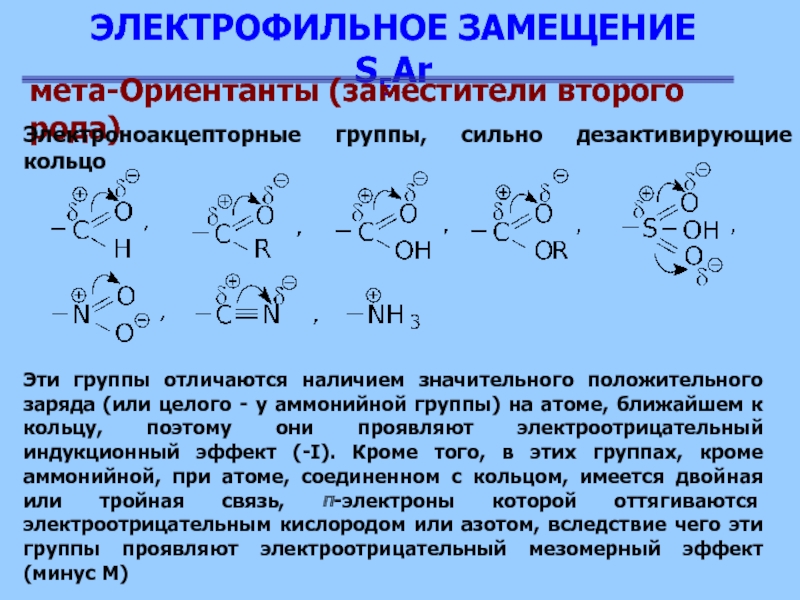
Электроноакцепторные группы, сильно дезактивирующие
кольцо
Эти группы отличаются наличием значительного положительного заряда (или целого
- у аммонийной группы) на атоме, ближайшем к кольцу, поэтому они проявляют электроотрицательный индукционный эффект (-I). Кроме того, в этих группах, кроме аммонийной, при атоме, соединенном с кольцом, имеется двойная или тройная связь, π-электроны которой оттягиваются электроотрицательным кислородом или азотом, вследствие чего эти группы проявляют электроотрицательный мезомерный эффект (минус М)
Слайд 37ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
мета-Ориентанты (заместители второго рода)
Общее снижение электронной плотности
особенно резко выражено в орто- и пара- положениях в результате
наложения одинаково направленных эффектов. В мета- положении только индуктивное влияние
Слайд 38ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
мета-Ориентанты (заместители второго рода)
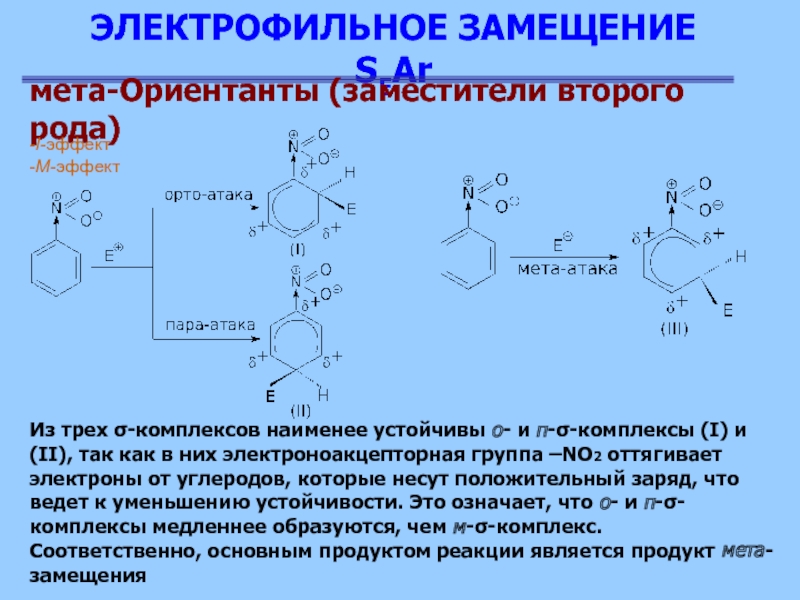
Из трех σ-комплексов наименее
устойчивы о- и п-σ-комплексы (I) и (II), так как в
них электроноакцепторная группа –NO2 оттягивает электроны от углеродов, которые несут положительный заряд, что ведет к уменьшению устойчивости. Это означает, что о- и п-σ-комплексы медленнее образуются, чем м-σ-комплекс. Соответственно, основным продуктом реакции является продукт мета- замещения
-I-эффект
-M-эффект
Слайд 39ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Рассмотрение механизма ориентации показывает, что все активирующие ориентанты
направляют электрофил в
орто- и пара-положения, а все дезактивирующие (
кроме галогенов ) - в мета-положение
Слайд 41ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
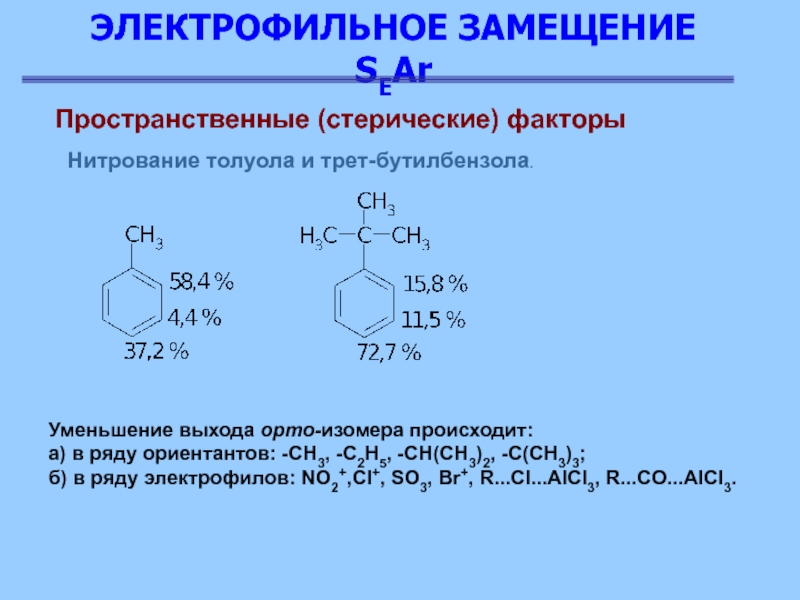
Пространственные (стерические) факторы
Нитрование толуола и трет-бутилбензола.
Уменьшение выхода
орто-изомера происходит:
а) в ряду ориентантов: -СН3, -С2Н5, -СН(СН3)2, -С(СН3)3;
б)
в ряду электрофилов: NO2+,Cl+, SO3, Br+, R...Cl...AlCl3, R...CO...AlCl3.
Слайд 42ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
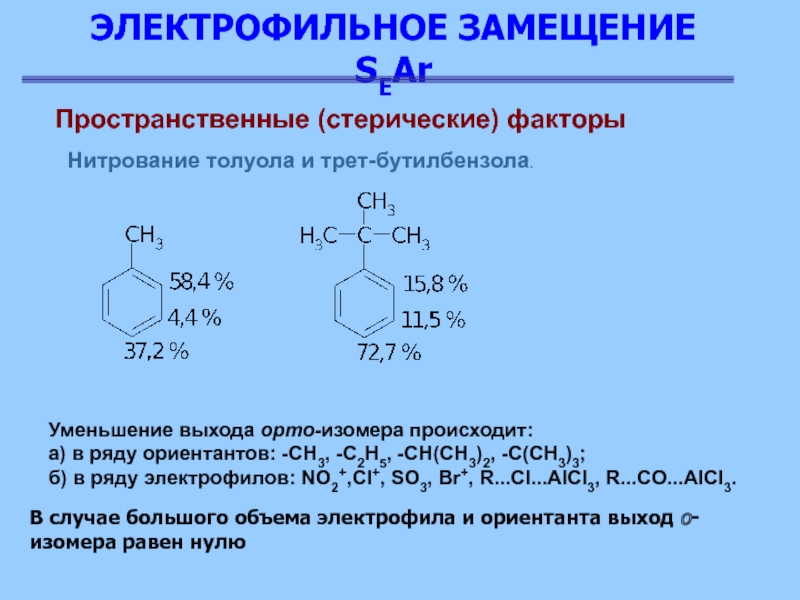
Пространственные (стерические) факторы
Нитрование толуола и трет-бутилбензола.
Уменьшение выхода
орто-изомера происходит:
а) в ряду ориентантов: -СН3, -С2Н5, -СН(СН3)2, -С(СН3)3;
б)
в ряду электрофилов: NO2+,Cl+, SO3, Br+, R...Cl...AlCl3, R...CO...AlCl3.
В случае большого объема электрофила и ориентанта выход о-изомера равен нулю
Слайд 43ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
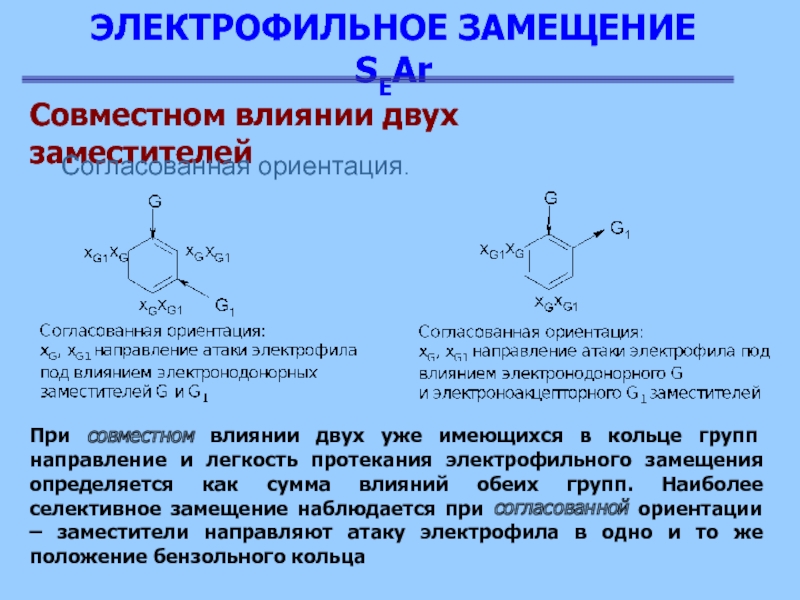
Совместном влиянии двух заместителей
Согласованная ориентация.
При совместном влиянии
двух уже имеющихся в кольце групп направление и легкость протекания
электрофильного замещения определяется как сумма влияний обеих групп. Наиболее селективное замещение наблюдается при согласованной ориентации – заместители направляют атаку электрофила в одно и то же положение бензольного кольца
Слайд 44ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
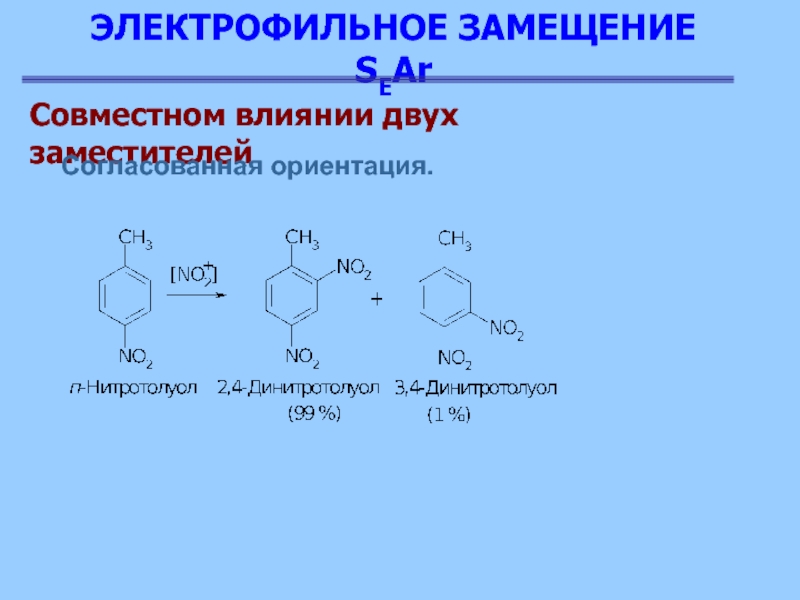
Совместном влиянии двух заместителей
Согласованная ориентация.
Слайд 45ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
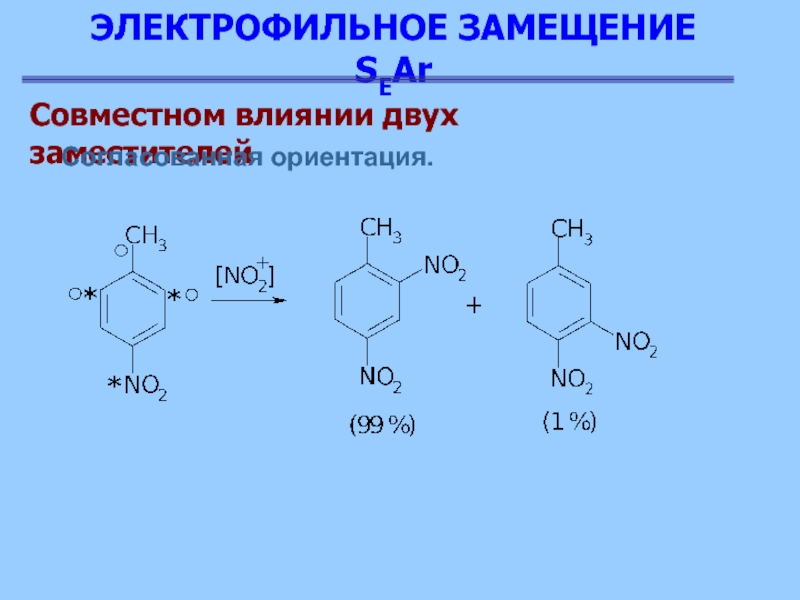
Совместном влиянии двух заместителей
Согласованная ориентация.
Слайд 46ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
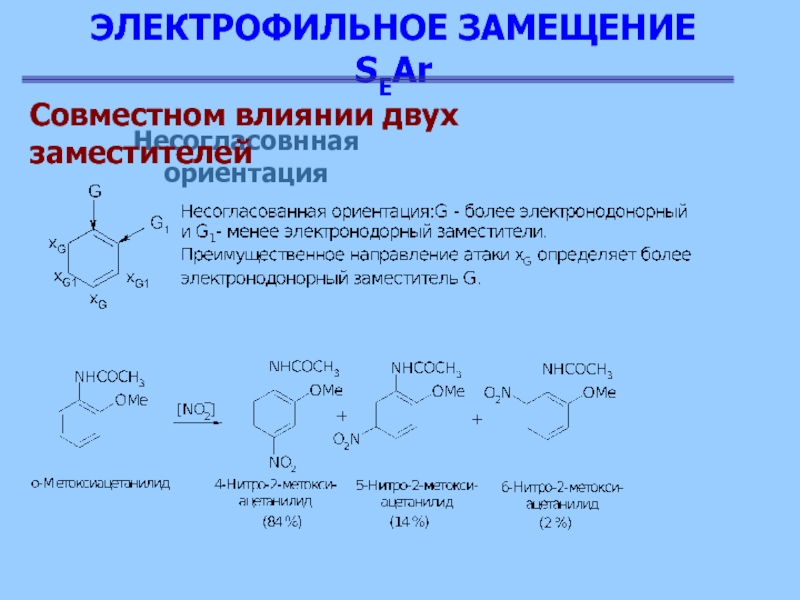
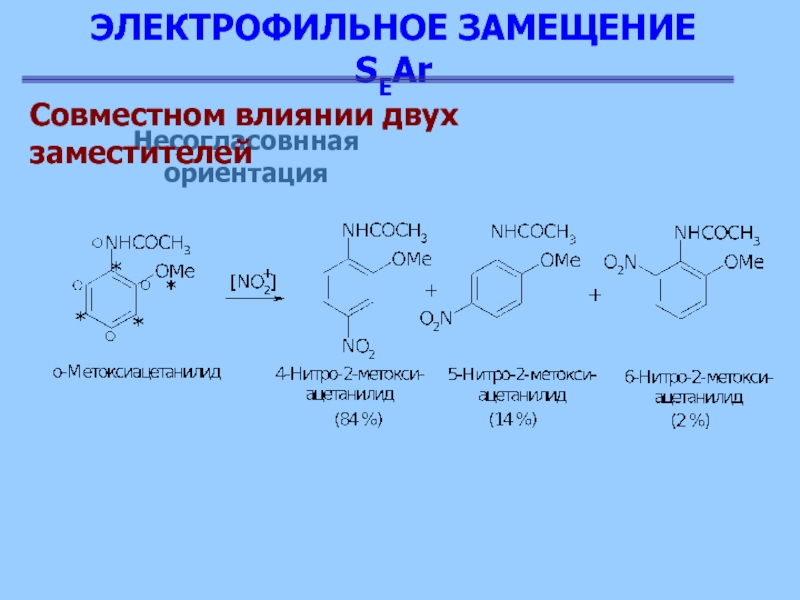
Несогласовнная ориентация
Совместном влиянии двух заместителей
Слайд 47ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
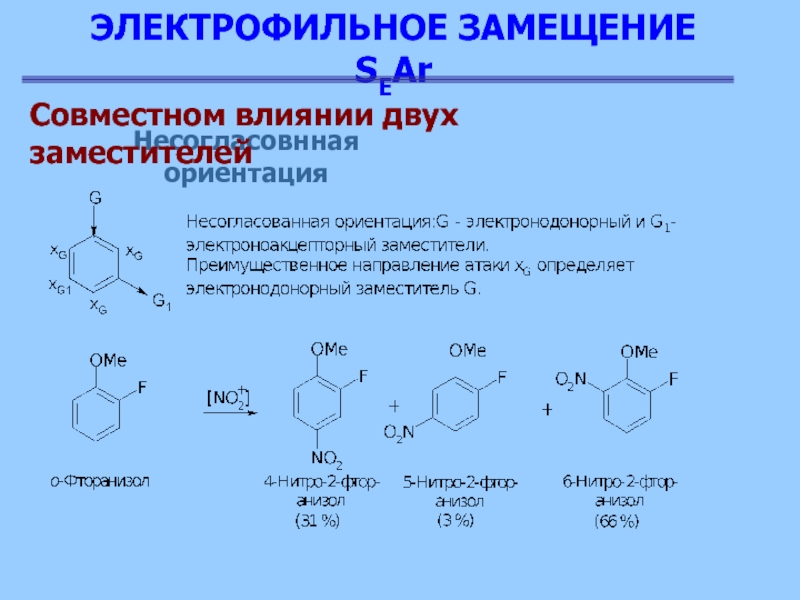
Несогласовнная ориентация
Совместном влиянии двух заместителей
Слайд 48ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
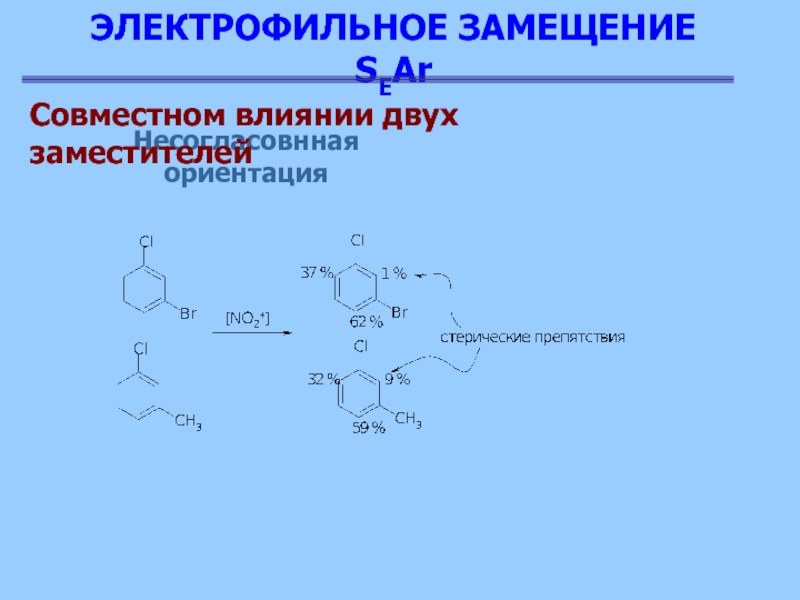
Несогласовнная ориентация
Совместном влиянии двух заместителей
Слайд 49ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Несогласовнная ориентация
Совместном влиянии двух заместителей
Слайд 50ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
Несогласовнная ориентация
Совместном влиянии двух заместителей
При несогласованной ориентации
существуют следующие правила:
1). Все орто-, пара-ориентанты доминируют над мета-ориентантами
2) все
активирующие орто-, пара-ориентанты доминируют над галогенами (дезактивирующие орто, пара-ориентанты)
3) сильно и умеренно активирующие орто, пара-ориентанты (NH2, OH, OCH3, NHCOCH3 и др.) доминируют над слабыми орто, пара-ориентантами (CH3 и др. алкилы).
Данные о сравнительной ориентирующей способности заместителей в бензольном кольце позволяют выбирать оптимальный путь синетза того или иного замещенного бензола
Слайд 51ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ SEAr
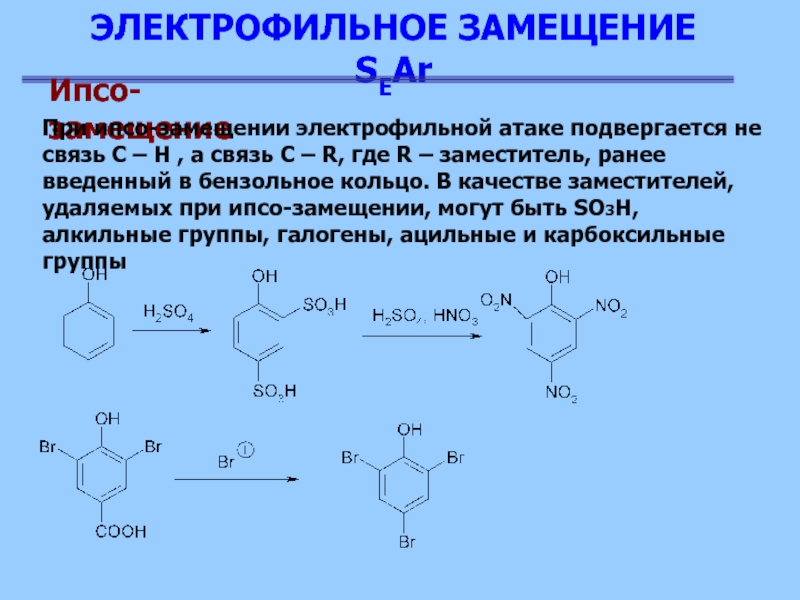
Ипсо-замещение
При ипсо-замещении электрофильной атаке подвергается не связь
C – H , а связь C – R, где
R – заместитель, ранее введенный в бензольное кольцо. В качестве заместителей, удаляемых при ипсо-замещении, могут быть SO3H, алкильные группы, галогены, ацильные и карбоксильные группы