ом-1
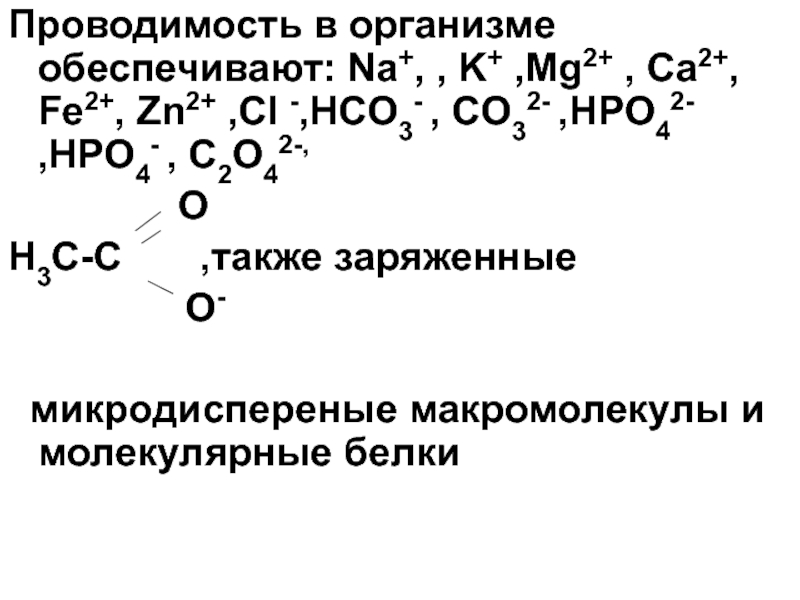
Х – удельная электрическая проводимость ; она характерезует свойства
проводящей ток среды, не зависит от формы и размеров электродов. Х равна количеству электричества, перенесенному ионами через раствор S=1см2 на расстояние в 1см в электрическом поле напряженностью в 1в/см.