Слайд 1
ФАРМАКОГЕНЕТИКА
Лекция СПбГУ №6
Слайд 2ПЛАН ЛЕКЦИИ
1.Определение понятий (фармакотипирование, генотипирование, фармакогенетика, фармакогеномика)
2.Метаболим лекарств
3.Фазы детоксикации
4.Химические реакции
биотрансформации
5.Индукция ферментов биотрансформации
6.Генетический полиморфизм ферментов
7.Взаимодействие цитохромов с лекарствами
8.Генетический полиморфизм и фармакотерапия
9.Чиповый метод анализа генетического полиморфизма
Слайд 4ОРГАНИЗМ И ЛЕКАРСТВО
Фармакокинетика – абсорбция, распределение,
метаболизм и выведение лекарства
Фармакодинамика – взаимоотношение между
концентрацией, местом действия и эффектом
Фенотипирование лекарства- прямой метод
определения активности лекарства по
фармакокинетике субстрата
Генотипирование - анализ полиморфизмов генов, определяющих метаболизм лекарства
Генетическая гетерогенность - генный полиморфизм
Фармакогенетика – индивидуальная реакция на лекарства
Фармакогеномика – союз функциональной геномики и
молекулярной фармакологии
Слайд 5Метаболизм лекарств
Лекарства с высоким печеночным клиренсом:
аминазин,
аспирин,кортизон, ,морфин, резерпин, метопролол, метилтестостерон, и др.
Лекарства с низким печеночным
клиренсом:
теофеллин, парацетомол
По скорости метаболизма лекарств различают:
«Экстенсивные » метаболизаторы- норма
«Медленные» метаболизаторы – сниженная
«Быстрые или сверхактивные» метаболизаторы
Слайд 6 ФАЗЫ ДЕТОКСИКАЦИИ
Фаза 1
Несинтетические реакции
(пролекарство –
лекарство)
Оксидазы со смешанной функцией
Реакции восстановления и гидролиза
Фаза II
Синтетические реакции
Коньюгация ЛС
через метаболически активные радикалы (фазы I)
Возможен метаболизм ЛС только за счет ферментов Фазы I или Фазы II
ФАЗА II
ФАЗА III
АКТИВАЦИЯ
КСЕНОБИОТИКОВ С
ОБРАЗОВАНИЕМ
АКТИВНЫХ
ПРОМЕЖУТОЧНЫХ
ЭЛЕКТРОФИЛЬНЫХ
МЕТАБОЛИТОВ
ПРЕОБРАЗОВАНИЕ
АКТИВНЫХ
ПРОМЕЖУТОЧНЫХ
ЭЛЕКТРОФИЛЬНЫХ
МЕТАБОЛИТОВ В
ВОДОРАСТВОРИМЫЕ
НЕТОКСИЧНЫЕ
КОМПОНЕНТЫ
ОКСИДАТИВНЫЙ
СТРЕСС,
ТОКСИЧНОСТЬ,
МУТАЦИИ, РАК
ЦИТОХРОМЫ
P450,
ЭЕПОКСИ
Д-
ГИДРОЛАЗЫ
И ДР.
ГЛЮТАТИОН
-
ТРАНСФЕРАЗЫ,
N-
АЦЕТИ
Л-
ТРАНСФЕРАЗЫ,
UDF-
ГЛЮКОРОН
-
СУЛЬФОТРАНСФЕРАЗЫ
И ДР.
ВЫВЕДЕНИЕ
ВОДОРАСТВОРИМЫХ
НЕТОКСИЧНЫХ
КОМПОНЕНТОВ ИЗ
ОРГАНИЗМА
ЛЕКАРСТВА,
ПИЩА.
КАНЦЕРОГЕНЫ,
ЗАГРЯЗНЕНИЕ
ВНЕШНЕЙ СРЕДЫ
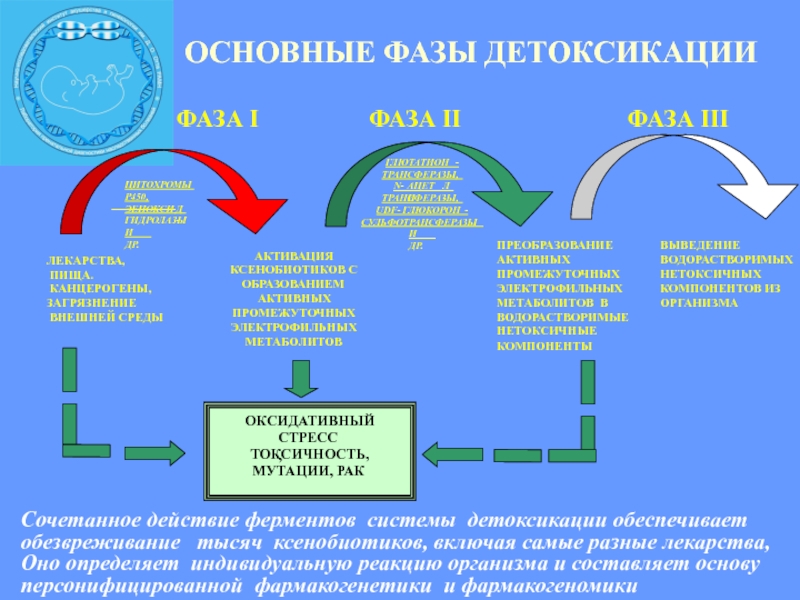
Сочетанное действие ферментов системы детоксикации обеспечивает обезвреживание тысяч ксенобиотиков, включая самые разные лекарства, Оно определяет индивидуальную реакцию организма и составляет основу персонифицированной фармакогенетики и фармакогеномики
ОСНОВНЫЕ ФАЗЫ ДЕТОКСИКАЦИИ
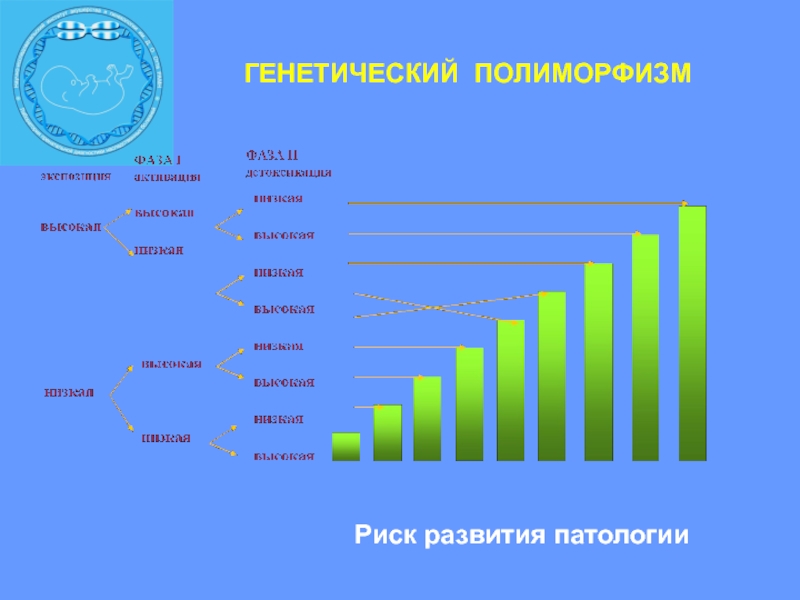
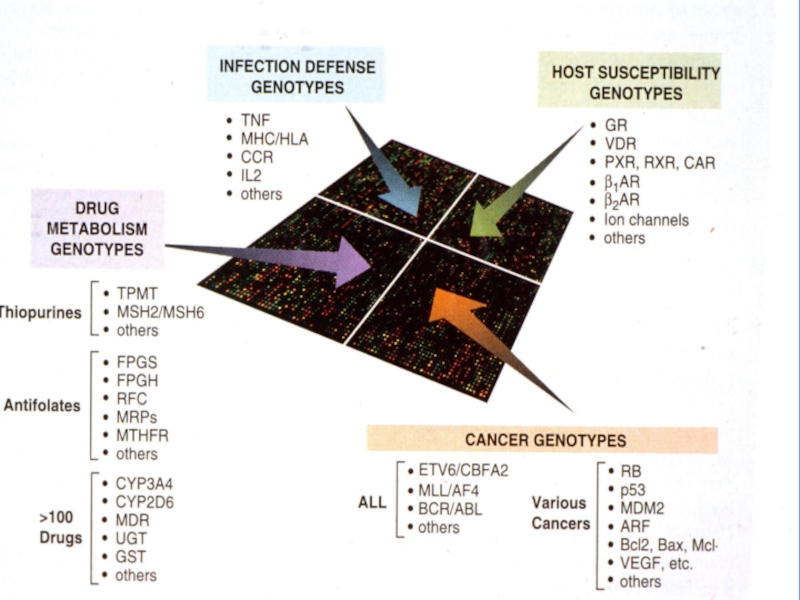
Слайд 8Риск развития патологии
ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ
Слайд 9Фаза 1
Фаза 2
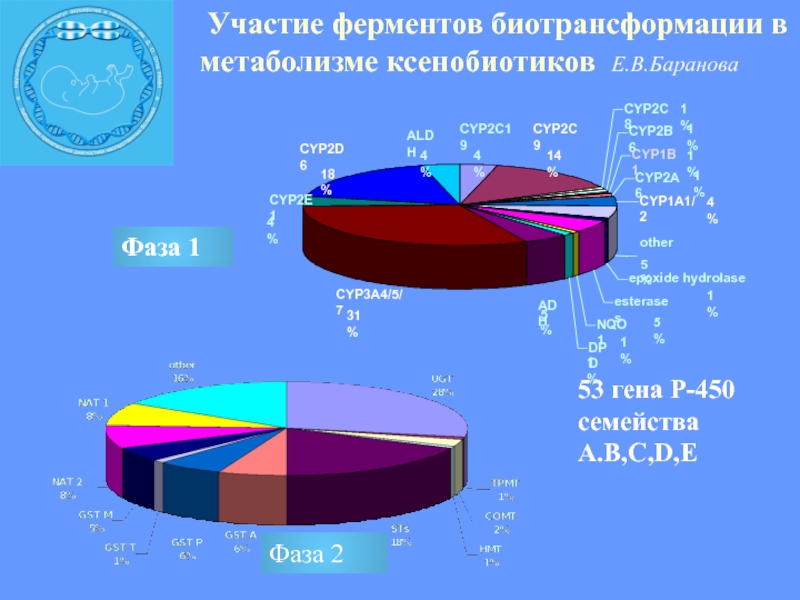
Участие ферментов биотрансформации в метаболизме
ксенобиотиков Е.В.Баранова
53 гена Р-450 семейства А.B,C,D,E
Основные химические реакции биотрансформации проканцерогенов с участием генов метаболизма
Слайд 11Индукция ферментов метаболизма
1.Фенобарбиталовый путь – активация промотора в
регуляторной области гена
Аутоиндукция – сам ксенобиотик активатор фермента
2.Рифампицин-дексаметазоновый тип –
взаимодействие индуктора с рецепторами-регуляторами транскрипции
3. Этаноловый тип –стабилизация молекулы фермента метаболизма путем образования комплекса с некоторыми ксенобиотиками
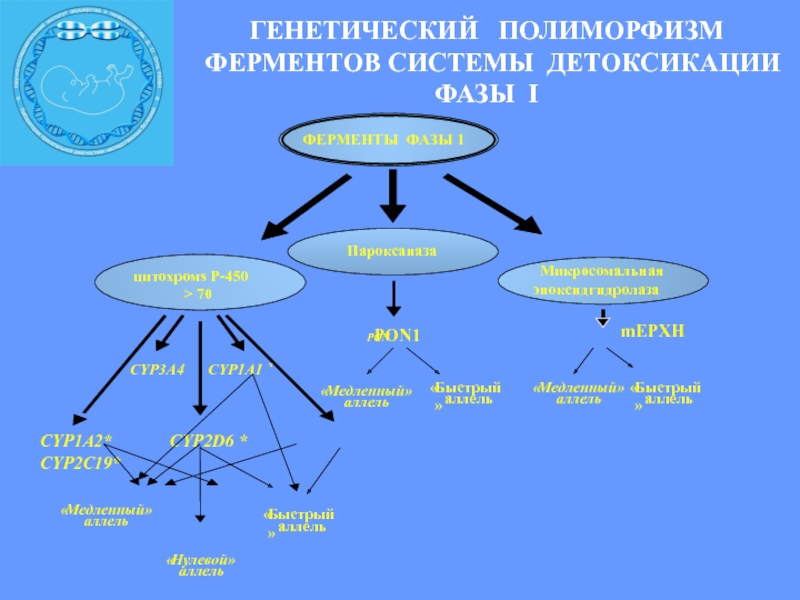
Слайд 13ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ
ФЕРМЕНТОВ CИСТЕМЫ ДЕТОКСИКАЦИИ
ФАЗЫ I
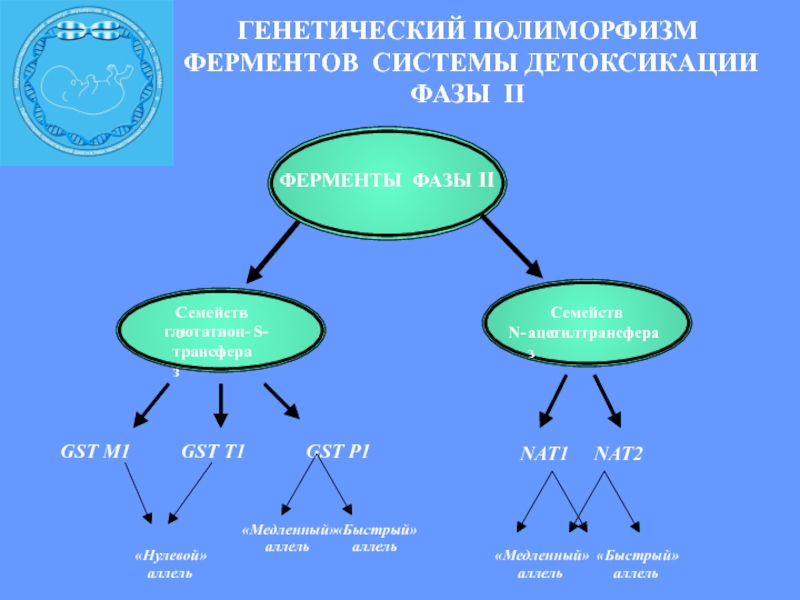
Слайд 14ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ
ФЕРМЕНТОВ СИСТЕМЫ ДЕТОКСИКАЦИИ
ФАЗЫ II
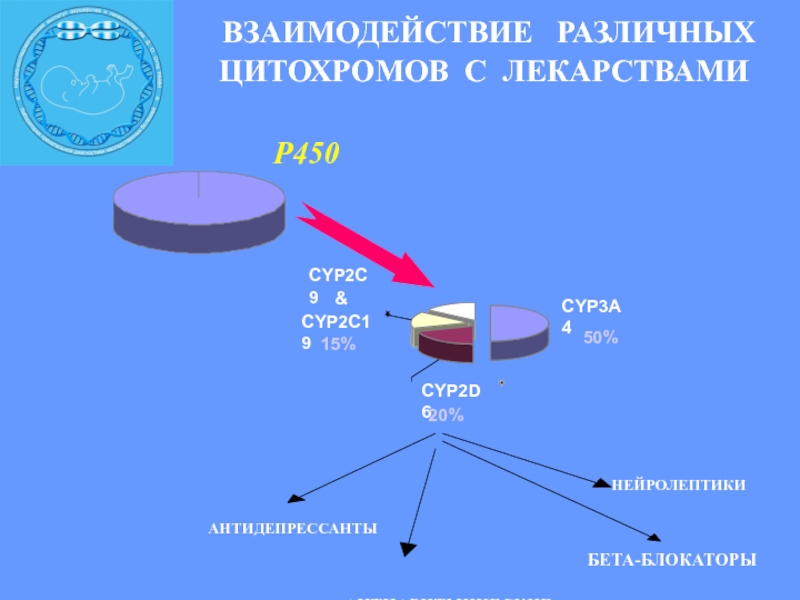
Слайд 15 ВЗАИМОДЕЙСТВИЕ РАЗЛИЧНЫХ ЦИТОХРОМОВ С
ЛЕКАРСТВАМИ
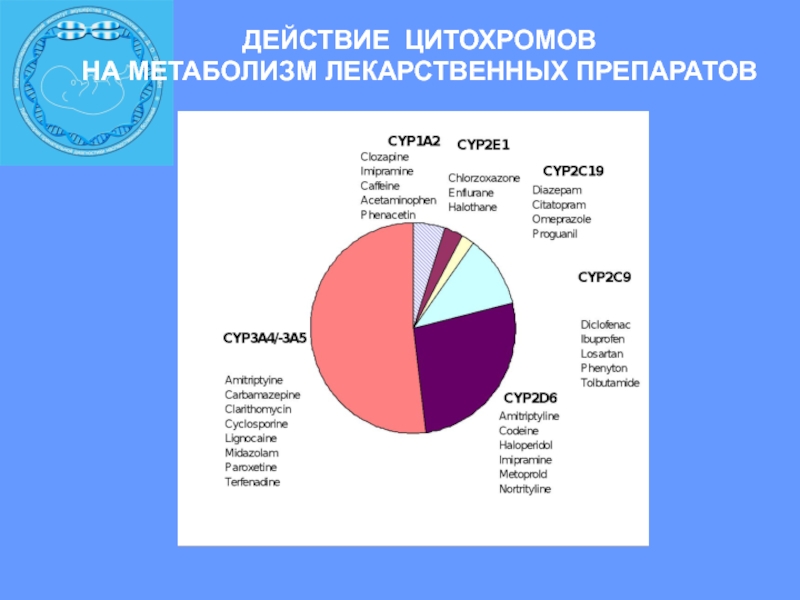
Слайд 16ДЕЙСТВИЕ ЦИТОХРОМОВ
НА МЕТАБОЛИЗМ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
Слайд 17 Генетические механизмы
индивидуальной
чувствительности к лекарствам
ФАРМАКОКИНЕТИЧЕСКИЕ:
изменение абсорбции - инотиазид – NAT2
превращение
в активную форму кодеин –морфин –CYP 2D6
системные особенности метаболизма
конкуренция препаратов за фермент
индукция ферментов метаболизма
индукция/ингибирование пищевыми продуктами
ФРАМАКОДИНАМИЧЕСКИЕ:
поступление /выведение препарата из клетки
изменения в белках рецепторах
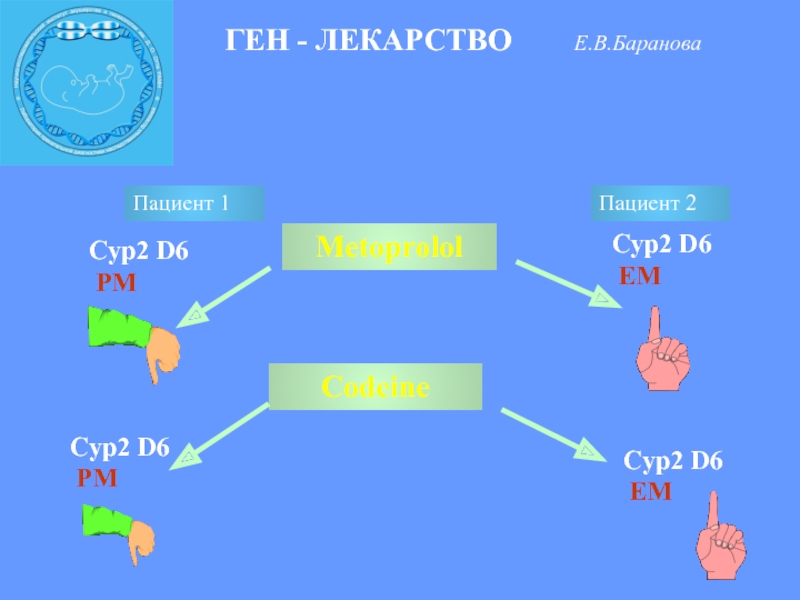
Слайд 18ГЕН - ЛЕКАРСТВО Е.В.Баранова
Metoprolol
Пациент 1
Пациент
2
Сyp2 D6
PM
Сyp2 D6
EM
Сodeine
Сyp2
D6
PM
Сyp2 D6
EM
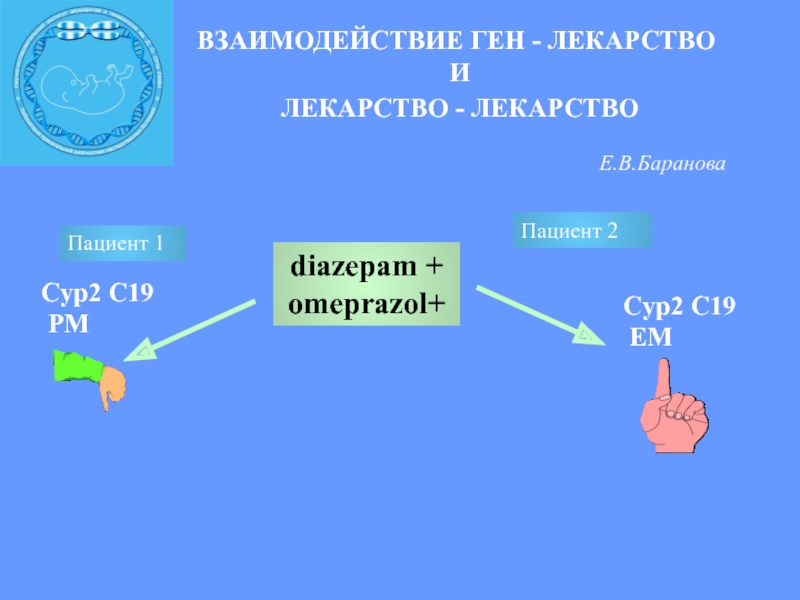
Слайд 19ВЗАИМОДЕЙСТВИЕ ГЕН - ЛЕКАРСТВО
И
ЛЕКАРСТВО - ЛЕКАРСТВО
Е.В.Баранова
diazepam + omeprazol+
Пациент 1
Пациент 2
Сyp2 С19
PM
Сyp2 С19
EM
Слайд 20 неэффективное лечение
эффективное лечение
Распределение
мутантных генотипов
CYP1A1, mEPHX1, GSTM1, GSTT1, NAT2
и эффективность лечения
эндометриоза
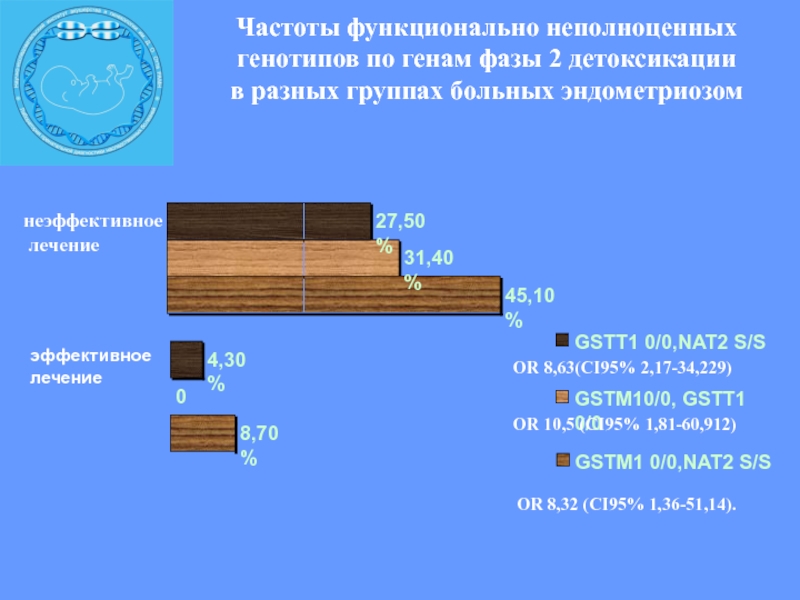
Слайд 21Частоты функционально неполноценных генотипов по генам фазы 2 детоксикации
в
разных группах больных эндометриозом
неэффективное
лечение
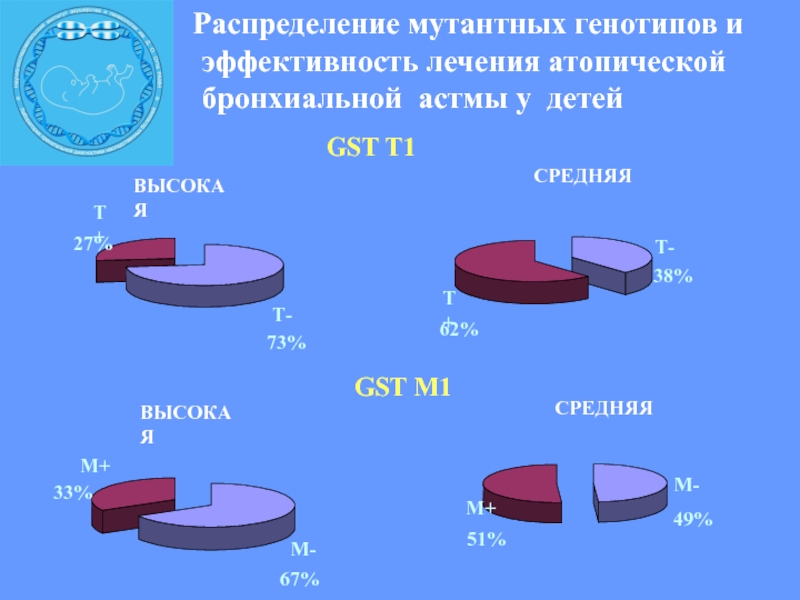
Слайд 22 Распределение мутантных генотипов и
эффективность лечения атопической
бронхиальной
астмы у детей
Биочип - упорядоченная матрица ячеек, каждая из которых
содержит молекулярный зонд (ДНК, РНК, белки, клетки)
Каждая ячейка биочипа – индивидуальная реакционная пробирка
Ячейки биочипа содержат ДНК-зонды, способные выявлять наличие определенной ДНК в образце, находить в ней фенотипически значимые мутации (наследственные заболевания, генетическую предрасположенность у человека, лекарственную устойчивость у бактерий и т.д.)
Слайд 25
Центр биологических микрочипов
ИМБ им.В.А.Энгельгардта РАН:
На
биочипе размещается несколько тысяч ячеек.
Каждая гелевая ячейка содержит уникальную пробу.
Диагностические биочипы содержат набор всех проб.
300мкм гелевые ячейки
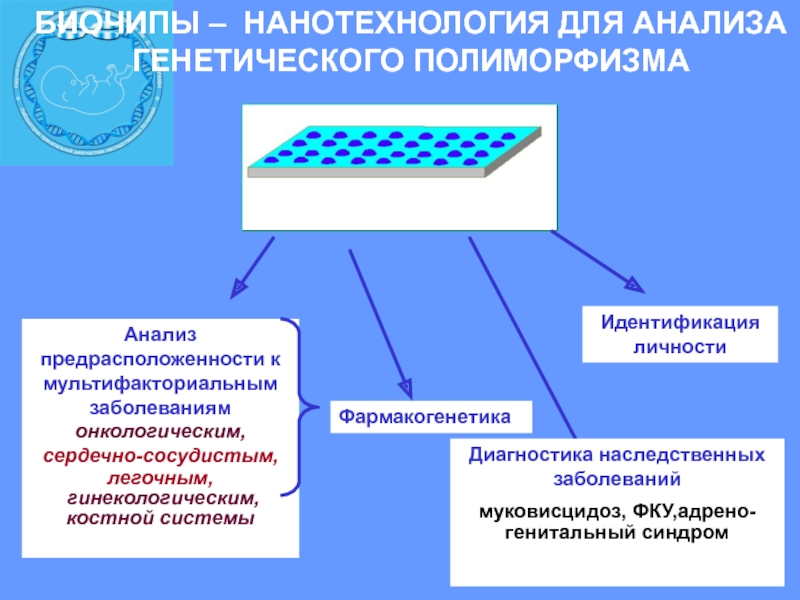
Слайд 26БИОЧИПЫ – НАНОТЕХНОЛОГИЯ ДЛЯ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА
Фармакогенетика
Идентификация личности
Анализ предрасположенности
к мультифакториальным заболеваниям онкологическим, сердечно-сосудистым,
легочным,
гинекологическим,
костной системы
Диагностика наследственных заболеваний
муковисцидоз,
ФКУ,адрено-генитальный синдром
Преимущества Биочиповой
технологии:
- возможность проведения множественного параллельного анализа биологических объектов (тысячи ячеек на 1 кв. см.)
- миниатюрность (удобство эксплуатации, экономия реактивов и т.д.)
- универсальность и дешевизна производства (одна производственная схема для различных микрочипов)
- возможность использования в качестве иммобилизованных зондов фрагментов ДНК, РНК, белков (с сохранением ферментативных или антигенных свойств), а также живых клеток-биосенсоров
Слайд 28Производство микрочипов путем сополимеризации
Высокопроизводительный
робот
Производство биочипов
Матрица с пробами
Ячейки геля с иммобили-зованными
пробами
robot pin
light
Слайд 29A
Б
Портативный анализатор
Результаты гибридизации регистрируются с помощью исследовательского (А) или портативного
(Б) анализатора биочипов, соединенного с персональным компьютером
Исследовательский анализатор
Анализаторы изображения
А
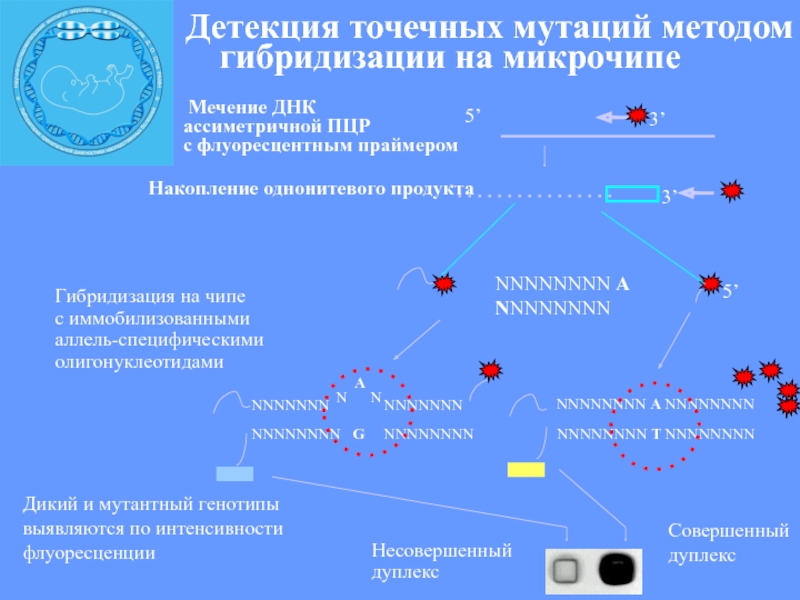
Слайд 30 Детекция точечных мутаций методом гибридизации
на микрочипе
5’
3’
3’
5’
NNNNNNNN A
NNNNNNNN
NNNNNNNN
G NNNNNNNN
NNNNNNNN A NNNNNNNN
NNNNNNNN T NNNNNNNN
NNNNNNN NNNNNNN
N N
A
Мечение ДНК
ассиметричной ПЦР
с флуоресцентным праймером
Накопление однонитевого продукта
Гибридизация на чипе с иммобилизованными аллель-специфическими олигонуклеотидами
Совершенный дуплекс
Несовершенный
дуплекс
Дикий и мутантный генотипы выявляются по интенсивности флуоресценции
Слайд 31
ФАРМАГЕН-БИОЧИП
14 мутаций в 8 генах
метаболизма
Блок 1 CYP1A1 - C4887A
A4889G T6235C
CYP2D6 - G1934A DelA2637
Блок 2 GSTM1 - 0/0 0/+ +/+
GSTT1 - 0/0 0/+ +/+
Блок-3 NAT2 - 481C>T 590 G>A 895G>A
MTHFR - C677T
Блок 4 СYP2C9 - C430T C61075T
CYP2C19 - G681A
Слайд 32 Вариант биочипа для детекции мутаций в генах
CYP1A1 (С4887А, A4889G и T6235C), CYP2D6
(G1934A, DelA2637), GSTM1(del) и GSTT1
Дикий тип:
CYP1A1 (СС, AA и TT соответственно),
CYP2D6 (GG и AA),
GSTM1 (+/+) и GSTT1 (+/+)
Примечание:
+ Положительный детектирующий олигонуклеотид
Мутантный детектирующий олигонуклеотид
* Положительный детектирующий олигонуклеотид с однонуклеотидной заменой
S-methyltransferase (TPMT) локализован на хромосоме 6p22.3 и состоит из 9
интронов и 10 экзонов.
Белковый продукт гена TPMT инактивирует противоопухолевые препараты: меркаптопурин, азатиопурин, тиогуанин.
1 из 300 европейцев является гомозиготой по аллелю с очень низкой ферментной активностью по данному локусу.
~ 10 % индивидов - гетерозиготы по аллелю со средней белковой активностью.
~ 89% людей - гомозиготы по аллелю с высокой белковой активностью.
Структура и аллельные варианты гена ТРМТ.
ТПМТ-БИОЧИП
Слайд 34УЖЕ СУЩЕСТВУЮЩИЕ И РАЗРАБАТЫВАЕМЫЕ МИКРОЧИПЫ
Фармбиочип
Тромбочип
Кардиочип
ТМПТ-биочип
Остеопороз
Муковисцидоз
Бронхиальная
астма
7.
Ожирение
Онкология
Слайд 35ВЫВОДЫ
1. Чувствительность человека к экзогенным факторам в т.ч.
к лекарственным препаратам
определяется состоянием и
функциональной активностью генов метаболизма
2. Основу индивидуальной чувствительности к
лекарственным препаратам составляют особенности
генетического полиморфизма
3. Выбор оптимальной индивидуальной дозировки
лекарства должен производиться с учетом результатов
тестирования соответствующих генов метаболизма
4. Технология биочипов существенно повышает
эффективность популяционных и скринирующих программ по фармакогенетике и предиктивной медицине.