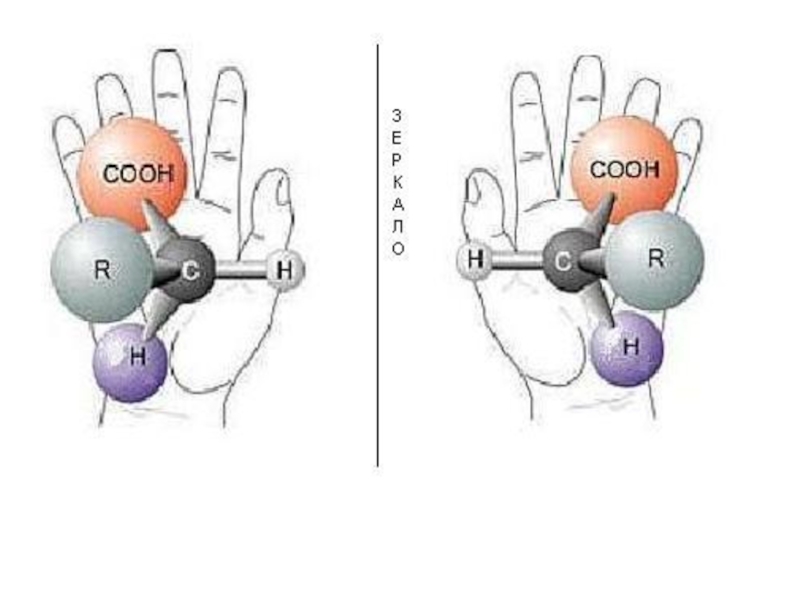
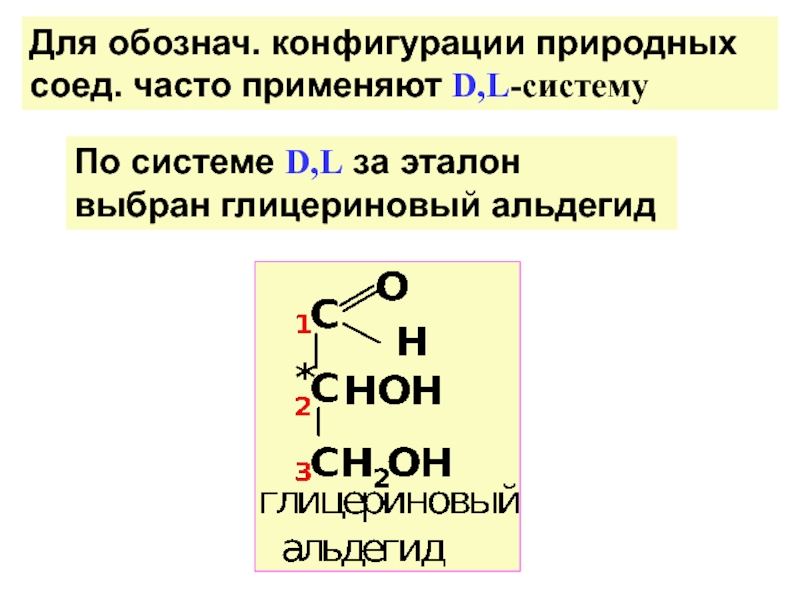
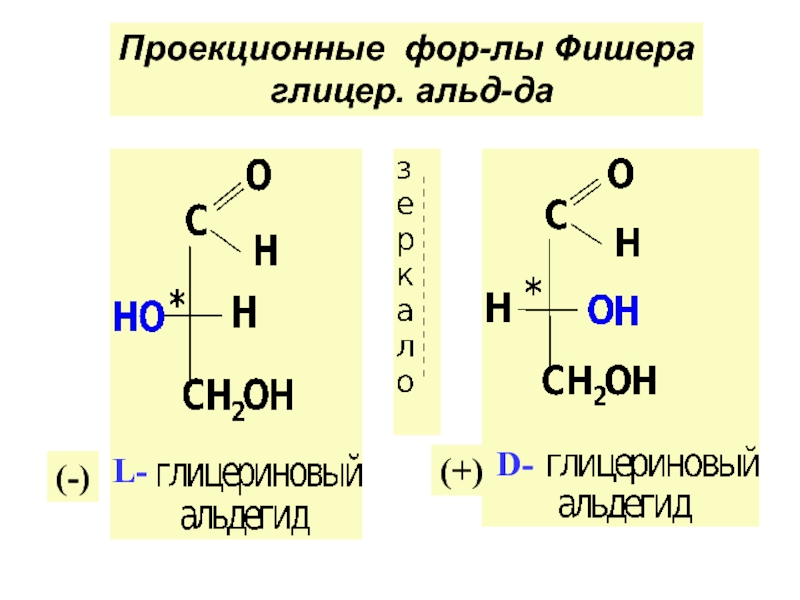
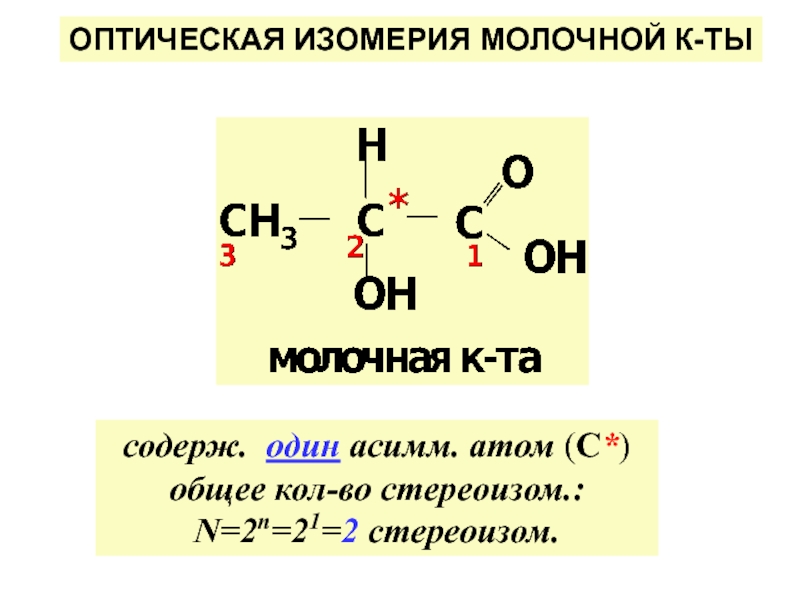
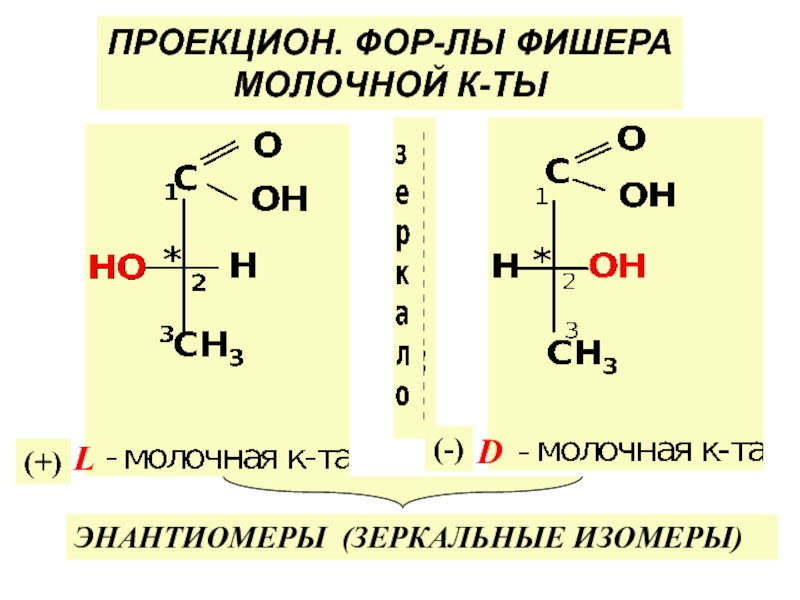
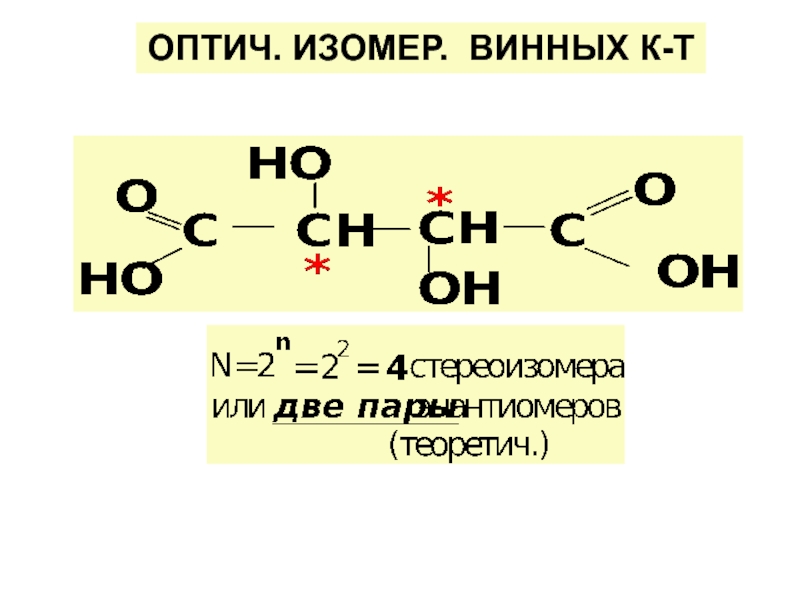
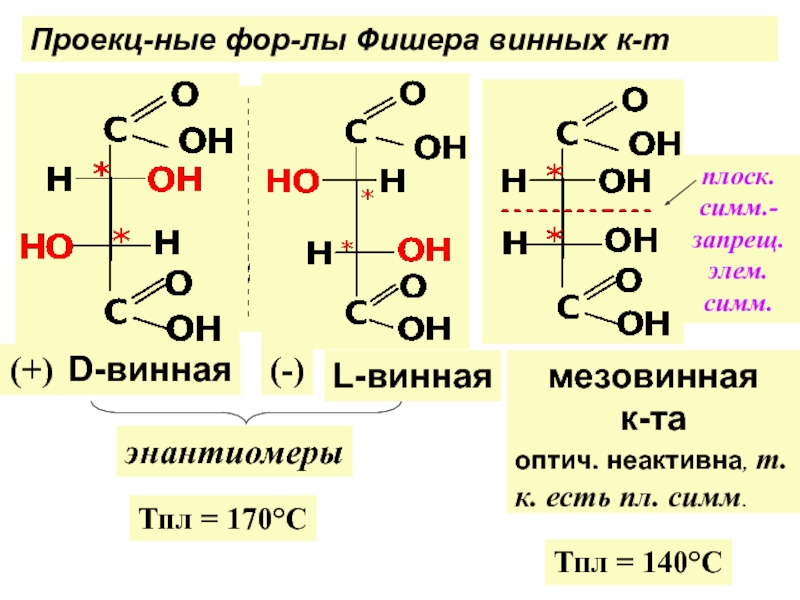
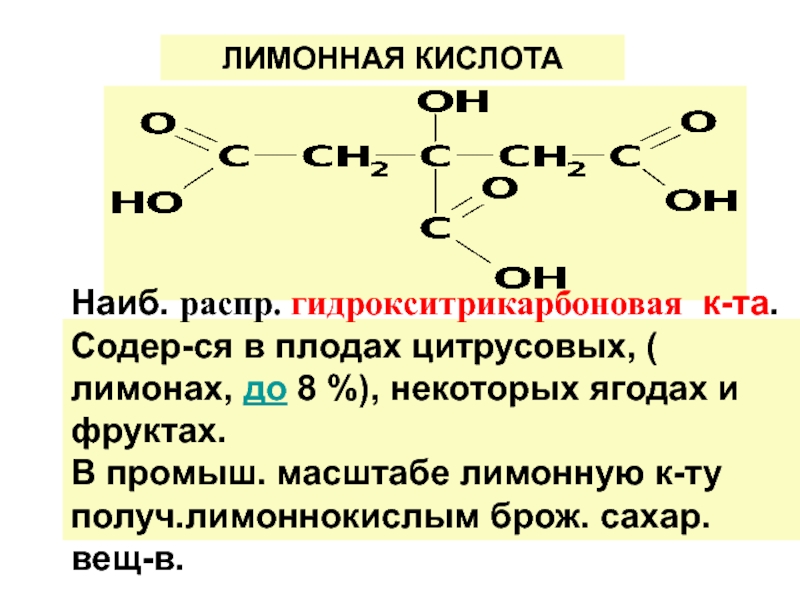
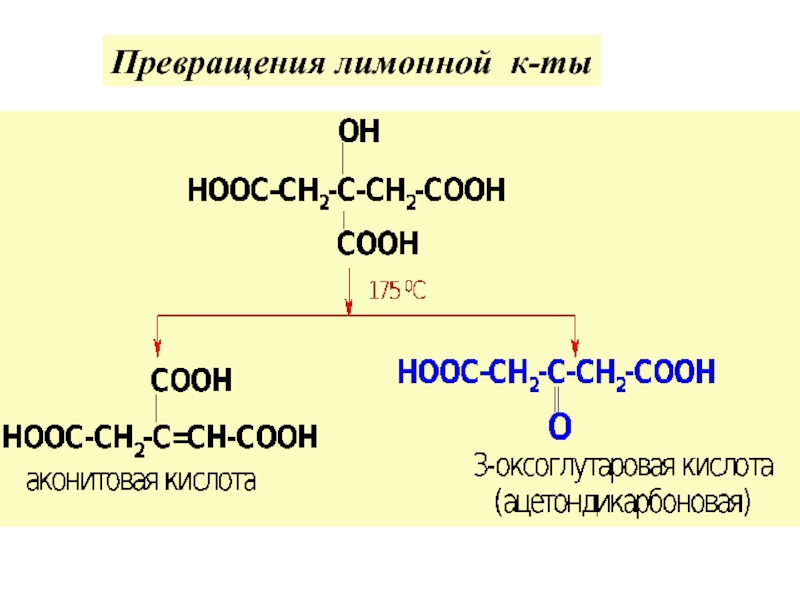
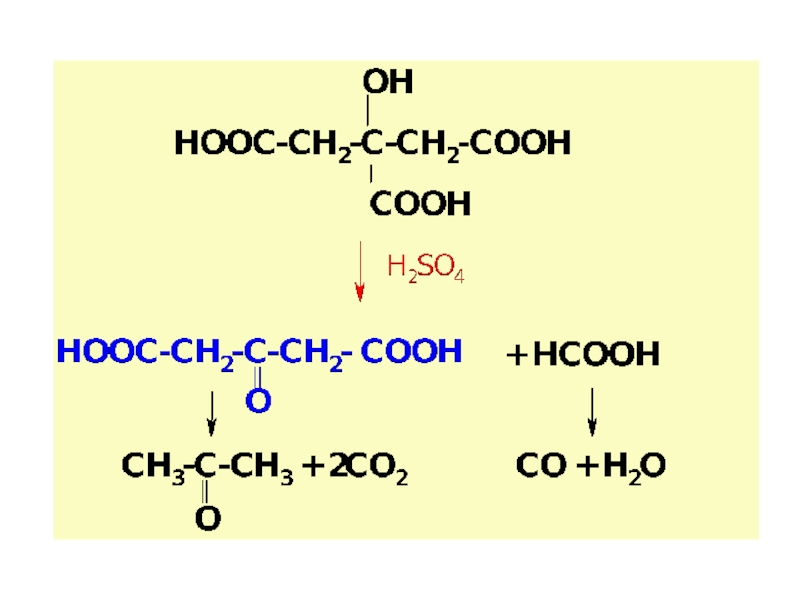
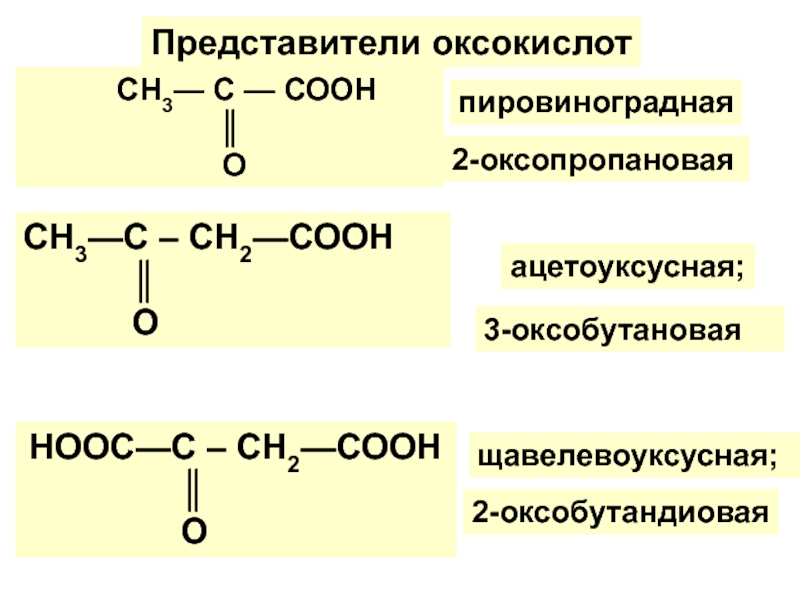
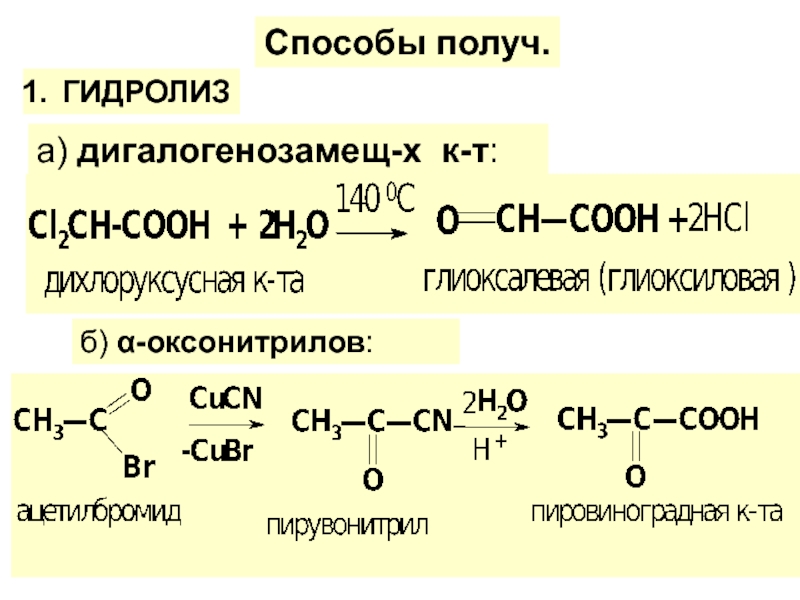
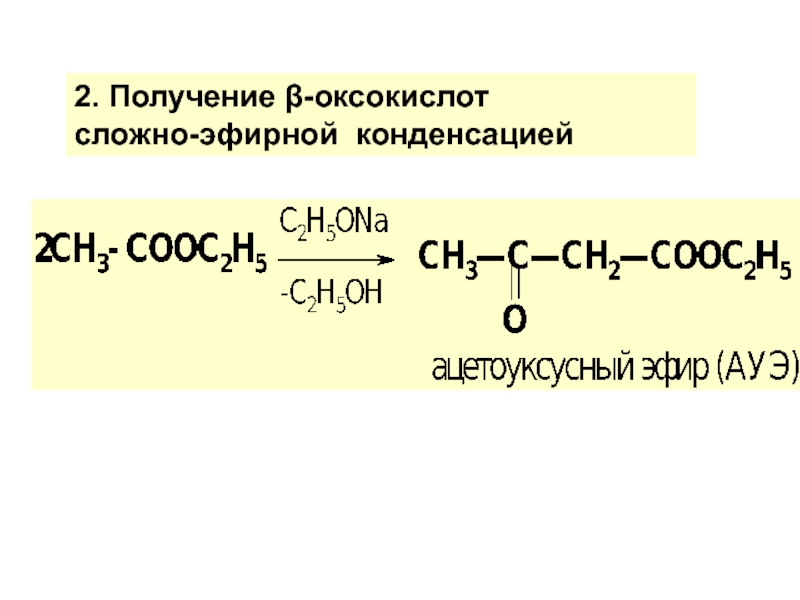
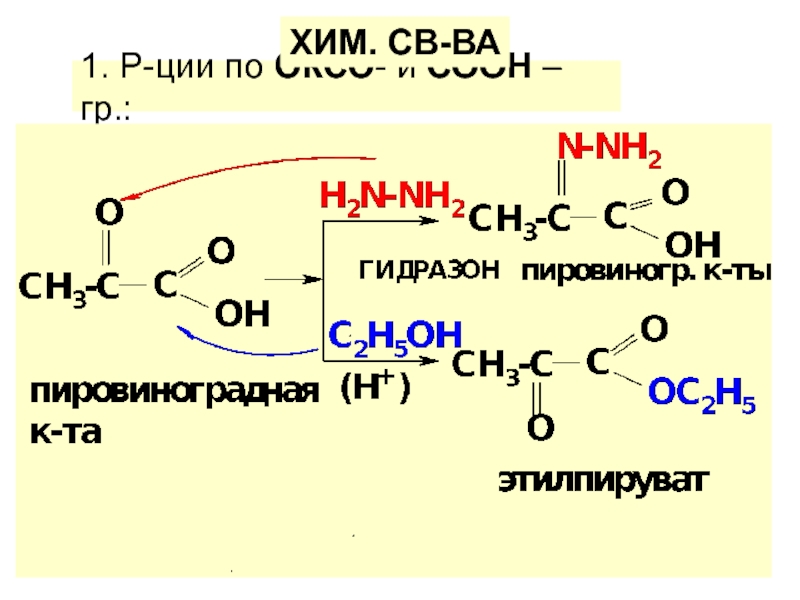
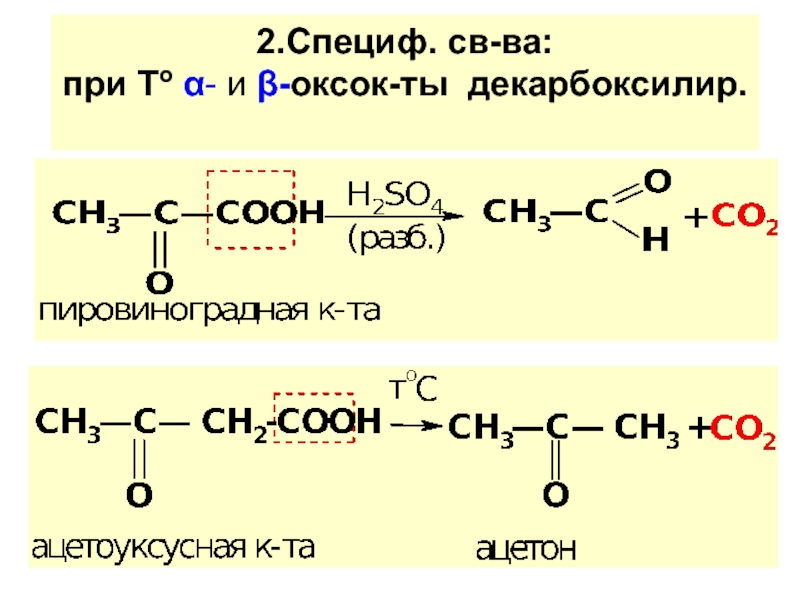
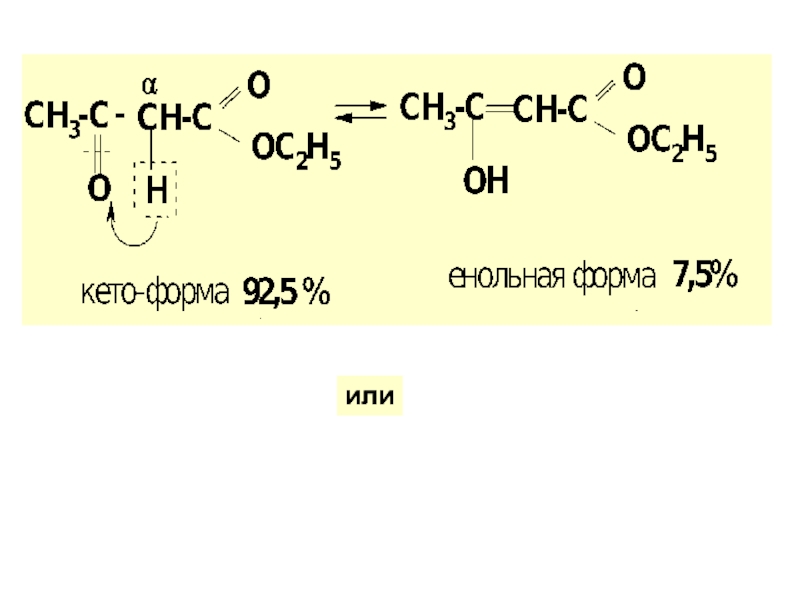
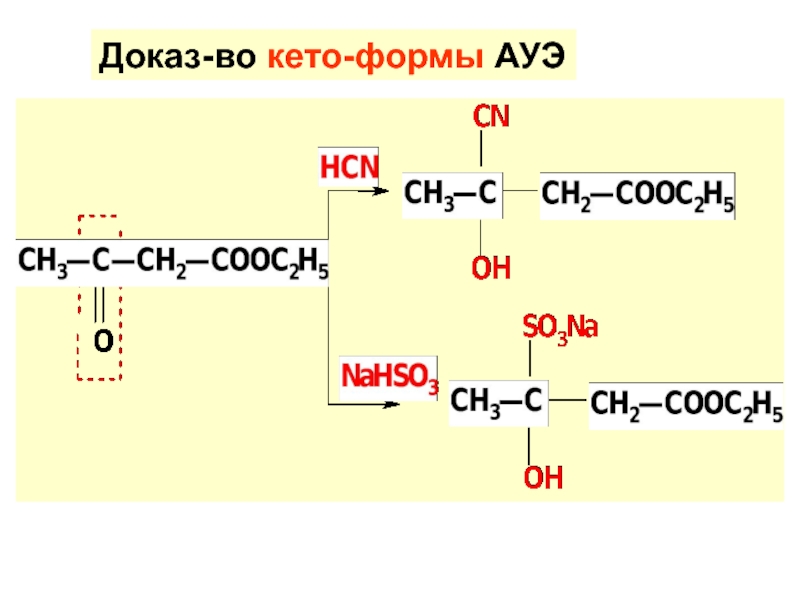
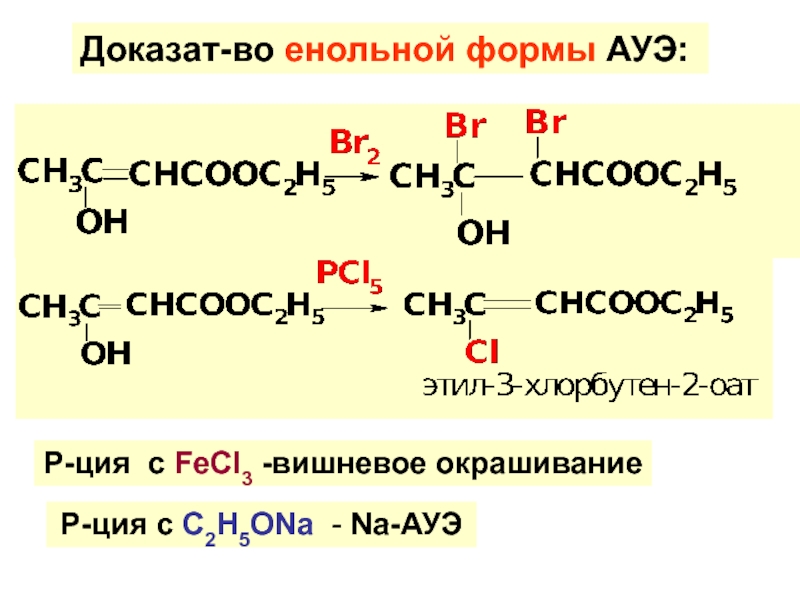
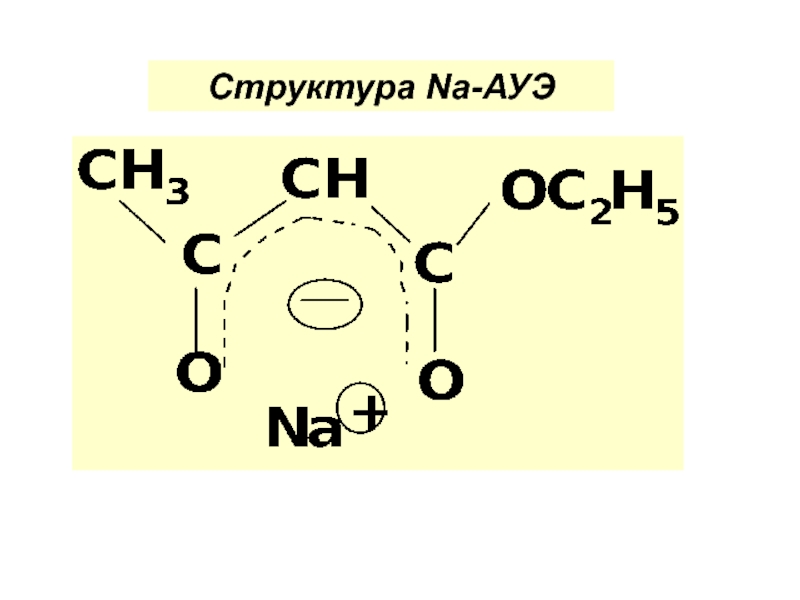
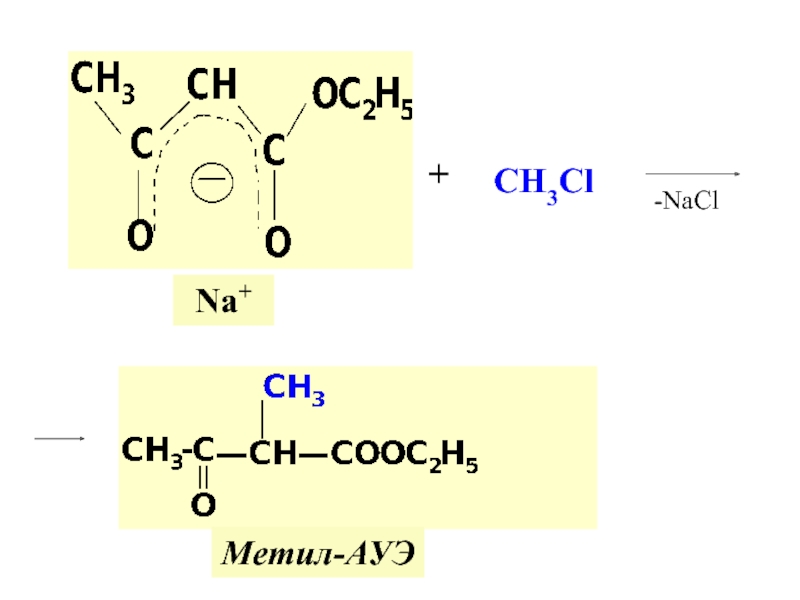
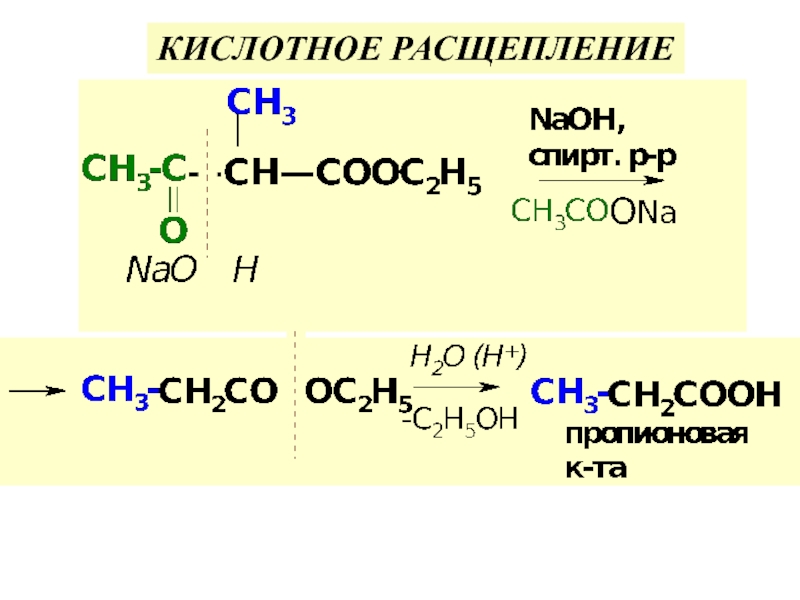
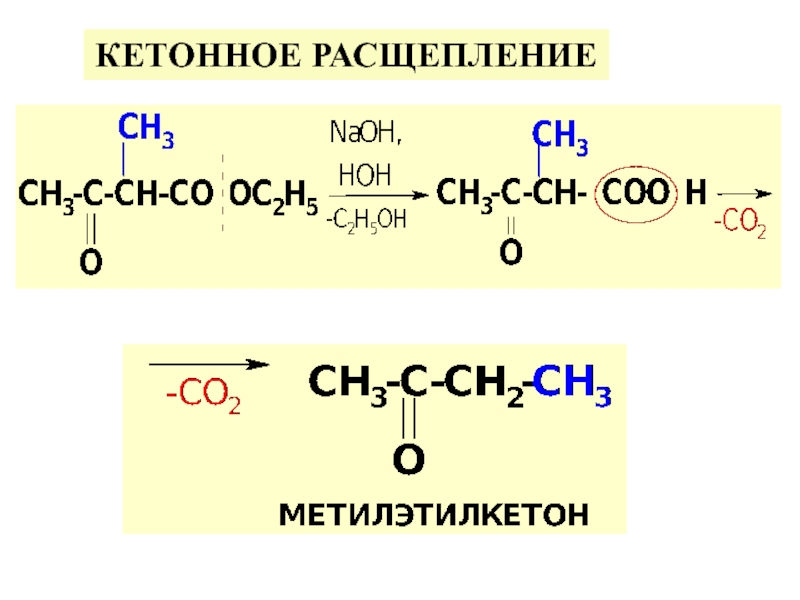
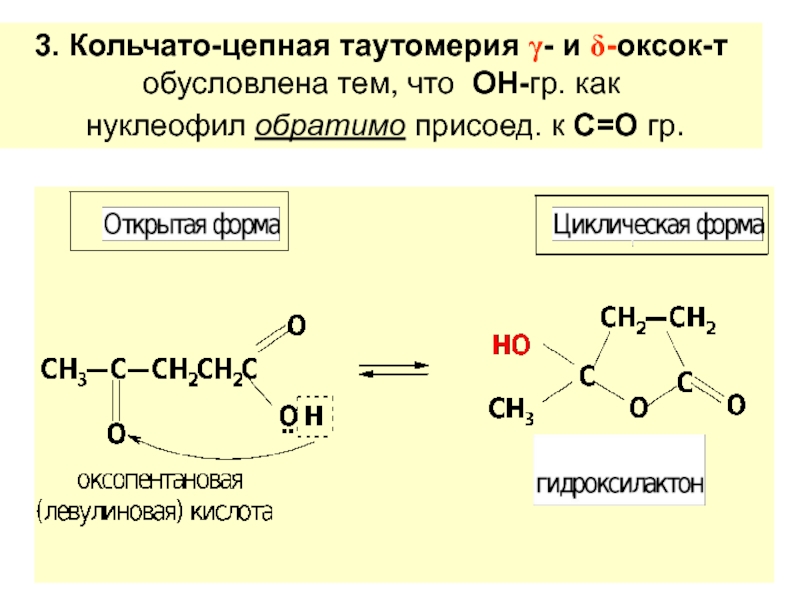
по у/в скелету:
алифат.; аромат., циклич.
2) по кол-ву СООН –групп:
моно-, ди- или трикарбоновые к-ты;
По взаимн. располож. функц. гр.:
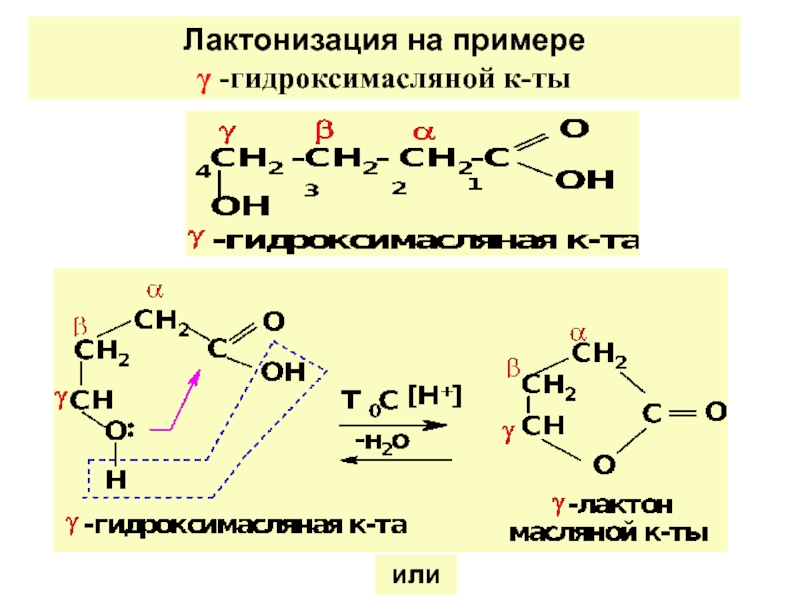
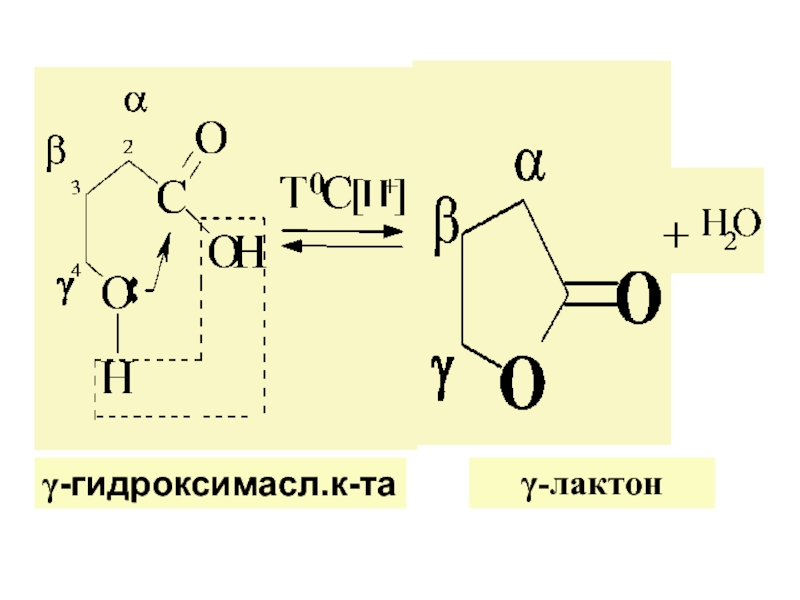
различ. α-, β-, γ-, δ- г/к.
3) по кол-ву ОН-гр.: ди-, три- , тетраГ/К.


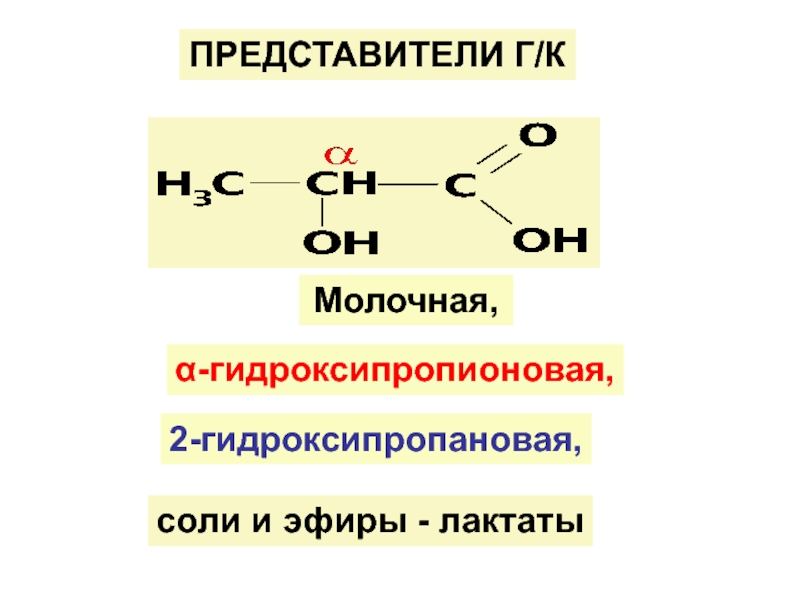
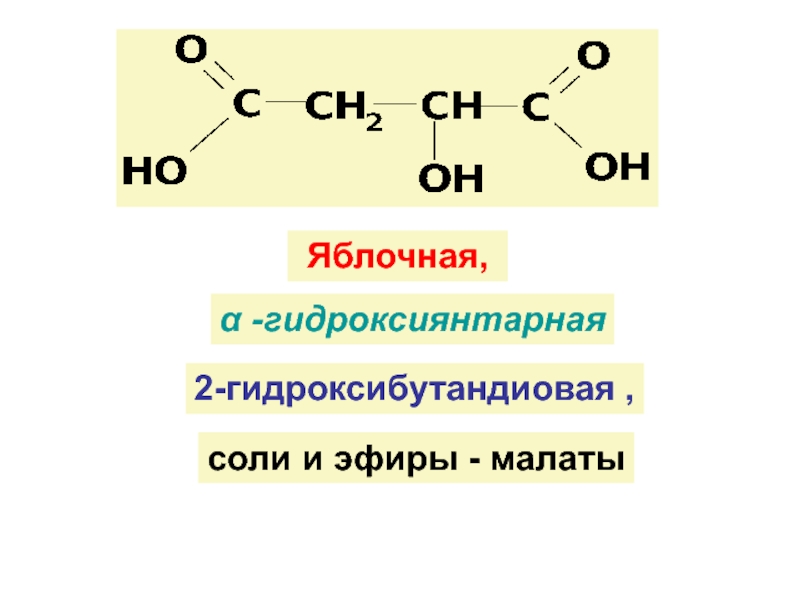
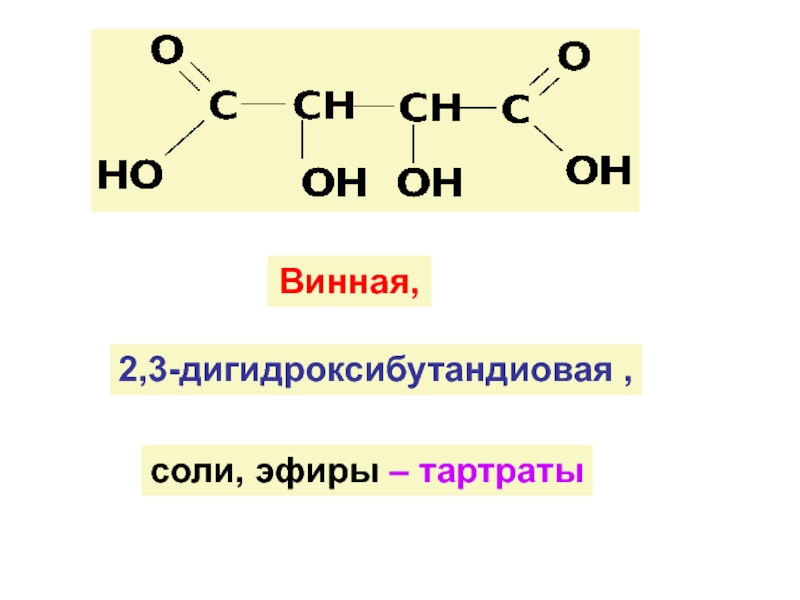
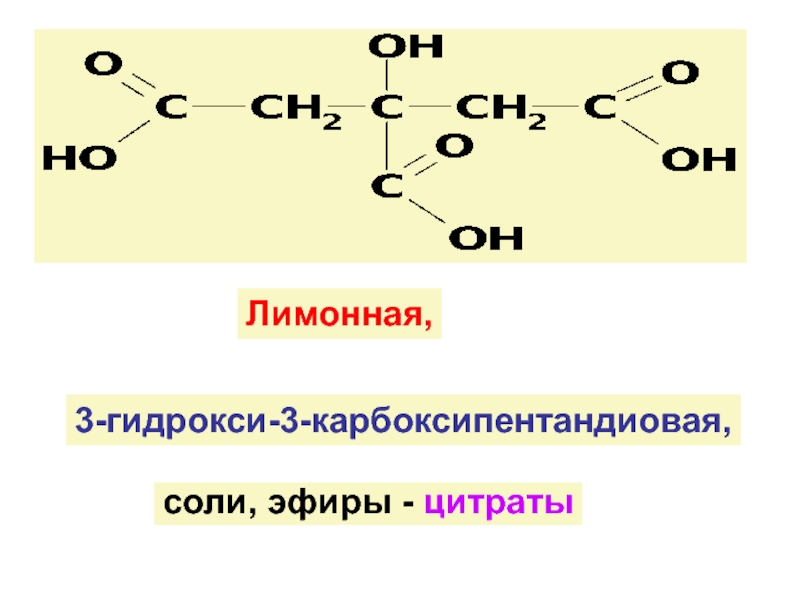
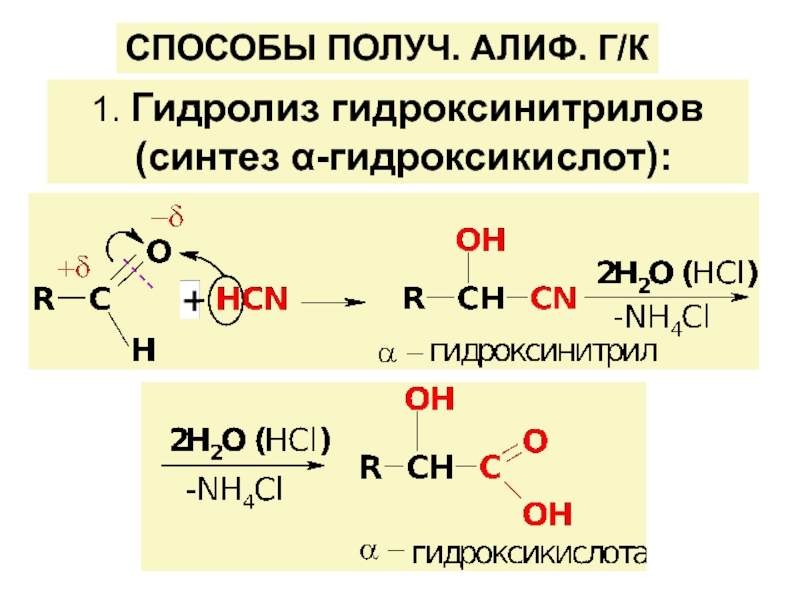
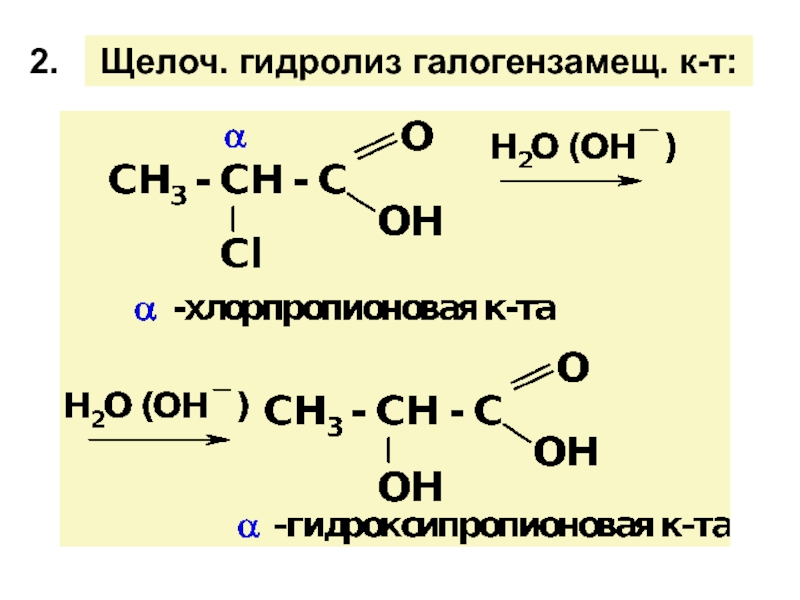
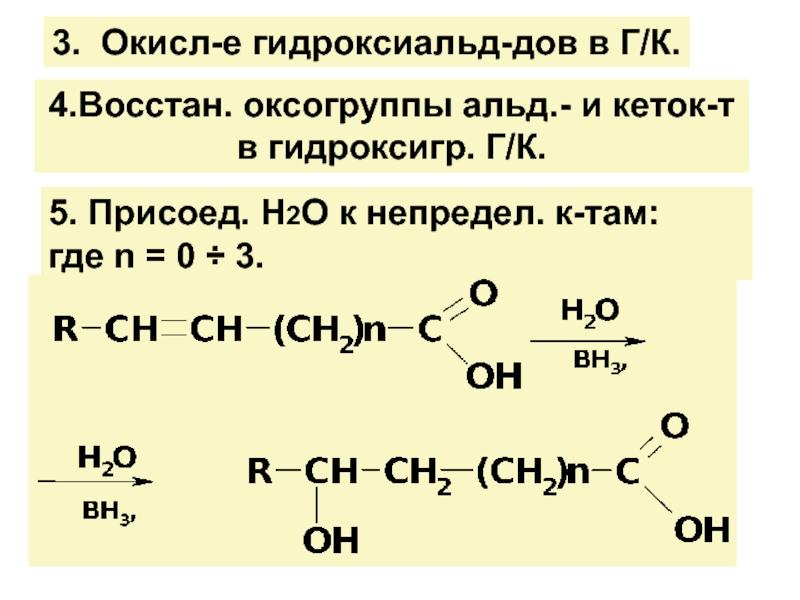
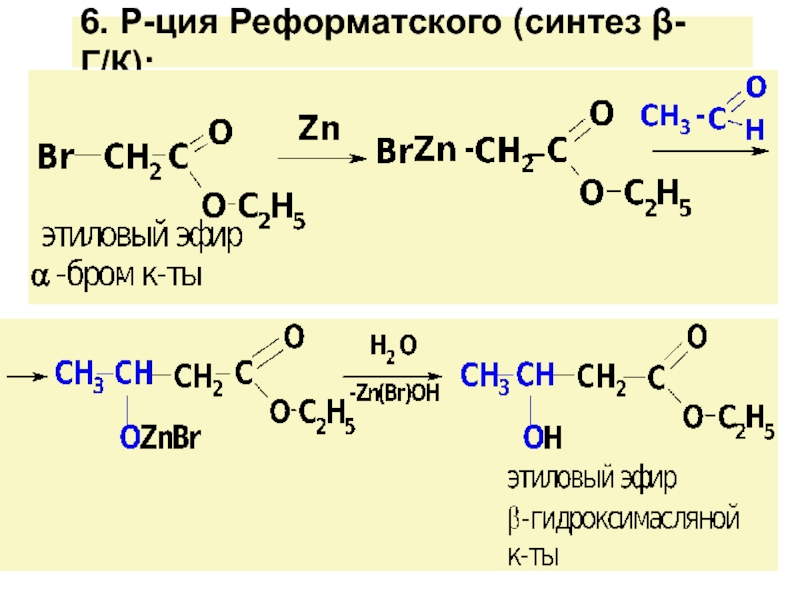
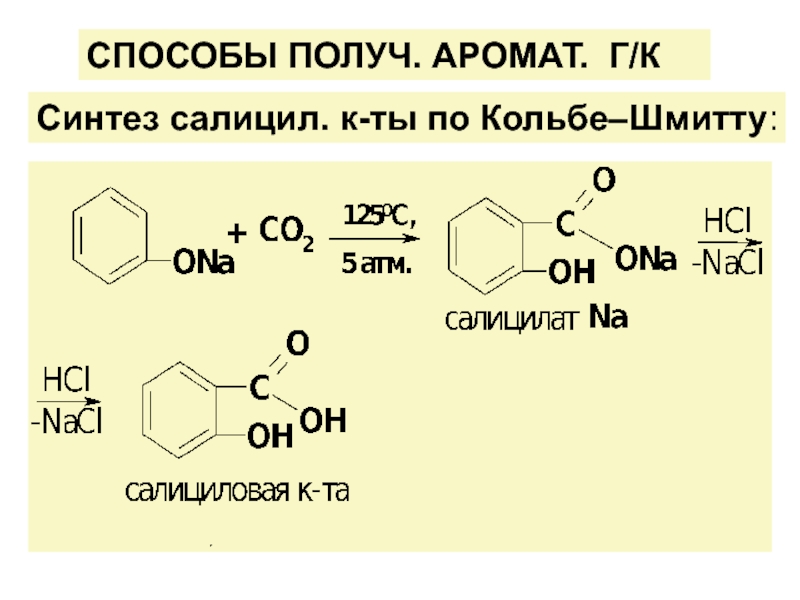

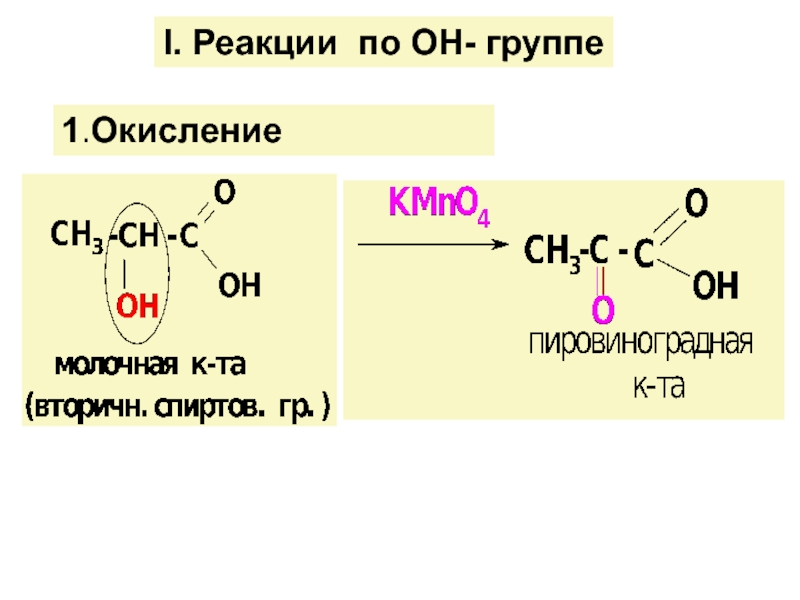
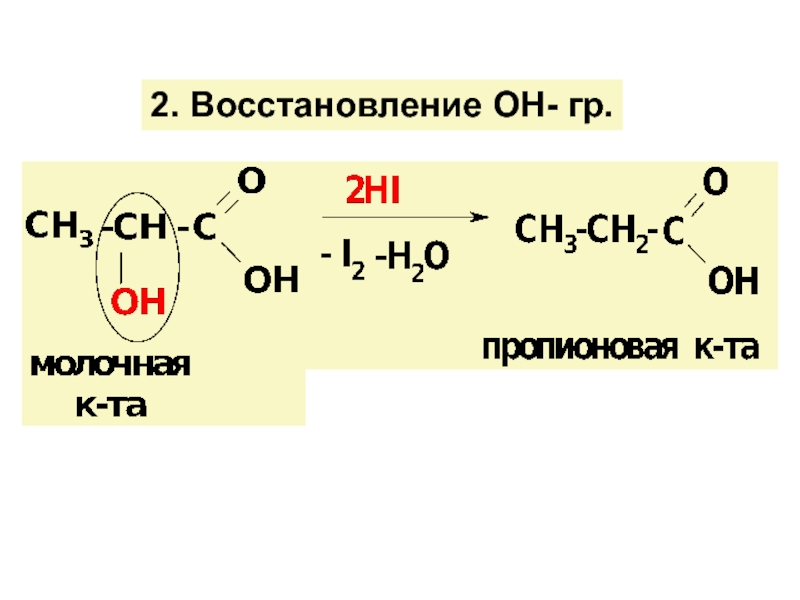
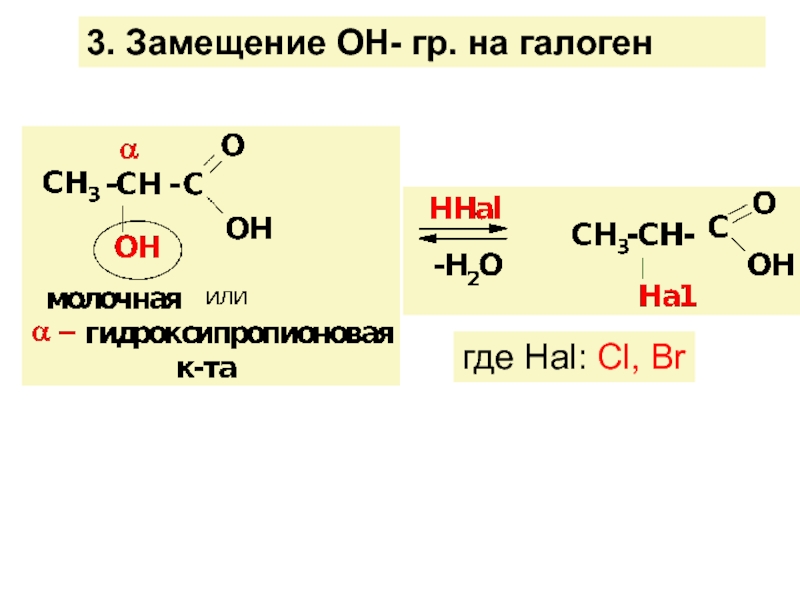
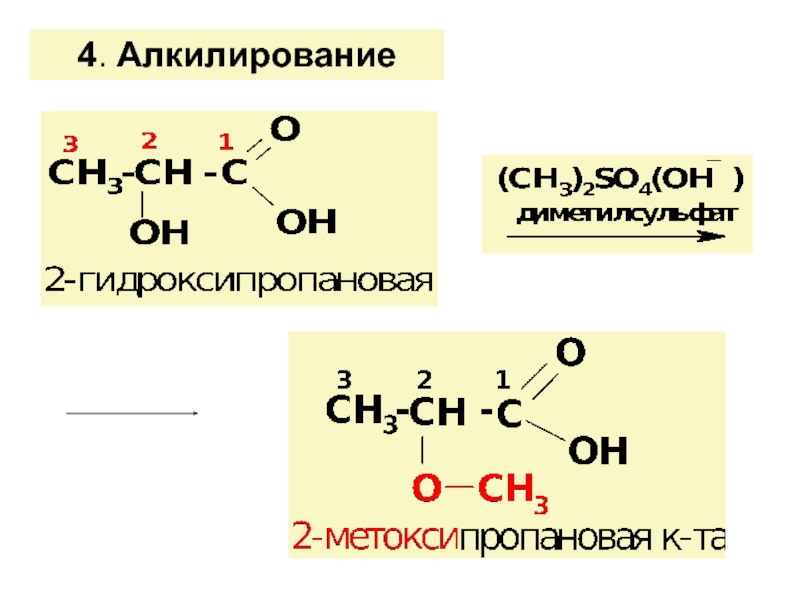
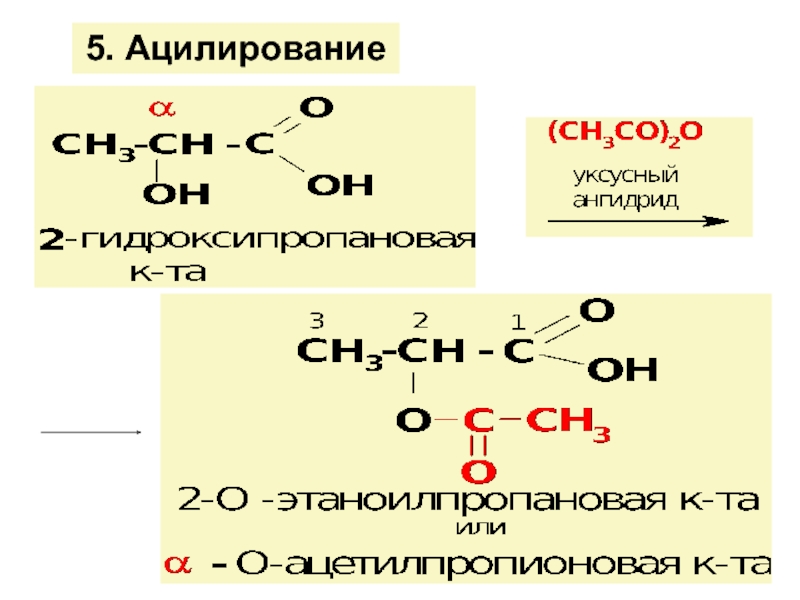
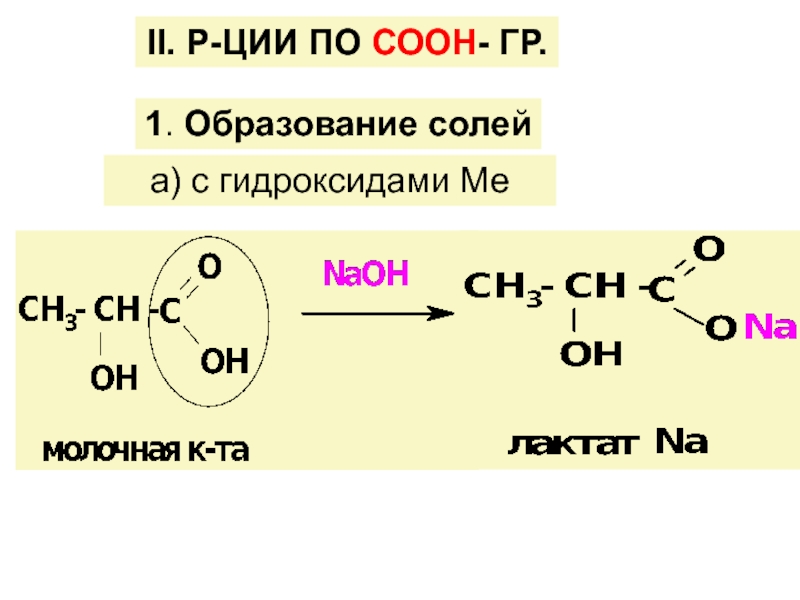
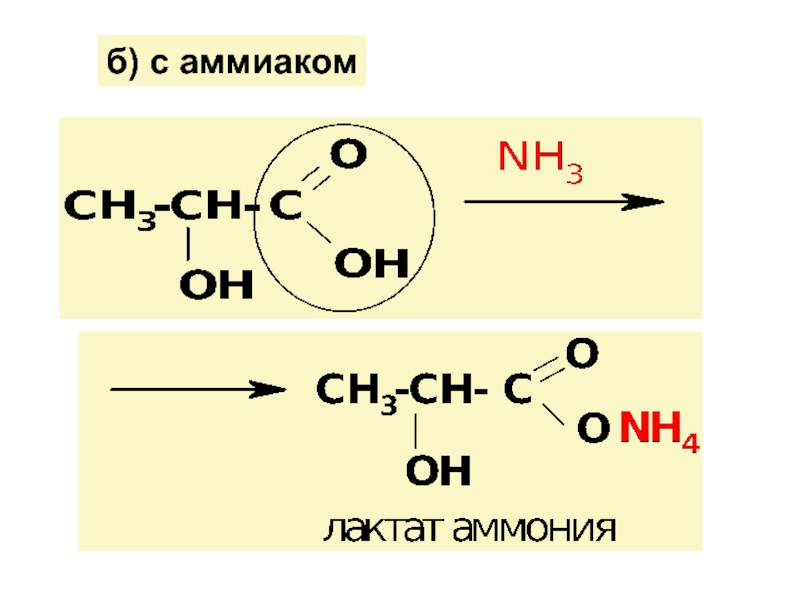
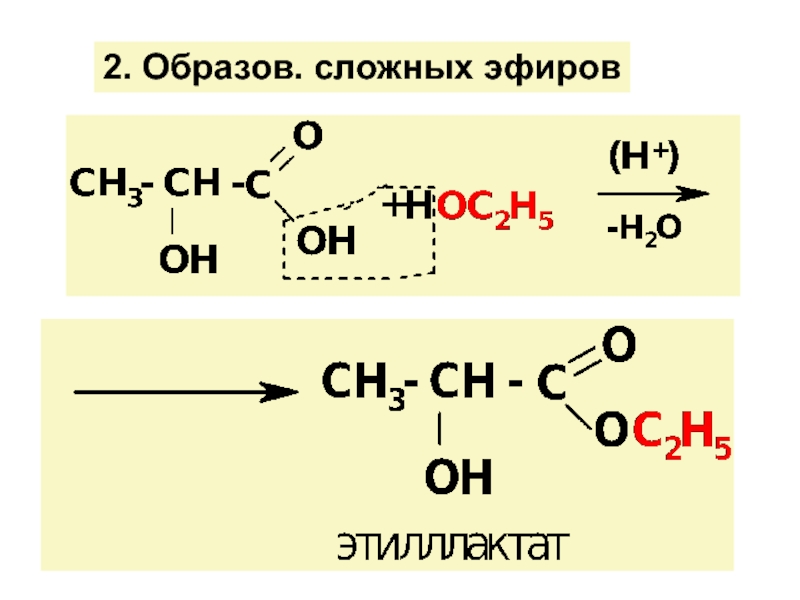
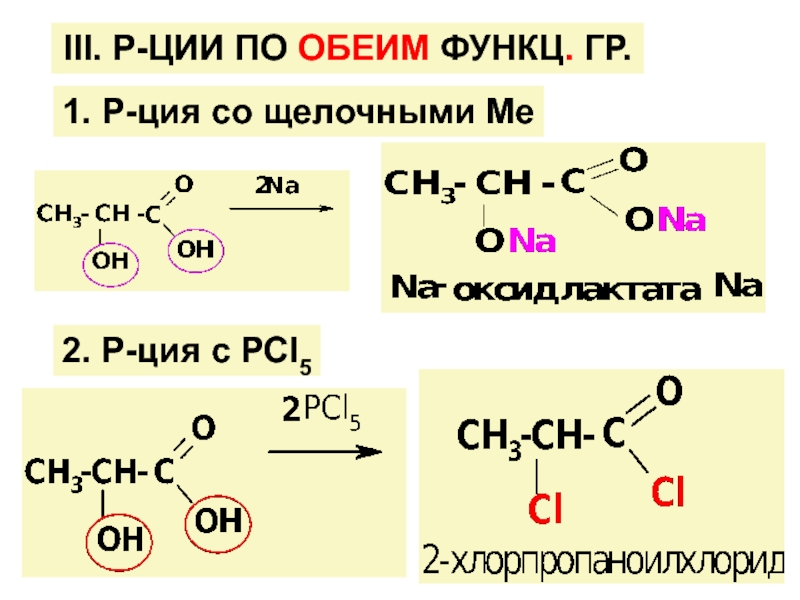

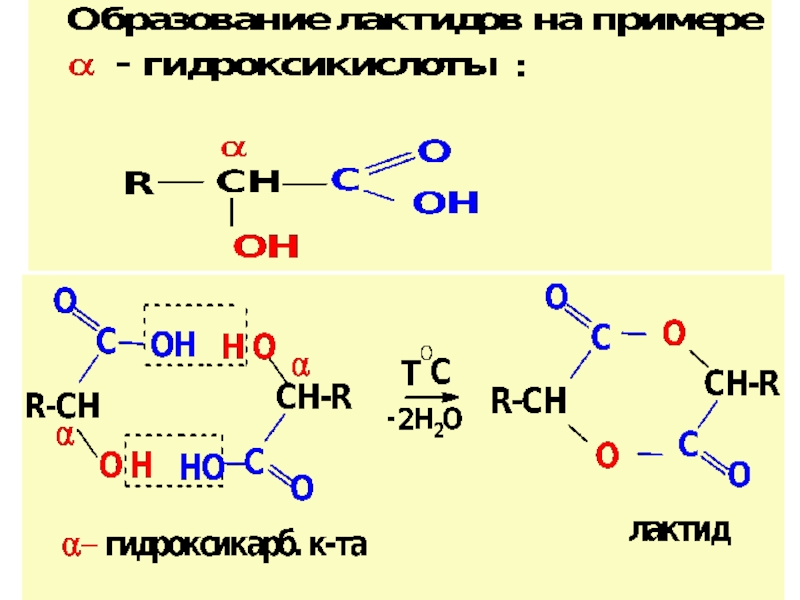
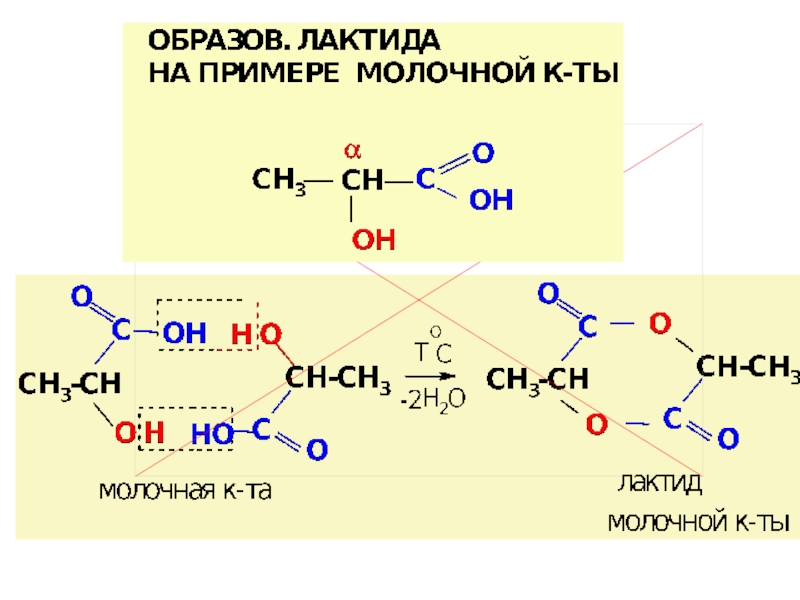
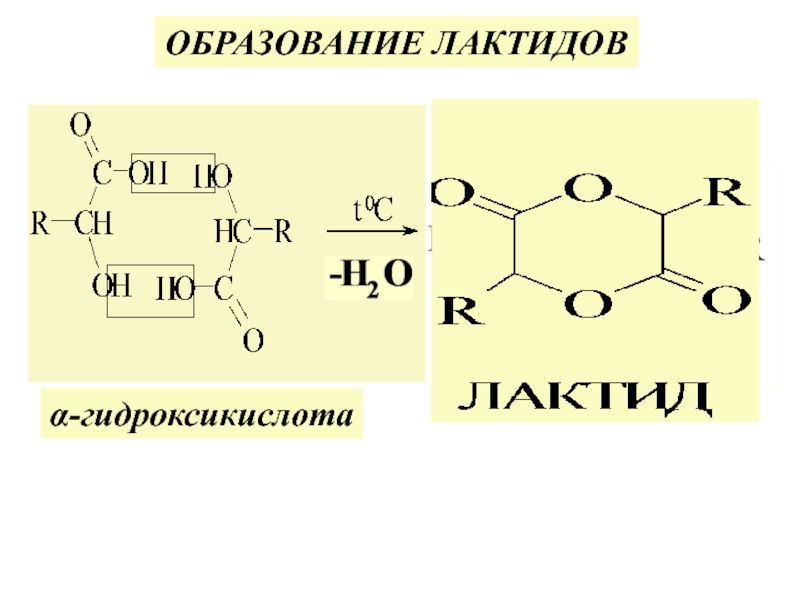
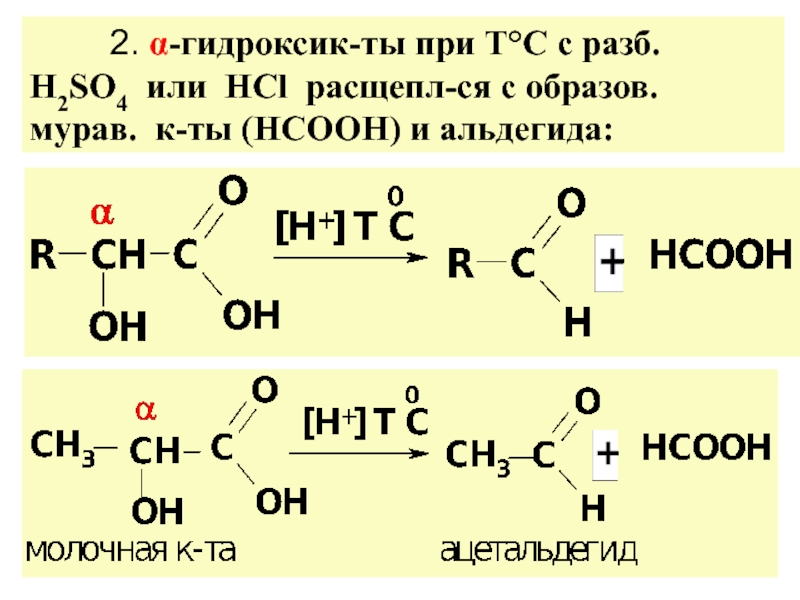
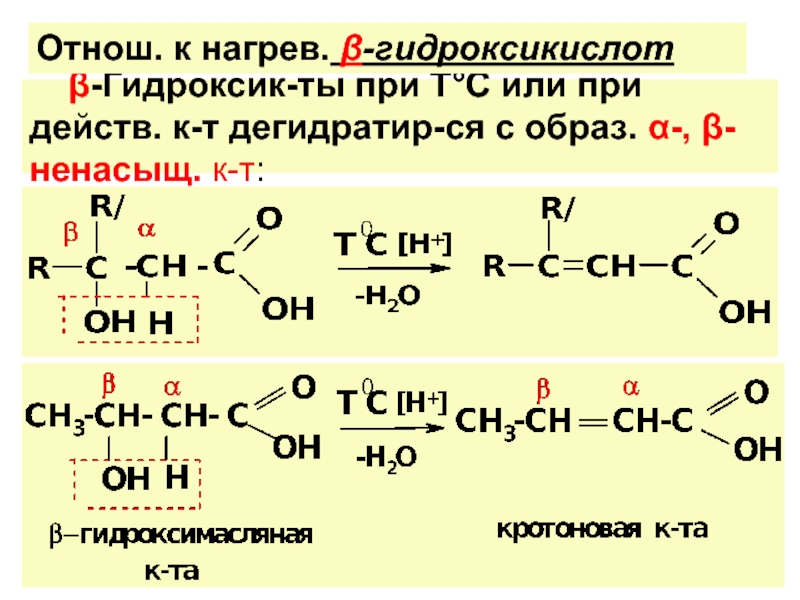


![ГИДРОКСИКИСЛОТЫ (Г/К)
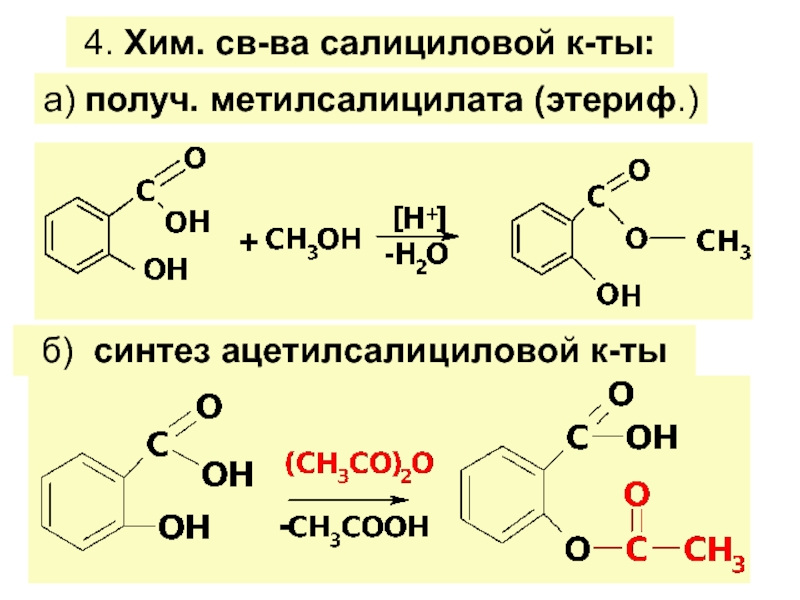
Функц. группы Г/К : ОН и СООН (старшая)
Классификация
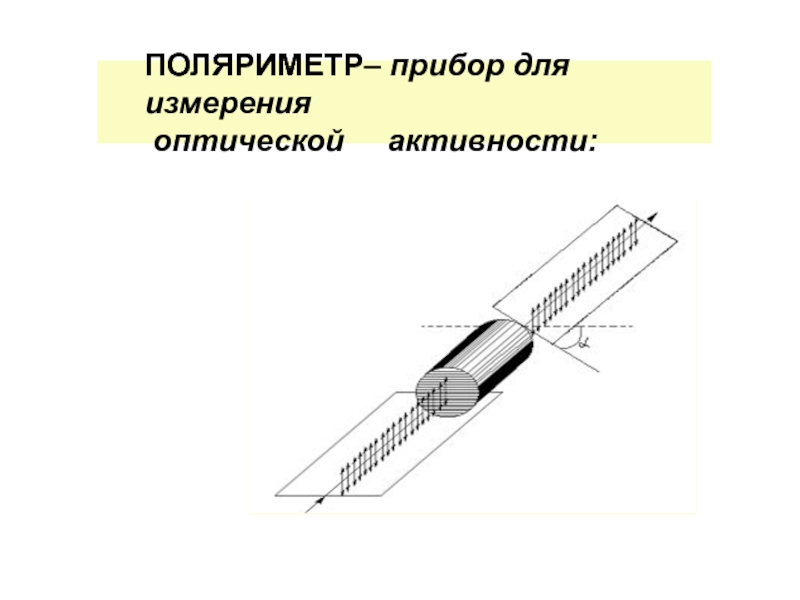
1) Единица измерения –удельное вращение [α]α –наблюдаемое вращениес – концентрация, l –длина трубки Единица измерения –удельное вращение [α]α –наблюдаемое вращениес – концентрация, l –длина трубки](/img/thumbs/676461afe69f98da7372a27987381d31-800x.jpg)