Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические реакции
Содержание
- 1. Химические реакции
- 2. ЯвленияФизические Химические Одни вещества превращаются в другие.Признаки
- 3. Реакции, протекающие с выделением теплоты и света, называют реакциями горения.Горение магнияГорение серы
- 4. РеакцииЭкзотермические Протекают с выделением теплоты (экзо – наружу).ЭндотермическиеПротекают с поглощением теплоты (эндо – внутрь).
- 5. Эндотермическая реакцияРеакция разложения ртути
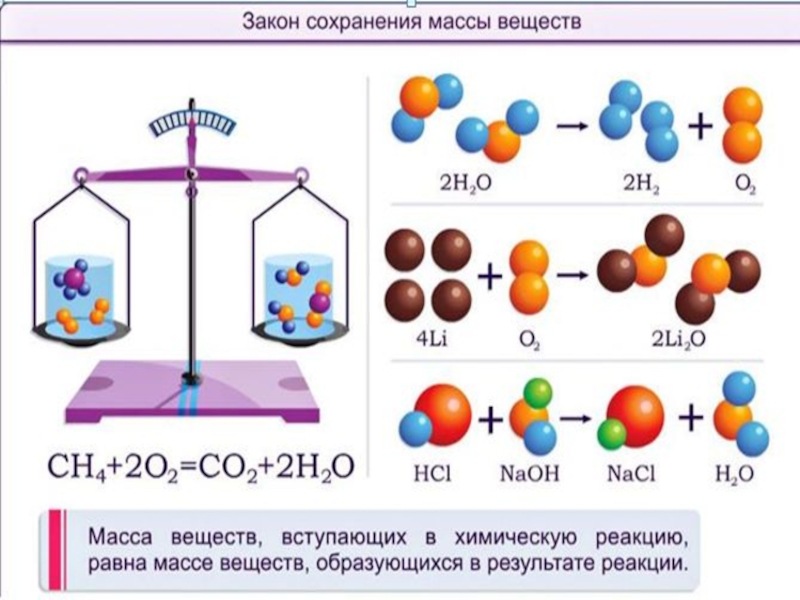
- 6. Закон сохранения массы веществ
- 7. В печи сожгли уголь массой 10кг, а масса образовавшейся золы составила всего 3кг. Почему?
- 8. В течение тысячелетий люди верили
- 9. Бойль проделал множество опытов по прокаливанию металлов
- 10. Подобно Бойлю русский ученый М.В.Ломоносов делал опыты
- 11. Слайд 11
- 12. Слайд 12
- 13. Химические уравнения. Химическое уравнение
- 14. Исходные вещества, принимающие участие в химических
- 15. Алгоритм составления уравнения химической реакции. P
- 16. Расставьте коэффициенты в следующих уравнениях:СuCl2 +
- 17. Уравнять следующие реакции:
- 18. Домашнее задание:Выучить § 27, 28.Стр. 166 вопр. 1, 2, 3
- 19. Скачать презентанцию
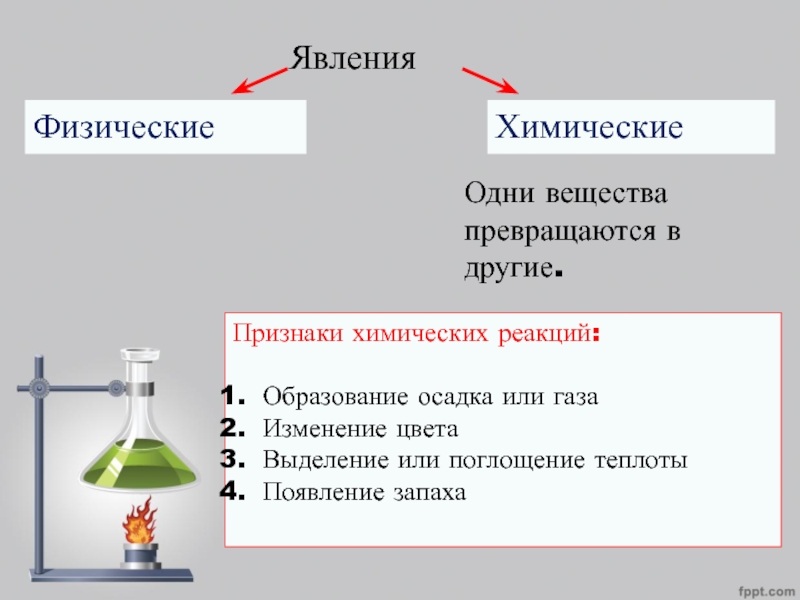
ЯвленияФизические Химические Одни вещества превращаются в другие.Признаки химических реакций:Образование осадка или газаИзменение цветаВыделение или поглощение теплотыПоявление запаха
Слайды и текст этой презентации
Слайд 2Явления
Физические
Химические
Одни вещества превращаются в другие.
Признаки химических реакций:
Образование осадка
или газа
Слайд 3 Реакции, протекающие с выделением теплоты и света, называют реакциями горения.
Горение
магния
Горение серы
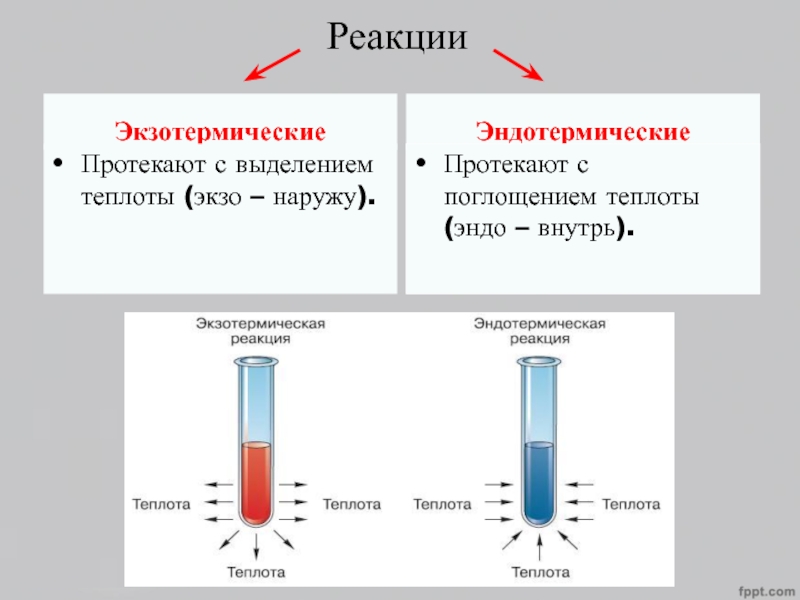
Слайд 4Реакции
Экзотермические
Протекают с выделением теплоты (экзо – наружу).
Эндотермические
Протекают с поглощением
теплоты (эндо – внутрь).
Слайд 8 В течение тысячелетий люди верили в то, что
вещество может бесследно исчезать, а также возникать из ничего.
Это чисто житейское утверждение подтвердил и такой известный ученый, как Роберт Бойль. Слайд 9 Бойль проделал множество опытов по прокаливанию металлов в незапаянных ретортах
и всякий раз масса оказывалась больше массы прокаливаемого металла.
Слайд 10Подобно Бойлю русский ученый М.В.Ломоносов делал опыты в запаянных ретортах.
Но, в отличие от Бойля, Ломоносов взвешивал сосуды как до,
так и после прокаливания, не вскрывая.Слайд 13
Химические уравнения.
Химическое уравнение – это условная запись химической
реакции посредством химических формул и коэффициентов.
Слайд 14
Исходные вещества, принимающие участие в химических реакциях называются реагентами.
Новые вещества,
образующиеся в результате химической реакции называются продуктами.
Слайд 15Алгоритм составления уравнения химической реакции.
P + O2 =
Помните! Молекулы
большинства простых газообразных веществ двухатомны –
H2; N2; O2;
F2; Cl2; Br2; I2. P2O5
2
5
4
Слайд 16
Расставьте коэффициенты в следующих уравнениях:
СuCl2 + Al = AlCl3 +
Cu
2) Н2 + N2 = NH3
3) CuOH = Cu2O +
H2O4) CS2 +O2 = CO2 + SO2
5) C2H2 + O2 = CO2 + H2O
6) Fe2 (SO4)3 + KOH = Fe(OH)3 + K2SO4
Слайд 17Уравнять следующие реакции:
1) Cl2O7 =
Cl2 + O2
2) KClO3 =
KCl + O23) C3H8 + O2 = CO2 + H2O
4) CO + O2 = CO2
5) AlCl3 + KOH = Al(OH)3 + KCl
6) H2SO4 + KOH = K2SO4 + H2O