Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ИНФУЗИОННАЯ ТЕРАПИЯ У ДЕТЕЙ. ВАЖЕН ЛИ ТОЧНЫЙ РАСЧЕТ?
Содержание
- 1. ИНФУЗИОННАЯ ТЕРАПИЯ У ДЕТЕЙ. ВАЖЕН ЛИ ТОЧНЫЙ РАСЧЕТ?
- 2. Основная цель интенсивной терапии – обеспечить доставку
- 3. ОСНОВНЫЕ ЗАДАЧИ ИТТ (Гельфанд Б.Р. и
- 4. Distribution of Water
- 5. Взаимосвязь между объем периоперационной ИТ и осложнениями (Bundgaard-Nielsen M, et al., Acta Anaesthesiol Scand. 2009 Aug;53(7):843-51)
- 6. ОСОБЕННОСТИ ИТ У Н/РНедостаточное назначение жидкости приводит
- 7. РАСЧЕТ ПОТРЕБНОСТИ В ЖИДКОСТИ ИСХОДЯ ИЗ:
- 8. Номограмма и формула для расчета площади поверхности тела (Briars G.L., Bailey B.J. Arch Dis Child 1994;70:246–247.)
- 9. МИНИМАЛЬНАЯ ФИЗИОЛОГИЧЕСКАЯ ПОТРЕБНОСТЬ И МАКСИМАЛЬНАЯ ТОЛЕРАНТНОСТЬ К ЖИДКОСТИ (Хартиг В., 1982)
- 10. РАСЧЕТ ОБЪЕМА ЖИДКОСТИ ДЛЯ (ФП) ПОДДЕРЖИВАЮЩЕЙ ИНФУЗИОННОЙ ТЕРАПИИ (Holliday M.A., Segar W.E., 1957)
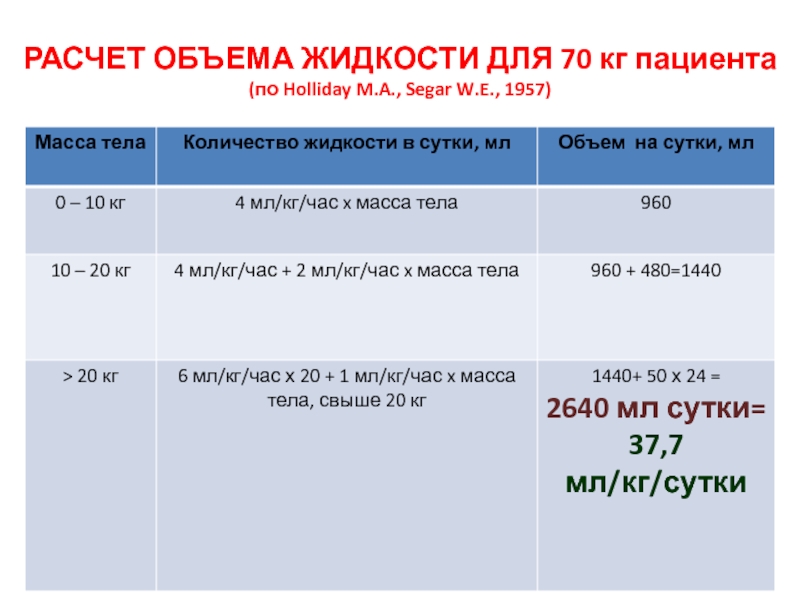
- 11. РАСЧЕТ ОБЪЕМА ЖИДКОСТИ ДЛЯ 70 кг пациента (по Holliday M.A., Segar W.E., 1957)
- 12. ФОРМУЛА ВАЛЛАЧИ100 – 3 x n
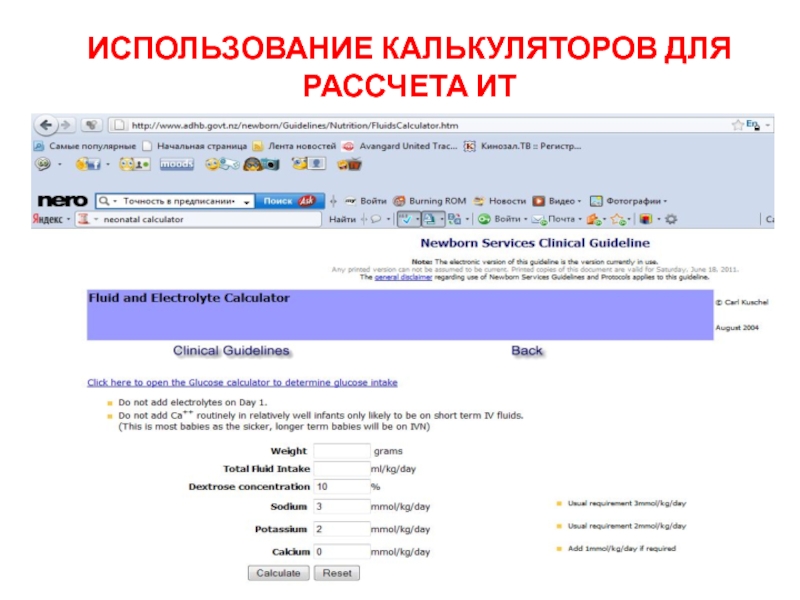
- 13. ИСПОЛЬЗОВАНИЕ КАЛЬКУЛЯТОРОВ ДЛЯ РАССЧЕТА ИТ
- 14. ДИАПАЗОН КОЛЕБАНИЙ РАСЧЕТНЫХ ВЕЛИЧИН ФП (Ю.В.Золотарев, Ю.Б. Жидков, 1998)
- 15. Неощутимые потери воды и потребность в жидкости
- 16. ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ
- 17. ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ
- 18. ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ
- 19. ПОТРЕБНОСТИ НОВОРОЖДЕННОГО РЕБЕНКА В ЖИДКОСТИ И ЭЛЕКТРОЛИТАХ (Р.А.ПОЛИН , А.Р. СПИТЦЕР, 2011)
- 20. Потребность в жидкости у новорожденных, отделение детской хирургии, госпиталь Sheffield, в мл/кг/день http://www.nda.ox.ac.uk/wfsa/html/u19/u1914_01.htm
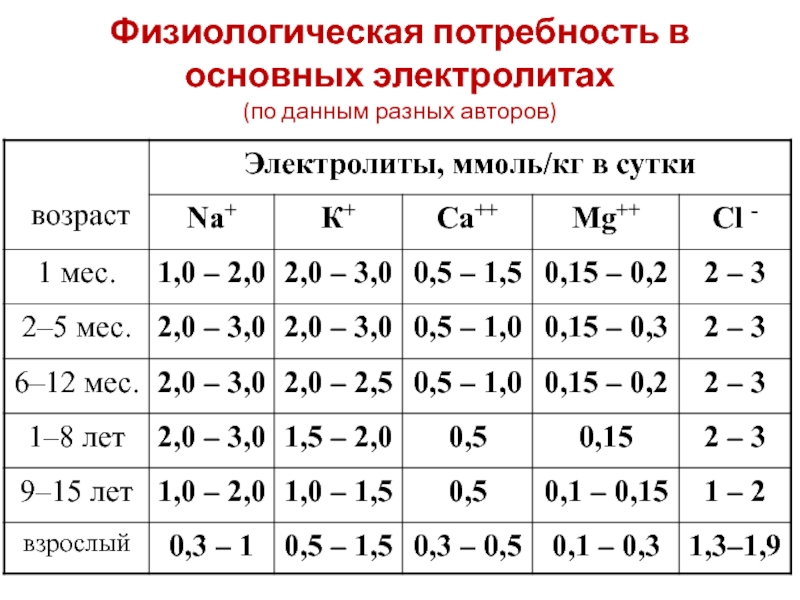
- 21. Физиологическая потребность в основных электролитах (по данным разных авторов)
- 22. ИНФУЗИОННАЯ ТЕРАПИЯОБЪЕМ ЖИДКОСТИ на СУТКИ ФИЗИОЛОГИЧЕСКАЯПОТРЕБНОСТЬДЕФИЦИТ ЖИДКОСТИПАТОЛОГИЧЕСКИЕ ПОТЕРИ
- 23. УРАВНЕНИЕ СТАРЛИНГА
- 24. Считалось, что в артериальном конце капилляра фильтруется
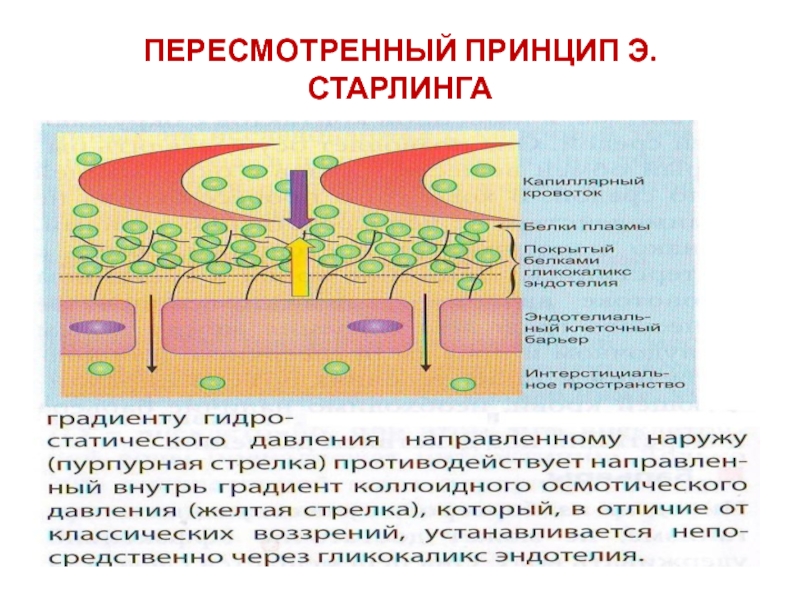
- 25. ПЕРЕСМОТРЕННЫЙ ПРИНЦИП Э.СТАРЛИНГА
- 26. Слайд 26
- 27. ЭЛЕКТРОННО-МИКРОСКОПИЧЕСКОЕ ИЗОБРАЖЕНИЕ ГЛИКОКАЛИКСА Sevoflurane reduces leukocyte and
- 28. Воздействие на объем коллоидов при гиперволемии и
- 29. Контрольная группа 5 пациентов, малая хирургия под
- 30. В течение многих десятилетий ‘третье пространство’ рассматривалось
- 31. Слайд 31
- 32. Дети с ОПН, которые требуют CRRT, при
- 33. Исследован 3141 лихорадящий ребенок с нарушением перфузии,
- 34. Смертность через 48 часов. (а) полная информация
- 35. 12. Flori HR, Church G, Liu KD,
- 36. Слайд 36
- 37. Слайд 37
- 38. Слайд 38
- 39. Перегрузка жидкостью и легкиеМеньшая продолжительность ИВЛ [6,3
- 40. Ограничительная стратегия ИТ предпочтительна в фазе послереанимационной
- 41. Фаза СПАСЕНИЯ – немедленная эскалация ИТ, для
- 42. СТАБИЛИЗАЦИЯ отражает точку, в которой пациент находится
- 43. 50 гемодинамически стабильных взрослых пациентов с гипоальбуминемией
- 44. Слайд 44
- 45. В пилотном проспективном рандомизированном контролируемом исследовании 64
- 46. Ежедневное увеличение объема вводимой жидкости (внутривенно +
- 47. Ограничение жидкости не вызвало побочных эффектов
- 48. Среднее значение BW, GA, и оценка SNAP-II
- 49. Слайд 49
- 50. Быстрая волемическая реанимация необходима для гипотензивных н/р
- 51. 16 из 22 смертельных случаев были признаны «не является неизбежным»!!!
- 52. Слайд 52
- 53. Слайд 53
- 54. Клиницисты имеют тенденцию вводить дополнительный объем в
- 55. Я продолжаю поддерживающую ИТ с той же
- 56. ФИО: ЗАНДата рождения: 26.11.2002Диагноз при поступлении: Посттравматический
- 57. При поступлении:15.12.15 выполнена Rg-грамма левого плечевого сустава
- 58. 17.12.15 под общим внутривенным наркозом проведена операция:
- 59. 19.12.2015 и 21.12.2015
- 60. -Аб терапия : цефтриаксон ( с 17.12.15-18.12.15)
- 61. 25.12.2015
- 62. Стратегия инфузионной терапии для пациентов ОРИТ
- 63. Слайд 63
- 64. КЛАССИФИКАЦИЯ ИНФУЗИОННЫХ РАСТВОРОВ ПО МЕХАНИЗМУ ТЕРАПЕВТИЧЕСКОГО ДЕЙСТВИЯ**предложена
- 65. ЯВЛЯЕТСЯ ЛИ ФИЗИОЛОГИЧЕСКИЙ РАСТВОР ФИЗИОЛОГИЧНЫМ?
- 66. ФИЗИОЛОГИЧЕСКИЕ ПРЕДПОСЫЛКИ ДЛЯ ПРИМЕНЕНИЯ ИНФУЗИОННОЙ ТЕРАПИИ У
- 67. СБАЛАНСИРОВАННЫЙ ЭЛЕКТРОЛИТНЫЙ РАСТВОР должен иметь физиологическую ионную
- 68. Ионный состав некоторых кристаллоидных растворов * Г - глюкоза
- 69. СтерофундинНатрий - 145,0ммоль/л, Калий - 4,0 ммоль/л,
- 70. Слайд 70
- 71. Parker R.I. Transfusion in Critically III Children: Indications, Risks, and Challenges (Crit Care Med 2014; 42:675-690).
- 72. КОНТРОЛЬ ЗА ПАЦИЕНТОМ, ПОЛУЧАЮЩИМ ИНФУЗИОННУЮ ТЕРАПИЮАНТРОПОМЕТРИЧЕСКИЙ КОНТРОЛЬ
- 73. Слайд 73
- 74. ВОПРОСЫ????
- 75. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ИНФУЗИОННАЯ ТЕРАПИЯ У ДЕТЕЙ.
ВАЖЕН ЛИ ТОЧНЫЙ РАСЧЕТ?
Ю.С. Александрович
Заведующий
кафедрой анестезиологии, реаниматологии и неотложной педиатрии ФП и ДПО
Слайд 2Основная цель интенсивной терапии – обеспечить доставку кислорода, соответствующую реальному
потреблению тканями
Мониторинг транспорта кислорода // © Ю.С. Александрович, 2010
(DO2) (VO2)
Слайд 3ОСНОВНЫЕ ЗАДАЧИ ИТТ
(Гельфанд Б.Р. и соавт., 2009)
Восстановление и поддержание
объема и состава всех водных секторов организма (сосудистого, интерстициального, клеточного)
Оптимизация
параметров центральной, регионарной гемодинамики и микроциркуляцииКоррекция параметров гомеостаза: поддержание водного и кислотно-основного равновесия, осмолярности и онкотического давления
Обеспечение адекватного транспорта кислорода к органам и тканям
Профилактика реперфузионных повреждений
Инфузионно-трансфузионная терапия в клинической медицине
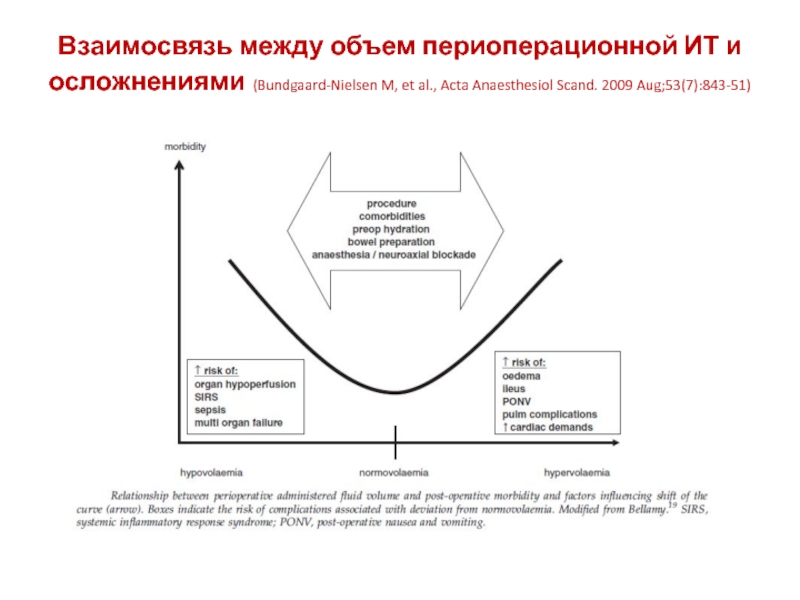
Слайд 5Взаимосвязь между объем периоперационной ИТ и осложнениями (Bundgaard-Nielsen M, et
al., Acta Anaesthesiol Scand. 2009 Aug;53(7):843-51)
Слайд 6ОСОБЕННОСТИ ИТ У Н/Р
Недостаточное назначение жидкости приводит к гиповолемии, гиперосмолярности,
нарушениям обмена веществ и почечной недостаточности.
Избыточное назначение жидкости зрелым
новорожденным приводит к общим отёкам и нарушению функции почек, а н-м с ОНMТ к ОАП и сердечно сосудистой недостаточности, ВЖК, НЭКу и БЛД.Слайд 7РАСЧЕТ ПОТРЕБНОСТИ В ЖИДКОСТИ
ИСХОДЯ ИЗ:
расчета расхода энергии
с помощью таблиц и номограмм (Darrow D.C., Pratt E.L. Fluid
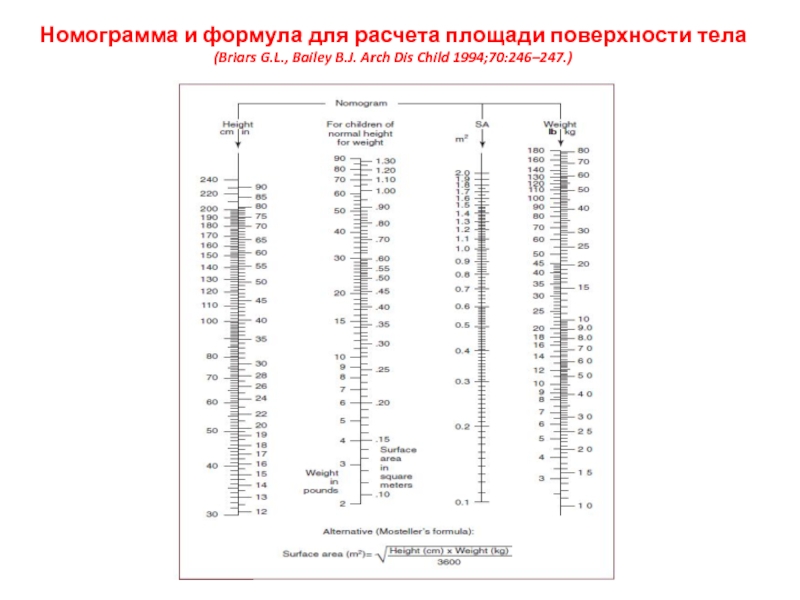
therapy, relation to tissue composition and expenditure of water and electrolyte. Council on Food and Nutrition. JAMA. 1950;143:365-373).площади поверхности тела – (Crawford D.J., Terry M., Roubke G. Simplification of Drug Dosage Calculation by Application of the Surface Area Principle. Pediatrics, 5:783-90, 1950).
возраста – (Wallace WM. Quantative requirements of infant and child for water and electrolyte under varying conditions. Am J Clin Pathol. 1953;23: 1133-1141).
веса – (Holliday MA, Segar WE. The maintenance need for water in parenteral fluid therapy. Pediatrics. 1957;19:823-832).
Слайд 8Номограмма и формула для расчета площади поверхности тела (Briars G.L.,
Bailey B.J. Arch Dis Child 1994;70:246–247.)
Слайд 9МИНИМАЛЬНАЯ ФИЗИОЛОГИЧЕСКАЯ ПОТРЕБНОСТЬ И
МАКСИМАЛЬНАЯ ТОЛЕРАНТНОСТЬ К ЖИДКОСТИ
(Хартиг В., 1982)
Слайд 10РАСЧЕТ ОБЪЕМА ЖИДКОСТИ ДЛЯ (ФП) ПОДДЕРЖИВАЮЩЕЙ ИНФУЗИОННОЙ ТЕРАПИИ (Holliday M.A., Segar
W.E., 1957)
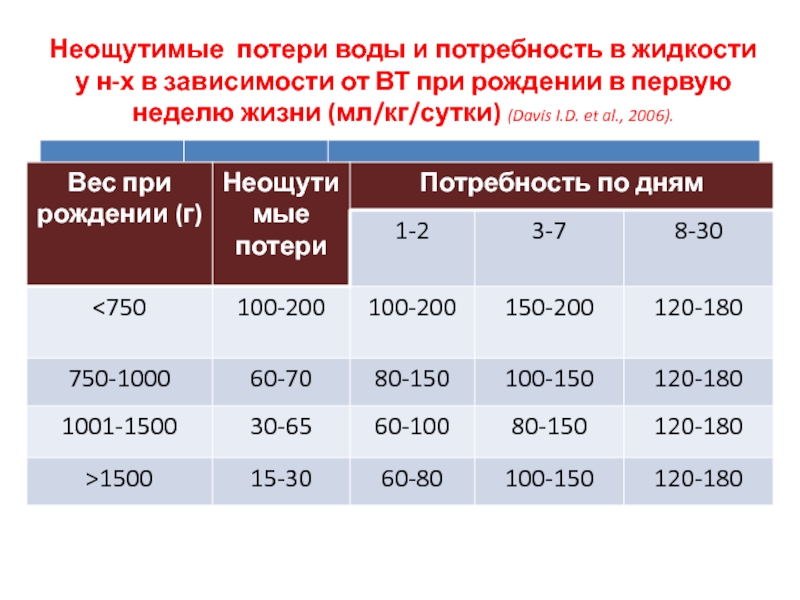
Слайд 15Неощутимые потери воды и потребность в жидкости у н-х в
зависимости от ВТ при рождении в первую неделю жизни (мл/кг/сутки)
(Davis I.D. et al., 2006).Слайд 16ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ В ТРАНЗИТОРНЫЙ
ПЕРИОД ДО 3-4 ДНЯ
(Н.Н. Володин, 2013)
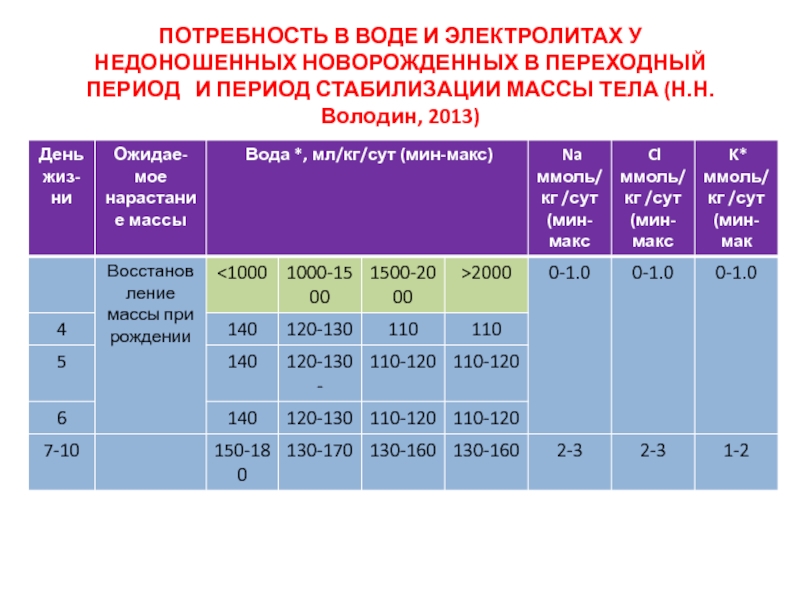
Слайд 17ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ В ПЕРЕХОДНЫЙ
ПЕРИОД И ПЕРИОД СТАБИЛИЗАЦИИ МАССЫ ТЕЛА (Н.Н. Володин, 2013)
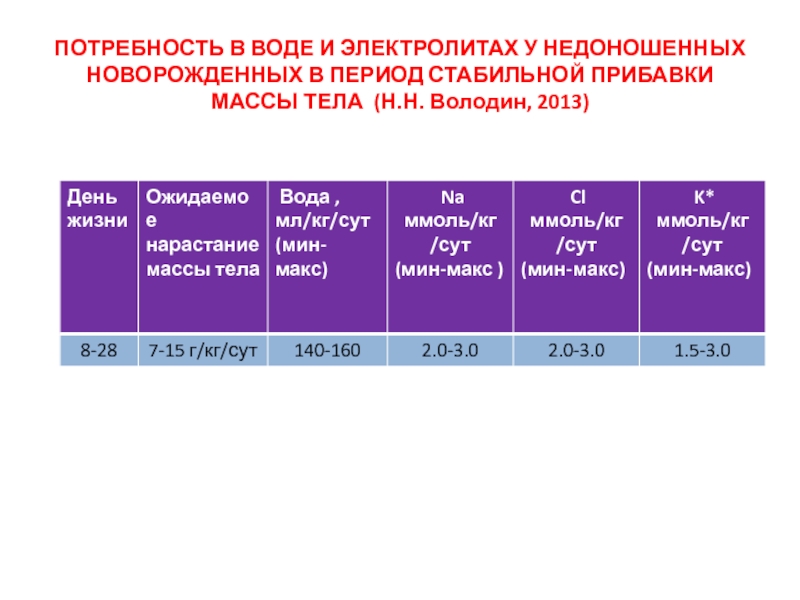
Слайд 18ПОТРЕБНОСТЬ В ВОДЕ И ЭЛЕКТРОЛИТАХ У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ В ПЕРИОД
СТАБИЛЬНОЙ ПРИБАВКИ МАССЫ ТЕЛА (Н.Н. Володин, 2013)
Слайд 19ПОТРЕБНОСТИ НОВОРОЖДЕННОГО РЕБЕНКА В ЖИДКОСТИ И ЭЛЕКТРОЛИТАХ (Р.А.ПОЛИН , А.Р.
СПИТЦЕР, 2011)
Слайд 20Потребность в жидкости у новорожденных, отделение детской хирургии, госпиталь Sheffield,
в мл/кг/день
http://www.nda.ox.ac.uk/wfsa/html/u19/u1914_01.htm
Слайд 22ИНФУЗИОННАЯ ТЕРАПИЯ
ОБЪЕМ
ЖИДКОСТИ
на
СУТКИ
ФИЗИОЛОГИЧЕСКАЯ
ПОТРЕБНОСТЬ
ДЕФИЦИТ ЖИДКОСТИ
ПАТОЛОГИЧЕСКИЕ
ПОТЕРИ
Слайд 24Считалось, что в артериальном конце капилляра фильтруется жидкость (гидростатическое Р
внутри капилляра больше онкотического Р в нём же); в венозном
- наоборот - реабсорбируется. Когда давление измерили, оказалось, что реабсорбции не происходит - ни в артериальном, ни в венозном конце капилляра. Гидростатическое давление интерстиция в норме отрицательное, а онкотическое - динамическое, но всегда большее, чем внутри капилляра. При повышении гидростатического Р внутри капилляра, фильтрация ж-ти увеличивается, разбавляя таким образом белки интерстиция и снижая онкотическое Р интрестиция - фильтрация снижается, наступает эквилибрий. "Классический" Старлинг - слева, "новый" - справа:J. Rodney Levick and C. Charles Michel, 2009
Слайд 27ЭЛЕКТРОННО-МИКРОСКОПИЧЕСКОЕ ИЗОБРАЖЕНИЕ ГЛИКОКАЛИКСА
Sevoflurane reduces leukocyte and platelet adhesion after
ischemia-reperfusion by protecting the endothelial glycocalyx. Chappell D. et al.,
Anesthesiology. 2011 Sep;115(3):483-91.Интактный гликокаликс после 25 мин неишемической перфузии (группа A).
Эндотелиальный гликокаликс после 20 минутной тепловой ишемии и 10 минутной непрерывной реперфузии (группа J).
(C) Гликокаликс после предварительной обработки 1 МАК севофлюрана, а затем 20 минутной тепловой (37°C) no-flow ишемии и 10 минутной реперфузии (группа L).
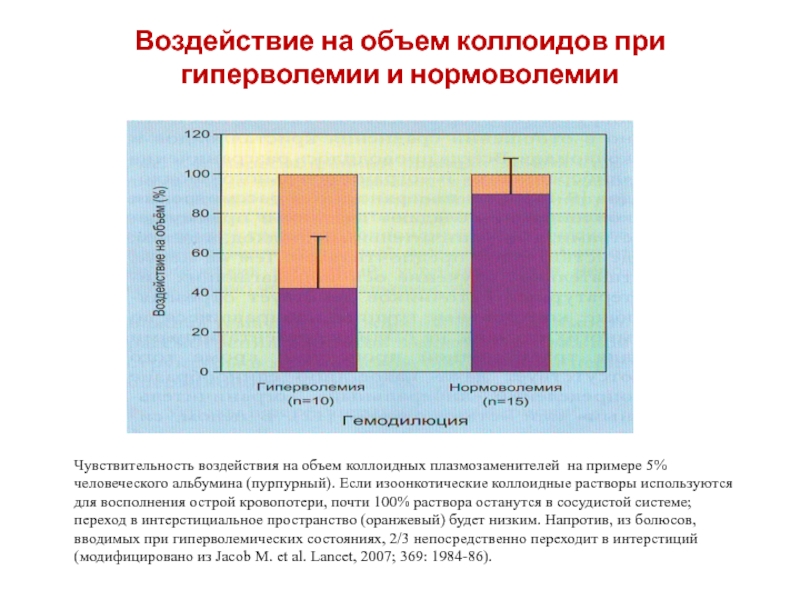
Слайд 28Воздействие на объем коллоидов при гиперволемии и нормоволемии
Чувствительность воздействия на
объем коллоидных плазмозаменителей на примере 5% человеческого альбумина (пурпурный). Если
изоонкотические коллоидные растворы используются для восполнения острой кровопотери, почти 100% раствора останутся в сосудистой системе; переход в интерстициальное пространство (оранжевый) будет низким. Напротив, из болюсов, вводимых при гиперволемических состояниях, 2/3 непосредственно переходит в интерстиций (модифицировано из Jacob M. et al. Lancet, 2007; 369: 1984-86).Слайд 29Контрольная группа 5 пациентов, малая хирургия под ОА. Не получали
жидкости или электролитов во время операции и были использованы для
демонстрации точности и воспроизводимости метода. Основная 13 взрослых , плановая хирургия. Возрастание функциональной потери внеклеточной жидкости с увеличением тяжести травмы.Слайд 30В течение многих десятилетий ‘третье пространство’ рассматривалось как активный водный
сектор организма, потребляющий жидкость. Поэтому, периоперационные режимы инфузионной терапии были
традиционно основаны на восполнении дефицита жидкости, возникающего из-за секвестрации воды в третьем пространстве. Последствием этого было возникновение выраженного положительного водного баланса, чтобы поддержать объем циркулирующей крови во время обширного оперативного вмешательства. Принимая во внимание, что неощутимые потери и предоперационный дефицит жидкости фактически очень часто бывают незначительными, а «третье пространство» в реальности не существует избыточно введенная жидкость накапливается в интерстициальном пространстве, что приводит к повреждению гликокаликса – ключевой структуры сосудистого барьера на фоне ятрогенной гиперволемии. Это объясняет, почему пациенты после больших хирургических вмешательств, у которых не восполнялся дефицит жидкости, обусловленный ее секвестрацией в «третье пространство», имеют лучшие исходы, что требует пересмотра традиционных взглядов на наличие «третьего пространства» в периоперационном периоде и оптимизации инфузионой терапии у данной категории пациентов.Best Pract Res Clin Anaesthesiol. 2009 Jun;23(2):145-57.
The 'third space'--fact or fiction? Jacob M, Chappell D, Rehm M.
Слайд 32Дети с ОПН, которые требуют CRRT, при наличии ПОН, сепсиса
и перегрузки объемом более 20% на момент начала CRRT имеют
более высокую смертность.Слайд 33Исследован 3141 лихорадящий ребенок с нарушением перфузии, которым после рандомизации
вводили:
20-40 мл/кг альбумина (болюс),
20-40 мл/кг физиологического раствора (болюс),
или
не вводили болюс. Смертность через 48 часов составила
10,6% (болюс альбумина),
10,5% (болюс физиологического раствора)
7,3%, в контрольной группе.
Смертность в течение 4 недель составила
12,2%, 12,0% и 8,7%, соответственно.
Слайд 34Смертность через 48 часов. (а) полная информация N=2396. (б) неполная
информация N=745. B: болюс; C: контроль
СМЕРТНОСТЬ БЫЛА ВЫШЕ ПРИ КОМБИНАЦИИ
ТРЕХ СИНДРОМОВ ПРИ ПОСТУПЛЕНИИ ПС (28% БОЛЮС, КОНТРОЛЬ 21%) И В СОЧЕТАНИИ ШОКА/ АЦИДОЗА И РЕСПИРАТОРНЫХ ПРОБЛЕМ (19% БОЛЮС, 18% КОНТРОЛЬ). Наибольшие различия в уровне смертности между болюсом и контролем были у тех, кто имел все три ПС (N=205), и только шок/ацидоз (N=693; 10% болюс, контроль 3%). Эти две группы включают 37% (898 из 2396) из всех случаев. Смертность была низкая при одной ДН (2% болюс, 5% контроль) или только при неврологии (4% болюс, 0% контроль). Небольшое количество, 363 из 2396 (15%) имели только критерии включения FEAST; 3 детей умерли в этой группе (2% болюс, контроль 0%).Слайд 3512. Flori HR, Church G, Liu KD, Gildengorin G, Matthay
MA (2011) Positive fluid balance is associated with higher mortality
and prolonged mechanical ventilation in pediatric patients with acute lung injury. CritCare Res Pract 854142. doi:10.1155/2011/854142
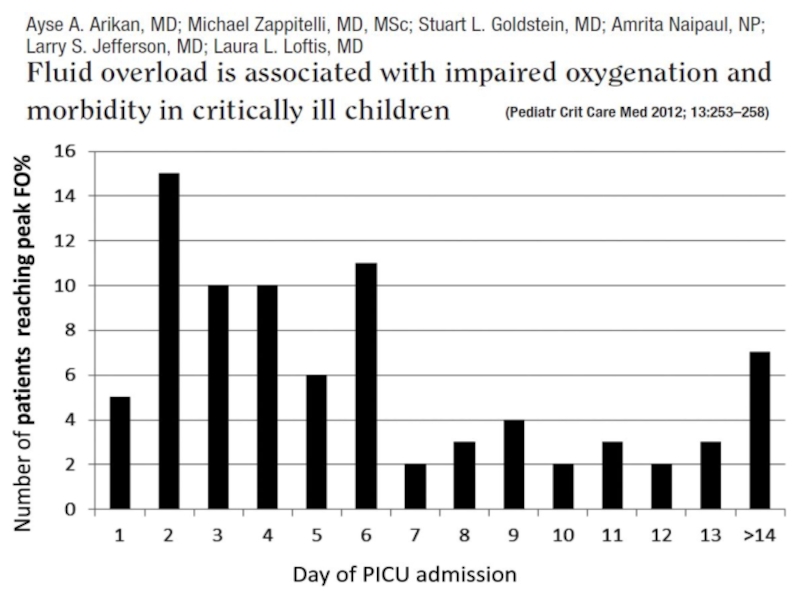
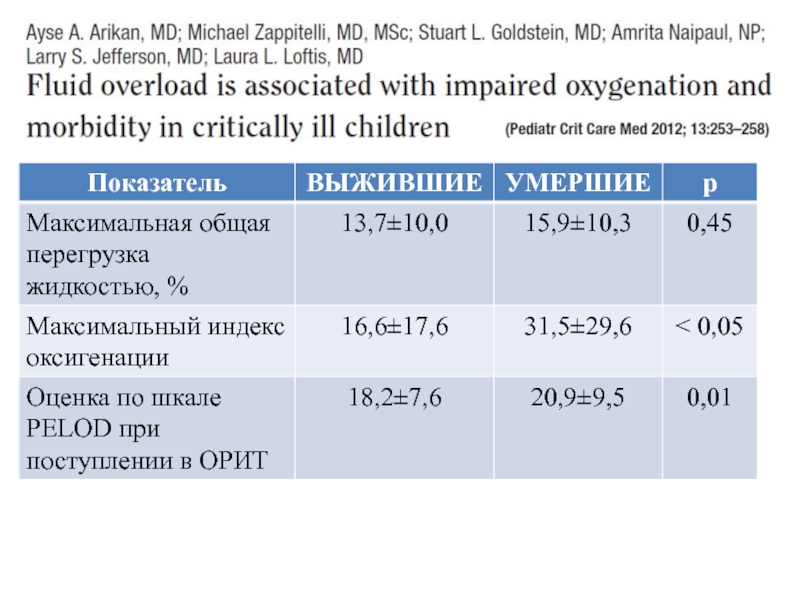
13. Arikan AA, Zappitelli M, Goldstein S, Naipaul A, Jefferson LS, Loftis L (2012) Fluid overload is associated with impaired oxygenation and morbidity in critically ill children. Pediatr Crit Care
Med 13:253–258
14. Valentine SL, Sapru A, Higgerson RA et al (2012) Fluid balance in critically ill children with acute lung injury. Crit Care Med 40:2883–2889
15. Sinitsky L, Walls D, Nadel S, Inwald DP (2015) Fluid overload at 48 hours is associated with respiratory morbidity but not mortality in a general PICU: retrospective cohort study. Pediatr CritCare Med 16:205–209
Слайд 39Перегрузка жидкостью и легкие
Меньшая продолжительность ИВЛ [6,3 ± 5,8 vs.9.9
± 5.2 дней; р = 0,012].
Слайд 40Ограничительная стратегия ИТ предпочтительна в фазе послереанимационной стабилизации у детей
с септическим шоком.
Уменьшается длительность пребывания в ОРИТ, улучшается функция
легких.Уменьшается время восстановления от шока [92,5 ± 68,8 vs.123 ± 87 часов; р = 0,05].
Смертность была схожа [18.5 vs.23.4%; р = 0,54].
Фуросемид является безопасным и эффективным в малых дозах путем непрерывной инфузии.
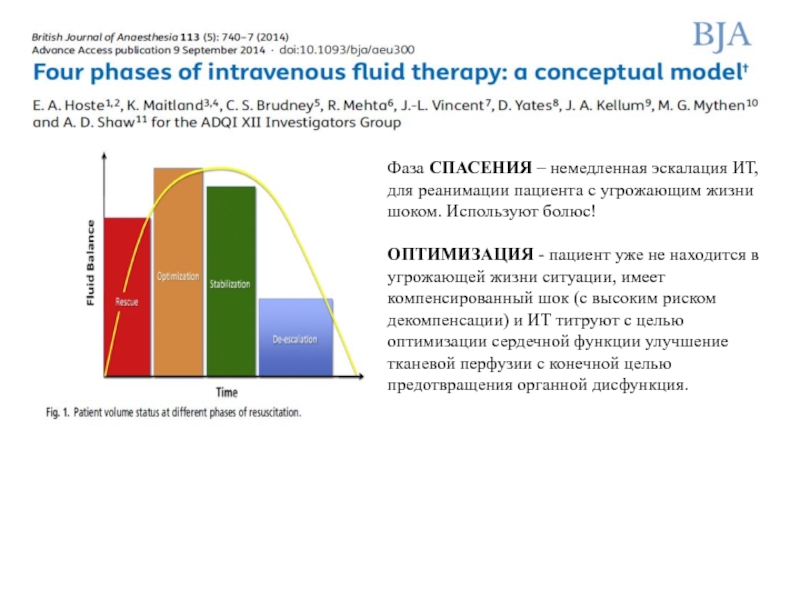
Слайд 41Фаза СПАСЕНИЯ – немедленная эскалация ИТ, для реанимации пациента с
угрожающим жизни шоком. Используют болюс!
ОПТИМИЗАЦИЯ - пациент уже не
находится в угрожающей жизни ситуации, имеет компенсированный шок (с высоким риском декомпенсации) и ИТ титруют с целью оптимизации сердечной функции улучшение тканевой перфузии с конечной целью предотвращения органной дисфункция.Слайд 42СТАБИЛИЗАЦИЯ отражает точку, в которой пациент находится в стабильном состоянии
и ИТ используется только для поддержания имеющихся потерь жидкости (через
почки, ЖКТ и др.), а также восстановление патологических потерь (в том числе регидратации). Этот этап отличается по сравнению с двумя предыдущими отсутствием шока (компенсированного или некомпенсированного) или непосредственной угрозой шока. ДЕЭСКАЛАЦИЯ - характеризуется продолжающимся восстановлением. Пациента отлучают от вентилятора и вазоактивной поддержки и удаляют накопленную жидкость. Терапия направлена на достижение отрицательного баланса жидкости. Идеальные механизмы избавления от накопленной жидкость (диуретики, ультрафильтрация) и оптимальная скорость, при которой жидкость может быть безопасно удалена, изучаются.Слайд 4350 гемодинамически стабильных взрослых пациентов с гипоальбуминемией (альбумин < 30
g/l, или общий белок < 60 g/l;), получали 100 мл
25% альбумина или физиологического раствора дважды в день, в общей сложности шесть доз (72 часа). Фуросемид давали два раза в день, в течение 2 часов после лечения.Исследование продемонстрировало, что сочетание 25% альбумина и диуретиков привело к снижению продолжительности ИВЛ, длительности пребывания в ОИТ и смертности.
Добавление 25% альбумина и диуретиков является перспективным вариантом удаления избытка жидкости у пациентов ОРИТ.
Слайд 45В пилотном проспективном рандомизированном контролируемом исследовании 64 недоношенных и доношенных
новорожденных с транзиторным тахипноэ были рандомизированы на стандартную инфузионную терапию
и умеренное ограничение жидкости. Первичной конечной точкой была продолжительность респираторной поддержки. Вторичные исходы: продолжительность пребывания в ОРИТ, время до первого энтерального питания, и расходы на лечение.Слайд 46Ежедневное увеличение объема вводимой жидкости (внутривенно + per os) составляло
20 мл/кг/день до достижения объема вводимой жидкости до 150 мл/кг/сутки
или перехода на полное энтеральное питаниеСлайд 47 Ограничение жидкости не вызвало побочных эффектов или опасного обезвоживания. Ограничение
жидкости значительно сократило продолжительность респираторной поддержки (P = 0,008) и
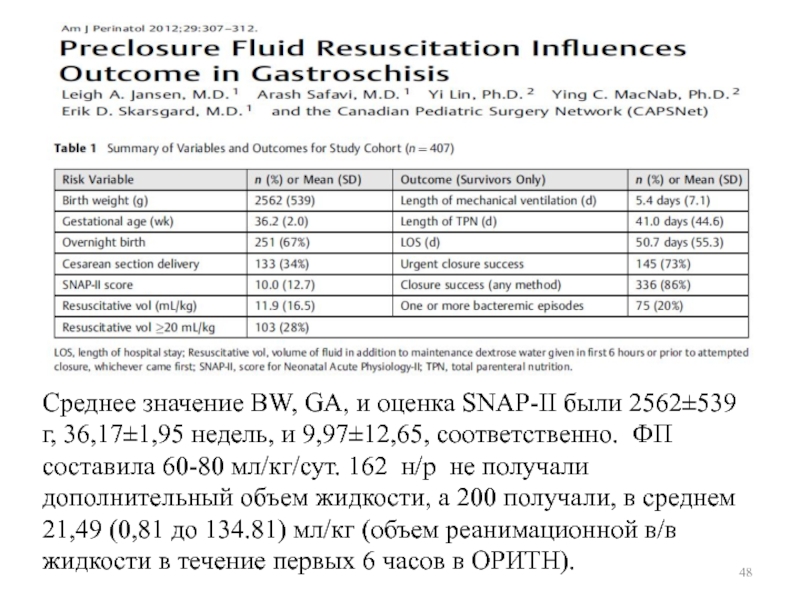
госпитальные расходы (P = 0,017) у новорожденных с тяжелым транзиторным тахипноэ.Слайд 48Среднее значение BW, GA, и оценка SNAP-II были 2562±539 г,
36,17±1,95 недель, и 9,97±12,65, соответственно. ФП составила 60-80 мл/кг/сут. 162
н/р не получали дополнительный объем жидкости, а 200 получали, в среднем 21,49 (0,81 до 134.81) мл/кг (объем реанимационной в/в жидкости в течение первых 6 часов в ОРИТН).Слайд 50Быстрая волемическая реанимация необходима для гипотензивных н/р (и часто инотропная
поддержка).
Большинство новорожденных с GS являются нормотензивными, и, как все
младенцы, имеют облигатный диурез, который инициируется предсердным натрийуретическим пептидом.
Незрелость тубулярной функции, особенно у недоношенных детей
приводит к уменьшению способности к экскреции натрия (задержка воды!).
Увеличение длительности ИВЛ (задержка воды в легких!).Длительность ТПП, пребывания в стационаре и количество бактериальных эпизодов можно объяснить кишечным отеком, который задерживает восстановление перистальтики и поглотительной функции в результате чего возрастает необходимость в ТПП и удлиняется пребывание в стационаре.
Повышенный риск из бактериемии может быть непосредственно связан с большей продолжительностью ТПП.
Слайд 54Клиницисты имеют тенденцию вводить дополнительный объем в следующих клинических ситуациях:
гипотония,
метаболический ацидоз
и плохая периферическая перфузия.
Слайд 55Я продолжаю поддерживающую ИТ с той же скоростью, что и
в предоперационном периоде.
Я использую растворы декстрозы с добавками натрия
и калия, вплоть до достижения фазы, в которой н/р находится в кардиореспираторной адаптации.Я оцениваю неощутимые потери с кожи, внутренних органов, дыхательных путей и учитываю диурез. Возмещаю эти потери сбалансированным солевым раствором Гартмана (нет никаких доказательств преимуществ ацетата на основе сбалансированных растворов солей у новорожденных) .
Я не компенсирую потери на «третье» пространство.
Прежде чем я начну переливать препараты крови я буду переливать 2 мл раствора Гартмана на каждые 1 мл кровопотери.
Я использую комбинацию классических параметров (АД, ЧСС, увеличение времени наполнения капилляров, градиент центральной и периферической температуры, дефицит оснований) и показатели чрезпищеводного Доплера (у новорожденных выше 2,5 кг), чтобы корригировать инфузионную терапию.
Я использую реакцию индекса ударного объема (ISV) на переливание 10 мл/кг раствора Гартмана.
Слайд 56ФИО: ЗАН
Дата рождения: 26.11.2002
Диагноз при поступлении: Посттравматический миозит области левого
плечевого сустава.
15.12.15 доставлена бригадой скорой медицинской помощи с Дs: Ушиб
и повреждение связок левого плечевого сустава от 14.12.15, для обследования и лечения.Из анамнеза: Со слов матери, около 2 недель назад (примерно 7.12.15) у девочки был фурункул в области правого локтевого сустава. Ко врачу не обращались, лечились самостоятельно на дому : местно — мазь с Аб , мазь Вишневского. На фоне проводимой терапии фурункул вскрылся. Системных антибиотиков ребенок не получал. 14.12.15 была получена травма на тренировке - упала из положения опоры на левую руку на область левого плечевого сустава. После этого появились боли в области в/3 левого плеча , в том числе ночные боли. Отмечалось увеличение температуры до 37.5 С. Конечность в объеме не увеличивалась. 15.12.15 была вызвана бригада СМП, девочка доставлена на 2 х.о СпбГПМУ.
Слайд 57При поступлении:
15.12.15 выполнена Rg-грамма левого плечевого сустава в 3-х проекциях
: костно-травматической патологии не выявлено.
17.12.15 выполненно МРТ левого плечевого сустава:
определяется отек параартикулярных мягких тканей и слой жидкости вдоль проксимального отдела левой плечевой кости.17.12.15 девочка была осмотрена хирургом : местно — отек в в/3 левого плеча незначительный. Кожа неизме нена, инфильтрация не определяется. Пальпация болезненная на всем протяжении кости, больше в в/3, болезненно покалачивание и движения в плечевом суставе. Установлен Дs : Острый гематогенный остеомиелит левой плечевой кости. Поставлены показания для оперативного лечения, девочка переведена на 3 х.о для выполнения хирургического вмешательства.
Клинический анализ крови:
Слайд 5817.12.15 под общим внутривенным наркозом проведена операция: Остеоперфорация в метаэпифизарной
зоне левой плечевой кости. Взят посев. Наложена асептическая повязка. Выполнена
фиксация съемным бейджем. Для дальнейшего лечения девочка была переведена на пост 3 хирургической реанимации.При поступлении в ПИТ 3 хир. реанимации 17.12.15: состояние ребенка было тяжелое, стабильное. Выход из наркоза без особенностей. Не лихорадила ( 36.7 С) . Предъявляла жалобы на боли в левой руке. Обезболивалась фентанилом. Неврологический статус без особенностей.
Гемодинамика стабильная: ЧСС 120 в мин, АД 105/55 ммHg. Тоны сердца звучные, ритмичные.
Дыхание везикулярное, самостоятельное, проводилось равномерно, хрипы не выслушивались. На этом фоне ЧД 20 в мин. ,SpO2 91-92% , FiO2= 0.21. С поддержкой увл. О2 через лицевую маску V= 2 л/мин SpO2 97-98%.
За время нахождения в АиР с 17.12.15-21.12.15 были проведены консультации:
Пульмонолог 18.12.15 - 2х сторонняя очаговая пневмония, ДН 2 ст. , терапия согласована; 21.12.15 ( в динамике ) : Правосторонняя пневмония н/ долевая и в/ долевая , тяжелое течение. Синпневмонический плеврит. ДН 2 ст. , проведена смена Аб-терапии.
- Консультация зав. отд. диализа : Проведено УФО крови (с 21.12.15-29.12.15)
- Окулист от 22.12.15: без патологии.
- 23.12.15 ребенок осмотрен и консультирован профессором Александровичем Ю.С. Тактика ведения согласована.
Слайд 60-Аб терапия : цефтриаксон ( с 17.12.15-18.12.15) → инванз (
с 18.12.15) ; амикацин ( с 17.12.15-20.12.15)→ ванкомицин ( с
21.12.15) ;-Н2 - блокаторы : квамател
-Обезболивание : Фентанил , кетонал
-Жаропонижающая терапия и дополнительное обезболивание : Ифимол 1%
-Иммуноглобулины : Иммуновенин (19.12.15)→ Пентаглобин ( с 21.12.15 , 23.12.15 )
-Частичное парентеральное питание: Аминоплазмаль 10%
-Энтеральное питание : вода, стол «индивидуальный»
-Инфузионная терапия: V=ФП в режиме нормогидратации ( с 17.12.15-20.12.15)→ V= 1.5 ФП в режиме гипергидратации с контролем диуреза и ЦВД
Слайд 62 Стратегия инфузионной терапии для пациентов ОРИТ должна быть индивидуализирована
и основана на клиническом статусе.
Длительность введения, тип и количество
жидкости у критически больных пациентов оказывают влияние на исходы лечения.Ранняя адекватная жидкостная реанимации с последующим ограничительным режимом введения жидкости обеспечивают лучшие результаты для критически больных пациентов.
Нет четких доказательств для использования альбумина в качестве инфузионной терапии в ОРИТ. Это подтверждается отсутствием выгоды (в отличие от отсутствия доказательств пользы), а также неблагоприятным фармако-экономическим балансом.
Использование коллоидов для реанимации больных с шоком обеспечивает более раннее его купирование и, возможно, улучшает результаты.
Современные ГЭК можно безопасно использовать во время операции, но следует избегать в ОРИТ, в частности, у пациентов, которые имеют высокий риск развития ОПП.
Слайд 64КЛАССИФИКАЦИЯ ИНФУЗИОННЫХ РАСТВОРОВ ПО МЕХАНИЗМУ ТЕРАПЕВТИЧЕСКОГО ДЕЙСТВИЯ*
*предложена А.А. Багдасаровым, П.С.
Васильевым, Д.М. Гроздовым и дополненная O.K. Гавриловым (1973)
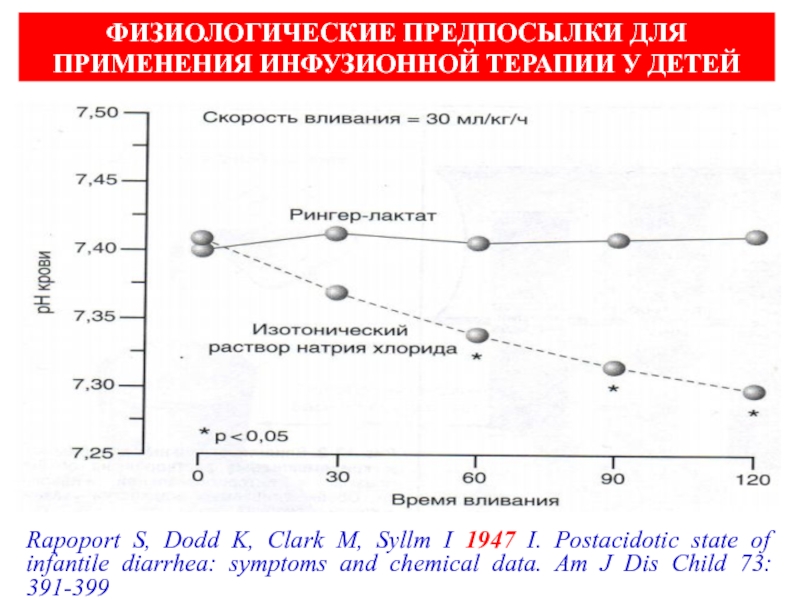
Слайд 66ФИЗИОЛОГИЧЕСКИЕ ПРЕДПОСЫЛКИ ДЛЯ ПРИМЕНЕНИЯ ИНФУЗИОННОЙ ТЕРАПИИ У ДЕТЕЙ
Rapoport S,
Dodd K, Clark M, Syllm I 1947 I. Postacidotic state
of infantile diarrhea: symptoms and chemical data. Am J Dis Child 73: 391-399Слайд 67СБАЛАНСИРОВАННЫЙ ЭЛЕКТРОЛИТНЫЙ РАСТВОР
должен иметь физиологическую ионную структуру, аналогичную плазме
в переводе на натрий, калий, кальций, магний, хлорид, быть изотоничным
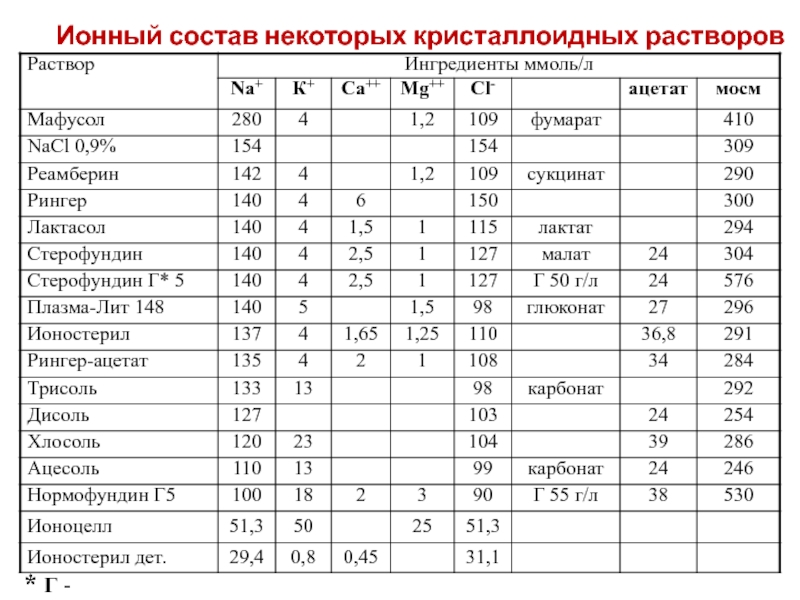
по отношению к плазме и достигать физиологического кислотно-основного баланса с бикарбонатными или метаболизирующимися анионами. Инфузия такого сбалансированного раствора избавляет от риска ятрогенных нарушений, за исключением возможности возникновения перегрузки системы кровообращения объемом вводимой жидкости.Слайд 69Стерофундин
Натрий - 145,0ммоль/л, Калий - 4,0 ммоль/л,
Магний - 1,0
ммоль/л,
Кальций - 2,5 ммоль/л,
Хлориды - 127,0 ммоль/л,
Ацетаты
- 24,0 ммоль/л, Малаты - 5,0 ммоль/л.
Теоретическая осмолярность - 309 мОсм/л,
рН - 5,1-5,9.
Натрий - 140,0 ммоль/л,
Калий - 4,0 ммоль/л,
Кальций - 2,5 ммоль/л,
Магний - 1,0 ммоль/л.
теоретическая осмолярность - 576 мОсм/л,
pH - 3,0-5,0.


























![ИНФУЗИОННАЯ ТЕРАПИЯ У ДЕТЕЙ. ВАЖЕН ЛИ ТОЧНЫЙ РАСЧЕТ? Перегрузка жидкостью и легкиеМеньшая продолжительность ИВЛ [6,3 ± 5,8 vs.9.9 ± Перегрузка жидкостью и легкиеМеньшая продолжительность ИВЛ [6,3 ± 5,8 vs.9.9 ± 5.2 дней; р = 0,012].](/img/tmb/3/258947/075cf159b3fbd68349187b12ae85b8c5-800x.jpg)