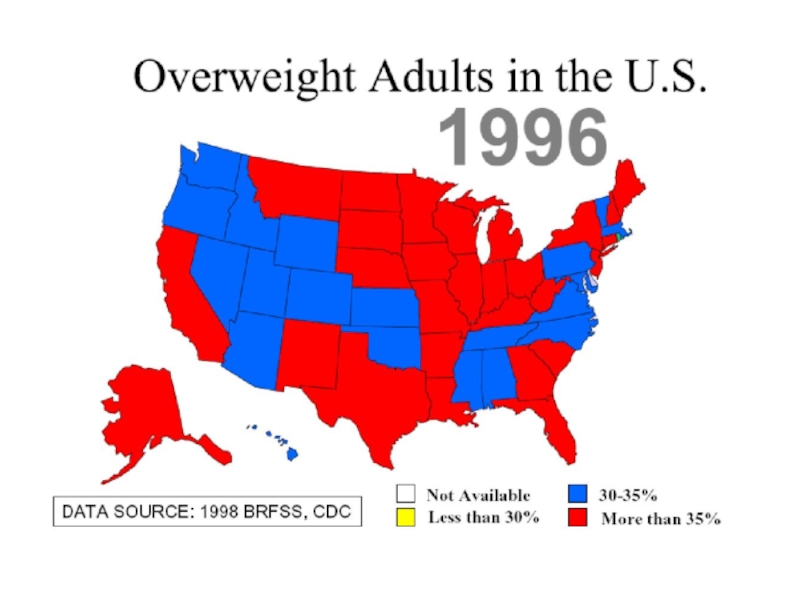
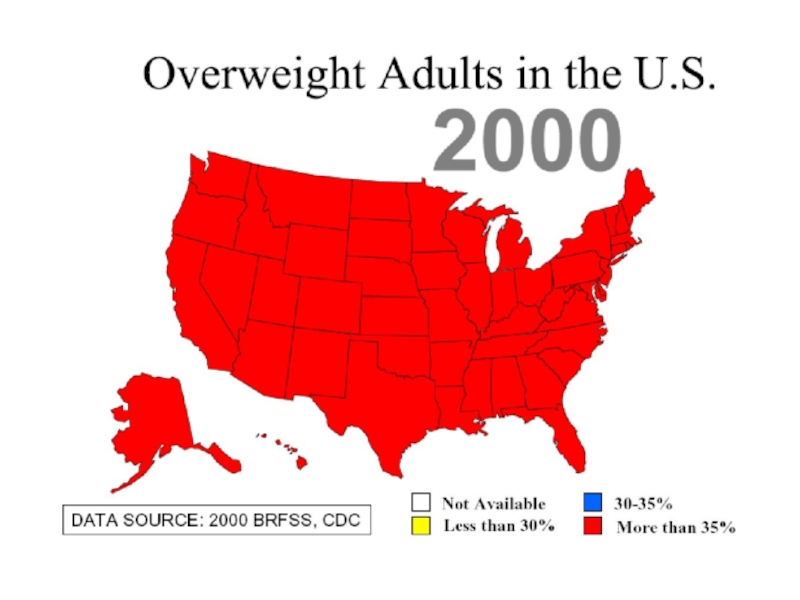
Слайд 1Инсулин, глюкагон, лептин, метаболический синдром
Лекция 15
Слайд 2Введение
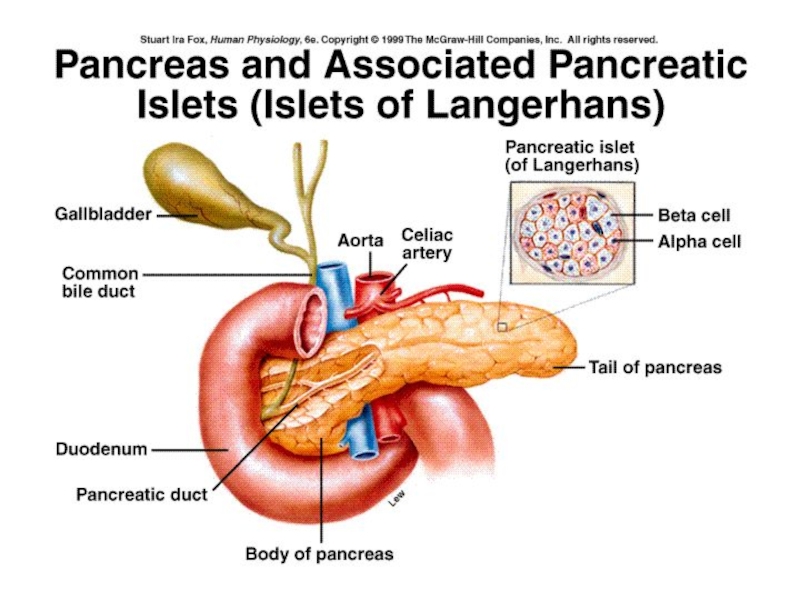
Инсулин - секретируется в кровь b-клетками островков Лангерганса поджелудочной железы.
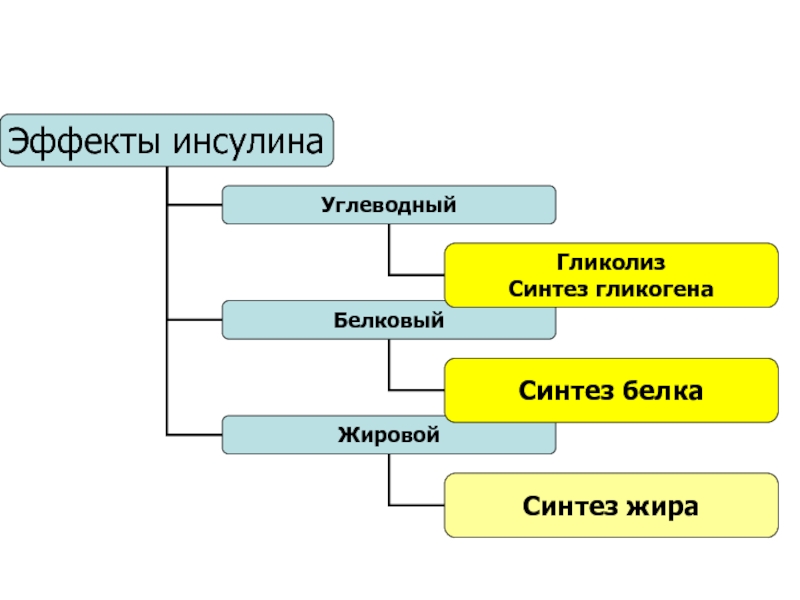
Главная функция инсулина - регуляция метаболизма белков, жиров, углеводов.
Это
анаболический гормон. Его эффекты на мышцы, печень и адипозную ткань: стимуляция захвата клетками глюкозы, аминокислот, жирных кислот; усиление синтеза гликогена, белков, триглицеридов; стимуляция гликолиза; а также торможение глюконеогенеза и распада гликогена, белков и триглицеридов.
Секреция инсулина минимальна при голодании, мышечной и нервной нагрузке, а также других формах стресса, когда возрастает потребность в использовании углеводов и жиров, и максимальна после приема пищи.
Слайд 3
Биосинтез инсулин млекопитающих кодируется одним геном (у некоторых видов -
двумя), определяющим образование одноцепочечного крупного белка - предшественника проинсулина (мол.
м. ок. 9000), из которого после ферментативного расщепления образуется гормон.
Слайд 4Осуществлен полный хим. синтез инсулин человека, разработаны способы трансформации инсулина
животных в инсулин человека, а также осуществлено получение инсулина человека
с применением методов генетической инженерии.
Активность инсулин определяют биол. методами по снижению содержания сахара в крови у кроликов или по судорожному эффекту.
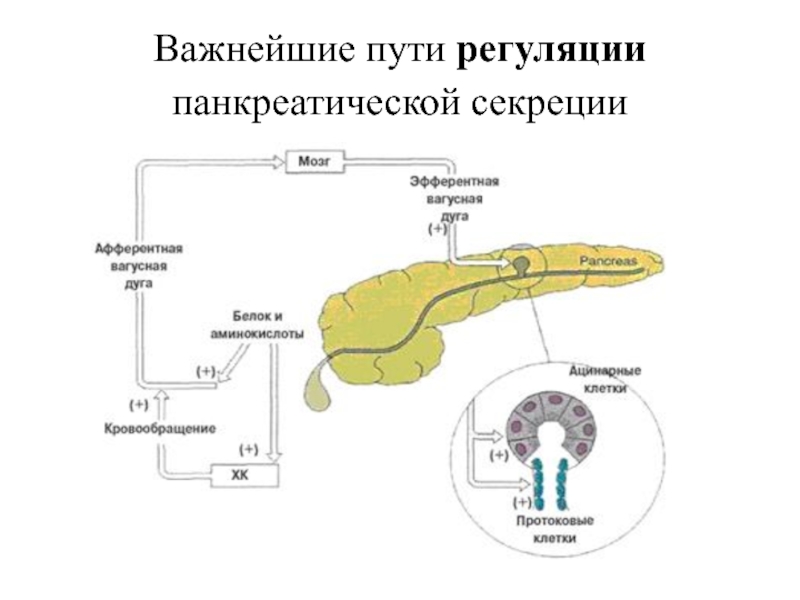
Слайд 7Важнейшие пути регуляции панкреатической секреции
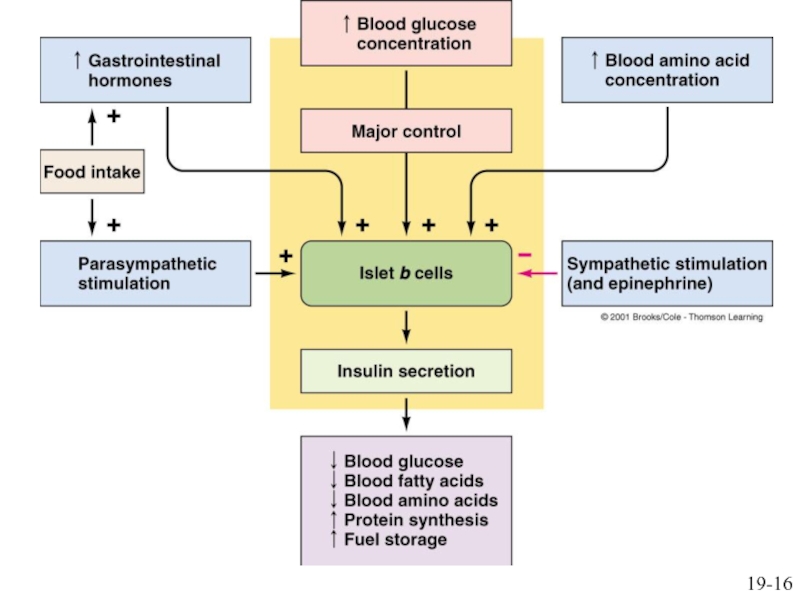
Слайд 8Секреция инсулина контролируется изменениями концентраций циркулирующих в крови нутриентов (глюкозы,
аминокислот, жирных кислот), гормонами желудочно-кишечного тракта, секретируемыми в нервно-гуморальную фазу
сокоотделения (например, гастрин, секретин) и различными нейромедиаторами (помимо классического ацетилхолина можно назвать такие пептидные медиаторы, как ВИП и холецистокинин). Перечисленные гормоны и медиаторы обуславливают так называемые энтероинсулярные стимулы секреции инсулина.
Но, главными стимулами служат "пищевые" стимулы. По мере того, как концентрация, например, глюкозы в крови увеличивается [обычно достигая уровня 6-9 ммоль/л (норма: 5 ммоль/л)], стимулируется секреция инсулина, и этот эффект усиливается гормонами желудочно-кишечного тракта
Слайд 9Эффекты нутриентов на секреторную активность b-клеток поджелудочной железы являются результатом
их прямого взаимодействия с клеточными мембранами железистых клеток. Глюкоза и
другие подвергающиеся метаболизму питательные вещества транспортируются в b-клетки островков Лангерганса, где в процессе их метаболизма образуется АТФ.
АТФ обеспечивает стимул для начала секреции инсулина изменением мембранного потенциала, в конечном итоге обеспечивающим поток ионов Са2+ в цитоплазму.
Слайд 10В состоянии покоя мембранный потенциал (МПП) на внутренней поверхности мембраны
b-клеток равен -50-70мВ.
В мембранах b-клеток существуют 2 типа калиевых
каналов (АТФ-чувствительные и Са-чувствительные), оба из которых участвуют в секреции инсулина.
Слайд 11Образовавшийся АТФ вызывает закрытие АТФ-чувствительных калиевых каналов.
Это предотвращает выход
К+ из клетки, что является результатом накопления в ней положительных
зарядов и, соответственно, деполяризации мембраны.
По достижении порога (снижение потенциала на 15 мВ) открываются потенциал-чувствительные Са каналы, обеспечивая поток ионов Са2+ в клетки.
Са-чувствительные калиевые каналы открываются по мере того, как Са2+ поступает в клетку, благодаря чему К+ выходит из нее, восстанавливая ПП.
Слайд 12Ионы Са2+ обеспечивают секрецию инсулина из секреторных гранул несколькими путями:
1) Положительно заряженные ионы Са2+ облегчают экзоцитоз инсулина.
2) Са2+
облегчает передвижение гранул внутри клеток, т. к. влияет на функцию сократительных белков, содержащих актин и тубулин.
3) Са2+ связывается с кальмодулином; это активирует фермент аденилатциклазу, катализирующую превращение АТФ в цАМФ. Циклический АМФ потенциирует секрецию инсулина путем увеличения чувствительности b-клеток к стимулирующему действию кальция.
4) Чувствительность b-клеток к Са2+ увеличивается и другими вторичными мессенджерами (инозитолтрифосфатом и диацилглицеролом)
Слайд 13Ингибиторами секреции инсулина является вещества, активирующиеся симпатической системой: соматостатин, гормоны
гипофиза (АКТГ, ГР, ТТГ, пролактин, вазопрессин), кортизол, тироксин, простагландины, адреналин,
норадреналин, серотонин.
Слайд 14Действие инсулина на клетки
Инсулин активирует транспортеры глюкозы, которые переносят глюкозу
в клетку.
Инсулин отвечает за синтез фермента гексокиназы, который фосфорилирует
глюкозу, как только она проникает в клетку.
Слайд 15Путь трансмембранного проведения гормонального сигнала - тирозинкиназный.
Инициация действия инсулина
обуславливается взаимодействием гормон-рецептор.
Рецепторы инсулина относятся к семейству гетеротетрамерных рецепторов
тирозинкиназы.
Слайд 16В связи с анаболической функцией инсулина стимуляция симпатической нервной системы
угнетает секрецию инсулина, а парасимпатической усиливает секрецию инсулина. С этим
связаны и циркадные ритмы секреции инсулина.
Как известно симпатическая система больше активна в дневное время, а парасимпатическая – в ночное.
Следовало бы ожидать снижение секреции инсулина в дневное время и стимуляции в ночное. Это верно, если вести речь о базальной секреции, которая призвана обеспечивать метаболизм клеток.
Помимо нее осуществляется более обильная прандиальная секреция. Прием пищи в современном обществе часто не согласуется ни с потребностями метаболизма, ни даже наличием чувства голода и аппетита,что нарушает согласованность функционирования отделов вегетативной системы.
Слайд 17Роль инсулина в регуляции обмена веществ выходит за рамки регуляции
уровня глюкозы в крови.
В мышечных клетках инсулин активизирует синтез гликогена.
В
жировой ткани инсулин с одной стороны стимулирует образование жиров - в норме 30-40% поглощенной глюкозы превращается в жир. С другой стороны, инсулин является мощным блокатором распада жиров. Жировая ткань - одна из самых инсулин-чувствительных тканей.
В мышцах инсулин способствует переходу аминокислот в клетки.
Белки - инсулин стимулирует их синтез и препятствует распаду.
Инсулин активизирует синтез АТФ, ДНК и РНК и, таким образом, стимулирует размножение клеток.
В целом, действие инсулина направлено на запасание организмом энергии и структурных материалов.
Слайд 18
Синтез инсулиновых рецепторов находится под контролем гена INSR. Существует множество
мутаций этого гена.
Кроме того, транспорт глюкозы зависит от состояния
клеточной мембраны, дефекты в которой тоже генетически запрограммированы.
Слайд 19Поэтому в человеческой популяции существует большая доля лиц с врожденной
резистентностью мышечной и жировой тканей к действию инсулина.
Если человек
будет вести активный образ жизни, правильно питаться - состояние выраженной инсулинорезистентности либо вообще не проявится при жизни, либо оно проявится в глубокой старости и выступит в качестве одного из механизмов умирания.
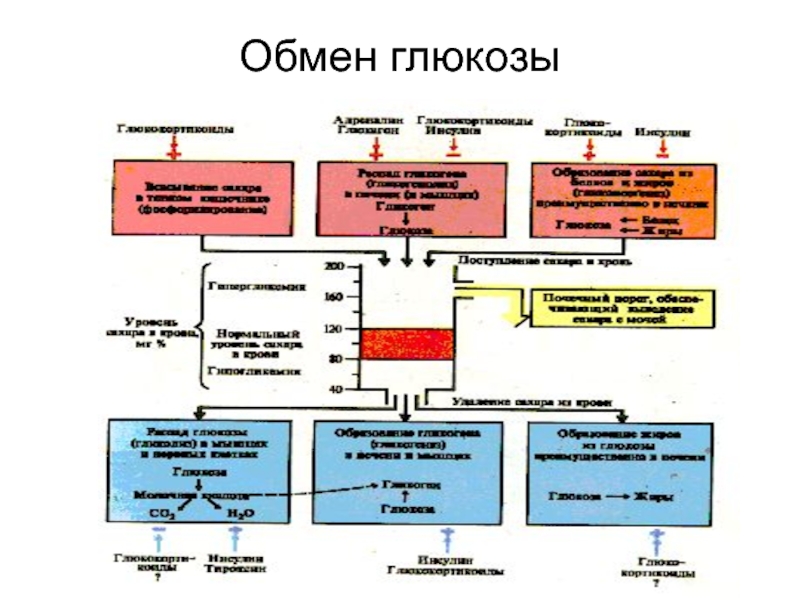
Слайд 20Регуляция уровня глюкозы в крови
Запасание
Инсулин
Соматотропин
Расход запасов
Глюкагон
Адреналин
Кортизол
Тироксин
Соматотропин
( длительная
секреция)
Слайд 21Гипоталамус способен стимулировать выделение инсулина из b-клеток панкреатических островков по
нервнопроводниковому пути, который назван «паравентрикуло-вагусным»..
Этот путь начинается от нервных
клеток паравентрикулярного ядра (ПВЯ) гипоталамуса, переключается синаптически в продолговатом мозге на нейроны дорсального ядра вагуса и достигает в составе волокон вагуса панкреатичес-ких островков. По нему к b-клеткам поступают стимулирующие сигналы.
Тормозящие сигналы приходят от нейронов ПВЯ гуморальным путём: в нейронах ПВЯ секретируется рилизинг-гормон кортиколиберин (КЛ), который стимулирует в гипофизе секрецию АКТГ и через его посредство секрецию глюкокортикоидов в коре надпочечников. Глюкокортикоиды тормозят выделение инсулина.
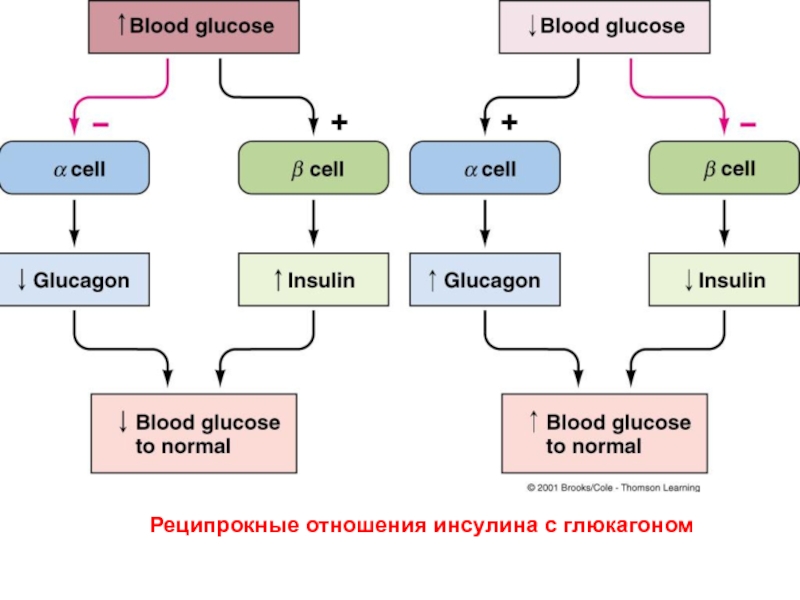
Слайд 22Глюкагон
Стимулирует распад гликогена в печени до глюкозы и повышает содержание
глюкозы в крови.
Глюкагон способствует мобилизации жира из жировых депо.
Слайд 24Реципрокные отношения инсулина с глюкагоном
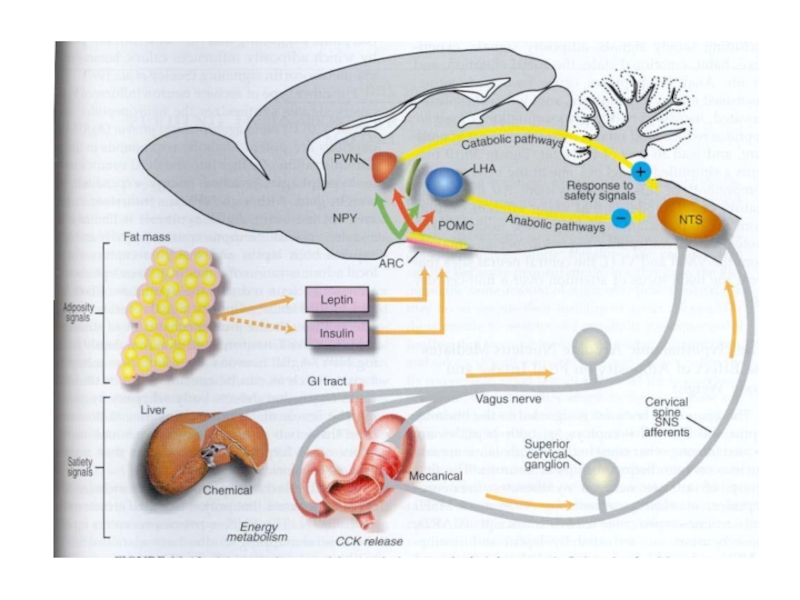
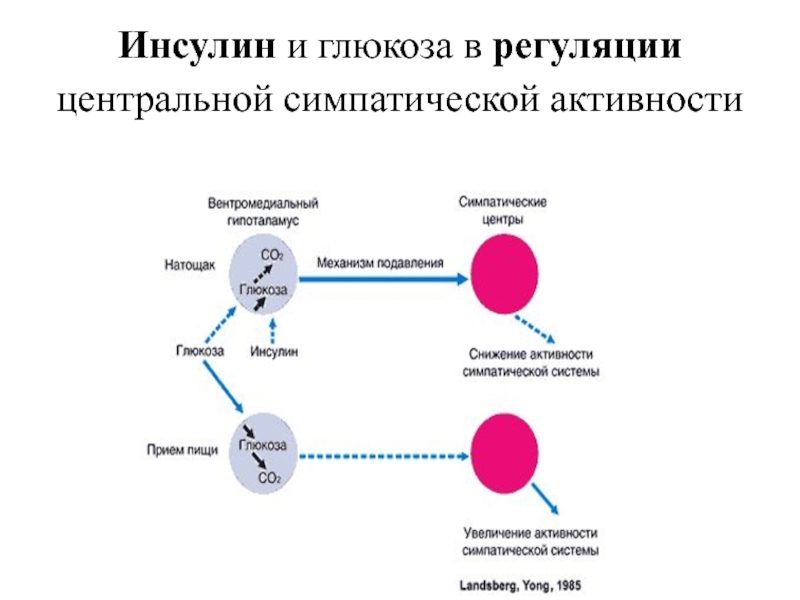
Слайд 26Инсулин и глюкоза в регуляции центральной симпатической активности
Слайд 28Лептин и его роль в регуляции метаболизма и физиологических функций
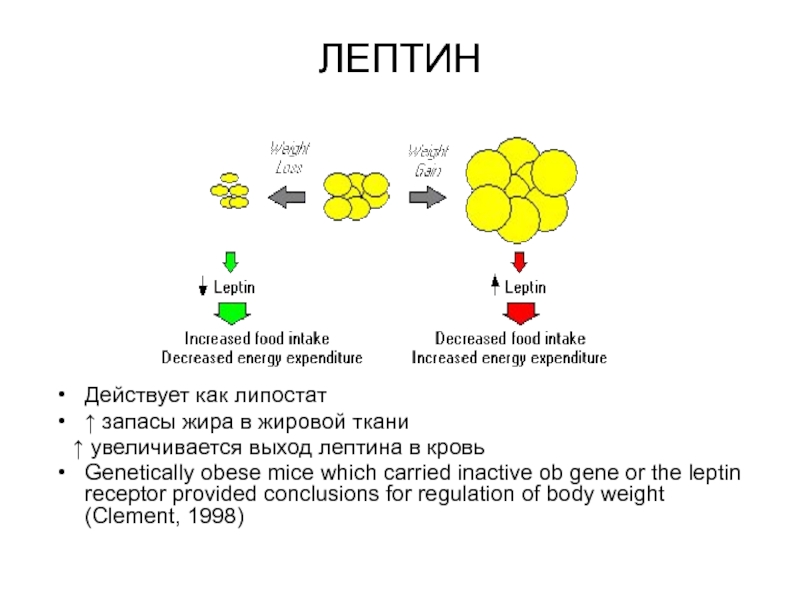
Слайд 29ЛЕПТИН
Действует как липостат
↑ запасы жира в жировой ткани
↑
увеличивается выход лептина в кровь
Genetically obese mice which carried inactive
ob gene or the leptin receptor provided conclusions for regulation of body weight (Clement, 1998)
Слайд 30Лептин - гормон, секретируемый жировыми клетками, циркулирующий в крови в
свободной и связанной формах.
Содержание лептина в общей циркуляции крови
подчиняется суточному ритму с ночным подъемом, а его секреция носит импульсный характер.
Синтез этого гормона контролируется ob-геном, геном ожирения.
Слайд 31Лептин частично связывается белками плазмы. Связанная фракция лептина м. достигать
80% у человека при мутациях рецепторов лептина, циркулирующих в крови
в больших количествах. Другой пул лептина связывается с тканью и участвует в поддержании постоянного уровня лептина в плазме.
Лептин оказывает влияние на энергетический баланс в основном действуя на головной мозг.
Внутривенные инъекции лептина активируют нейроны в arcuate вентромедиальных и дорсомедиальных гипоталамических ядрах, участвующих в регуляции поведения приема пищи и баланса энергии
Слайд 32Концентрация лептина тесно коррелирует с индексом массы тела (ИМТ).
Лептин
регулирует чувство насыщения на уровне дугообразного ядра гипоталамуса, тесно связанного
с паравентрикулярным ядром, стимуляция которого приводит к активации симпатической нервной системы.
Слайд 33На уровень лептина влияет уменьшение количества жировой ткани (снижение веса
тела на 10% приводит к 53%-му снижению концентрации лептина, но
гораздо большее влияние оказывает голодание, которое резко снижает цифры до критических.
Напротив, 10%-ый набор веса на 300% (!) увеличивает уровень сывороточного лептина. Всего один день капитального переедания на 40% поднимает уровень лептина.
Слайд 34Уровень лептина регулируется и другими факторами.
Пик уровня глюкокортикоида совпадает
с самым низким уровнем лептина в начале светового цикла у
человека, и самый низкий уровень глюкокортикоида связан с пиком уровня лептина ночью.
Слайд 35И именно падение уровня сывороточного лептина в результате болезни или
радикальных диет запускает компенсаторный механизм, снижающий термогенез и увеличивающий потребление
пищи до тех пор, пока не будет достигнут уровень лептина, являющийся нормой для данного индивидуума.
В результате, к выздоравливающим и, увы, желающим похудеть, возвращаются былые формы.
Слайд 36Основные действия лептина
- повышение печеночного глюкогенолиза и захвата глюкозы скелетными
мышцами;
- повышение скорости липолиза и уменьшение содержания триглицеридов в белой
жировой ткани;
- усиление термогенеза;
- стимуляция ЦНС;
- снижение содержания триглицеридов в печени, скелетных мышцах и поджелудочной железе без повышения НЭЖК в плазме.
Слайд 37Действие лептина на липидный обмен
осуществляется через стимуляцию экспрессии гена ПОМКосуществляется
через стимуляцию экспрессии гена ПОМК в меланокортинэргических нейронах гипоталамуса .
Из ПОМК образуется альфа-МСГИз ПОМК образуется альфа-МСГ , который после связывания с меланокортиновым рецептором MC-4RИз ПОМК образуется альфа-МСГ , который после связывания с меланокортиновым рецептором MC-4R в мозгу вызывает снижение аппетитаИз ПОМК образуется альфа-МСГ , который после связывания с меланокортиновым рецептором MC-4R в мозгу вызывает снижение аппетита и активирует липидный обмен . Пациенты с мутациями в гене MC-4R страдали только ожирением, но их рост и половое развитие проходили нормально
Слайд 38Первые сообщения о том, что меланокортины вовлечены в регуляцию пищевого
поведенияПервые сообщения о том, что меланокортины вовлечены в регуляцию пищевого
поведения появились в середине 70-х годов, когда стало известно, что центральное введение a-МСГПервые сообщения о том, что меланокортины вовлечены в регуляцию пищевого поведения появились в середине 70-х годов, когда стало известно, что центральное введение a-МСГ уменьшает количество потребляемой пищи.
Слайд 39
Таким образом.
Потребление пищи зависят от двух типов эффекторных систем в
ЦНС и гипоталамусе.
Первая - анаболическая - запускается низким уровнем
лептина
Вторая система - катаболическая -представлена меланокортином, кортикотропин-рилизинг фактором.
Слайд 40В организме существует как долговремен-ная, так и кратковременная система контроля
пищевого поведения и расхода энергии. Концентрация в плазме глюкозы и
аминокислот, холецистокинин (cholecystokinin, CCK) и масса других веществ гормональной и иной природы являются компонентами системы «быстрого реагирования».
Концентрация же лептина после еды возрастает незначительно. И сам по себе лептин не прекращает трапезу, его влияние на пищевое поведение проявляется в рамках «долгоиграющей» системы
Слайд 41Содержание лептина в крови может служить сигналом, указывающим на готовность
организма к выполнению репродуктивной функции и на наличие в нем
достаточных запасов питательных веществ, необходимых для ее нормального протекания.
Быстрое падение содержания лептина в крови голодающих животных, например, может вызывать такие изменения нейроэндокринных процессов, которые полностью блокируют функционирование репродуктивной системы.
Слайд 42Обратная корреляция между пульсирующей секрецией лептина и кортизола и адренокортикотропина
(АСТН) известна у человека.
Препубертальное увеличение экспрессии лептина предшествует увеличению
тестостерона и эстрадиола и, по-видимому, связано с созреванием гонадной оси.
Синтез лептина ингибируется тестостероном, но не овариальными половыми стероидами
Слайд 43Вывод: нормальное функционирование рецептора лептина необходимо не только для регуляции
веса тела, но также для регуляции полового созревания и поддержания
нормальной секреции ростового: нормальное функционирование рецептора лептина необходимо не только для регуляции веса тела, но также для регуляции полового созревания и поддержания нормальной секреции ростового и тиреотропного гормонов. Полученные данные показали, что эффективное функционирование системы проведения гормонального сигнала с участием активного рецептора лептина необходимо для нормального полового развития и созревания женщин.
Слайд 44По современным представлениям лептин подает сигнал в гипоталамус через активацию
специфического лептинового рецептора, что проявляется уменьшением потребления пищи и увеличением
расхода энергии. При этом через специфические рецепторы в гипоталамусе он подавляет синтез нейропептида Y (NPY), продуцируемого нейронами дугообразного ядра, что приводит к снижению аппетита, повышению тонуса симпатической нервной системы и расходу энергии, а также изменению обмена веществ в периферических органах и тканях
Слайд 45лептиновый рецептор (Ob-R) был выделен из мышиного хороидного (сосудистого) сплетения
и был идентифицирован как представитель цитокинового семейства рецепторов
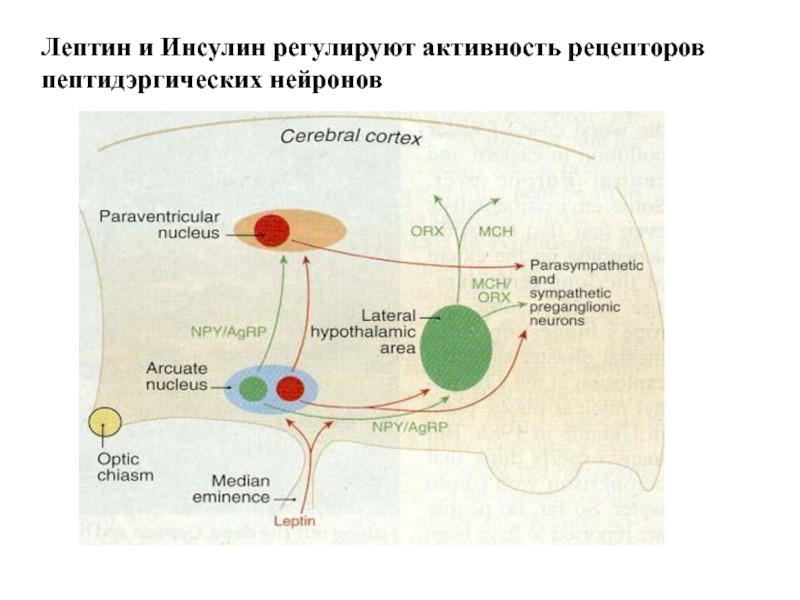
Слайд 46была подтверждена экспрессия Ob-Rb в ядрах гипоталамуса: аркуатном (дугообразном), дорсомедиальном,
паравентрикулярном, вентромедиальном, а также латеральном.
Эти зоны являются местом главной
экспрессии лептинового рецептора в ЦНС, и именно они играют важную роль в регуляции веса тела. Латеральное ядро называют еще «центром голода», а вентромедиальное — «центром насыщения». Причем «центр голода» большую часть времени тормозит «центр насыщения». Электрическая стимуляция или разрушение этих центров приводит к противоположному влиянию на пищевое поведение. Разрушение латерального ядра приводит к потере аппетита, в то время как разрушение вентромедиального ядра вызывает ярость и чрезмерный аппетит
Слайд 47Таблица 3. Гипоталамические регуляторы пищевого поведения [1]
Слайд 49Лептин и Инсулин регулируют активность рецепторов пептидэргических нейронов
Слайд 50.
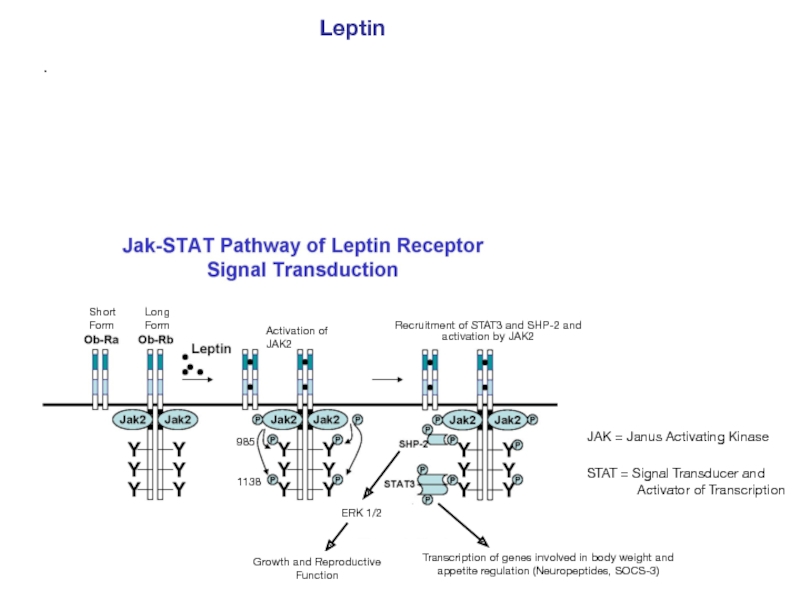
Leptin
JAK = Janus Activating Kinase
STAT = Signal Transducer and
Activator of Transcription
Short
Form
Long
Form
985
1138
Activation of JAK2
Recruitment of
STAT3 and SHP-2 and
activation by JAK2
ERK 1/2
Growth and Reproductive
Function
Transcription of genes involved in body weight and appetite regulation (Neuropeptides, SOCS-3)
Слайд 51
Intracellular
Leptin
Nucleus
Extracellular
DNA
JAK
Kinase
JAK
Kinase
OB-R
Leptin
STAT
STAT
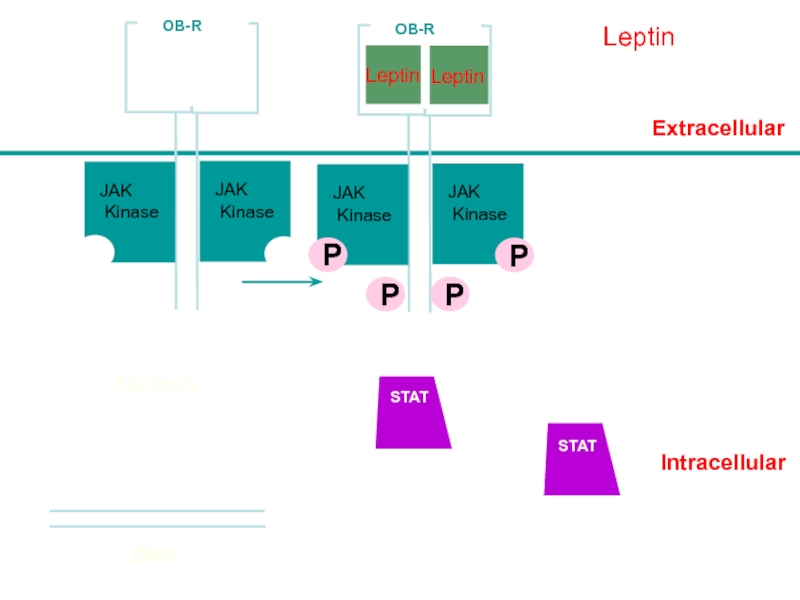
Слайд 52Intracellular
Leptin
Lepn
Extracellular
STAT
JAK
Kinase
JAK
Kinase
OB-R
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
Leptin
STAT
Nucleus
DNA
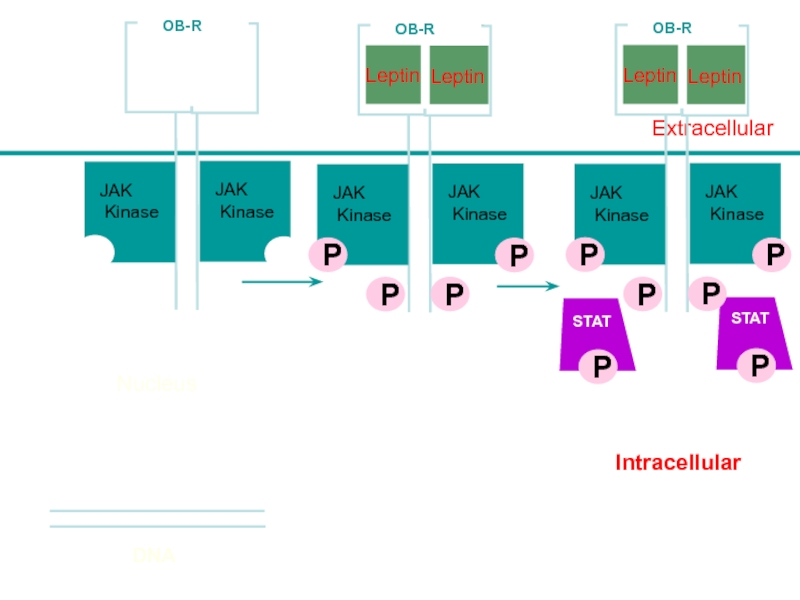
Слайд 53Intracellular
Leptin
Lepn
Extracellular
STAT
STAT
JAK
Kinase
JAK
Kinase
OB-R
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
Leptin
Lepn
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
P
P
Nucleus
DNA
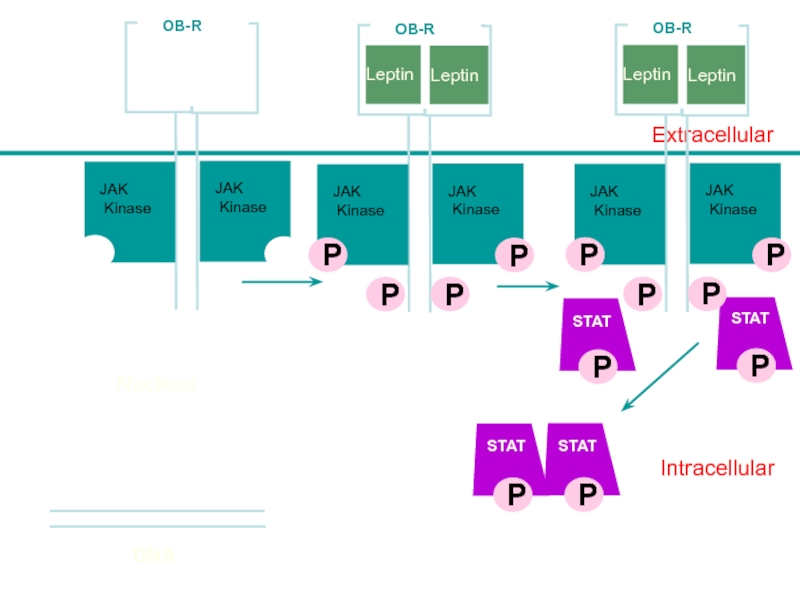
Слайд 54Intracellular
Leptin
Lepn
Extracellular
STAT
STAT
JAK
Kinase
JAK
Kinase
OB-R
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
Leptin
Lepn
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
P
P
STAT
P
STAT
P
Nucleus
DNA
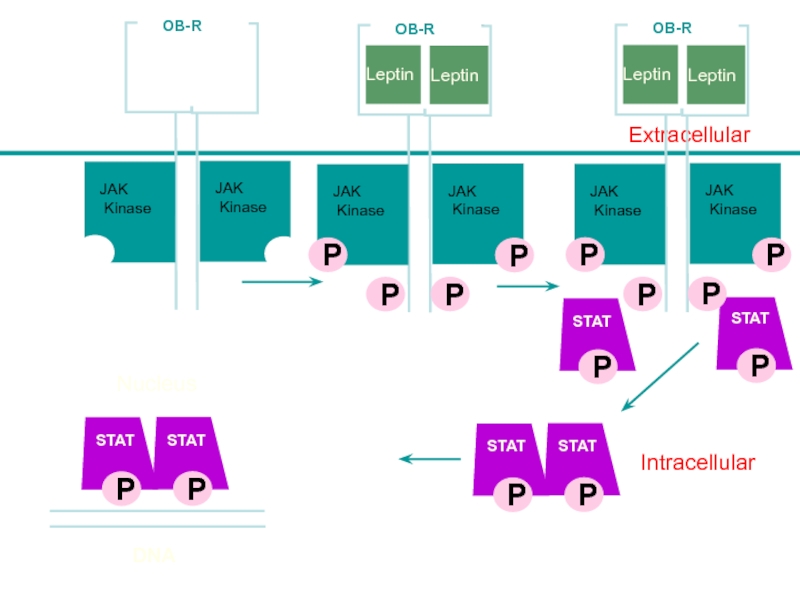
Слайд 55Intracellular
Leptin
Lepn
Extracellular
STAT
STAT
JAK
Kinase
JAK
Kinase
OB-R
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
Leptin
Lepn
JAK
Kinase
JAK
Kinase
OB-R
P
P
P
P
Leptin
Leptin
P
P
STAT
P
STAT
P
Nucleus
DNA
STAT
P
STAT
P
Слайд 56Еще одним ярким примером нейроиммуноэндокринных взаимодействий является развитие сахарного диабета.
Нередко у лиц среднего и пожилого возраста после перенесенного психоэмоционального
стресса (смерть близкого человека, конфликтные ситуации в быту или на службе и т.д.) наблюдаются нарушения углеводного гомеостаза.
Одним из ранних признаков бывает повышение сахара в крови.
Слайд 57Метаболический синдром (основные дефиниции)
Слайд 58История вопроса
В 1948 г. известный клиницист Е. М. Тареев писал:
«Представление о гипертонике наиболее часто ассоциируется с ожирелым гиперстеником, с
возможным нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза — холестерином, мочевой кислотой...» Таким образом, более 50 лет назад было практически сформировано представление о метаболическом синдроме (МС).
Слайд 59Метаболический синдром
(История вопроса)
В 1988 г. G.Reaven высказал предположение об участии
инсулинорезистентности и гиперинсулинемии в патогенезе артериальной гипертонии (АГ), СД типа
2 и ишемической болезни сердца (ИБС) и предложил термин – "синдром Х", или метаболический синдром, который включал гиперинсулинемию, нарушение толерантности к глюкозе, инсулинорезистентность, повышение холестерина (ХС) липопротеидов низкой плотности, низкий уровень ХС липопротеидов высокой плотности, АГ .
В 1989 г. N.M.Kaplan ввел термин "смертельный квартет", или синдром инсулинорезистентности, и объединил в его составе андроидное ожирение, нарушение толерантности к глюкозе, гиперинсулинемию, АГ.
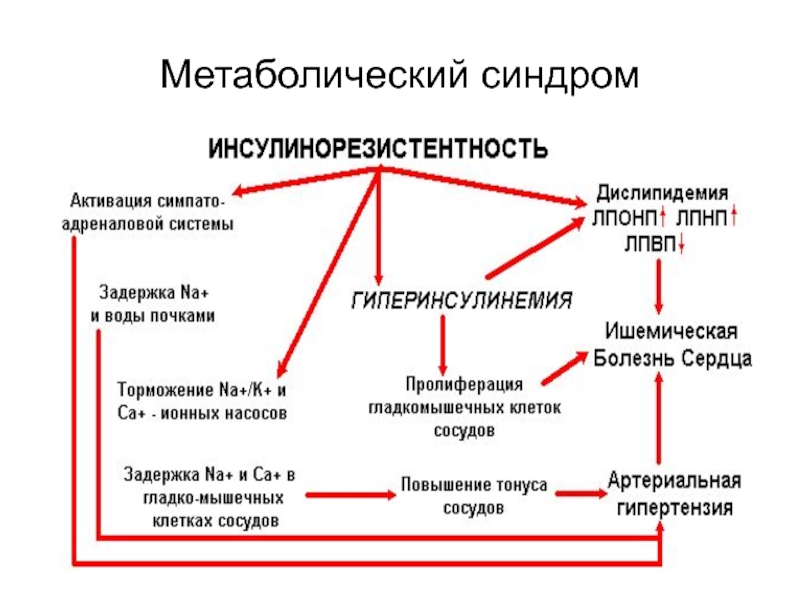
Слайд 60МЕТАБОЛИЧЕСКИЙ X СИНДРОМ
1. ИНСУЛИНОРЕЗИСТЕНТНОСТЬ
2. ГИПЕРИНСУЛИНЕМИЯ
3. СНИЖЕНИЕ ТОЛЕРАНТНОСТИ К
ГЛЮКОЗЕ
4. ДИСЛИПИДЕМИЯ
5. ОЖИРЕНИЕ
6. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
Слайд 62Основные причины развития метаболического синдрома
Метаболический синдром – причины:
Снижение физической
активности.
Высокоуглеводный характер питания.
Недостаток биологически активных веществ в пище
Влияние
неблагоприятных экологических факторов
Генетические факторы
Слайд 63Основными механизмами, приводящими к повышению АД при метаболическом синдроме, являются
гиперволемия, обусловленная повышенной реабсорбцией натрия в проксимальных канальцах почек и
вызывающая повышение сердечного выброса; активация симпатической нервной системы, также вызывающая рост сердечного выброса и приводящая к спазму периферических сосудов и повышению общего периферического сопротивления сосудов (ОПСС).
Слайд 64Патогенез МС (роль глюкозы)
Повышение уровня глюкозы в крови сопровождается неферментативным
образованием различных соединений глюкозы с белками.
Гликозилирование белков приводит приводит
к повреждению их структуры и функции.
Повреждение белков сосудистой стенки ведет к атеросклеротическим изменениям, белков кожи - к образованию морщин, белков мозга - развитию болезни Альцгеймера или другим неврологическим нарушениям.
Глюкоза - это молекула с большим энергетическим потенциалом, которая легко окисляется. Поэтому увеличение ее концентрации в крови сопровождается усилением образования свободных радикалов.
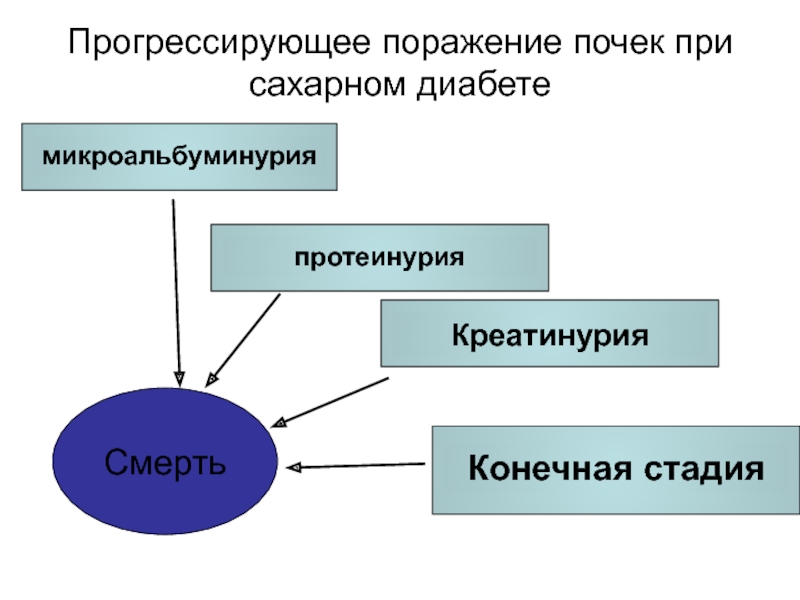
Слайд 65Прогрессирующее поражение почек при сахарном диабете
CV Events
Death
Смерть
Слайд 66Упрощенные критерии инсулинорезистентности
Национальным институтом здоровья США в 2001
году были сформулированы более упрощённые критерии, позволяющие диагностировать МС в
рутинной клинической практике:
абдоминальное ожирение (ОТ более 102 см у мужчин и более 88 см у женщин);
гипертриглицеридемия (уровень ТГ более 1,7 ммоль/л);
снижение уровня холестерина ЛПВП (менее 1,0 ммоль/л у мужчин и менее 1,3 ммоль/л у женщин);
АГ (АД более 130/85 мм рт. ст.);
гипергликемия натощак (более 6,0 ммоль/л).
Наличие любых трёх факторов позволяет констатировать МС.






































![Инсулин, глюкагон, лептин, метаболический синдром Таблица 3. Гипоталамические регуляторы пищевого поведения [1] Таблица 3. Гипоталамические регуляторы пищевого поведения [1]](/img/tmb/2/148060/b3d44224060671d19cdb9836d738de06-800x.jpg)