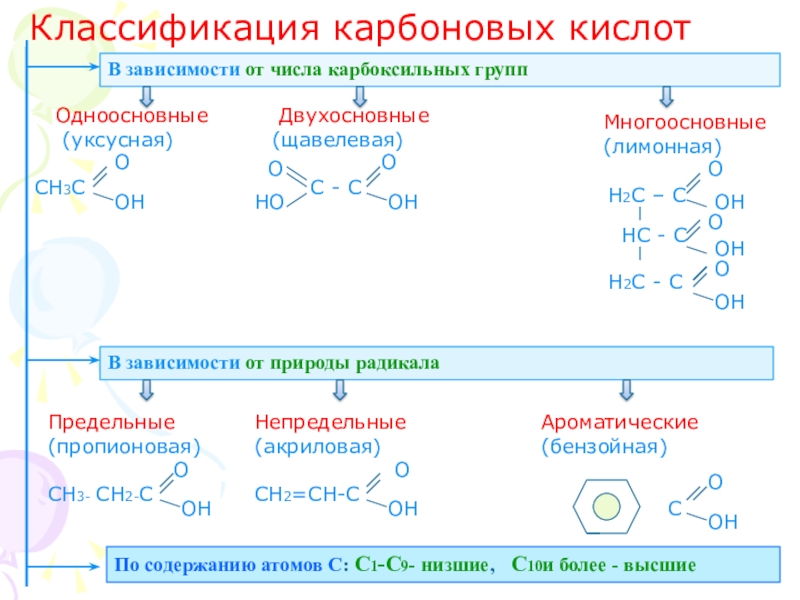
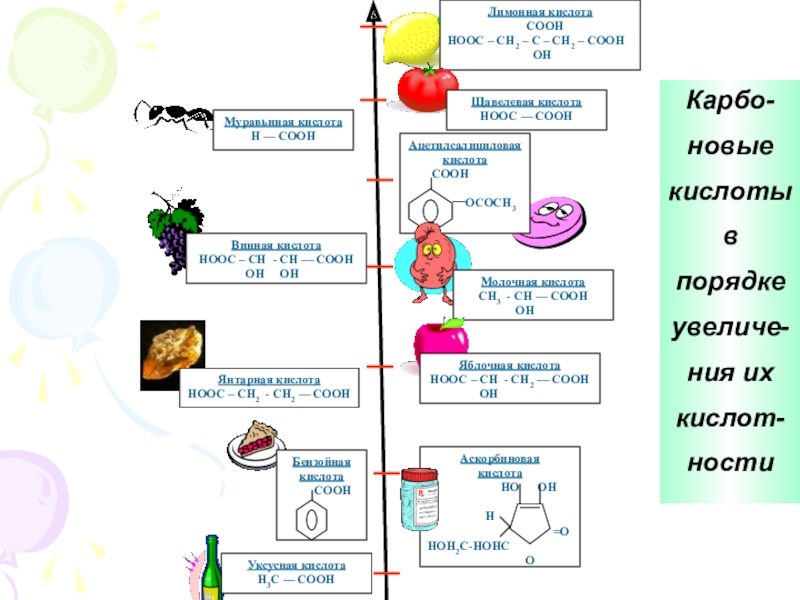
3. Изучить классификацию карбоновых кислот.
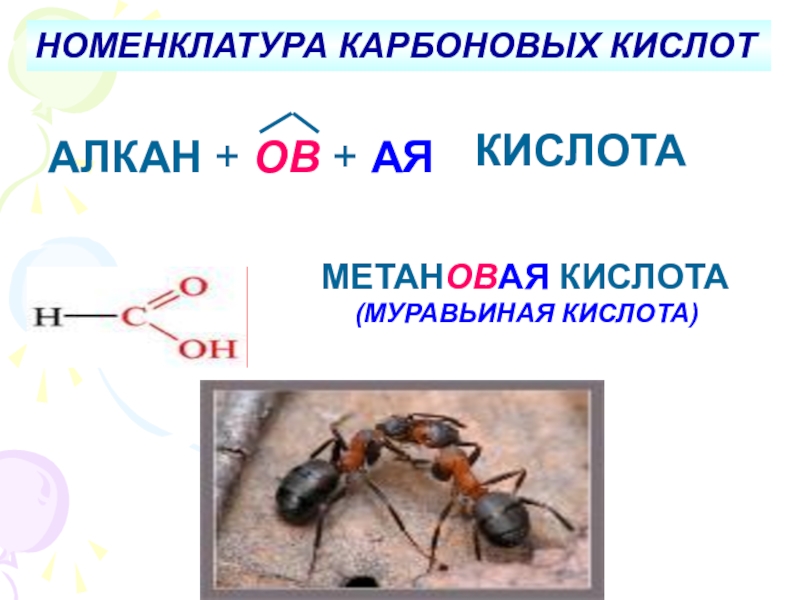
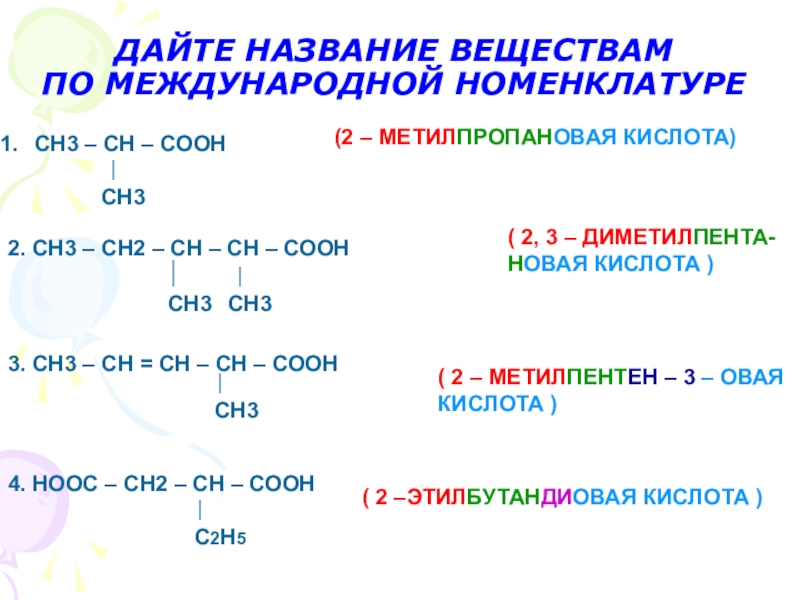
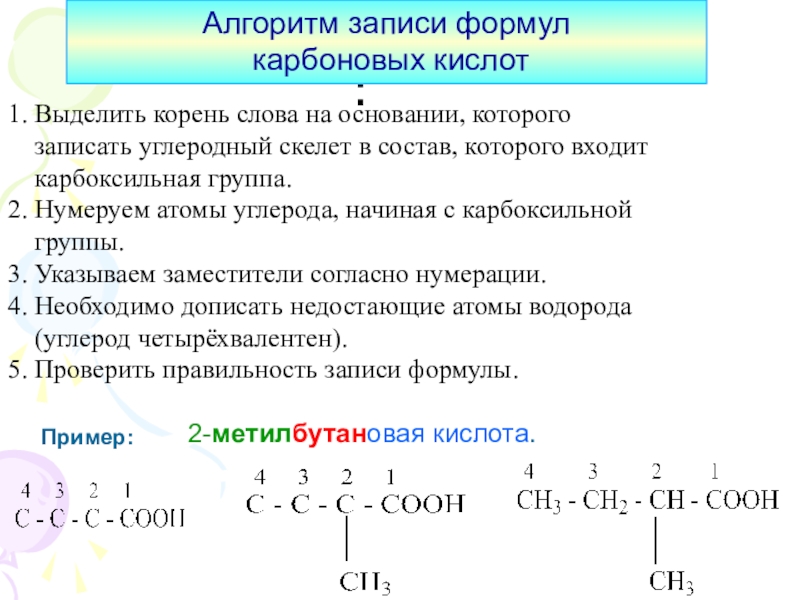
4. Овладеть навыками номенклатуры.
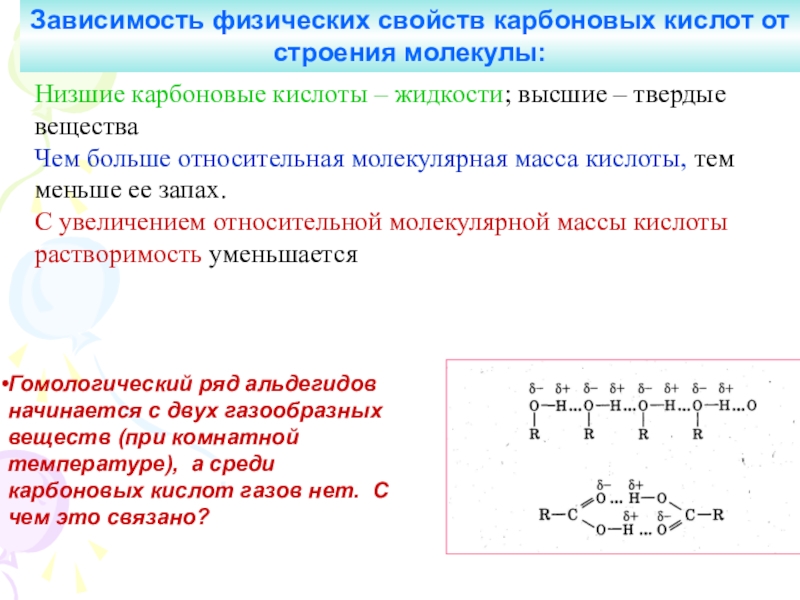
5. Рассмотреть физические
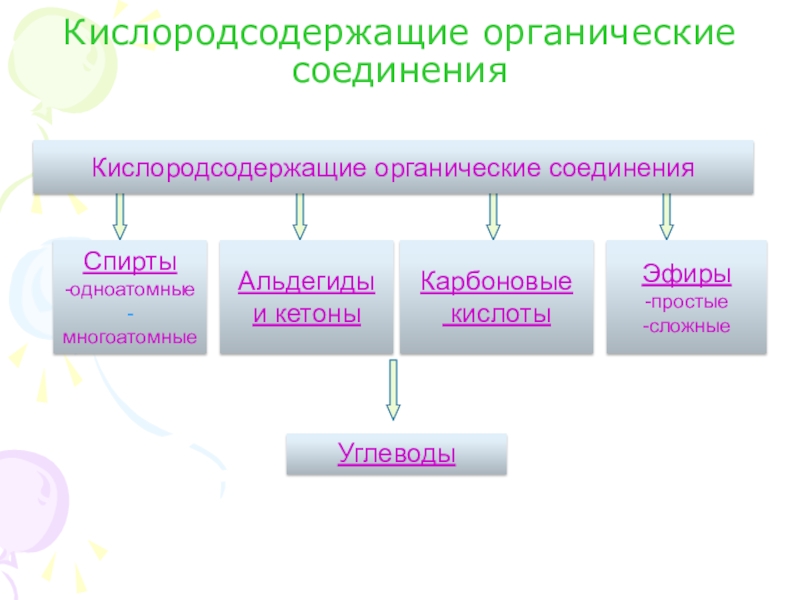
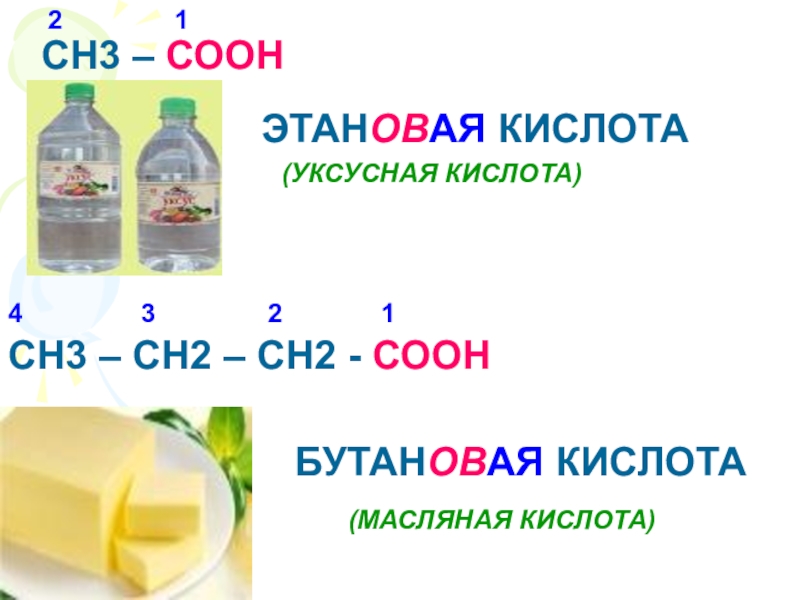
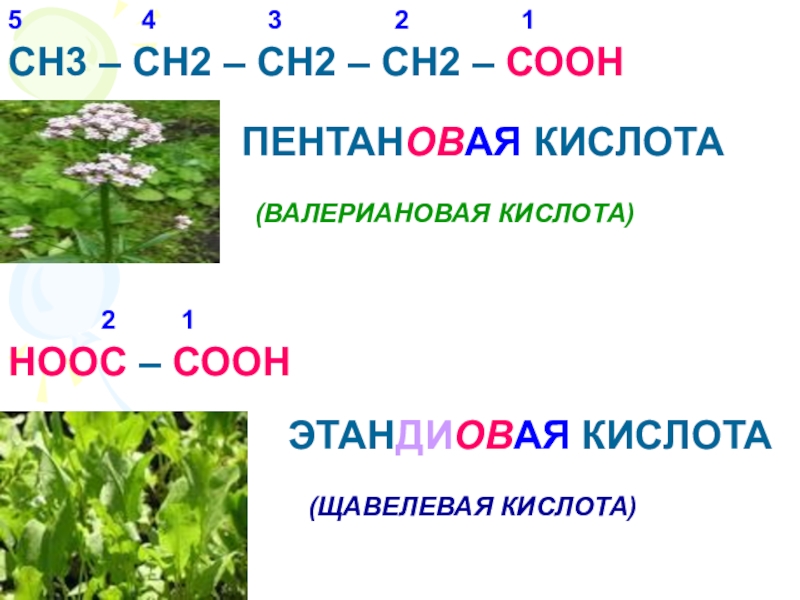
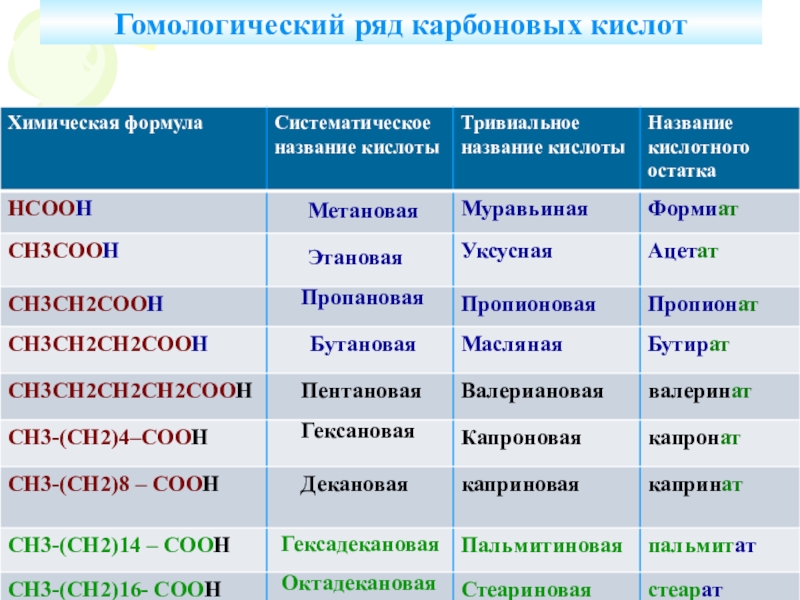
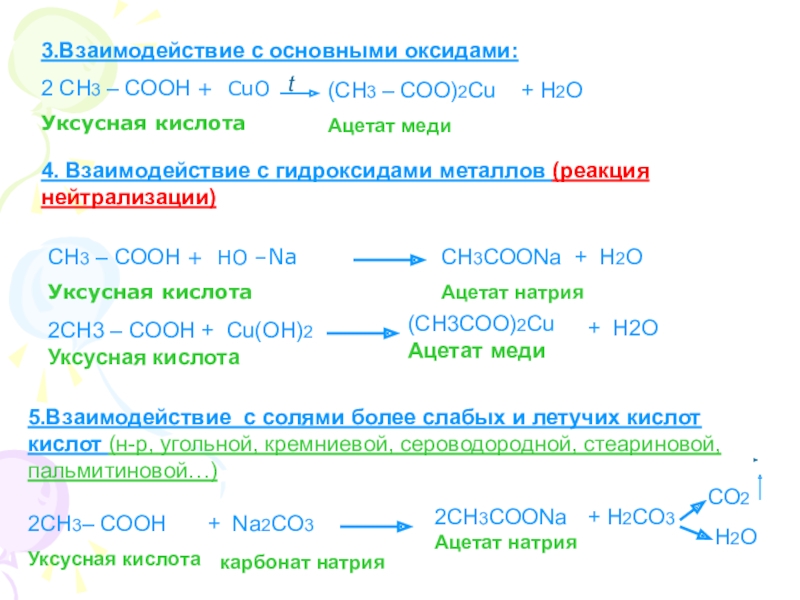
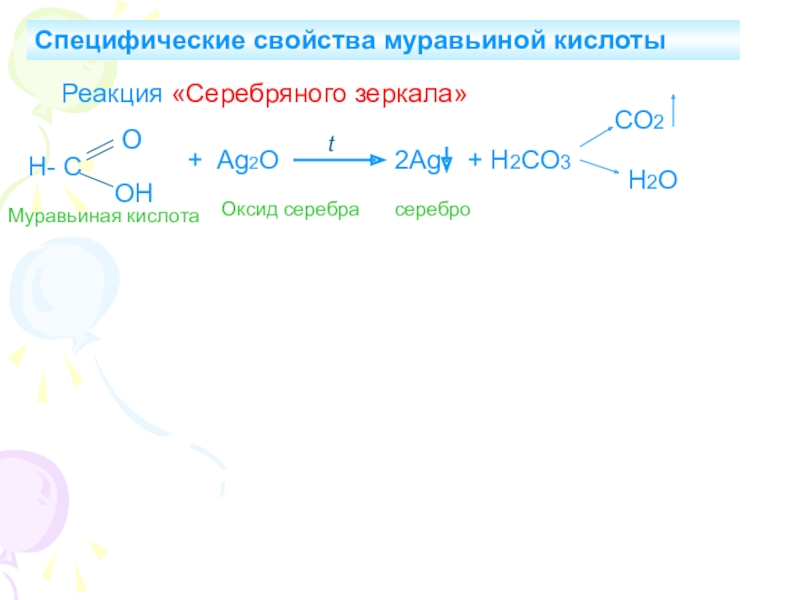
и химические свойства наиболее важных карбоновых кислот.6. Выяснить области применения некоторых карбоновых кислот.