Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Комбинаторная химия
Содержание
- 1. Комбинаторная химия
- 2. Основы комбинаторной химии
- 3. Основы комбинаторной химии Высокопроизводитель-ная хроматография High Throughput Chromatography
- 4. Основы комбинаторной химии 80th199019921998199921 ctВозникновение комбинаторной химии.Конец
- 5. COMPANY PROFILE Основы комбинаторной химии История комбинаторной
- 6. COMPANY PROFILE Основы комбинаторной химии 2) Твердофазный
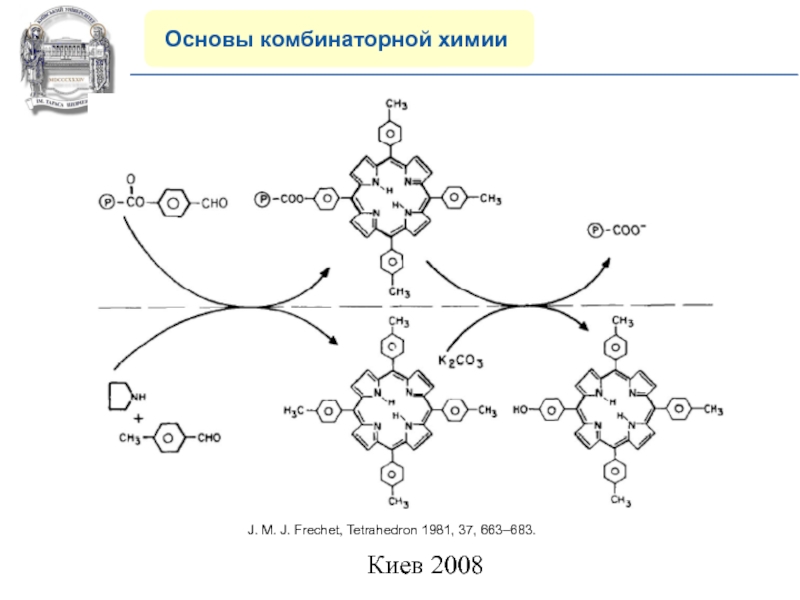
- 7. COMPANY PROFILE Основы комбинаторной химии J. M. J. Frechet, Tetrahedron 1981, 37, 663–683.
- 8. COMPANY PROFILE Основы комбинаторной химии J. I.
- 9. COMPANY PROFILE Основы комбинаторной химии 3) Твердофазный
- 10. COMPANY PROFILE Основы комбинаторной химии S. P.
- 11. COMPANY PROFILE Основы комбинаторной химии 4) Полуавтоматический
- 12. COMPANY PROFILE Основы комбинаторной химии 5) Разделительная
- 13. COMPANY PROFILE Основы комбинаторной химии 6) Жидкофазный
- 14. COMPANY PROFILE Основы комбинаторной химии 7) Жидкофазный
- 15. COMPANY PROFILE Основы комбинаторной химии A. Studer,
- 16. COMPANY PROFILE Основы комбинаторной химии 8) Многообразие современных реакций на полимерной подложке.
- 17. COMPANY PROFILE Основы комбинаторной химии
- 18. COMPANY PROFILE Основы комбинаторной химии
- 19. COMPANY PROFILE Основы комбинаторной химии
- 20. COMPANY PROFILE Основы комбинаторной химии P. H.
- 21. COMPANY PROFILE Основы комбинаторной химии 9) Синтезы с полимерными реагентами.
- 22. COMPANY PROFILE Основы комбинаторной химии Современное
- 23. COMPANY PROFILE Основы комбинаторной химии 2) Тотальный
- 24. COMPANY PROFILE Основы комбинаторной химии 3) Оптимизация
- 25. COMPANY PROFILE Основы комбинаторной химии
- 26. COMPANY PROFILE Основы комбинаторной химии 4) Изучение
- 27. COMPANY PROFILE Основы комбинаторной химии B. M.
- 28. COMPANY PROFILE Основы комбинаторной химии M. S.
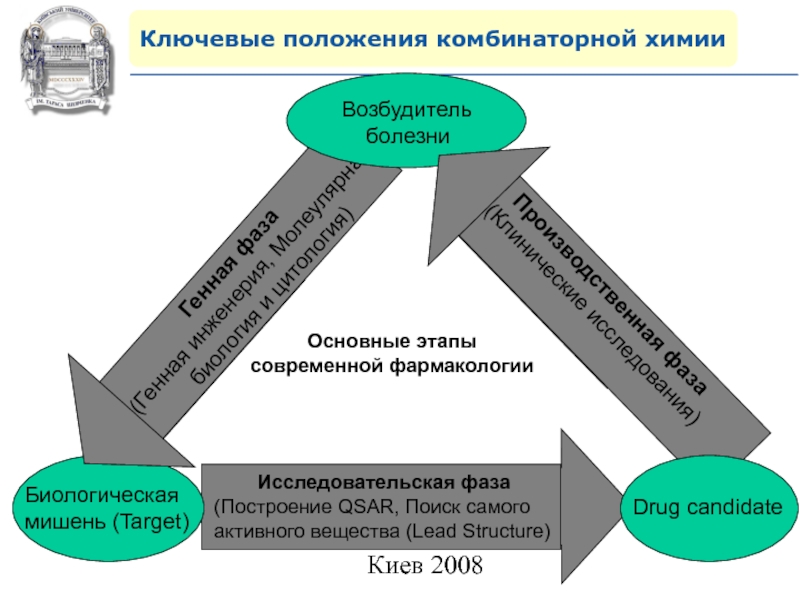
- 29. Основные этапы современной фармакологииКлючевые положения комбинаторной химии
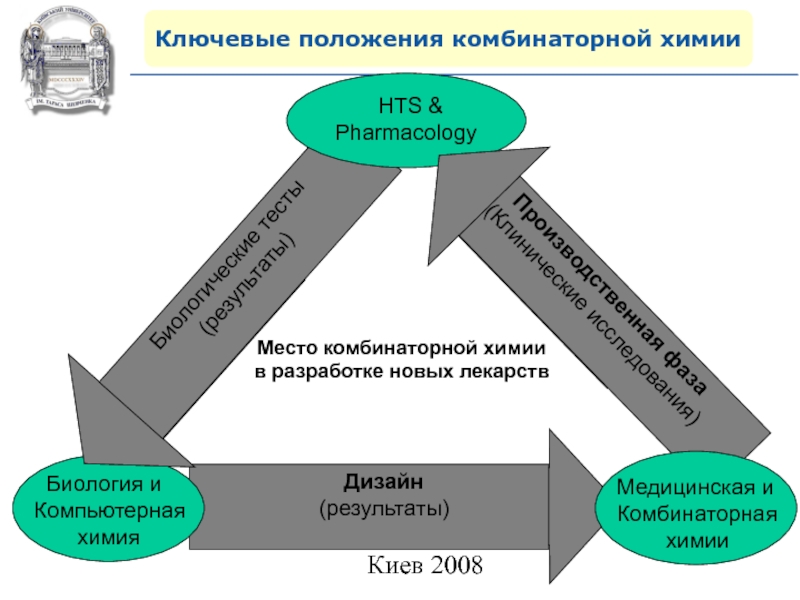
- 30. Ключевые положения комбинаторной химииМесто комбинаторной химии в разработке новых лекарств
- 31. Ключевые положения комбинаторной химии1. Синтез серии соединений
- 32. Ключевые положения комбинаторной химии10 (А) + 10
- 33. Ключевые положения комбинаторной химии3. Качественный дизайн продуктов
- 34. Ключевые положения комбинаторной химии8. Анализ структуры и
- 35. Инструменты комбинаторной химииТвердофазный комбинаторный синтез
- 36. Инструменты комбинаторной химии3. Возможность проведения внутримолекулярных реакций, значительно затрудненных в “классическом” органическом синтезе.
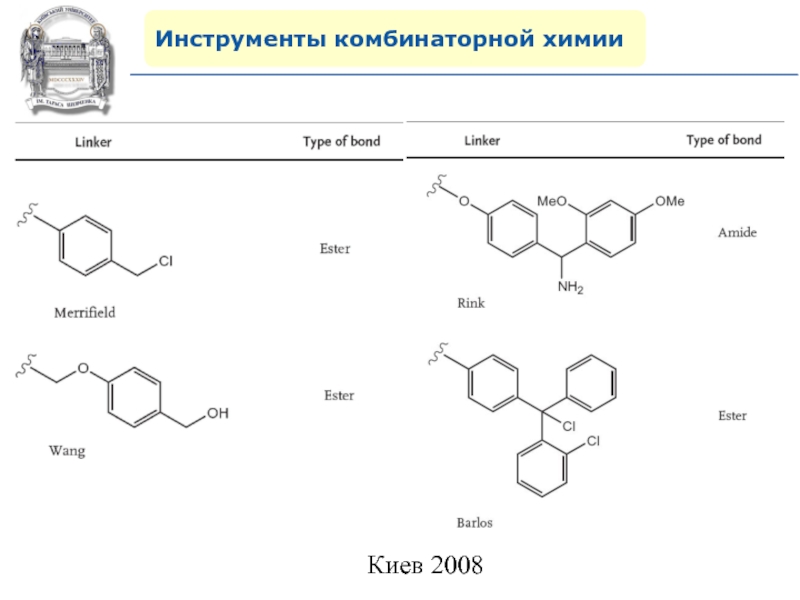
- 37. Инструменты комбинаторной химии4. Поиск удобного линкера – залог успешного протекания синтеза на полимерной подложке.
- 38. Инструменты комбинаторной химии
- 39. Инструменты комбинаторной химии5. Набор растворителей пригодный для
- 40. Инструменты комбинаторной химии9. Использование полимерной подложки наиболее
- 41. Инструменты комбинаторной химии10. Каждая новая реакция на
- 42. Инструменты комбинаторной химии Комбинаторный синтез в растворе(Solution
- 43. Инструменты комбинаторной химии1.2. Использование конденсирующих реагентов:Создание амидной связи.
- 44. Инструменты комбинаторной химииОсновные реакции с участием карбонильных соединенийКонденсацииСинтез оснований ШиффаГетероциклизацииВыделение H2O
- 45. Инструменты комбинаторной химииустойчивость к действию воздуха и
- 46. Инструменты комбинаторной химииReagentsProducts-H2OMe3SiClFirst reports:Izv. АN. USSR, Chem.1985,
- 47. Инструменты комбинаторной химии2. Использование избытков в комбинаторном
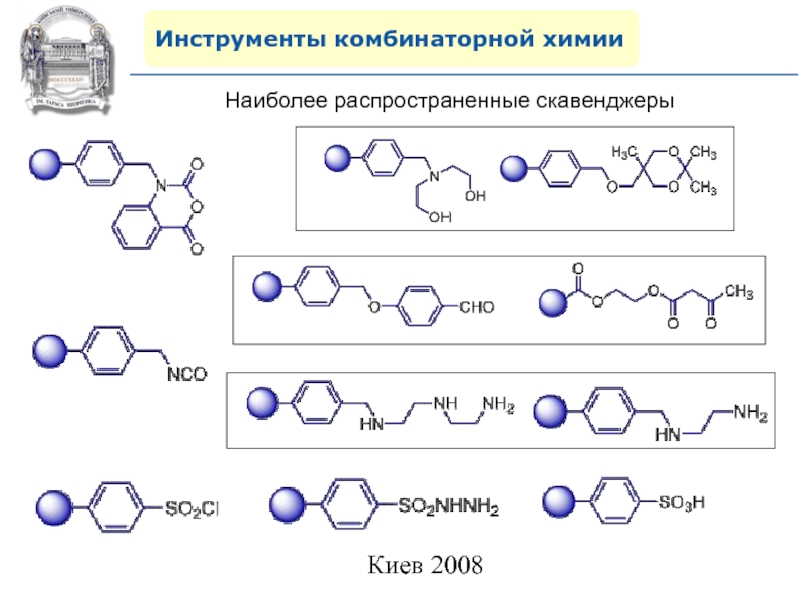
- 48. Инструменты комбинаторной химииНаиболее распространенные скавенджеры
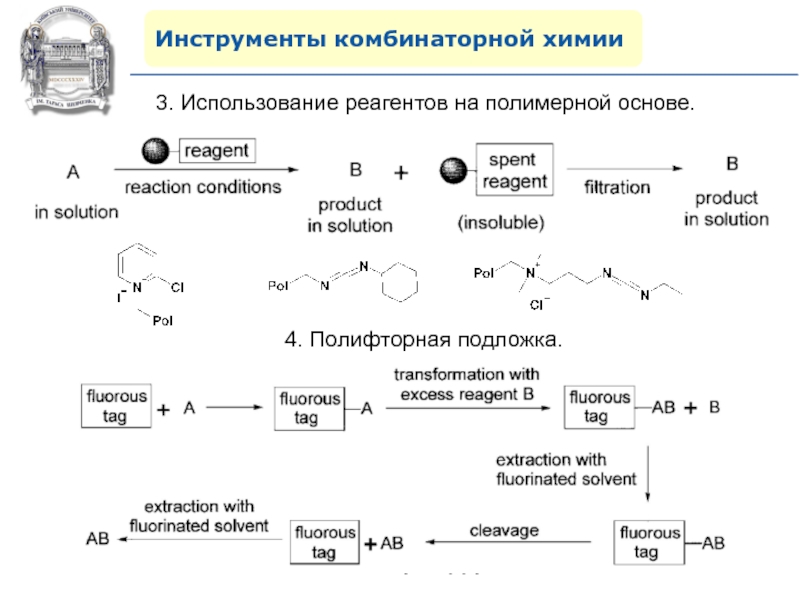
- 49. Инструменты комбинаторной химии3. Использование реагентов на полимерной основе.4. Полифторная подложка.
- 50. Полимеры для твердофазного синтезаЧто такое полистирен?StyreneDivinylbenzenePS-DVBStyreneDVBVinylbenzylchlorideCMS
- 51. Полимеры для твердофазного синтезаОсновные характеристики полимеров:1. Размер
- 52. Полимеры для твердофазного синтезаМакропористая резина (>5% DVB)Высокое
- 53. Полимеры для твердофазного синтезаОсновные кросслинкеры:1. DVB (дивинилбензол
- 54. Полимеры для твердофазного синтезаМикропористая резина (1-2% DVB)Низкое
- 55. Полимеры для твердофазного синтезаФизические свойстваa) Обработка ТГФ,
- 56. Полимеры для твердофазного синтезаГибридные резины1. PEG-resins0.1 –
- 57. Полимеры для твердофазного синтеза2. ROMP-resinsВысокая емкость –
- 58. Полимеры для твердофазного синтеза3. Rasta silanesВысокая емкость
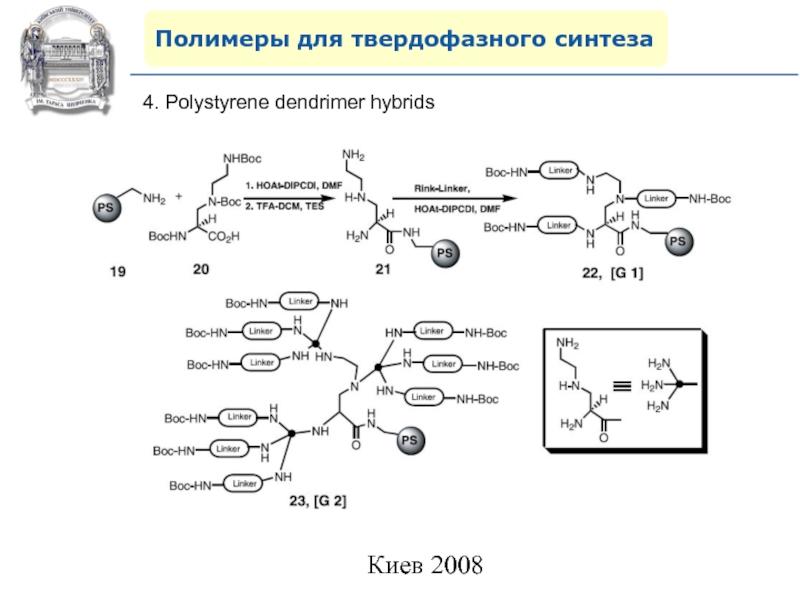
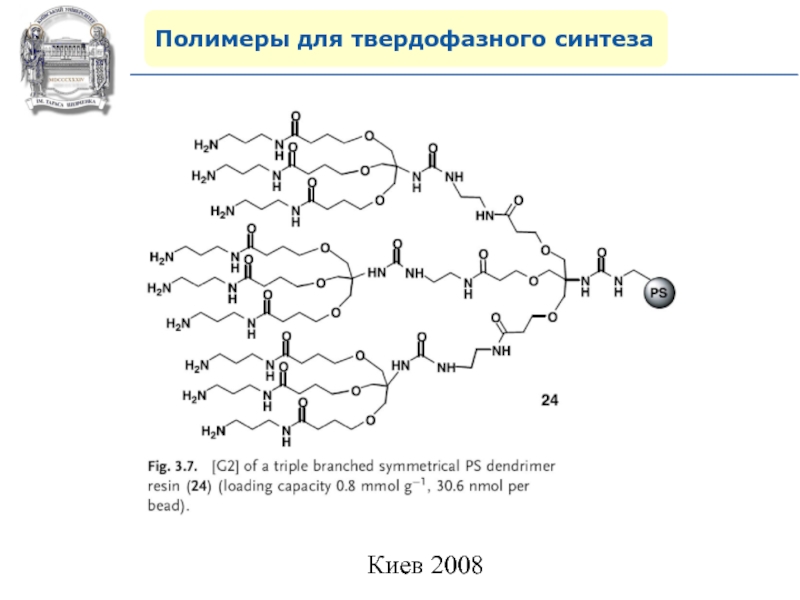
- 59. Полимеры для твердофазного синтеза4. Polystyrene dendrimer hybrids
- 60. Полимеры для твердофазного синтеза
- 61. Полимеры для твердофазного синтеза
- 62. Полимеры для твердофазного синтеза5. Эмульсионные полимерыPolyHIPE. Емкость > 5 ммоль/г!!!Pepsyn-K. Емкость > 5 ммоль/г!!!
- 63. Полимеры для твердофазного синтеза
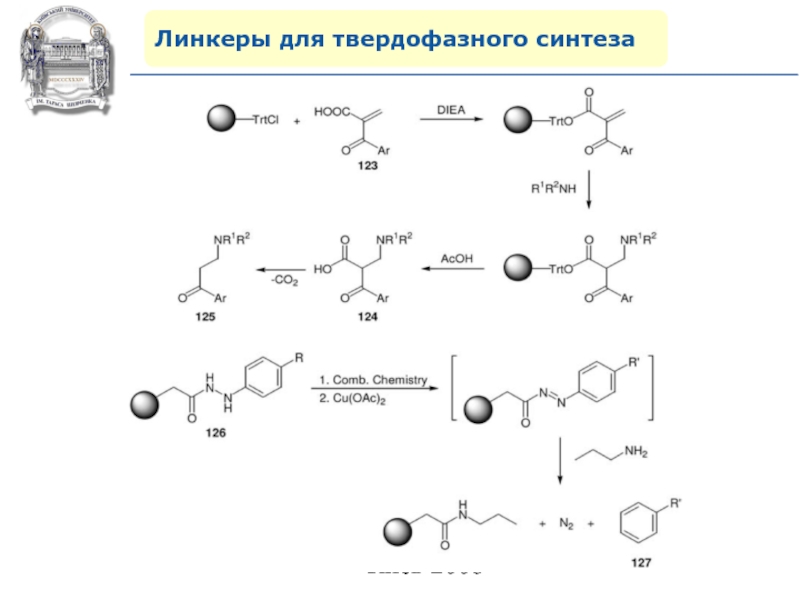
- 64. Линкеры для твердофазного синтезаЛинкеры – бифункциональные химические
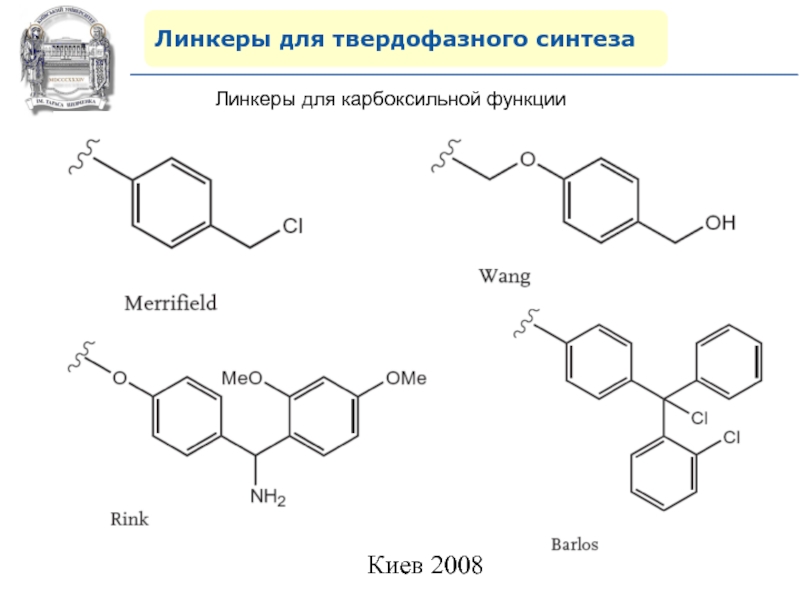
- 65. Линкеры для твердофазного синтезаЛинкеры для карбоксильной функции
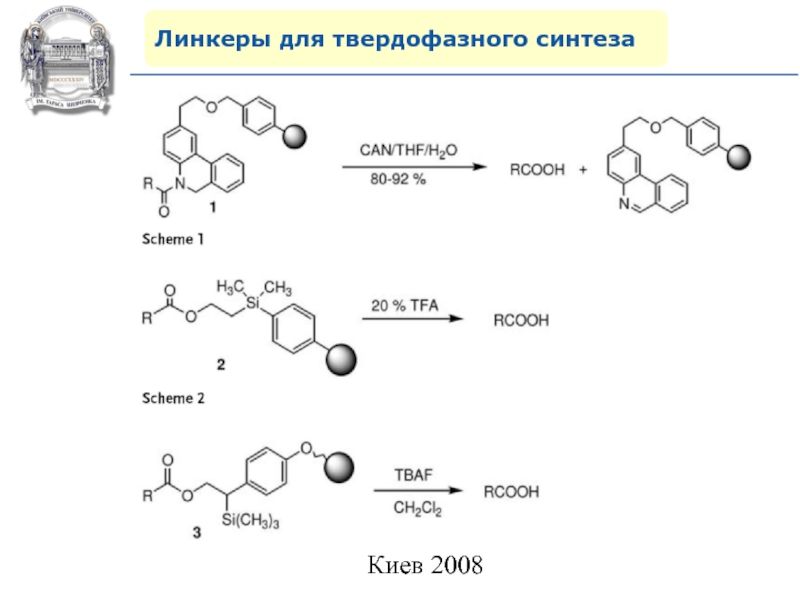
- 66. Линкеры для твердофазного синтеза
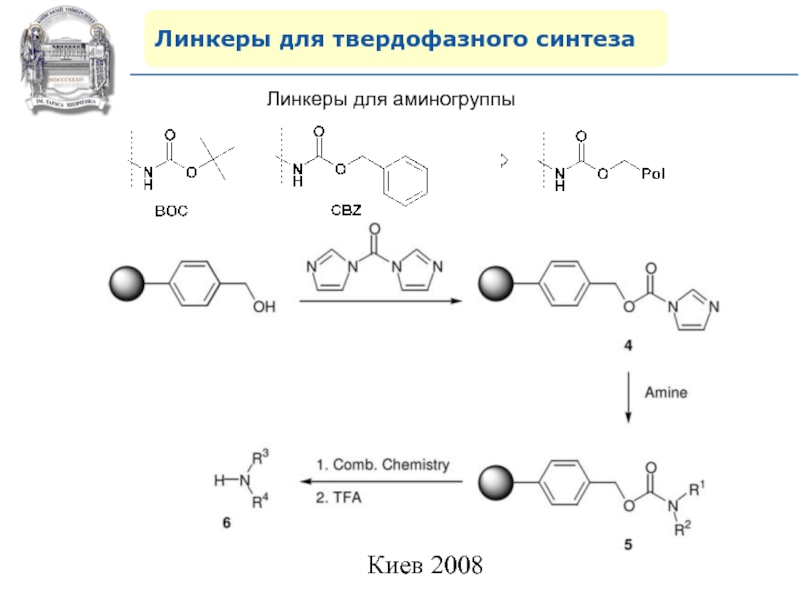
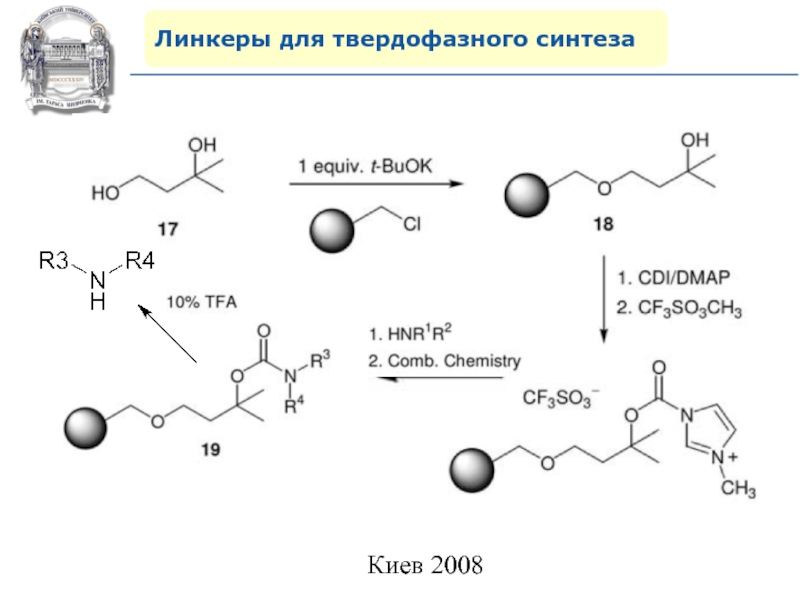
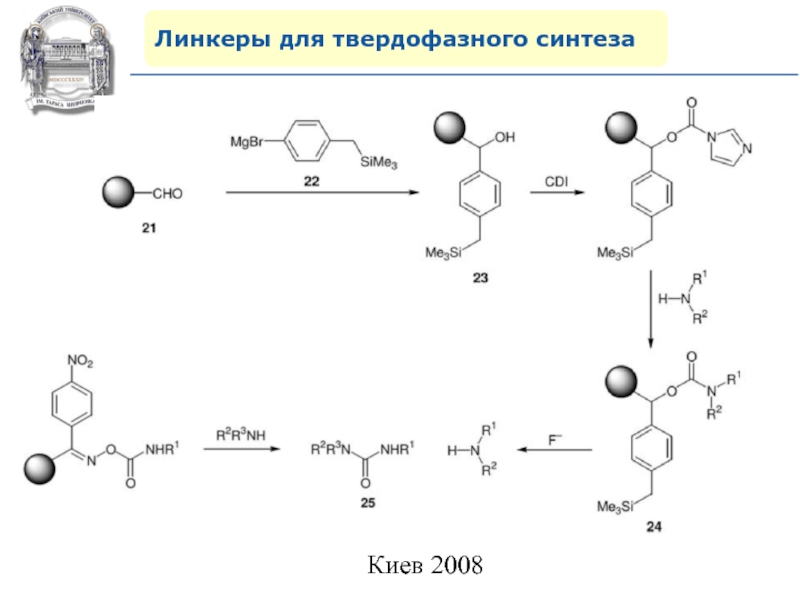
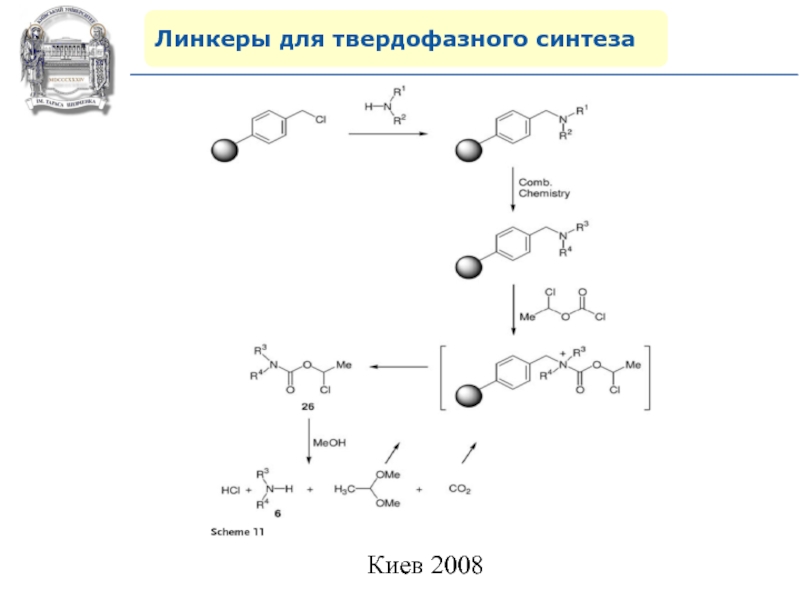
- 67. Линкеры для твердофазного синтезаЛинкеры для аминогруппы
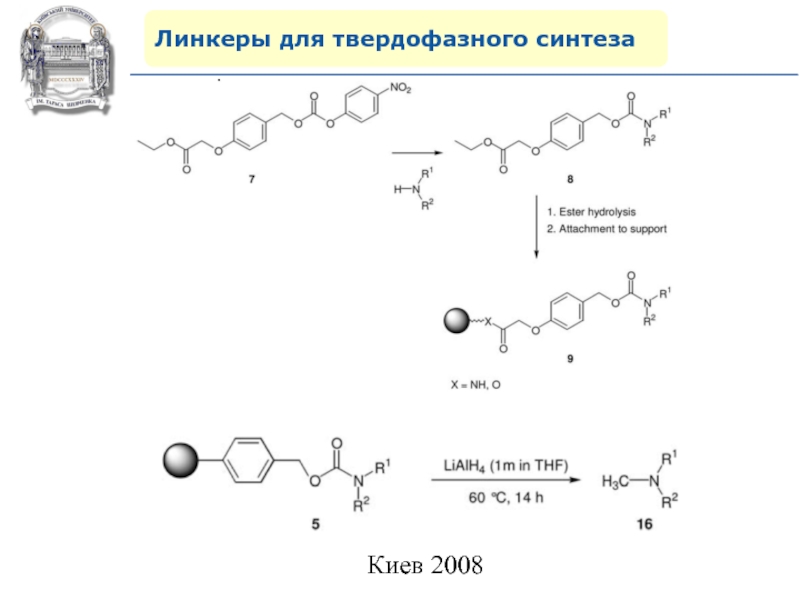
- 68. Линкеры для твердофазного синтеза
- 69. Линкеры для твердофазного синтеза
- 70. Линкеры для твердофазного синтеза
- 71. Линкеры для твердофазного синтеза
- 72. Линкеры для твердофазного синтеза
- 73. Линкеры для твердофазного синтеза
- 74. Линкеры для твердофазного синтеза
- 75. Линкеры для твердофазного синтеза
- 76. Линкеры для твердофазного синтеза
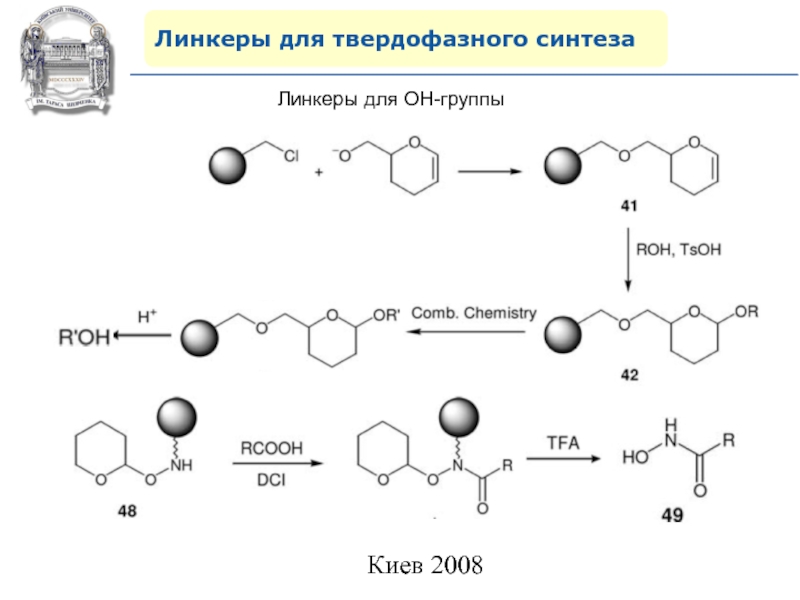
- 77. Линкеры для твердофазного синтезаЛинкеры для ОН-группы
- 78. Линкеры для твердофазного синтеза
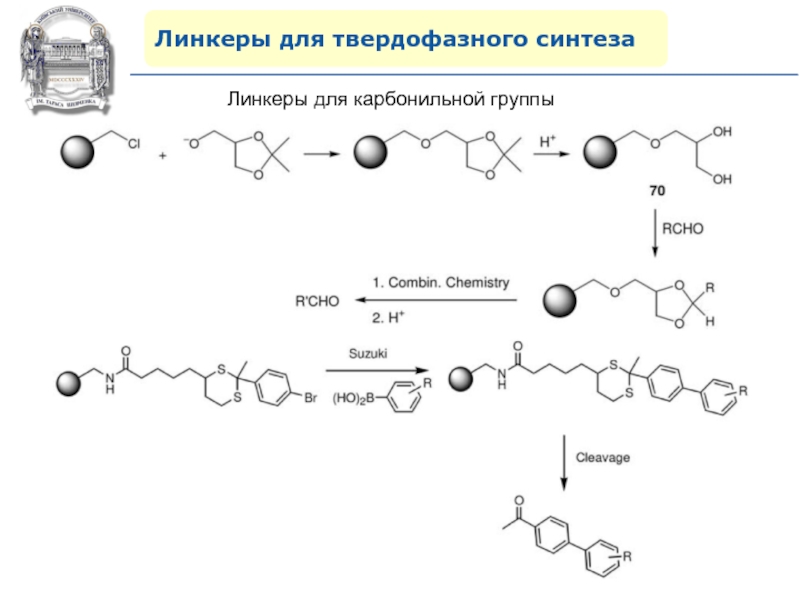
- 79. Линкеры для твердофазного синтезаЛинкеры для карбонильной группы
- 80. Линкеры для твердофазного синтеза
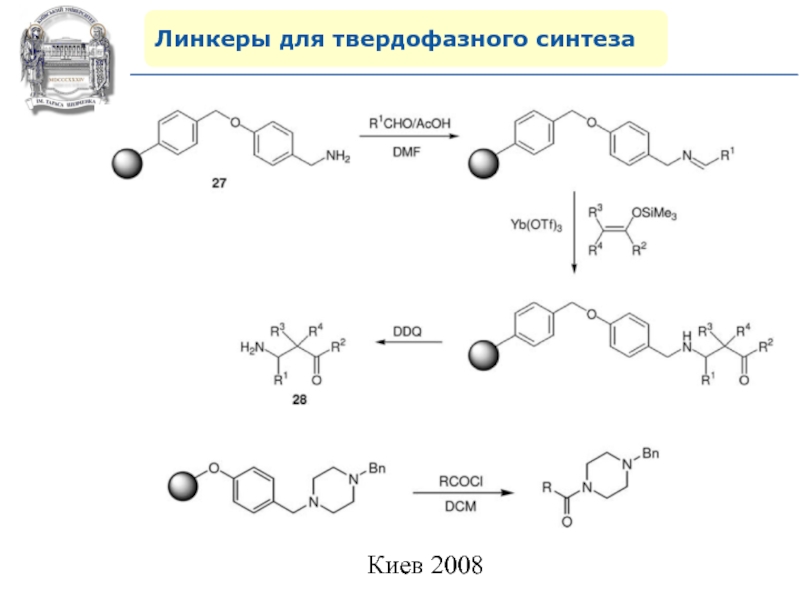
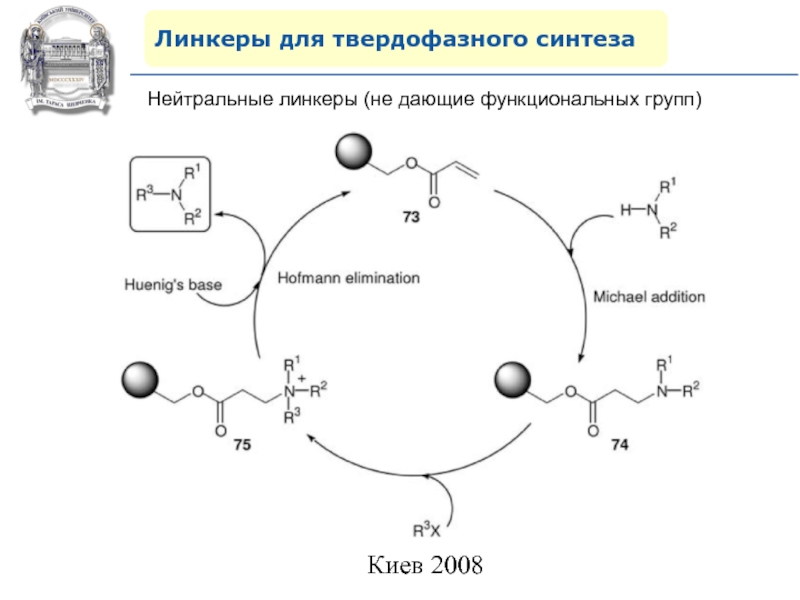
- 81. Линкеры для твердофазного синтезаНейтральные линкеры (не дающие функциональных групп)
- 82. Линкеры для твердофазного синтеза
- 83. Линкеры для твердофазного синтеза
- 84. Линкеры для твердофазного синтеза
- 85. Линкеры для твердофазного синтеза
- 86. Линкеры для твердофазного синтеза
- 87. Молекулярное моделированиеКритерии для комбинаторных библиотек. Правила Липинского
- 88. Молекулярное моделированиеПравила Вебера (правила 4, Weber’s rules of 4):1) Молекулярный вес. 150
- 89. Молекулярное моделирование
- 90. Линкеры для твердофазного синтезаRNG – количество цикловRTB
- 91. Молекулярное моделированиеТипы библиотек:1) Первичная библиотека для скрининга.
- 92. Молекулярное моделированиеДискрипторы:1) Одномерные (1D). (MW, ClogP, Hbond
- 93. Молекулярное моделирование
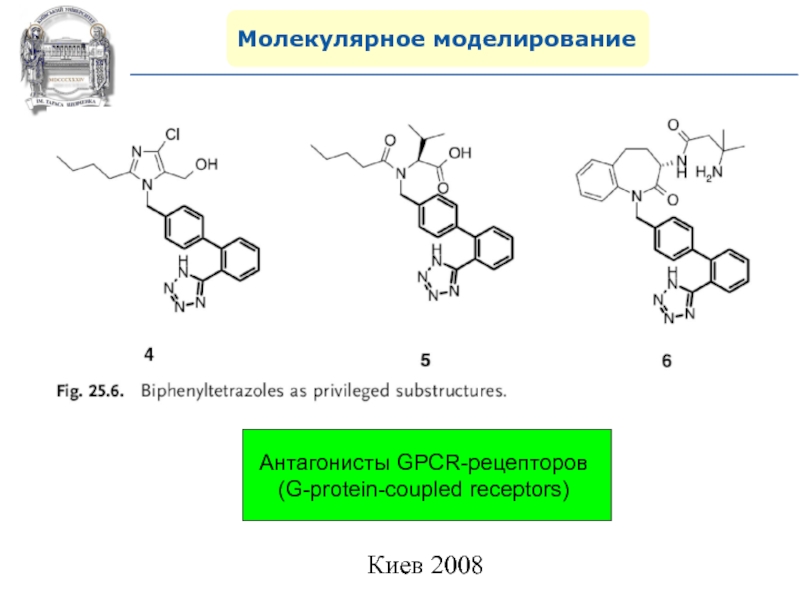
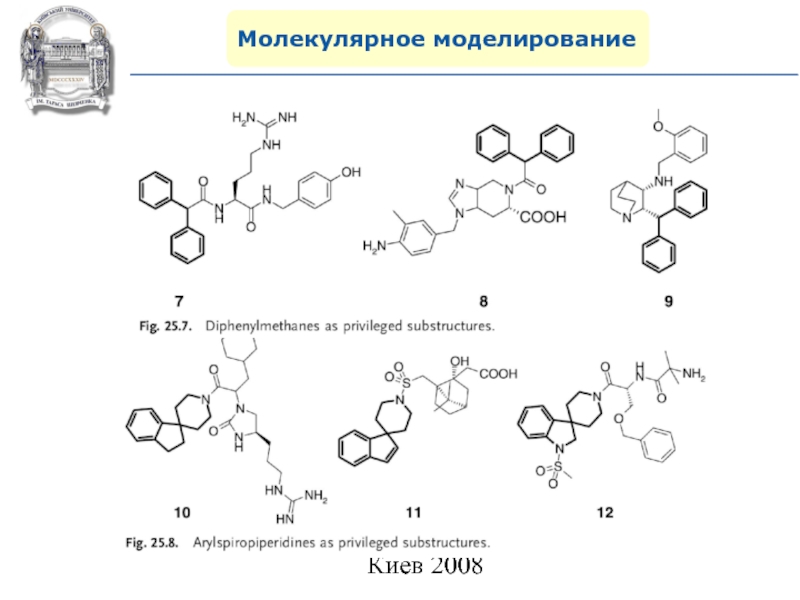
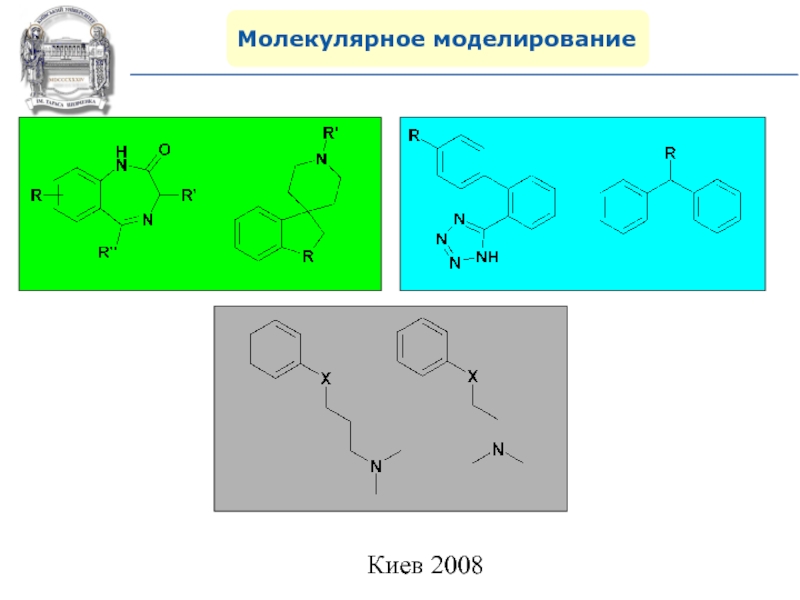
- 94. Молекулярное моделированиеПривилегированные структуры (Privileged structures) и лекарственно
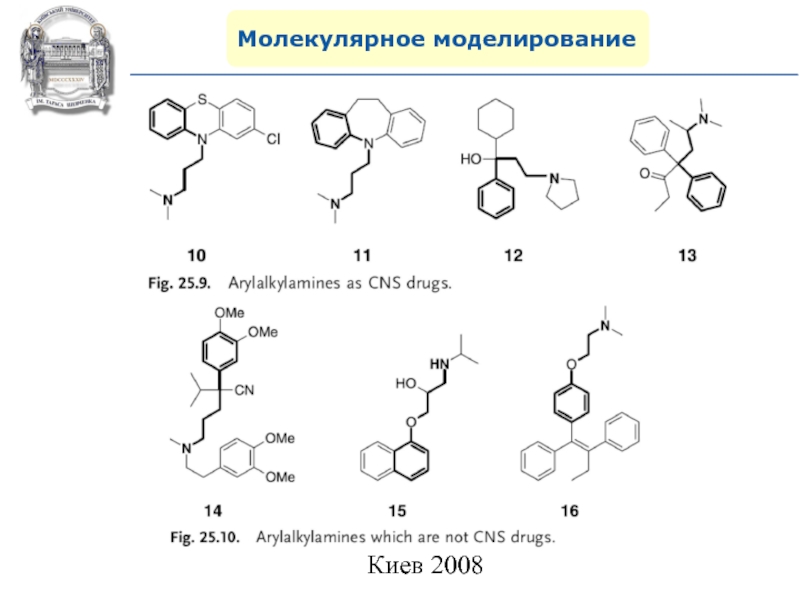
- 95. Молекулярное моделирование
- 96. Молекулярное моделирование
- 97. Молекулярное моделирование
- 98. Молекулярное моделирование
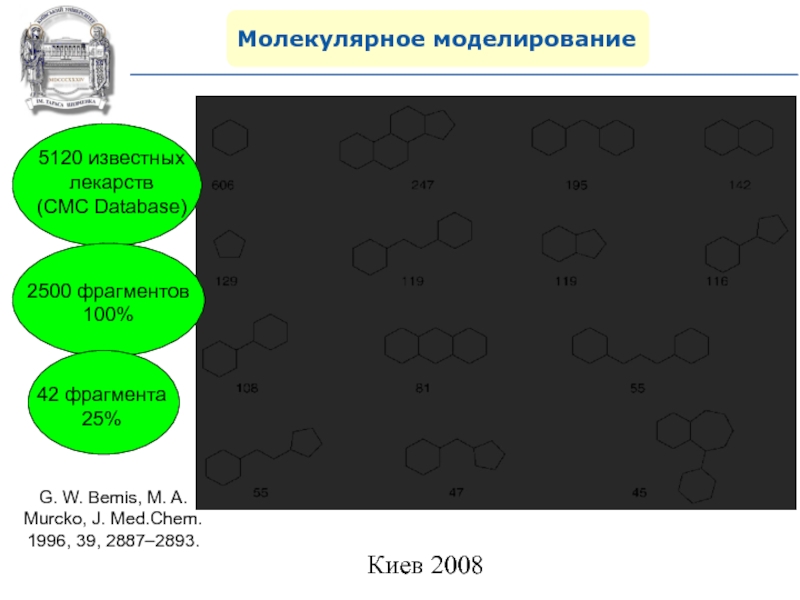
- 99. Молекулярное моделированиеG. W. Bemis, M. A. Murcko, J. Med.Chem. 1996, 39, 2887–2893.
- 100. Молекулярное моделирование
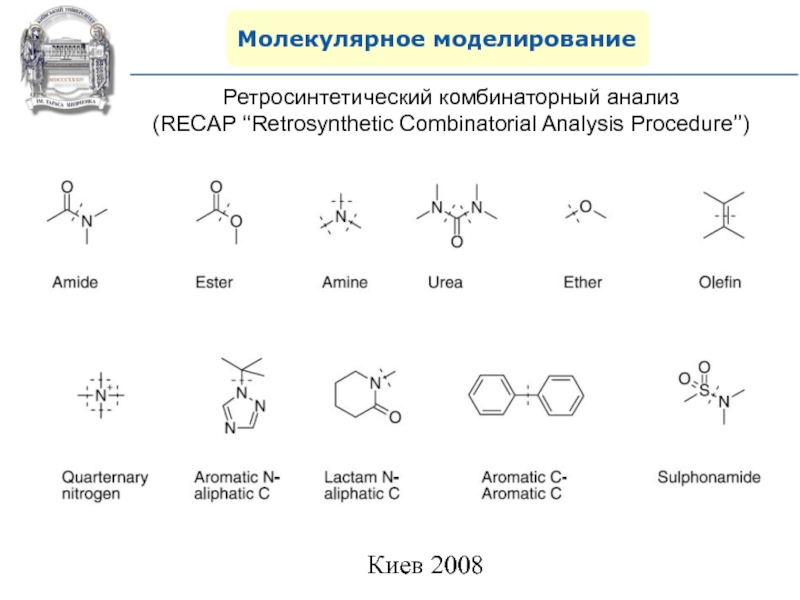
- 101. Молекулярное моделированиеРетросинтетический комбинаторный анализ (RECAP ‘‘Retrosynthetic Combinatorial Analysis Procedure’’)
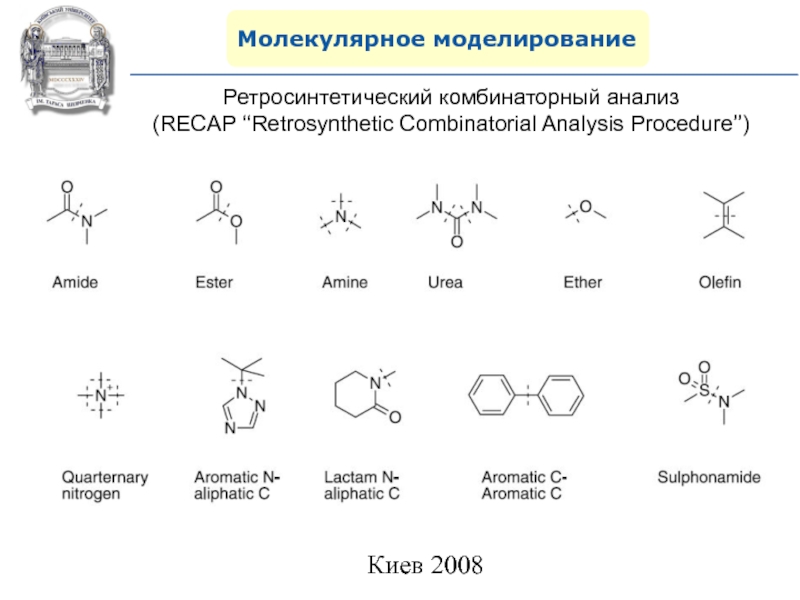
- 102. Молекулярное моделированиеРетросинтетический комбинаторный анализ (RECAP ‘‘Retrosynthetic Combinatorial Analysis Procedure’’)
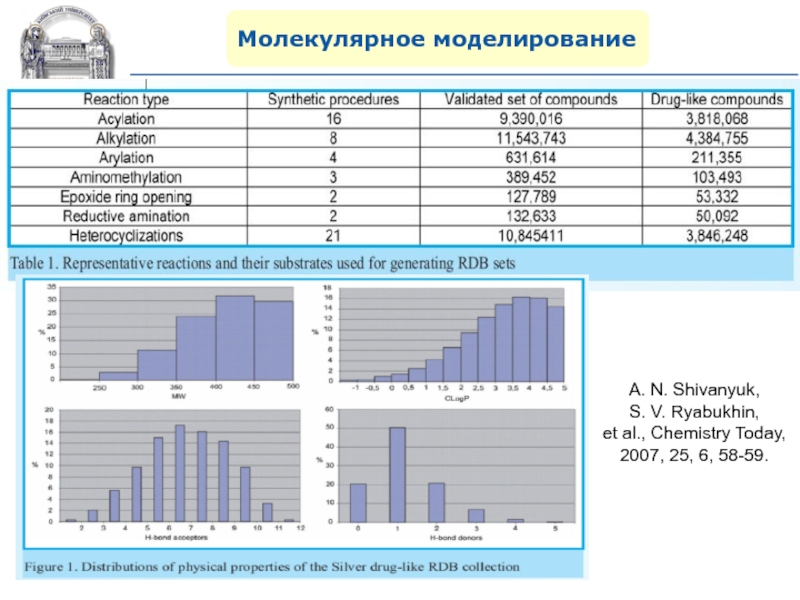
- 103. Молекулярное моделированиеA. N. Shivanyuk, S. V. Ryabukhin, et al., Chemistry Today, 2007, 25, 6, 58-59.
- 104. Молекулярное моделированиеСовременные “drug-like” библиотеки.1) Соблюдение правила 4
- 105. Молекулярное моделированиеСовременные “drug-like” библиотеки.1) Соблюдение правила 4
- 106. Молекулярное моделирование
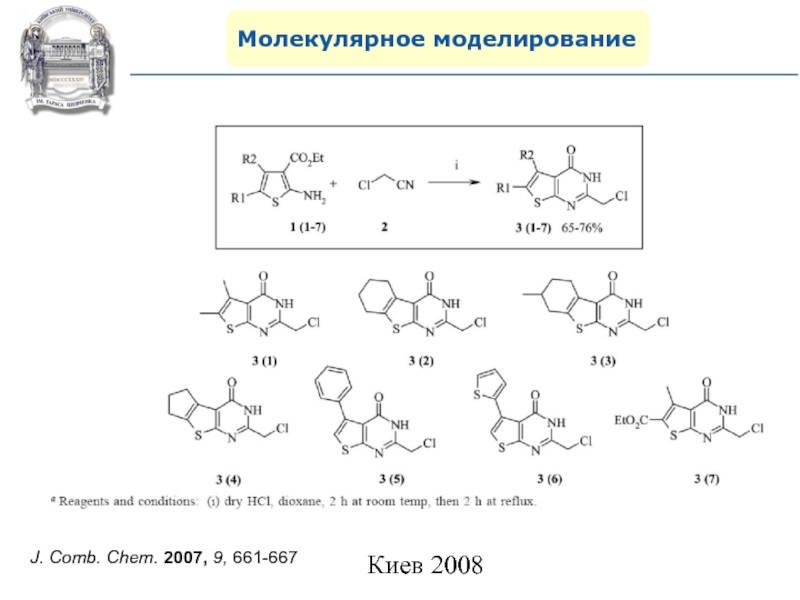
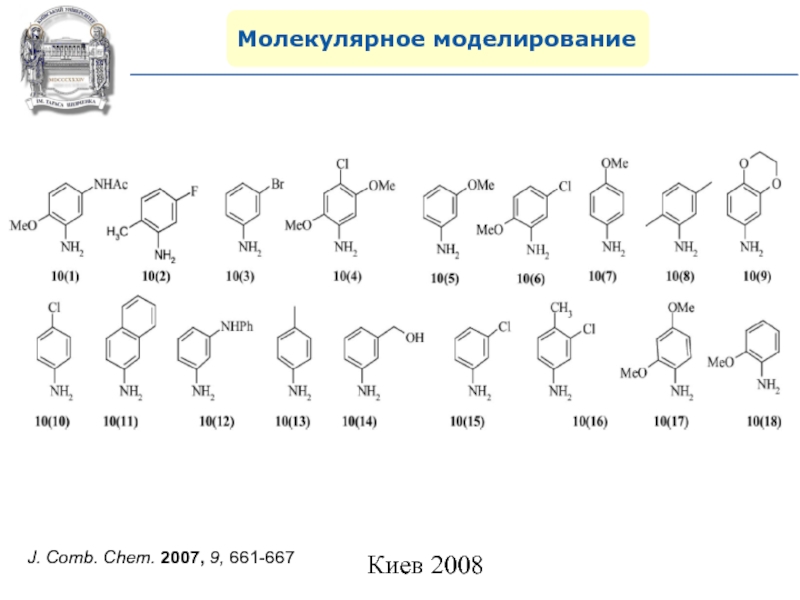
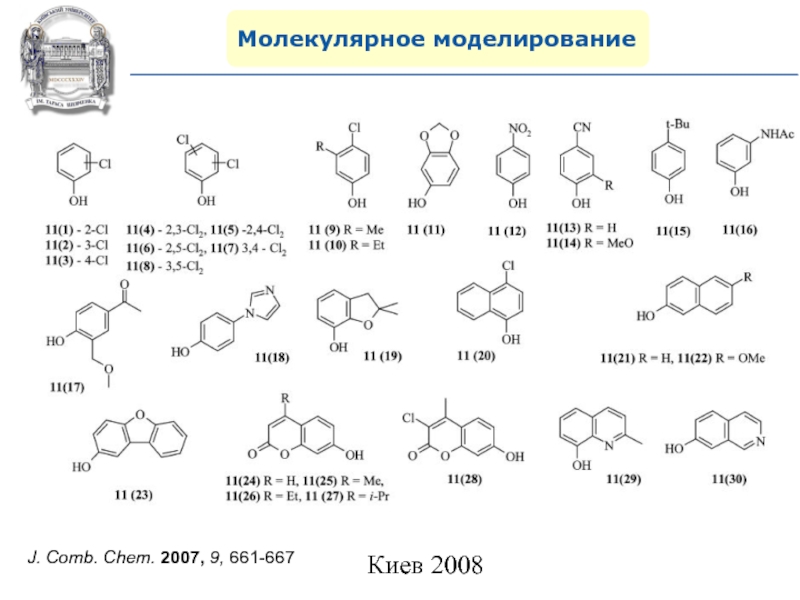
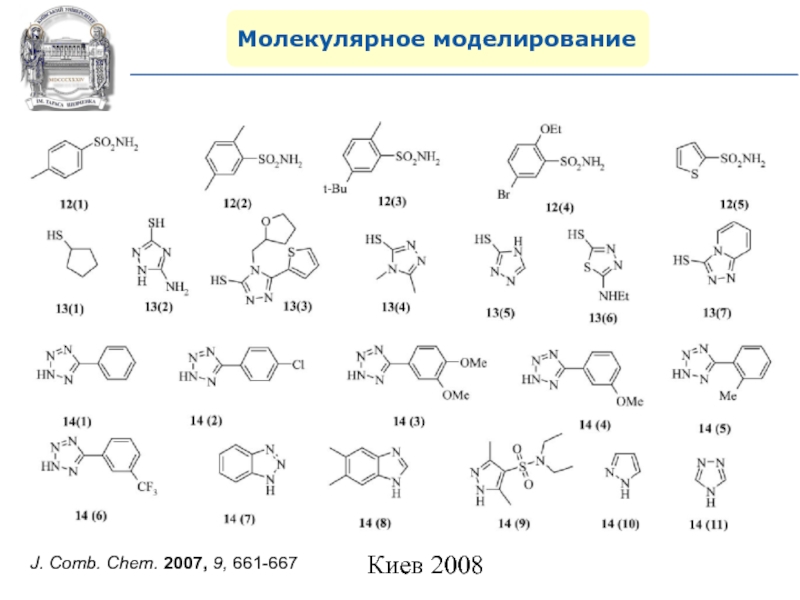
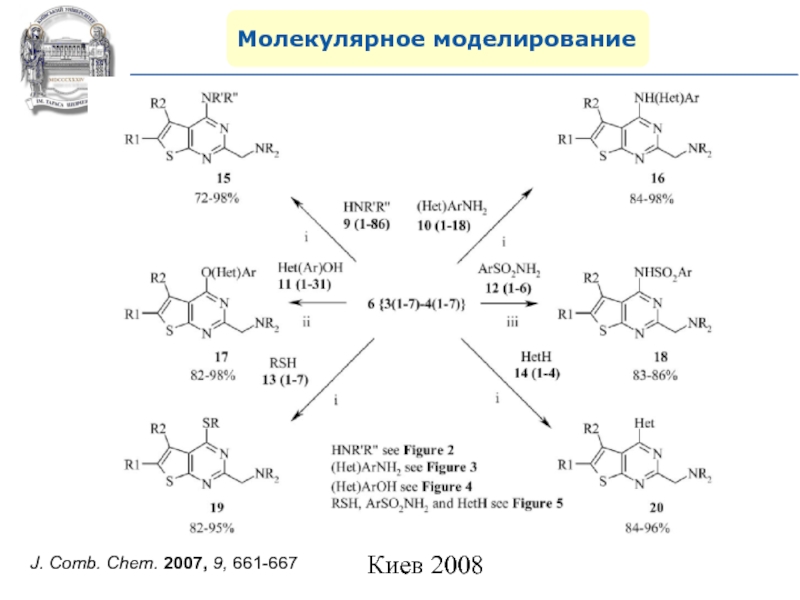
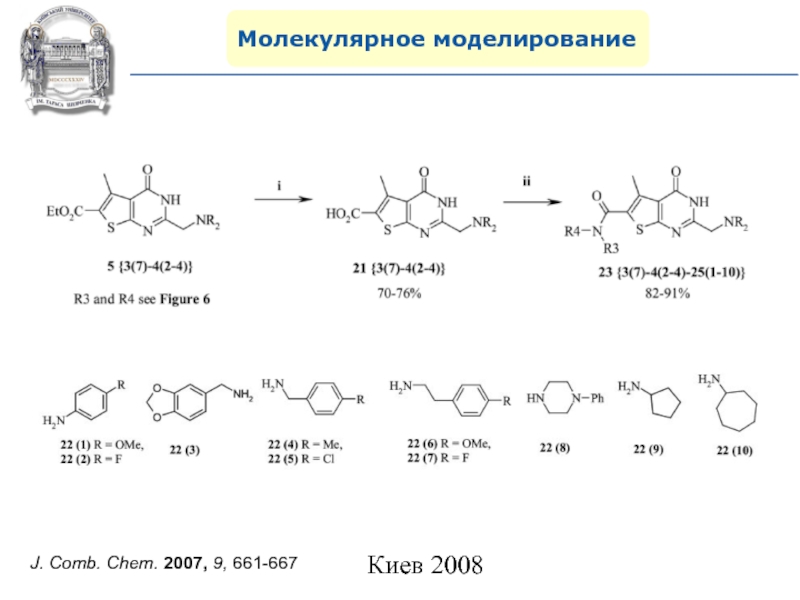
- 107. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
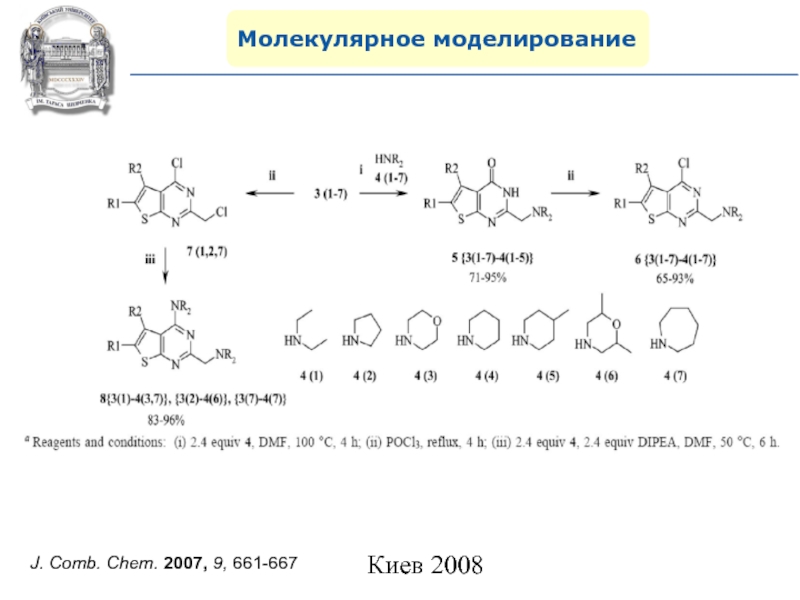
- 108. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
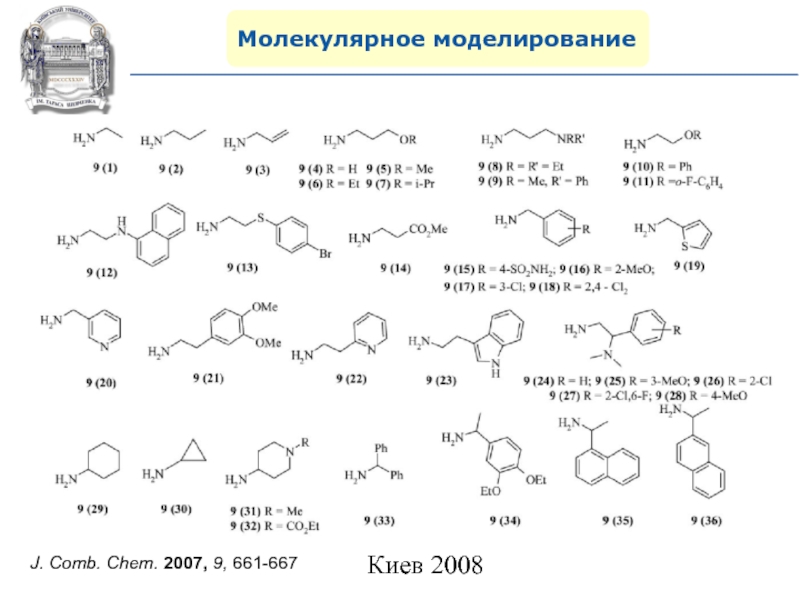
- 109. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
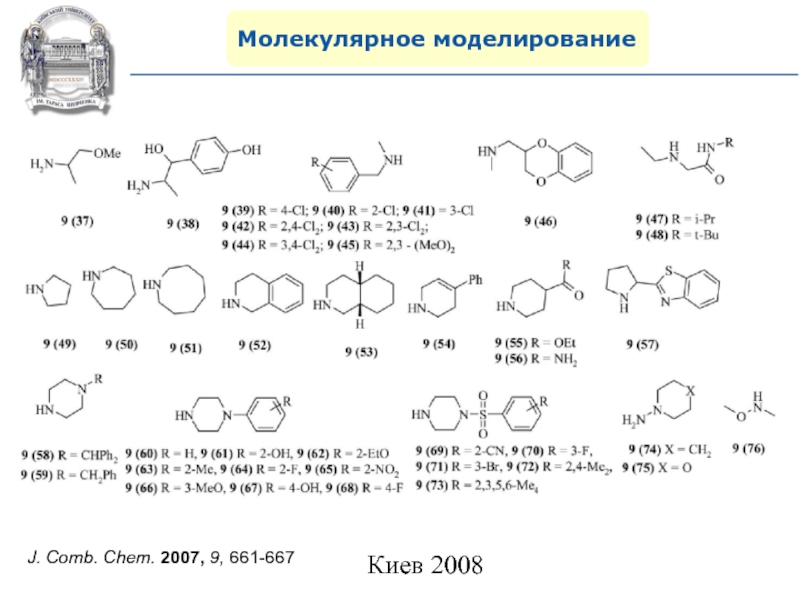
- 110. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 111. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 112. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 113. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 114. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 115. Молекулярное моделированиеJ. Comb. Chem. 2007, 9, 661-667
- 116. Молекулярное моделирование
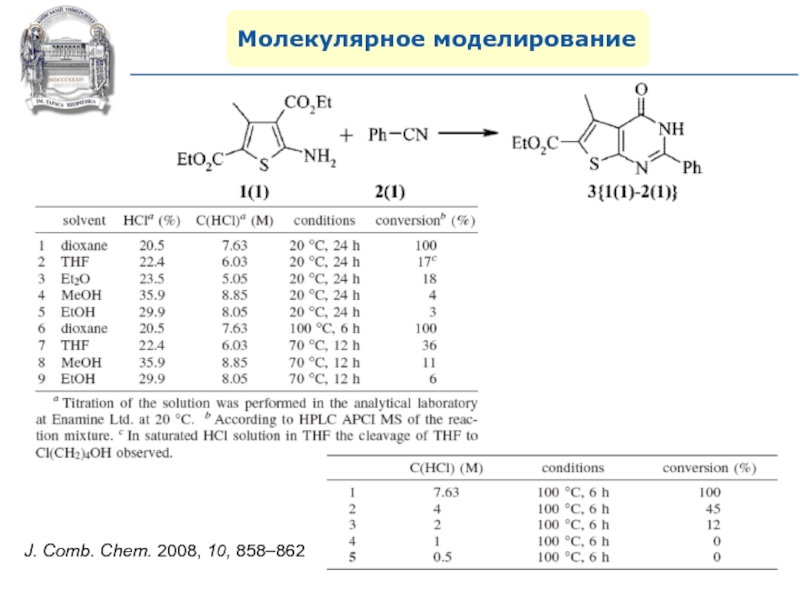
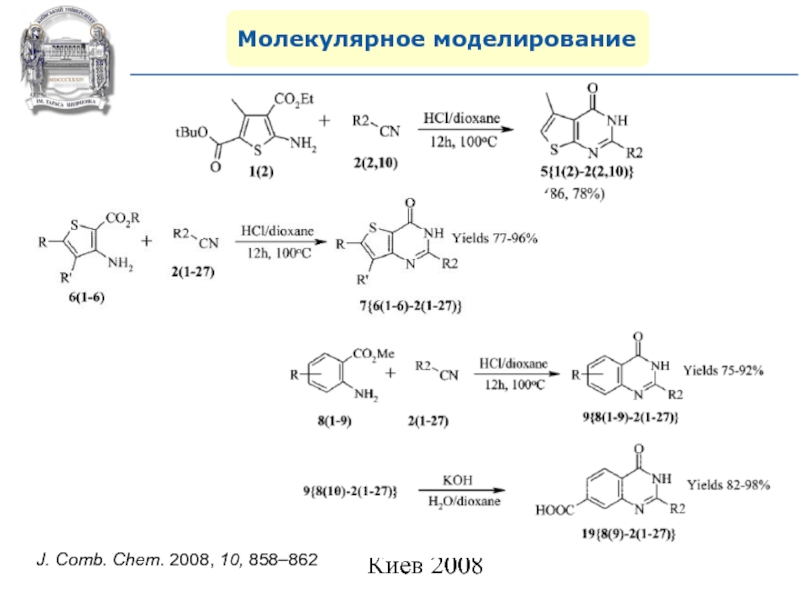
- 117. Молекулярное моделированиеJ. Comb. Chem. 2008, 10, 858–862
- 118. Молекулярное моделирование
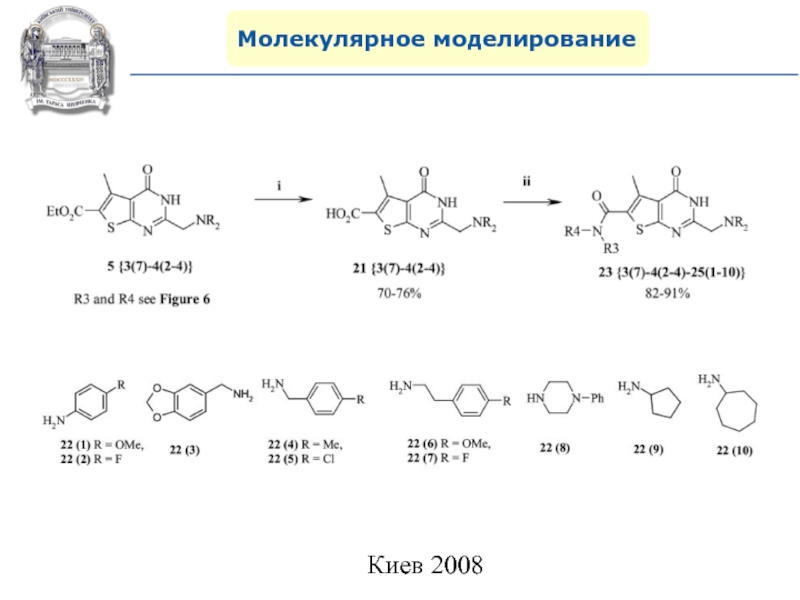
- 119. Молекулярное моделированиеJ. Comb. Chem. 2008, 10, 858–862
- 120. Молекулярное моделирование
- 121. Молекулярное моделирование
- 122. Молекулярное моделирование
- 123. Молекулярное моделирование
- 124. Молекулярное моделирование
- 125. Молекулярное моделирование
- 126. Молекулярное моделирование
- 127. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Комбинаторная химия
Курс лекций для студентов химического факультета
КНУ имени Шевченко
Рябухин
С. В.
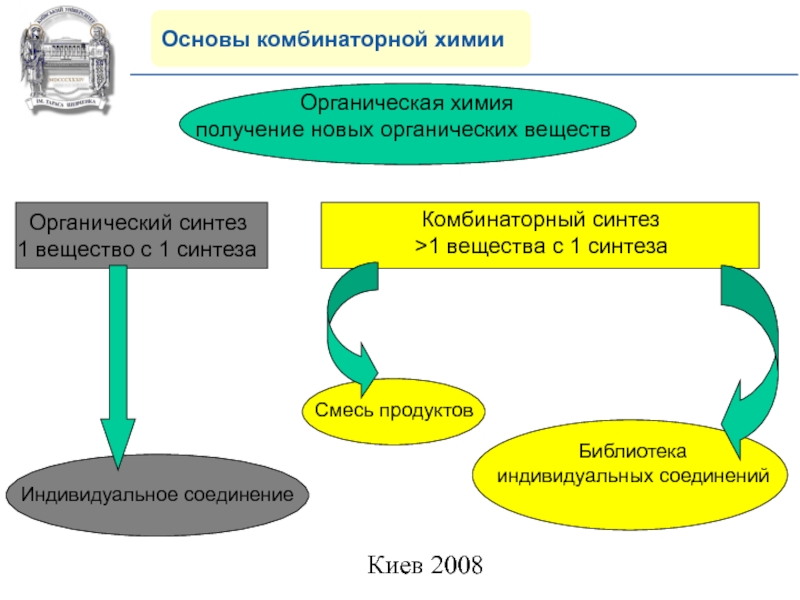
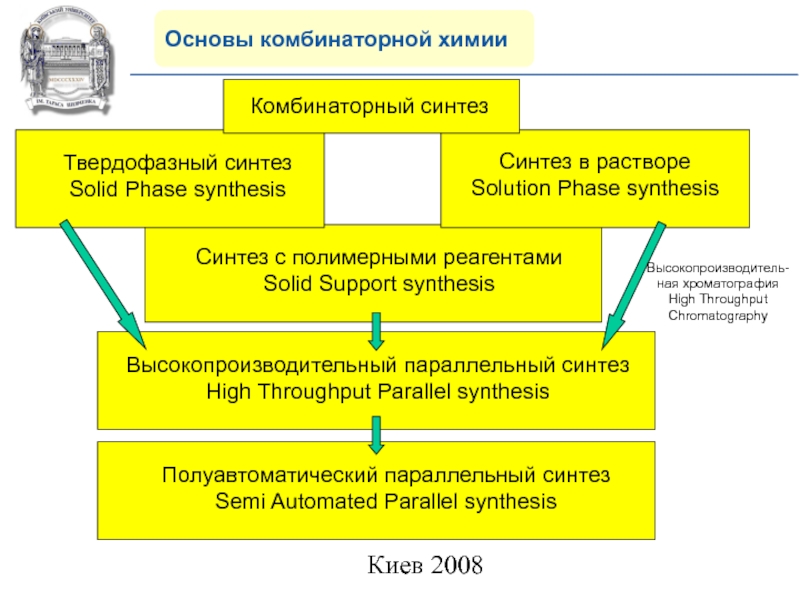
Слайд 3Основы комбинаторной химии
Высокопроизводитель-ная хроматография High Throughput Chromatography
Слайд 4Основы комбинаторной химии
80th
1990
1992
1998
1999
21 ct
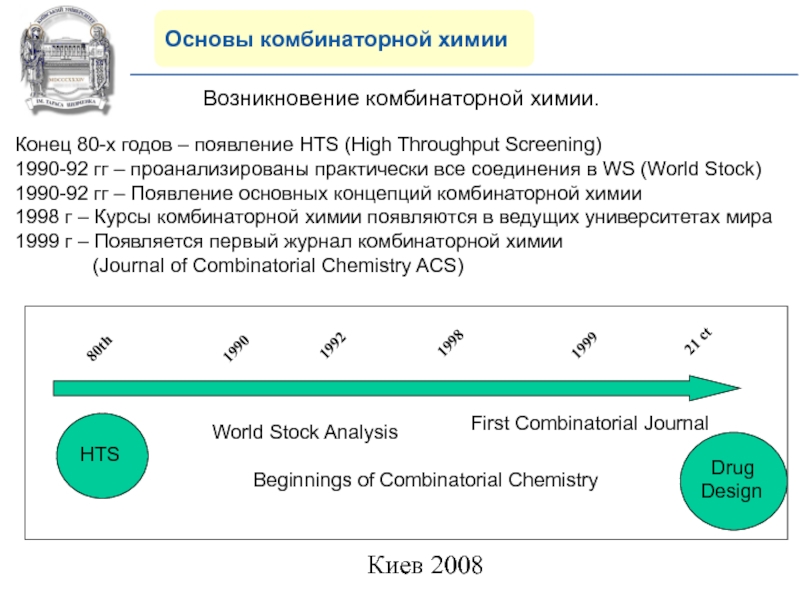
Возникновение комбинаторной химии.
Конец 80-х годов –
появление HTS (High Throughput Screening)
1990-92 гг – проанализированы практически все
соединения в WS (World Stock)1990-92 гг – Появление основных концепций комбинаторной химии
1998 г – Курсы комбинаторной химии появляются в ведущих университетах мира
1999 г – Появляется первый журнал комбинаторной химии (Journal of Combinatorial Chemistry ACS)
World Stock Analysis
Beginnings of Combinatorial Chemistry
First Combinatorial Journal
Слайд 5COMPANY PROFILE
Основы комбинаторной химии
История комбинаторной химии.
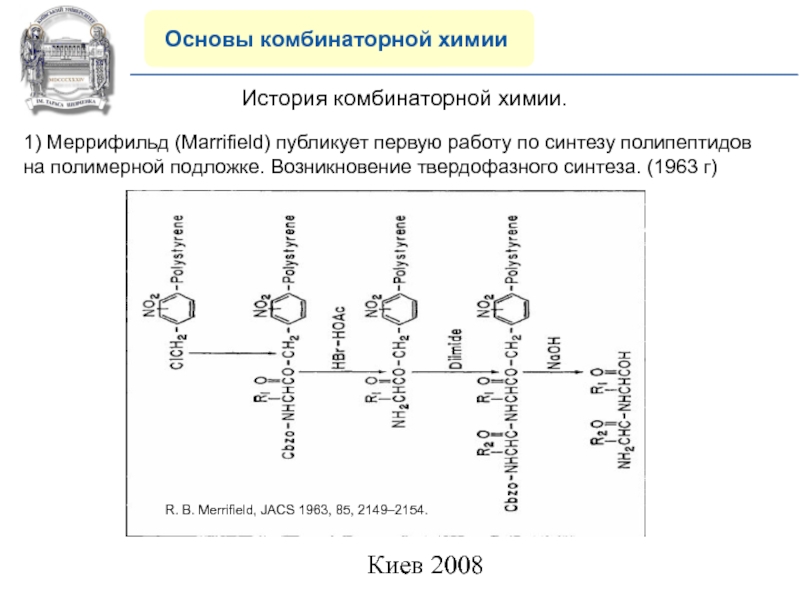
1) Меррифильд (Marrifield)
публикует первую работу по синтезу полипептидов на полимерной подложке. Возникновение
твердофазного синтеза. (1963 г)R. B. Merrifield, JACS 1963, 85, 2149–2154.
Слайд 6COMPANY PROFILE
Основы комбинаторной химии
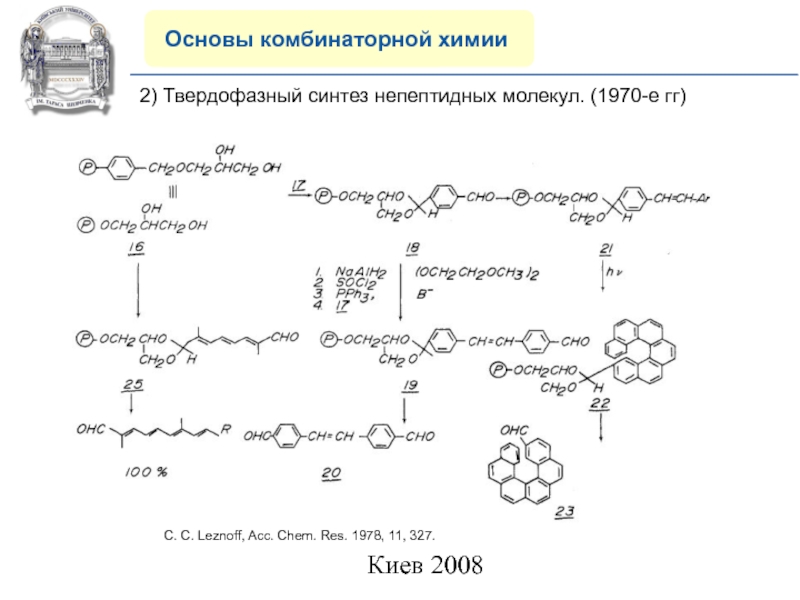
2) Твердофазный синтез непептидных молекул.
(1970-е гг)
C. C. Leznoff, Acc. Chem. Res. 1978, 11, 327.
Слайд 8COMPANY PROFILE
Основы комбинаторной химии
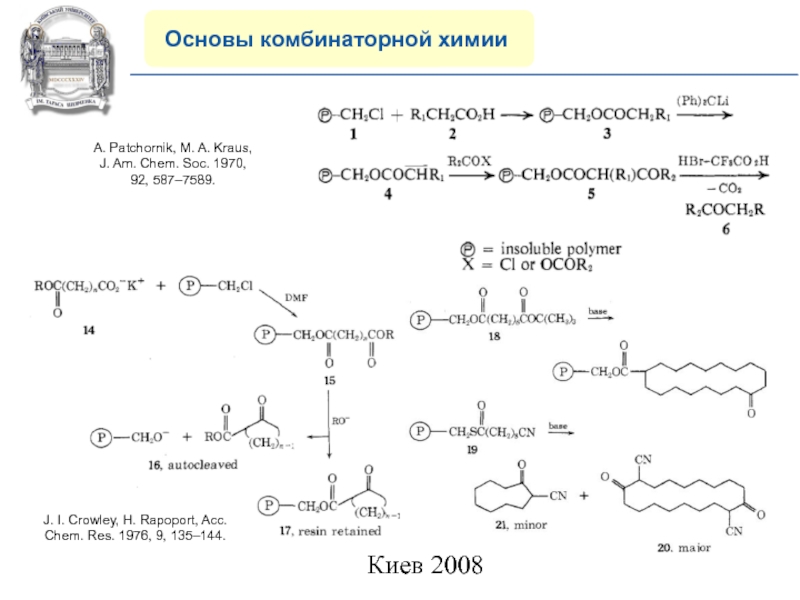
J. I. Crowley, H. Rapoport,
Acc. Chem. Res. 1976, 9, 135–144.
A. Patchornik, M. A. Kraus,
J. Am. Chem. Soc. 1970, 92, 587–7589.Слайд 9COMPANY PROFILE
Основы комбинаторной химии
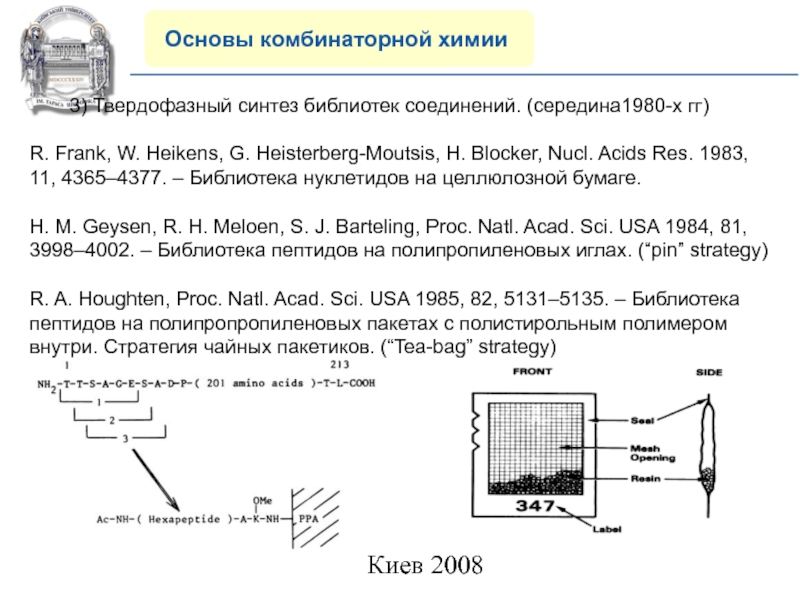
3) Твердофазный синтез библиотек соединений.
(середина1980-х гг)
R. Frank, W. Heikens, G. Heisterberg-Moutsis, H. Blocker, Nucl.
Acids Res. 1983, 11, 4365–4377. – Библиотека нуклетидов на целлюлозной бумаге.H. M. Geysen, R. H. Meloen, S. J. Barteling, Proc. Natl. Acad. Sci. USA 1984, 81, 3998–4002. – Библиотека пептидов на полипропиленовых иглах. (“pin” strategy)
R. A. Houghten, Proc. Natl. Acad. Sci. USA 1985, 82, 5131–5135. – Библиотека пептидов на полипропропиленовых пакетах с полистирольным полимером внутри. Стратегия чайных пакетиков. (“Tea-bag” strategy)
Слайд 10COMPANY PROFILE
Основы комбинаторной химии
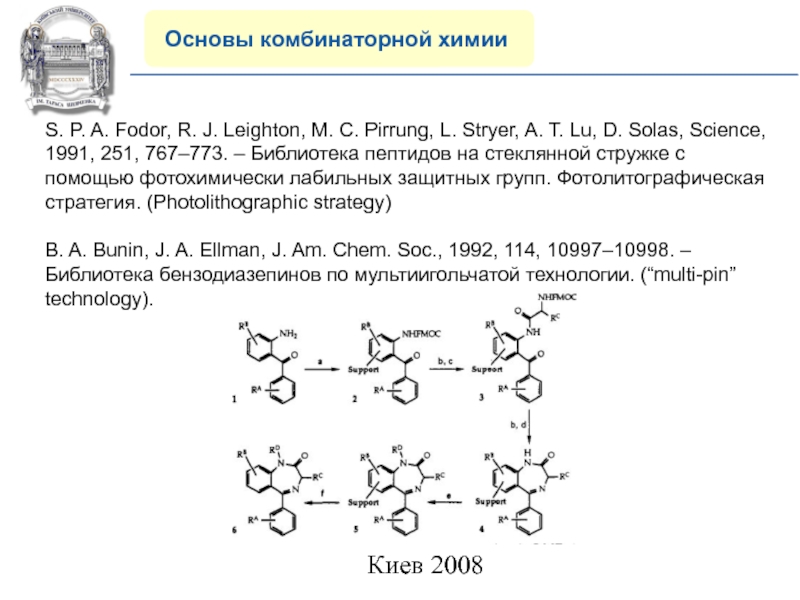
S. P. A. Fodor, R.
J. Leighton, M. C. Pirrung, L. Stryer, A. T. Lu,
D. Solas, Science, 1991, 251, 767–773. – Библиотека пептидов на стеклянной стружке с помощью фотохимически лабильных защитных групп. Фотолитографическая стратегия. (Photolithographic strategy)B. A. Bunin, J. A. Ellman, J. Am. Chem. Soc., 1992, 114, 10997–10998. – Библиотека бензодиазепинов по мультиигольчатой технологии. (“multi-pin” technology).
Слайд 11COMPANY PROFILE
Основы комбинаторной химии
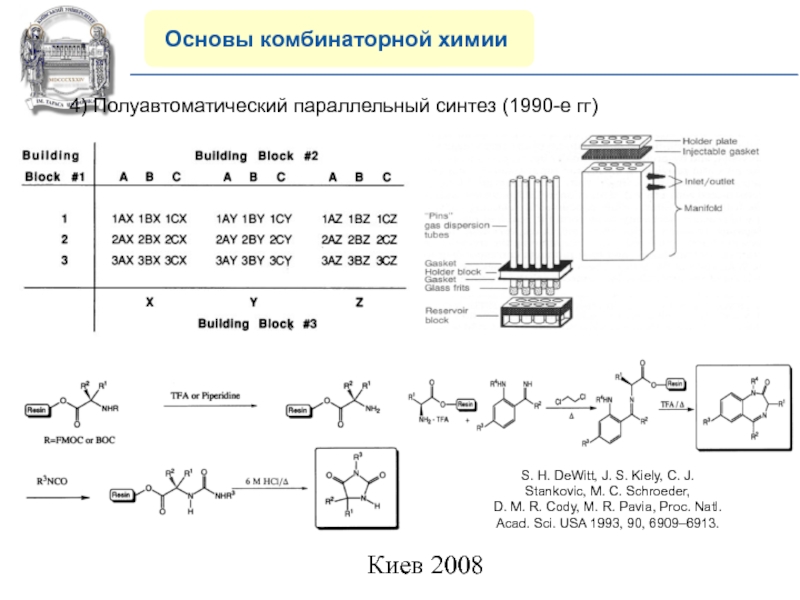
4) Полуавтоматический параллельный синтез (1990-е
гг)
S. H. DeWitt, J. S. Kiely, C. J.
Stankovic, M. C.
Schroeder,D. M. R. Cody, M. R. Pavia, Proc. Natl.
Acad. Sci. USA 1993, 90, 6909–6913.
Слайд 12COMPANY PROFILE
Основы комбинаторной химии
5) Разделительная стратегия (“Split” strategy,
or “split & pool”). (1991 г)
A. Furka, F. Sebestyen, M.
Asgedom, G. Dibo, Int. J. Peptide Prot. Res. 1991, 37, 487–493.K. S. Lam, S. E. Salmon, E. M., Hersh, V. J. Hruby, W. M. Kazmierski, R. J. Knapp, Nature, 1991, 354, 82–84.
R. A. Houghten, C. Pinilla, S. E., Blondelle, J. R., Appel, C. T. Dooley, J. H. Cuervo, Nature 1991, 354, 84–86.
Слайд 13COMPANY PROFILE
Основы комбинаторной химии
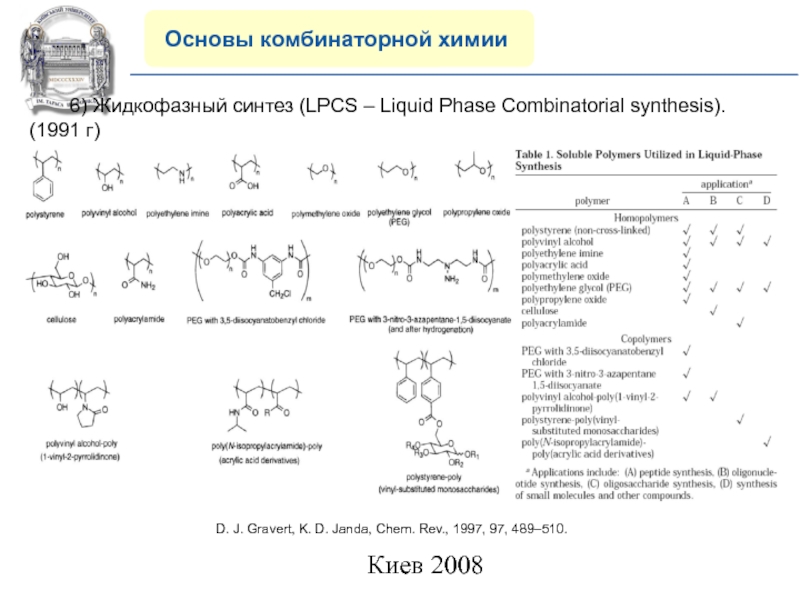
6) Жидкофазный синтез (LPCS –
Liquid Phase Combinatorial synthesis). (1991 г)
D. J. Gravert, K. D.
Janda, Chem. Rev., 1997, 97, 489–510.Слайд 14COMPANY PROFILE
Основы комбинаторной химии
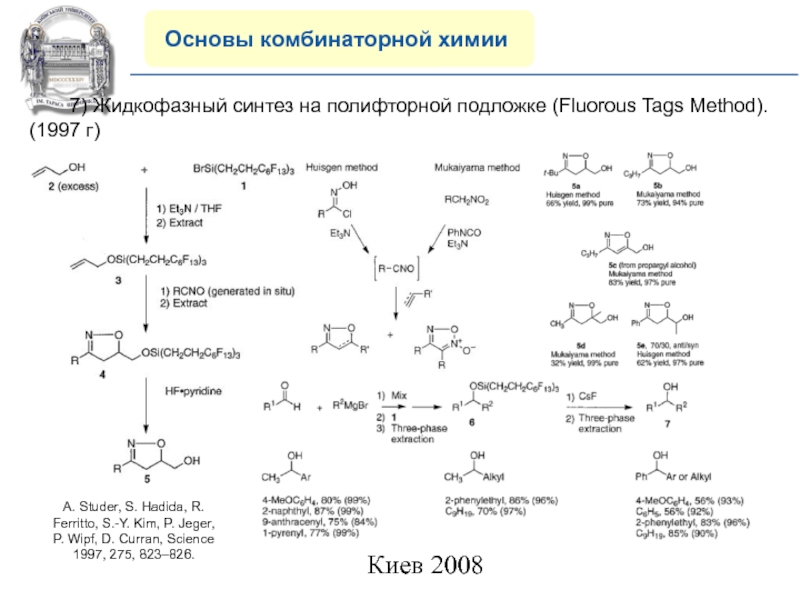
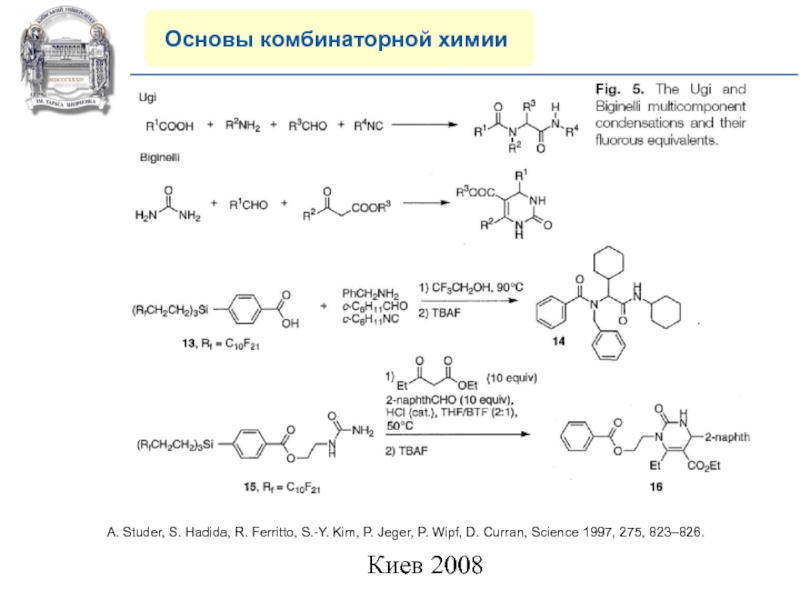
7) Жидкофазный синтез на полифторной
подложке (Fluorous Tags Method). (1997 г)
A. Studer, S. Hadida, R.
Ferritto, S.-Y. Kim, P. Jeger, P. Wipf, D. Curran, Science 1997, 275, 823–826.Слайд 15COMPANY PROFILE
Основы комбинаторной химии
A. Studer, S. Hadida, R.
Ferritto, S.-Y. Kim, P. Jeger, P. Wipf, D. Curran, Science
1997, 275, 823–826.Слайд 16COMPANY PROFILE
Основы комбинаторной химии
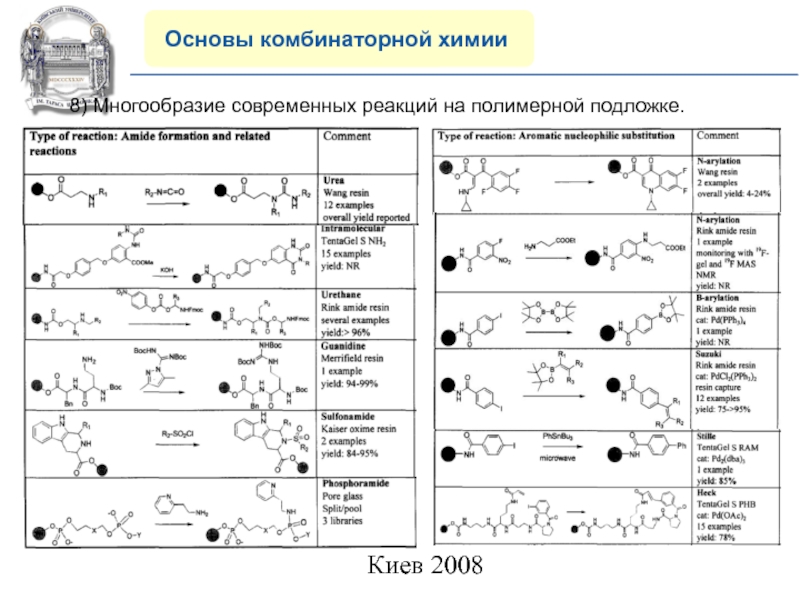
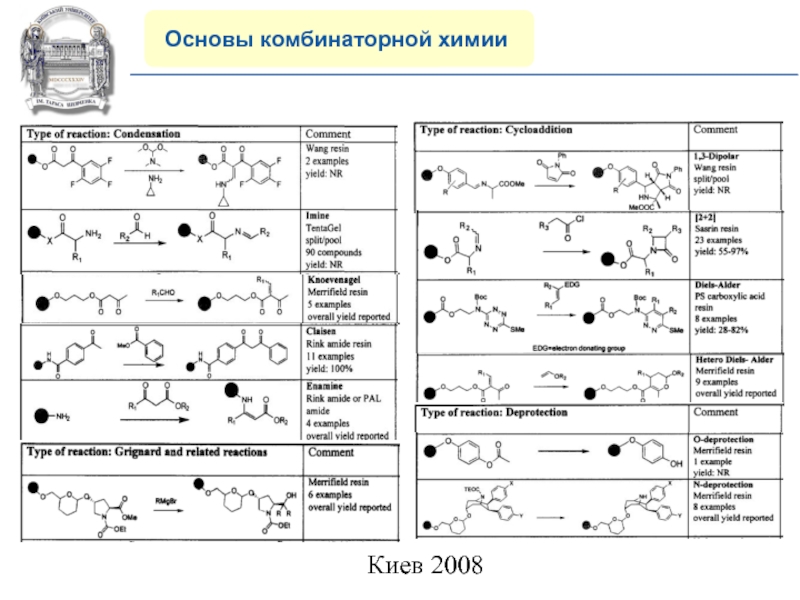
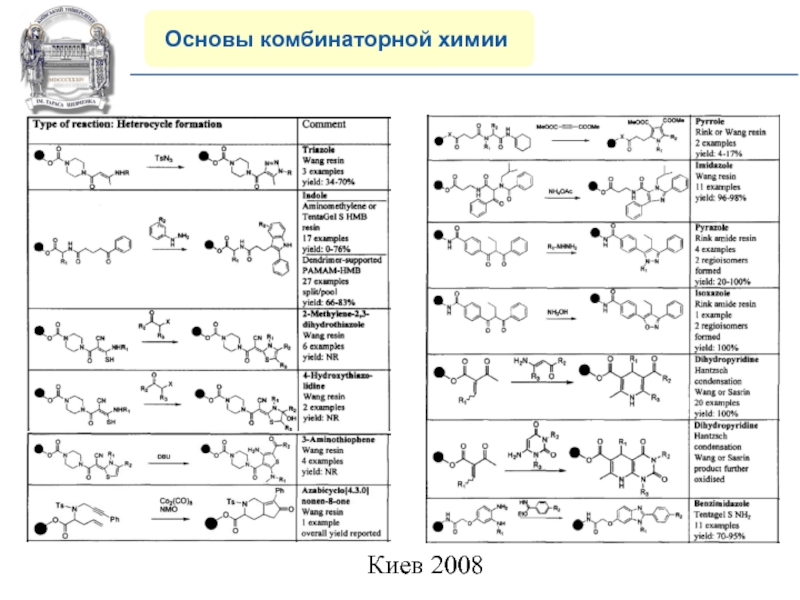
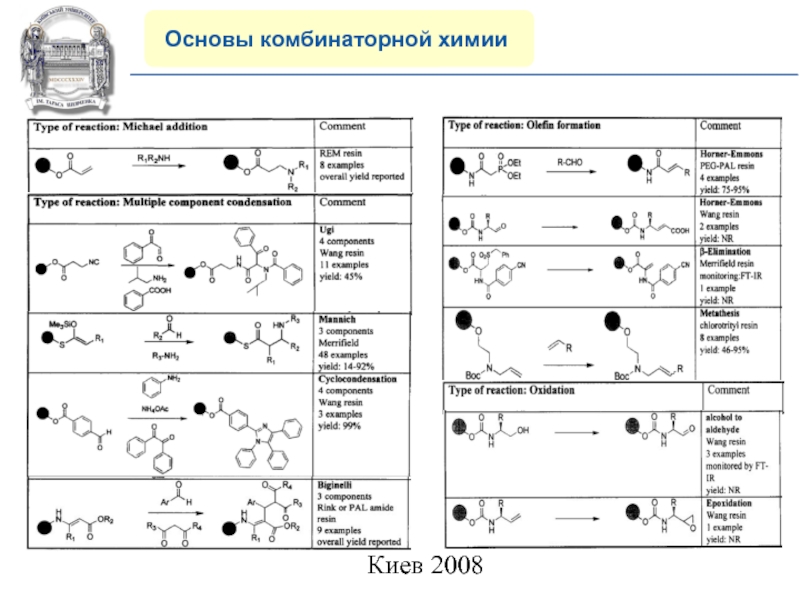
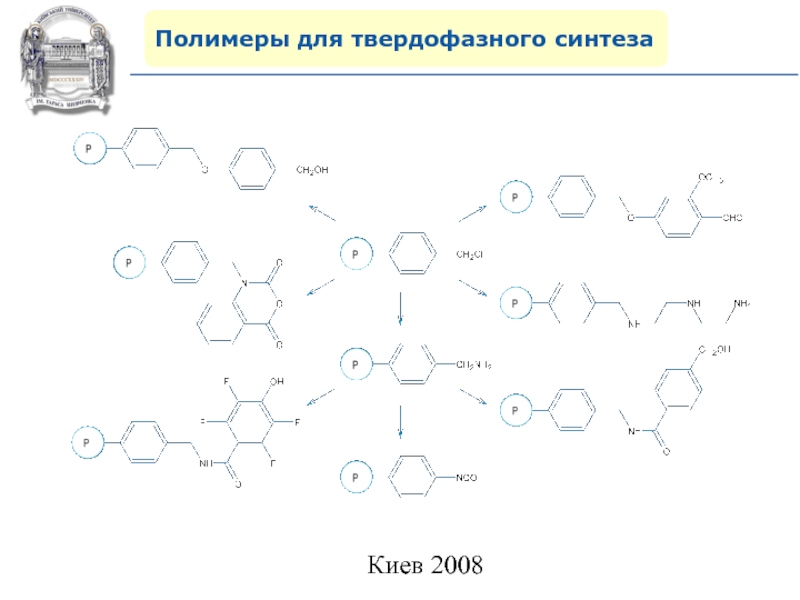
8) Многообразие современных реакций на
полимерной подложке.
Слайд 20COMPANY PROFILE
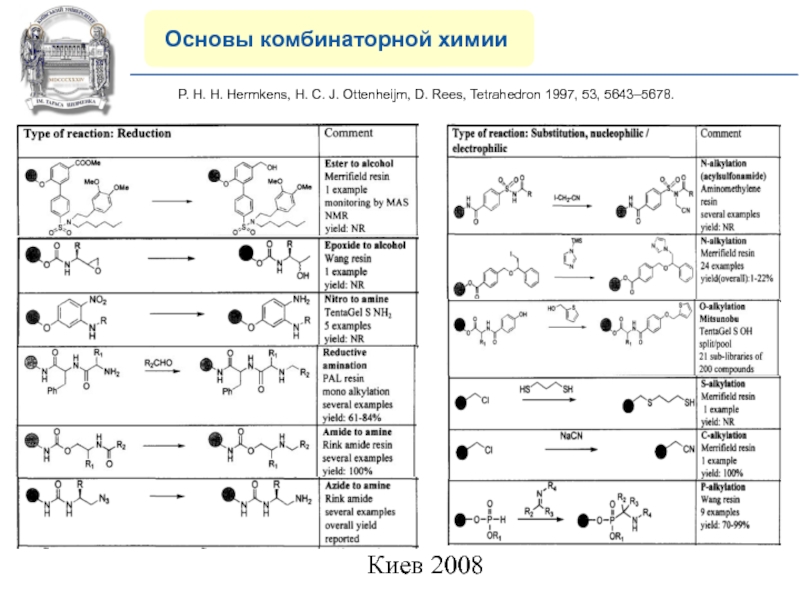
Основы комбинаторной химии
P. H. H. Hermkens, H.
C. J. Ottenheijm, D. Rees, Tetrahedron 1997, 53, 5643–5678.
Слайд 22COMPANY PROFILE
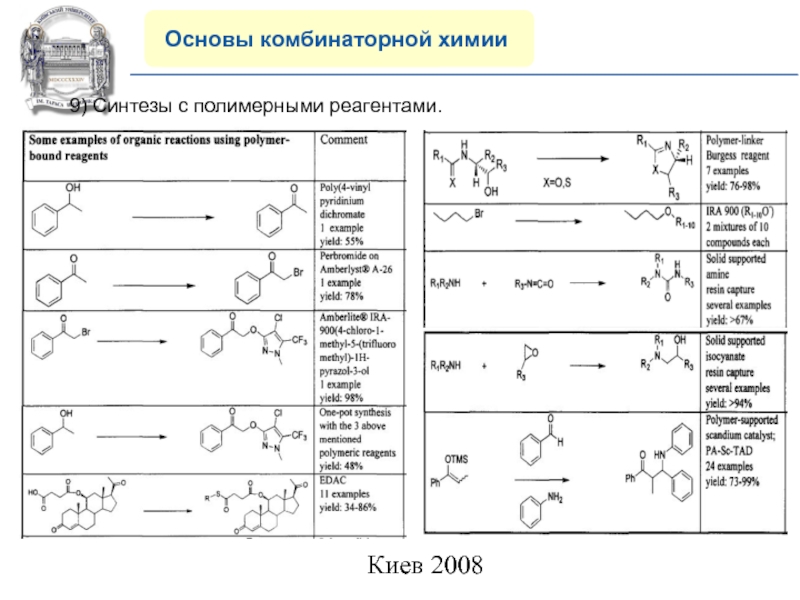
Основы комбинаторной химии
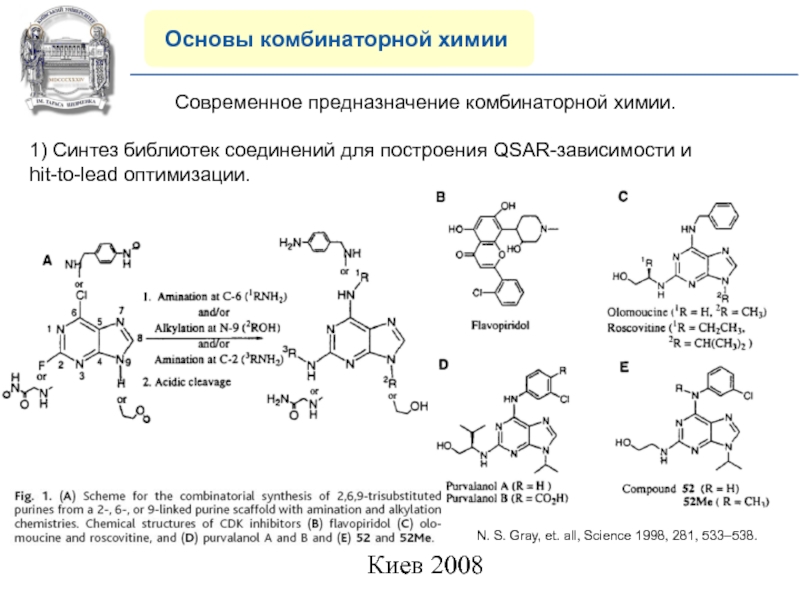
Современное предназначение комбинаторной химии.
1) Синтез библиотек соединений для построения QSAR-зависимости и hit-to-lead оптимизации.
N. S. Gray, et. all, Science 1998, 281, 533–538.
Слайд 23COMPANY PROFILE
Основы комбинаторной химии
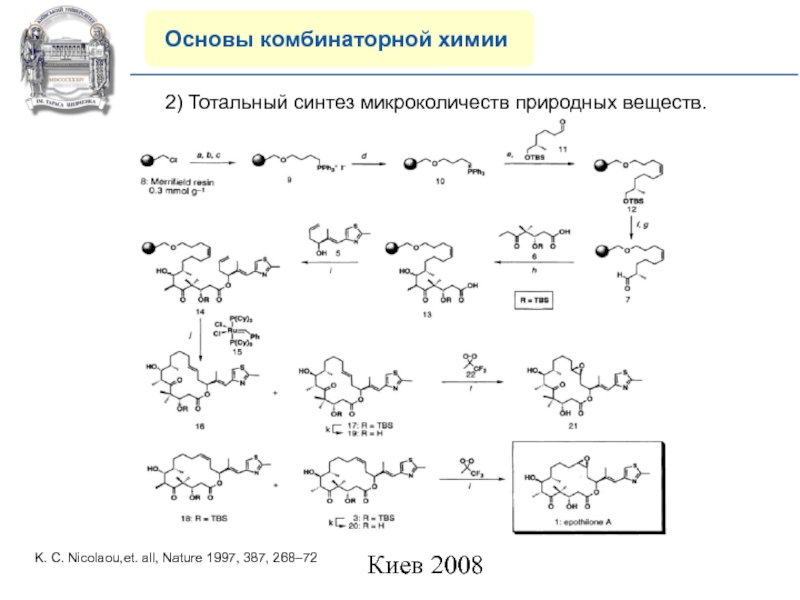
2) Тотальный синтез микроколичеств природных
веществ.
K. C. Nicolaou,et. all, Nature 1997, 387, 268–72
Слайд 24COMPANY PROFILE
Основы комбинаторной химии
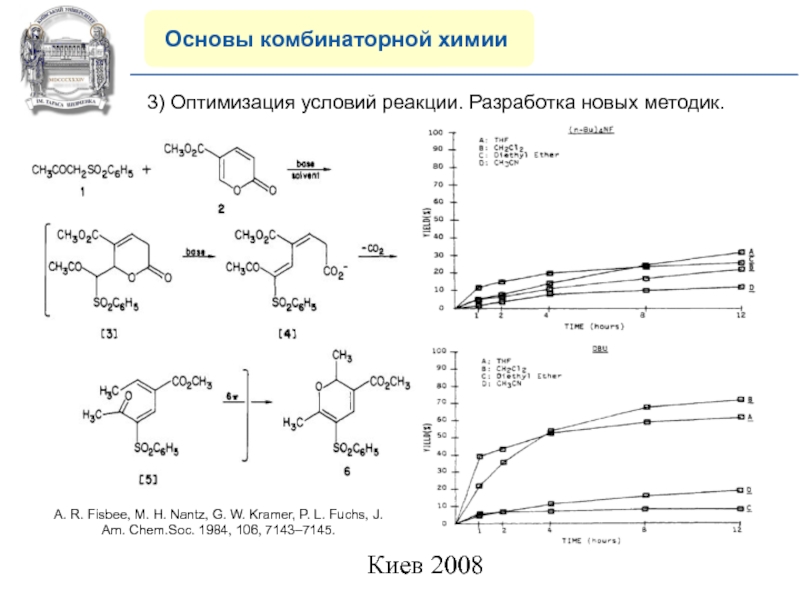
3) Оптимизация условий реакции. Разработка
новых методик.
A. R. Fisbee, M. H. Nantz, G. W. Kramer,
P. L. Fuchs, J. Am. Chem.Soc. 1984, 106, 7143–7145.Слайд 25COMPANY PROFILE
Основы комбинаторной химии
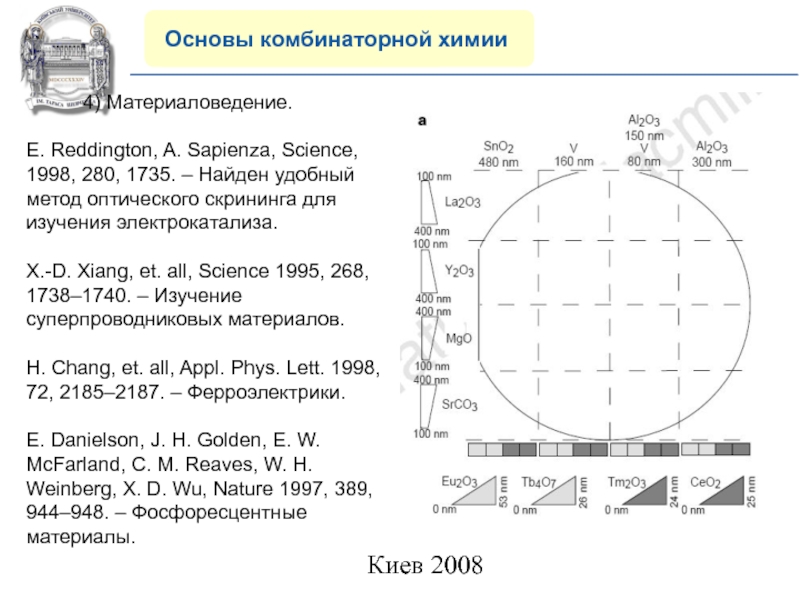
4) Материаловедение.
E. Reddington,
A. Sapienza, Science, 1998, 280, 1735. – Найден удобный метод
оптического скрининга для изучения электрокатализа.X.-D. Xiang, et. all, Science 1995, 268, 1738–1740. – Изучение суперпроводниковых материалов.
H. Chang, et. all, Appl. Phys. Lett. 1998, 72, 2185–2187. – Ферроэлектрики.
E. Danielson, J. H. Golden, E. W. McFarland, C. M. Reaves, W. H. Weinberg, X. D. Wu, Nature 1997, 389, 944–948. – Фосфоресцентные материалы.
Слайд 26COMPANY PROFILE
Основы комбинаторной химии
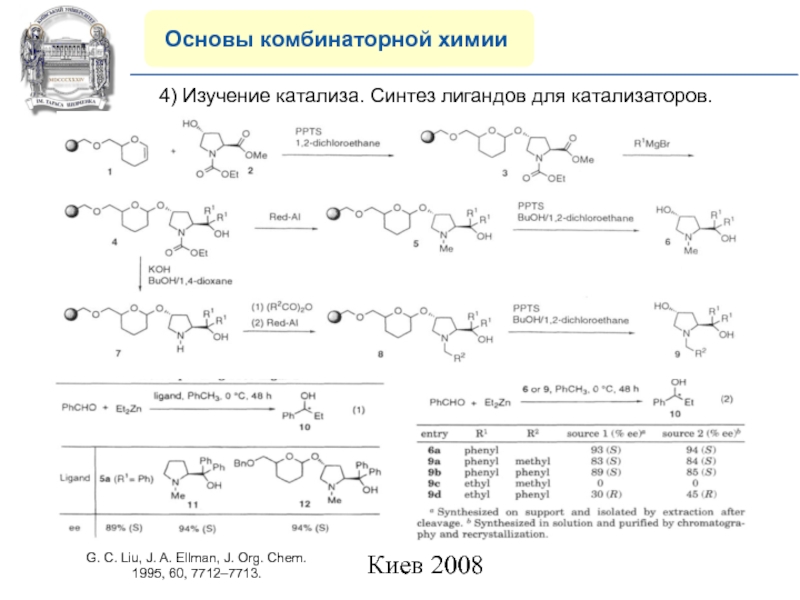
4) Изучение катализа. Синтез лигандов
для катализаторов.
G. C. Liu, J. A. Ellman, J. Org. Chem.
1995, 60, 7712–7713.Слайд 27COMPANY PROFILE
Основы комбинаторной химии
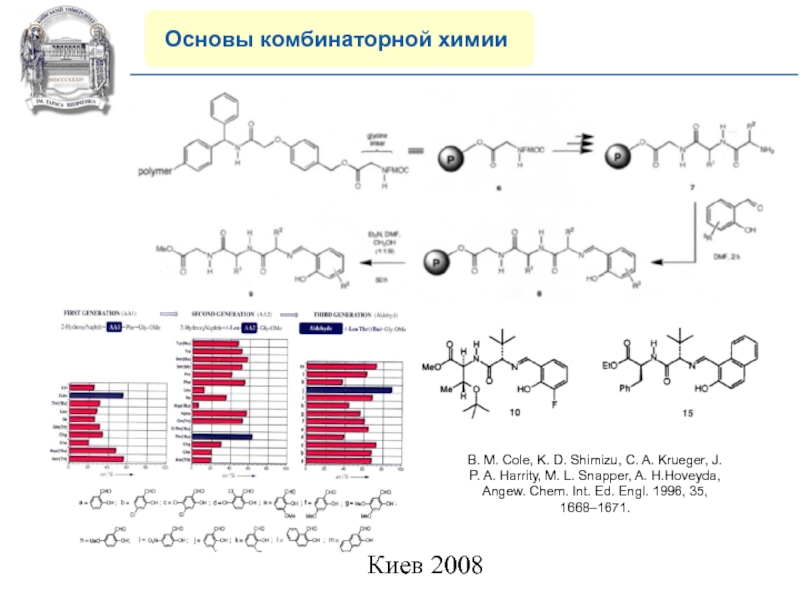
B. M. Cole, K. D.
Shimizu, C. A. Krueger, J. P. A. Harrity, M. L.
Snapper, A. H.Hoveyda, Angew. Chem. Int. Ed. Engl. 1996, 35, 1668–1671.Слайд 28COMPANY PROFILE
Основы комбинаторной химии
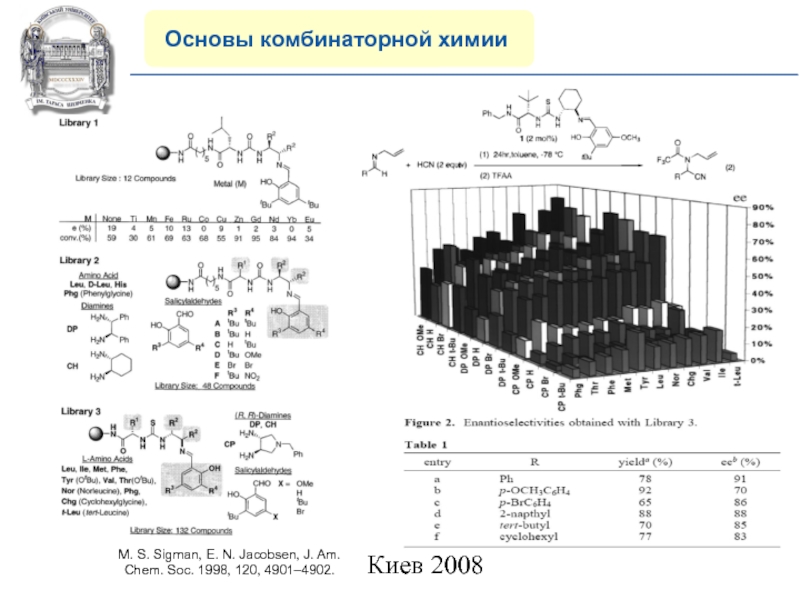
M. S. Sigman, E. N.
Jacobsen, J. Am.
Chem. Soc. 1998, 120, 4901–4902.
Слайд 31Ключевые положения комбинаторной химии
1. Синтез серии соединений одновременно гораздо более
эффективен чем синтез одного вещества.
2. Любая синтетическая схема может быть
превращена в такую, что ведет к образованию библиотеки веществ (комбинаторную), посредством замены одного (или нескольких) реагентов на их серии.10 диенов (А) + 10 диенофилов (В) = 10х10 = 100 аддуктов Дильса-Альдера
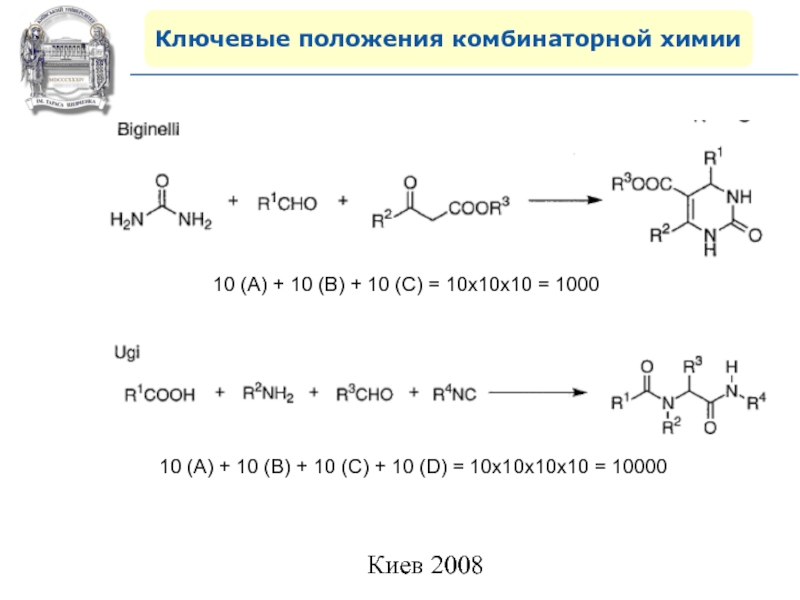
Слайд 32Ключевые положения комбинаторной химии
10 (А) + 10 (В) + 10
(С) = 10х10х10 = 1000
10 (А) + 10 (В) +
10 (С) + 10 (D) = 10х10х10x10 = 10000Слайд 33Ключевые положения комбинаторной химии
3. Качественный дизайн продуктов синтеза критичен.
Большой
набор соединений не компенсирует плохого дизайна.
4. Производительность “классической” органической химии
может быть значительно увеличена заменяя последовательную обработку синтезов параллельной.5. Лабораторная автоматизация, робототехника и мультизадачное химическое оборудование являются неотъемлемой частью комбинаторной химии.
6. Разумный синтетический путь обязан гарантировать желательный результат.
7. Эффективная электронная система контроля синтезов – необходимая часть комбинаторной химии.
Слайд 34Ключевые положения комбинаторной химии
8. Анализ структуры и контроль качества настолько
же важны для комбинаторной химии, как и для любой другой,
однако время в данном случае становится критичным.9. Поскольку цель комбинаторной химии состоит в том, чтобы облегчить открытие новых соединений с полезными свойствами, комбинаторные синтезы должны быть воспроизводимыми и масштабируемыми. 10. Комбинаторная химия - увеличивающий производительность инструмент для химиков, занятых в фармацевтических и агрохимических исследованиях, изучении катализа, материаловедении, то есть в любой области химии, где получение и тестирование новых соединений - существенный элемент открытия.
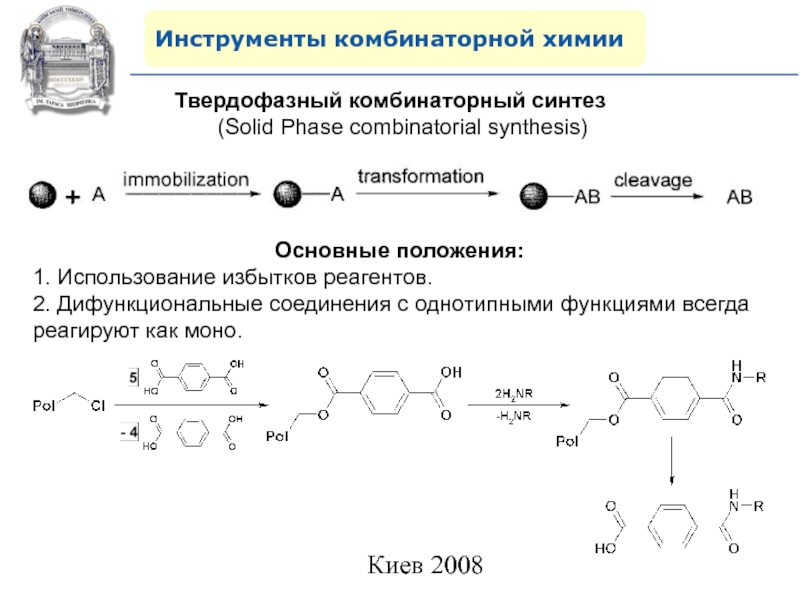
Слайд 35Инструменты комбинаторной химии
Твердофазный комбинаторный синтез
(Solid Phase
combinatorial synthesis)
Основные положения:
1. Использование избытков реагентов.
2. Дифункциональные соединения с однотипными
функциями всегда реагируют как моно.Слайд 36Инструменты комбинаторной химии
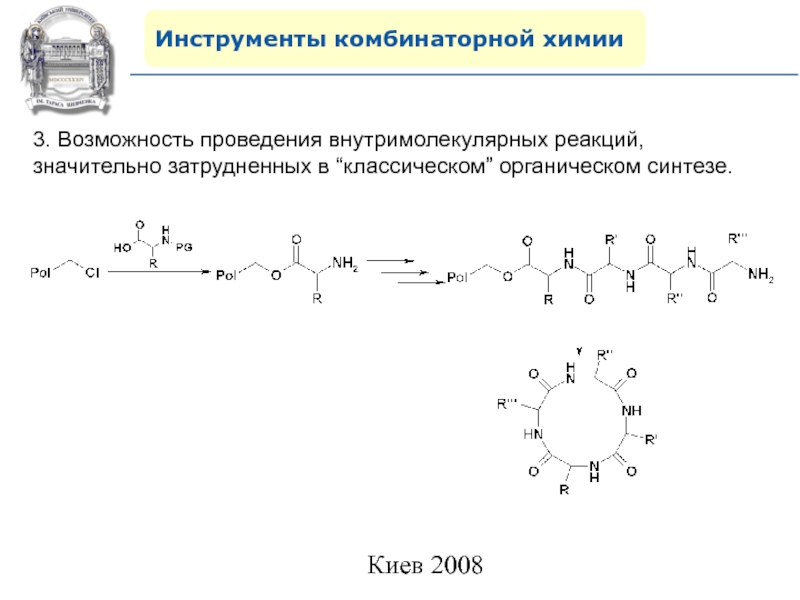
3. Возможность проведения внутримолекулярных реакций, значительно затрудненных в
“классическом” органическом синтезе.
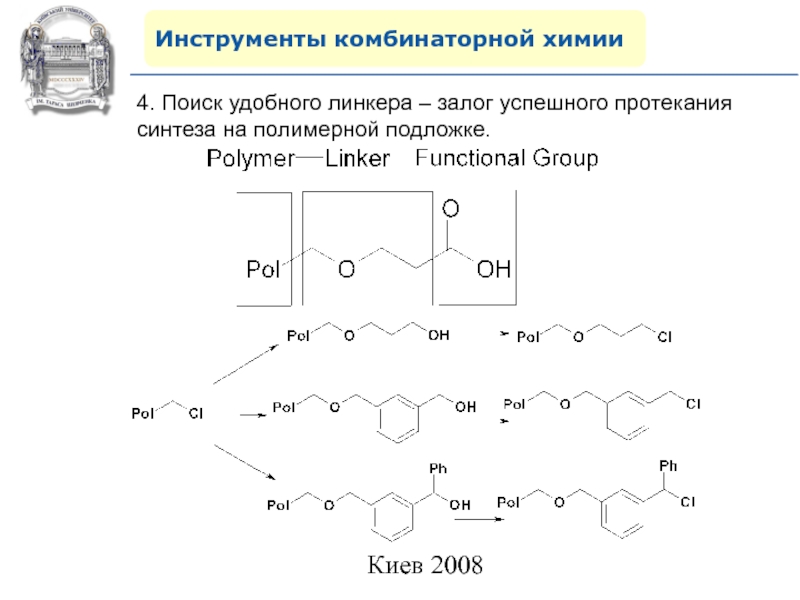
Слайд 37Инструменты комбинаторной химии
4. Поиск удобного линкера – залог успешного протекания
синтеза на полимерной подложке.
Слайд 39Инструменты комбинаторной химии
5. Набор растворителей пригодный для твердофазного синтеза ограничен,
и зависит от типа полимера.
6. Диапазон температур комфортный для проведения
твердофазных реакций 20ºС - 90ºС7. В твердофазном синтезе эффективна только одна твердая фаза.
8. Анализ веществ на полимерной подложке сильно затруднен.
Слайд 40Инструменты комбинаторной химии
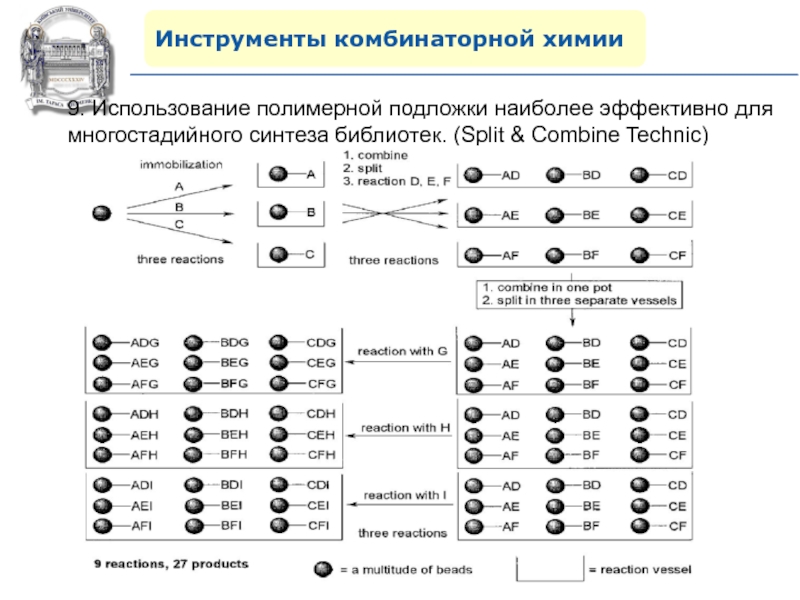
9. Использование полимерной подложки наиболее эффективно для многостадийного
синтеза библиотек. (Split & Combine Technic)
Слайд 41Инструменты комбинаторной химии
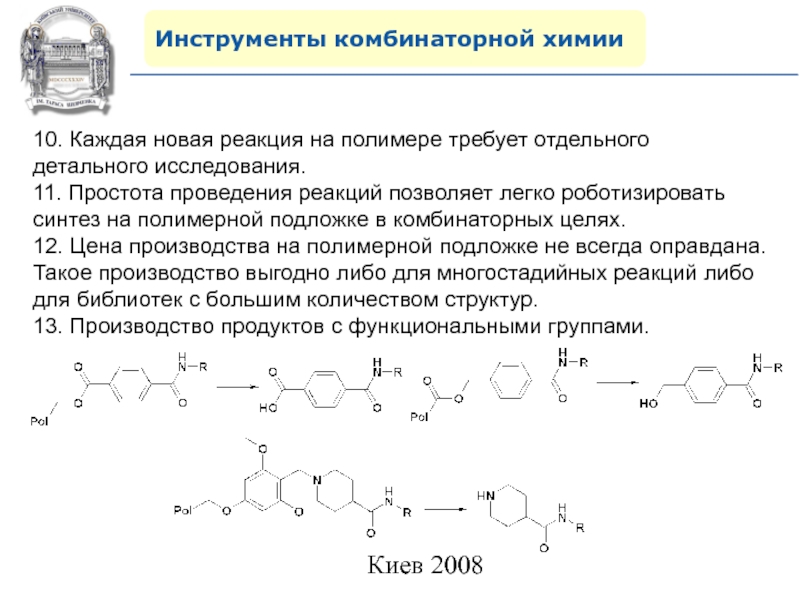
10. Каждая новая реакция на полимере требует отдельного
детального исследования.
11. Простота проведения реакций позволяет легко роботизировать синтез на
полимерной подложке в комбинаторных целях.12. Цена производства на полимерной подложке не всегда оправдана. Такое производство выгодно либо для многостадийных реакций либо для библиотек с большим количеством структур.
13. Производство продуктов с функциональными группами.
Слайд 42Инструменты комбинаторной химии
Комбинаторный синтез в растворе
(Solution Phase Combinatorial Synthesis)
Основные положения:
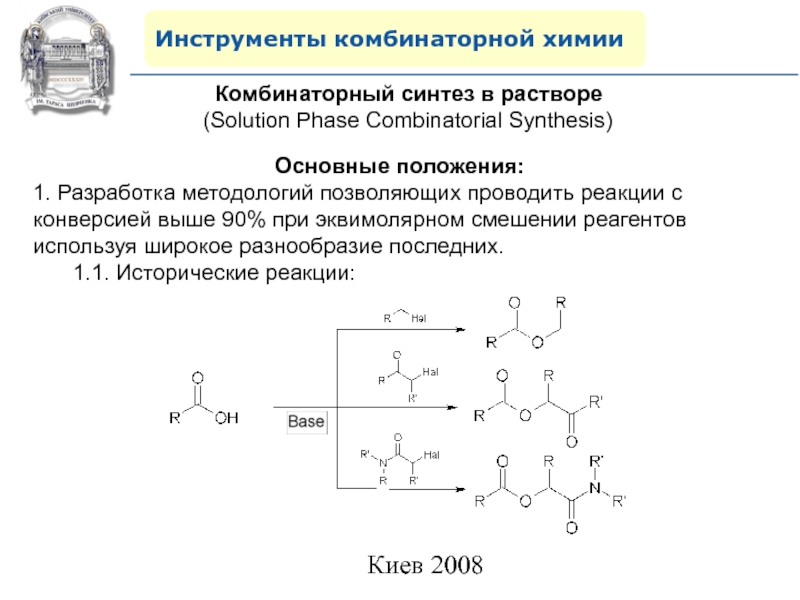
1. Разработка методологий позволяющих проводить реакции с конверсией выше
90% при эквимолярном смешении реагентов используя широкое разнообразие последних.1.1. Исторические реакции:
Слайд 43Инструменты комбинаторной химии
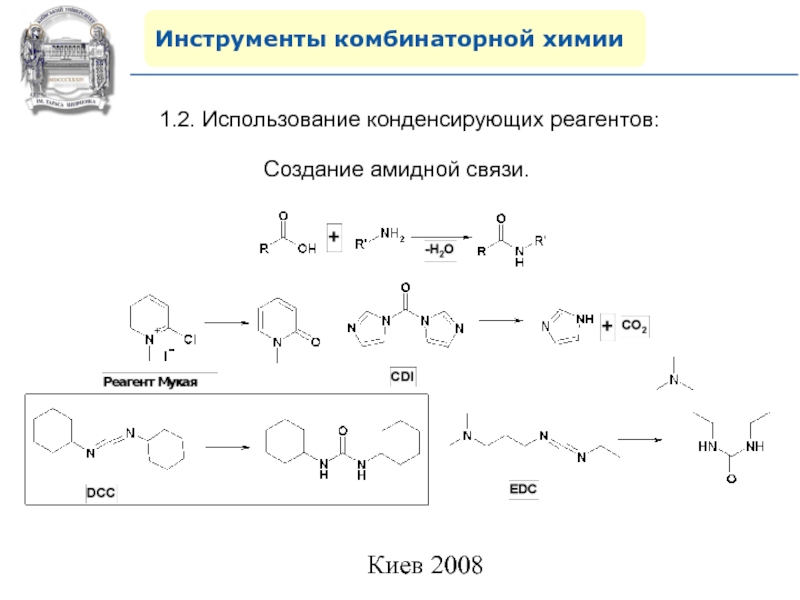
1.2. Использование конденсирующих реагентов:
Создание амидной связи.
Слайд 44Инструменты комбинаторной химии
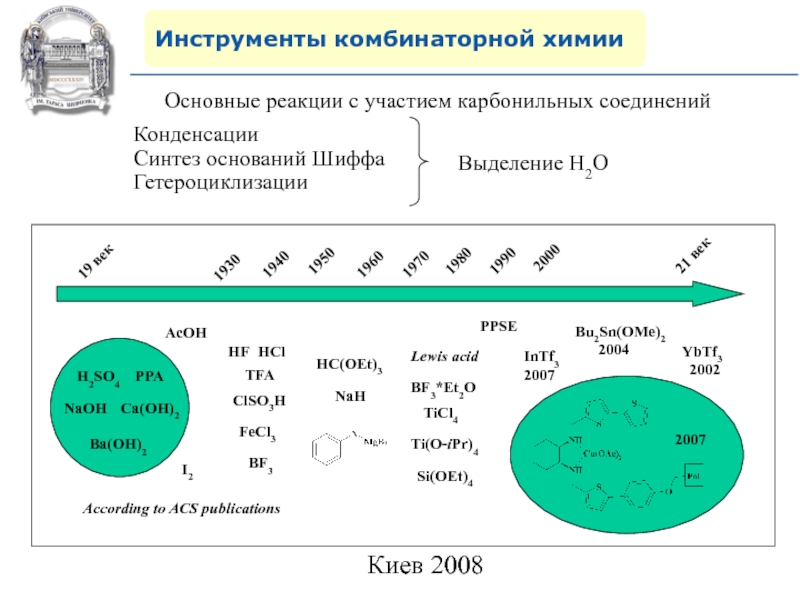
Основные реакции с участием карбонильных соединений
Конденсации
Синтез оснований Шиффа
Гетероциклизации
Выделение
Слайд 45Инструменты комбинаторной химии
устойчивость к действию воздуха и устойчивость во времени
при хранении и использовании
легкая доступность
широкие границы применения
возможность использования в смеси
с органическими растворителя-ми и другими реагентамивысокая активность при нормальных условиях и возможность использования при повышенной температуре
простая и удобная синтетическая процедура применения
высокая хемоселективность и степень конверсии
удобная процедура очистки целевых продуктов от избытка реагента и продуктов его модификации
Современные критерии поиска новых конденсирующих реагентов для комбинаторного синтеза
Слайд 46Инструменты комбинаторной химии
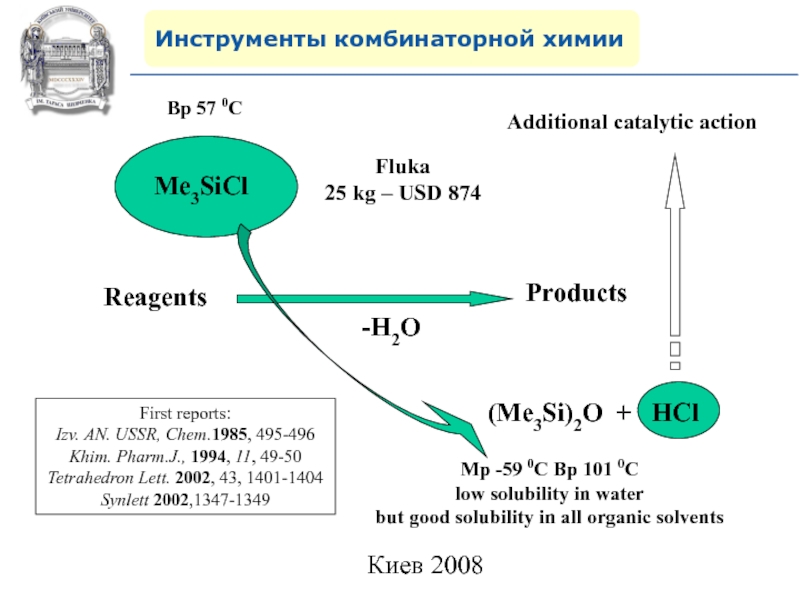
Reagents
Products
-H2O
Me3SiCl
First reports:
Izv. АN. USSR, Chem.1985, 495-496
Khim. Pharm.J., 1994,
11, 49-50
Tetrahedron Lett. 2002, 43, 1401-1404
Synlett 2002,1347-1349
Слайд 47Инструменты комбинаторной химии
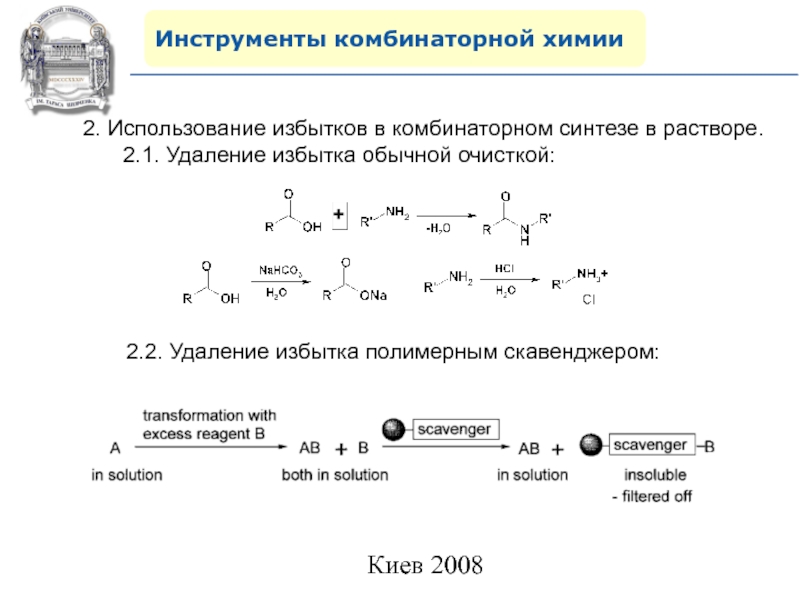
2. Использование избытков в комбинаторном синтезе в растворе.
2.1.
Удаление избытка обычной очисткой:
2.2. Удаление избытка полимерным скавенджером:
Слайд 49Инструменты комбинаторной химии
3. Использование реагентов на полимерной основе.
4. Полифторная подложка.
Слайд 50Полимеры для твердофазного синтеза
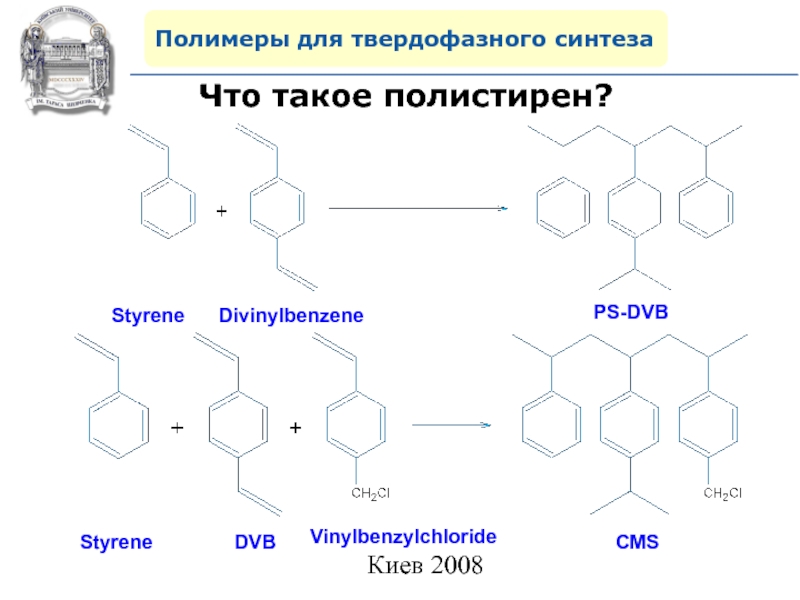
Что такое полистирен?
Styrene
Divinylbenzene
PS-DVB
Styrene
DVB
Vinylbenzylchloride
CMS
Слайд 51Полимеры для твердофазного синтеза
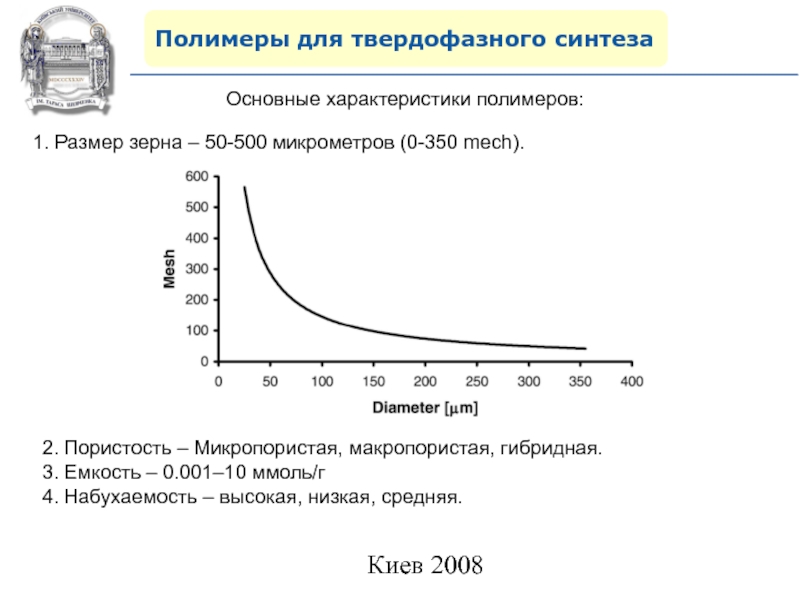
Основные характеристики полимеров:
1. Размер зерна – 50-500
микрометров (0-350 mech).
2. Пористость – Микропористая, макропористая, гибридная.
3. Емкость –
0.001–10 ммоль/г4. Набухаемость – высокая, низкая, средняя.
Слайд 52Полимеры для твердофазного синтеза
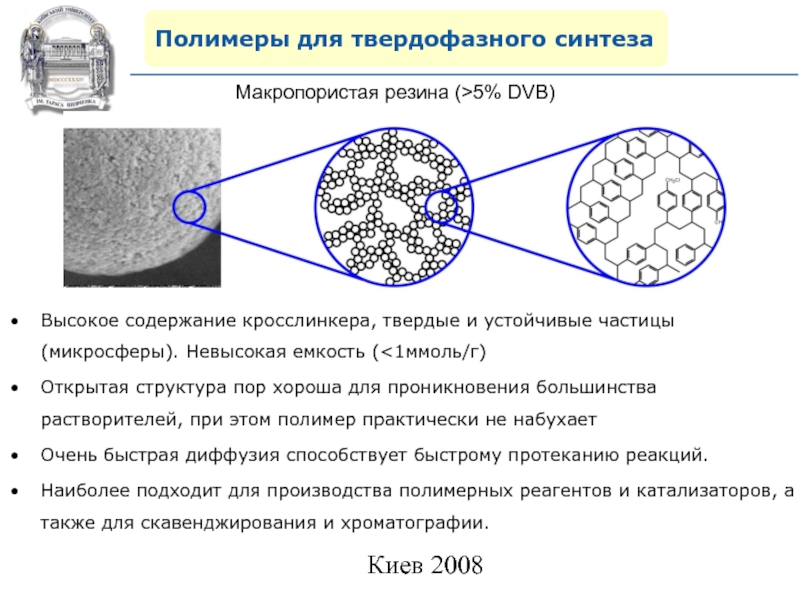
Макропористая резина (>5% DVB)
Высокое содержание кросслинкера, твердые
и устойчивые частицы (микросферы). Невысокая емкость (
для проникновения большинства растворителей, при этом полимер практически не набухаетОчень быстрая диффузия способствует быстрому протеканию реакций.
Наиболее подходит для производства полимерных реагентов и катализаторов, а также для скавенджирования и хроматографии.
Слайд 53Полимеры для твердофазного синтеза
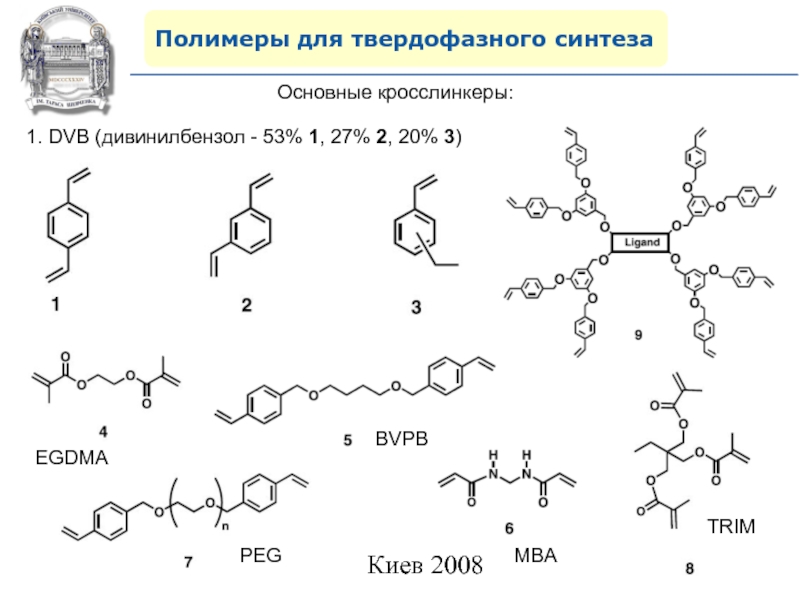
Основные кросслинкеры:
1. DVB (дивинилбензол - 53% 1,
27% 2, 20% 3)
EGDMA
PEG
MBA
BVPB
TRIM
Слайд 54Полимеры для твердофазного синтеза
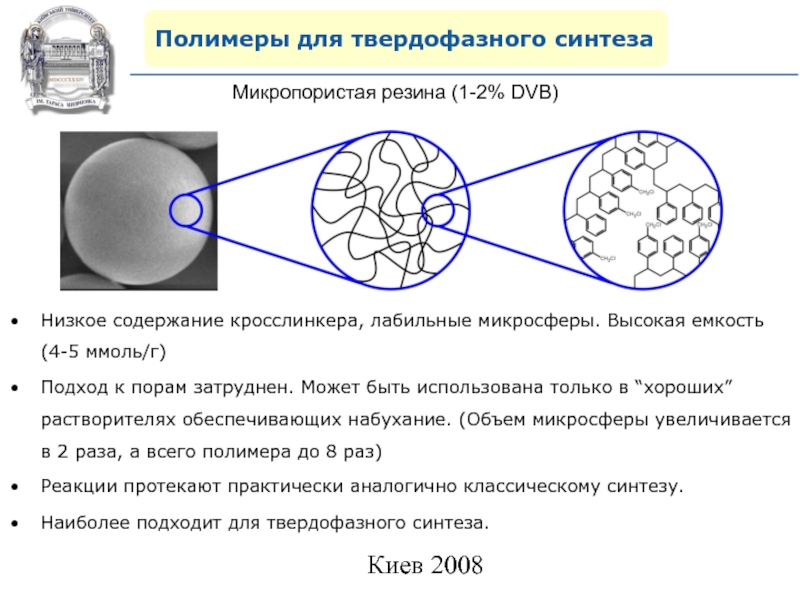
Микропористая резина (1-2% DVB)
Низкое содержание кросслинкера, лабильные
микросферы. Высокая емкость (4-5 ммоль/г)
Подход к порам затруднен. Может быть
использована только в “хороших” растворителях обеспечивающих набухание. (Объем микросферы увеличивается в 2 раза, а всего полимера до 8 раз)Реакции протекают практически аналогично классическому синтезу.
Наиболее подходит для твердофазного синтеза.
Слайд 55Полимеры для твердофазного синтеза
Физические свойства
a) Обработка ТГФ, фильтрование и осушка
на воздухе.
b) давление 100 атм.
c) Перемешивание на магнитной мешалке (24
ч, 300 об/мин, 20 C, DMF)d) Механическое перемешивание (7 дн, 60 об/мин, 20 C, DMF)
Слайд 56Полимеры для твердофазного синтеза
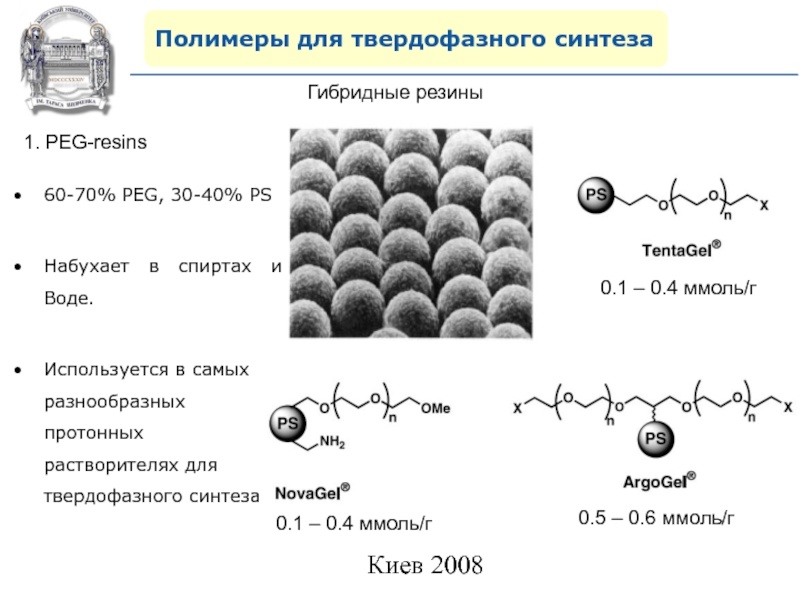
Гибридные резины
1. PEG-resins
0.1 – 0.4 ммоль/г
0.1 –
0.4 ммоль/г
0.5 – 0.6 ммоль/г
60-70% PEG, 30-40% PS
Набухает в спиртах
и Воде.Используется в самых разнообразных протонных растворителях для твердофазного синтеза
Слайд 57Полимеры для твердофазного синтеза
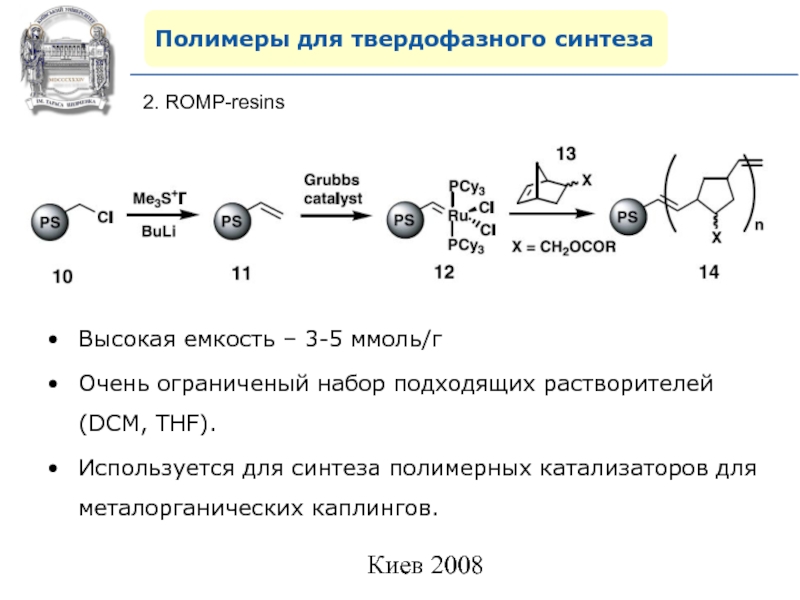
2. ROMP-resins
Высокая емкость – 3-5 ммоль/г
Очень ограниченый
набор подходящих растворителей (DCM, THF).
Используется для синтеза полимерных катализаторов для
металорганических каплингов.Слайд 58Полимеры для твердофазного синтеза
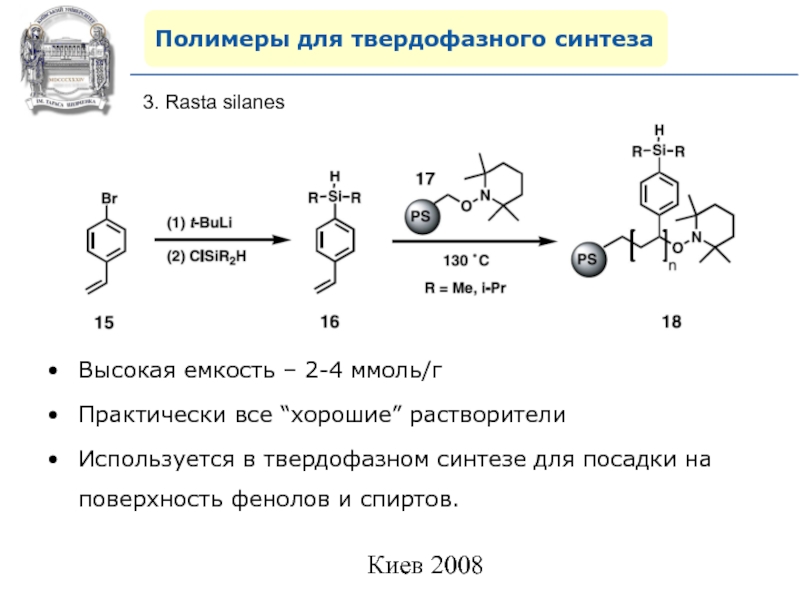
3. Rasta silanes
Высокая емкость – 2-4 ммоль/г
Практически
все “хорошие” растворители
Используется в твердофазном синтезе для посадки на поверхность
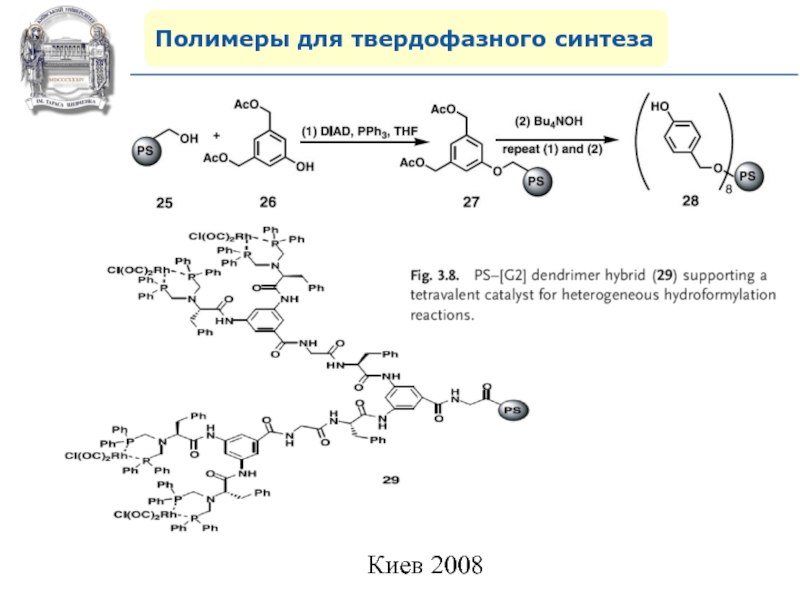
фенолов и спиртов.Слайд 62Полимеры для твердофазного синтеза
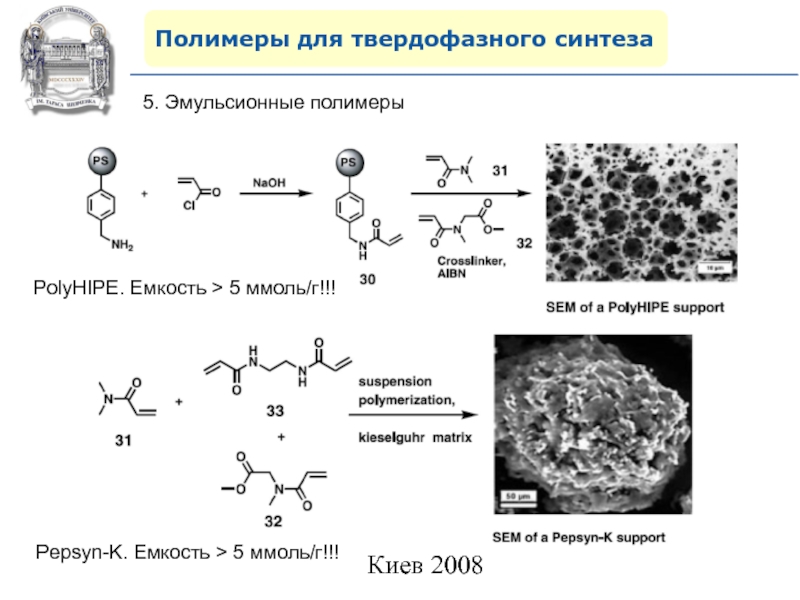
5. Эмульсионные полимеры
PolyHIPE. Емкость > 5 ммоль/г!!!
Pepsyn-K.
Емкость > 5 ммоль/г!!!
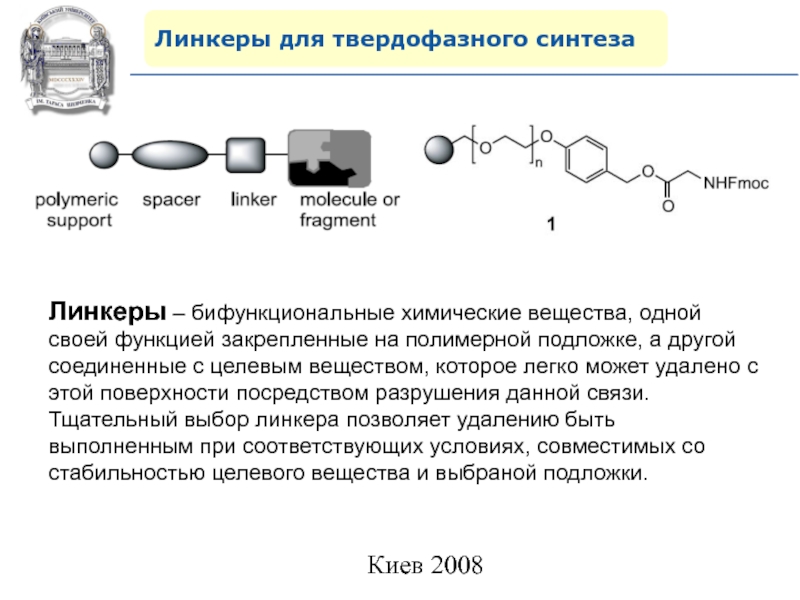
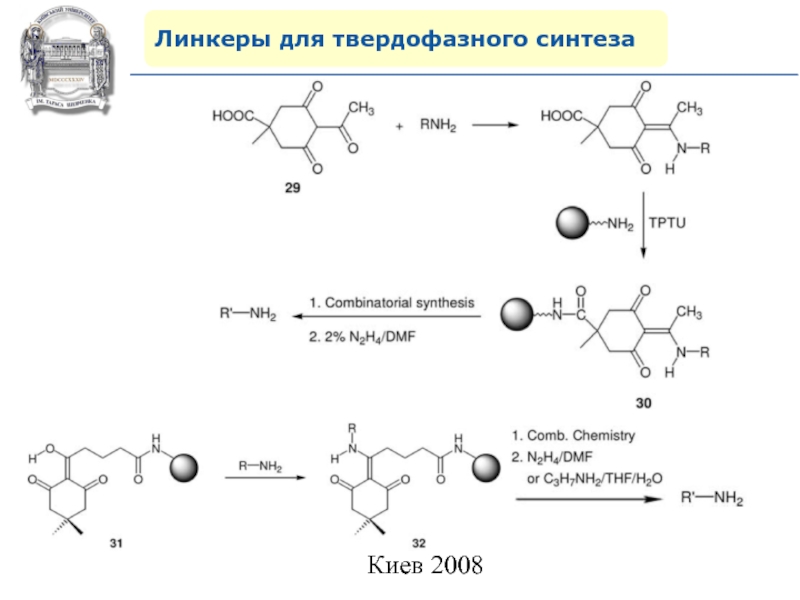
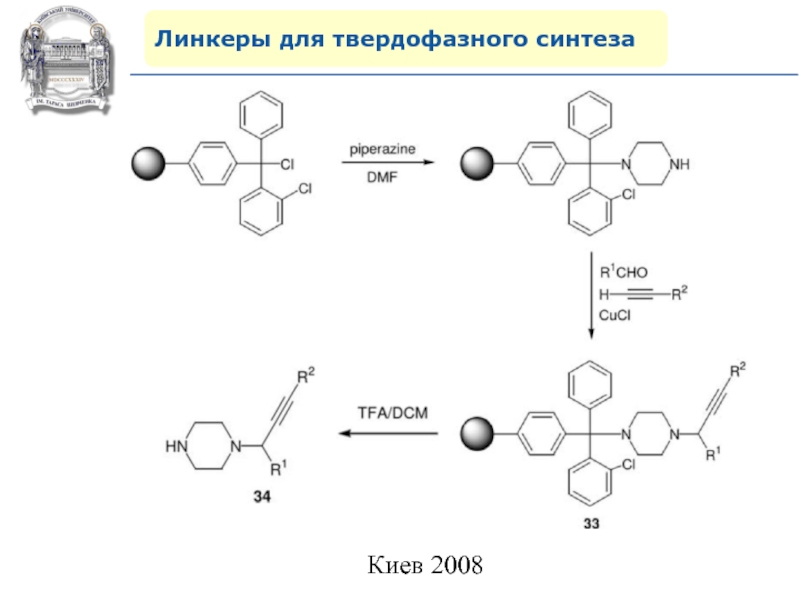
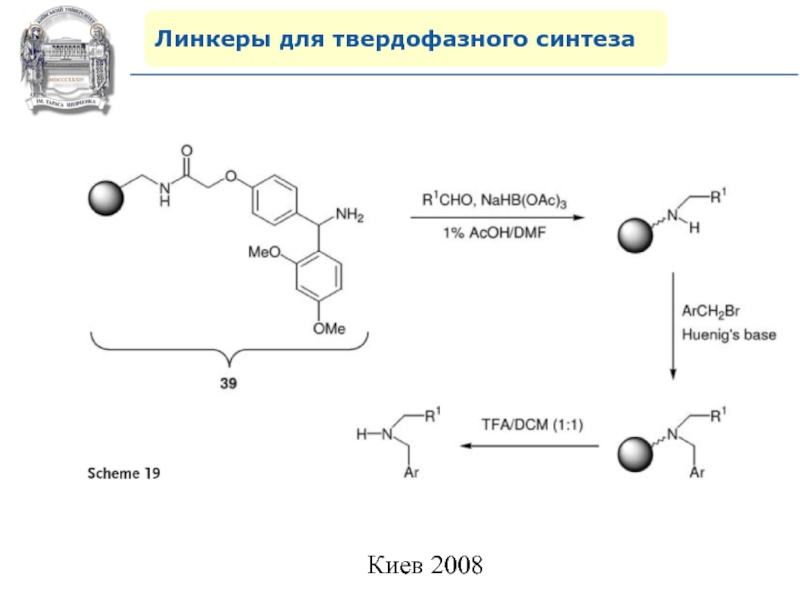
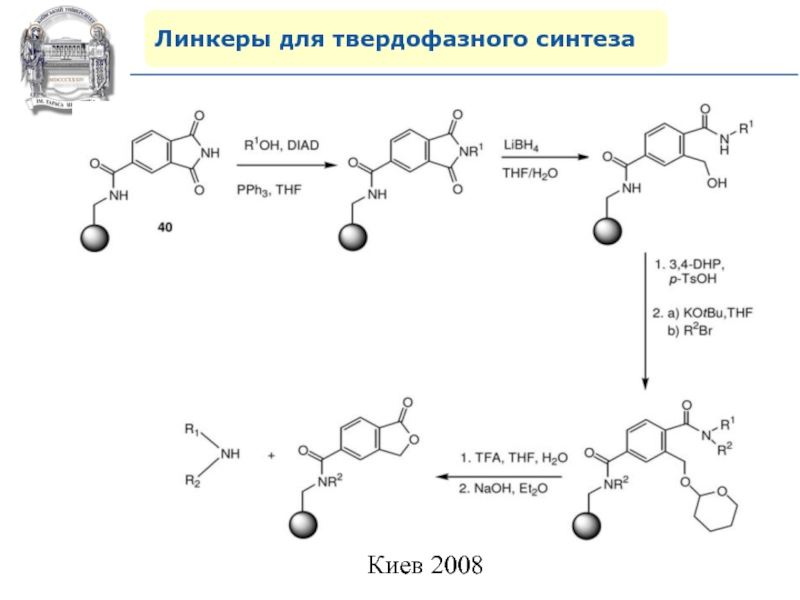
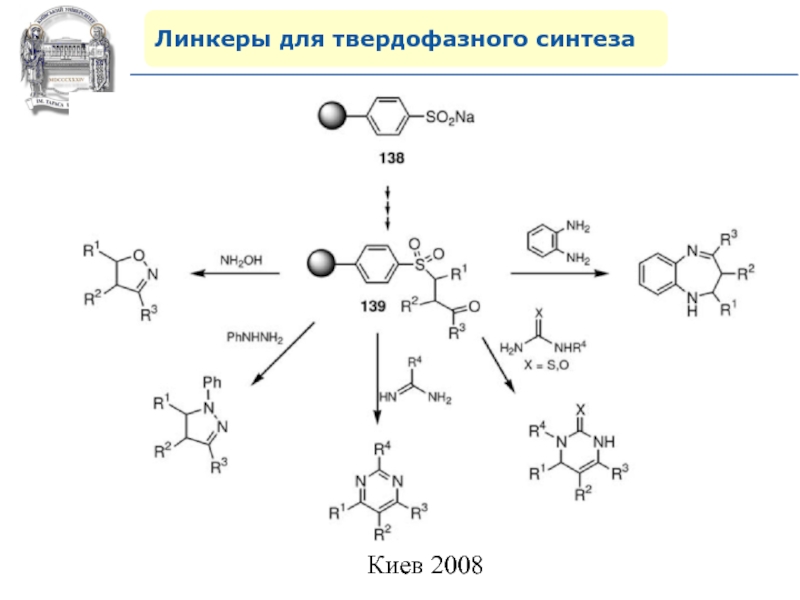
Слайд 64Линкеры для твердофазного синтеза
Линкеры – бифункциональные химические вещества, одной своей
функцией закрепленные на полимерной подложке, а другой соединенные с целевым
веществом, которое легко может удалено с этой поверхности посредством разрушения данной связи. Тщательный выбор линкера позволяет удалению быть выполненным при соответствующих условиях, совместимых со стабильностью целевого вещества и выбраной подложки.Слайд 87Молекулярное моделирование
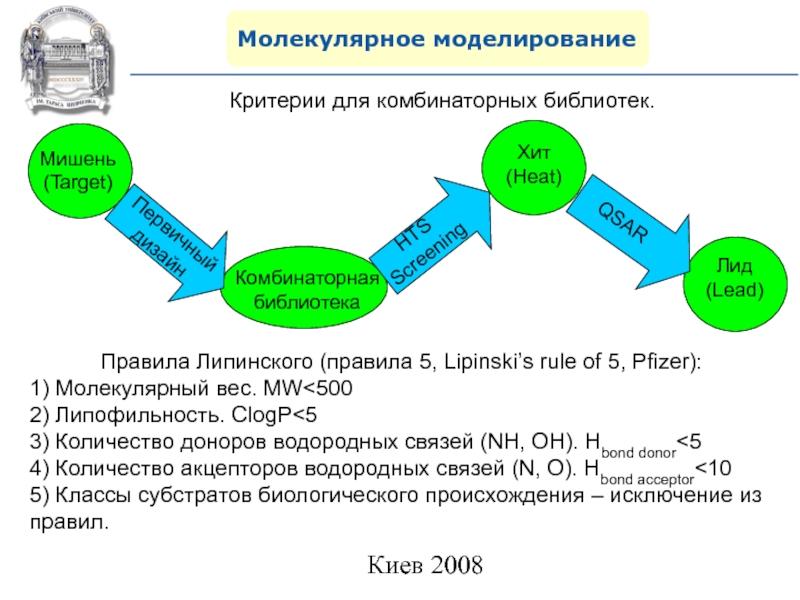
Критерии для комбинаторных библиотек.
Правила Липинского (правила 5, Lipinski’s
rule of 5, Pfizer):
1) Молекулярный вес. MW
доноров водородных связей (NH, OH). Hbond donor<54) Количество акцепторов водородных связей (N, O). Hbond acceptor<10
5) Классы субстратов биологического происхождения – исключение из правил.
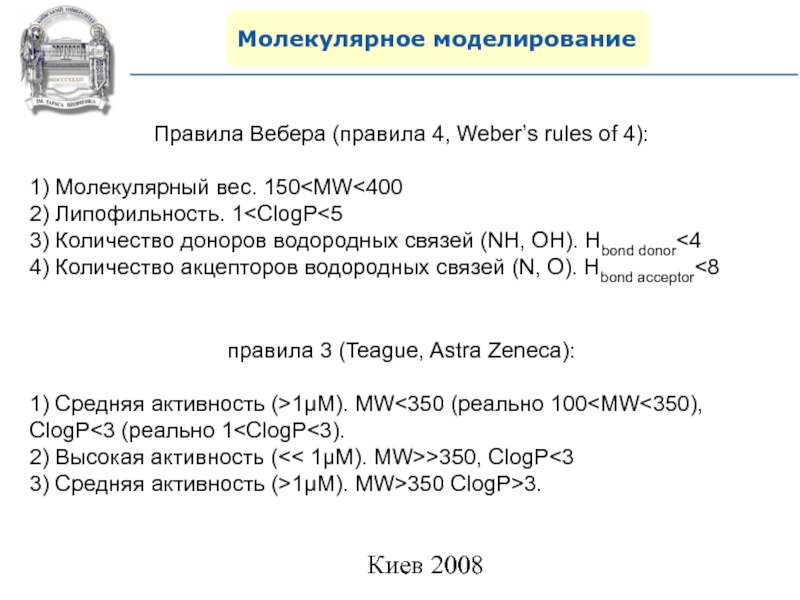
Слайд 88Молекулярное моделирование
Правила Вебера (правила 4, Weber’s rules of 4):
1) Молекулярный
вес. 150
Hbond donor<44) Количество акцепторов водородных связей (N, O). Hbond acceptor<8
правила 3 (Teague, Astra Zeneca):
1) Средняя активность (>1μM). MW<350 (реально 100
3) Средняя активность (>1μM). MW>350 ClogP>3.
Слайд 90Линкеры для твердофазного синтеза
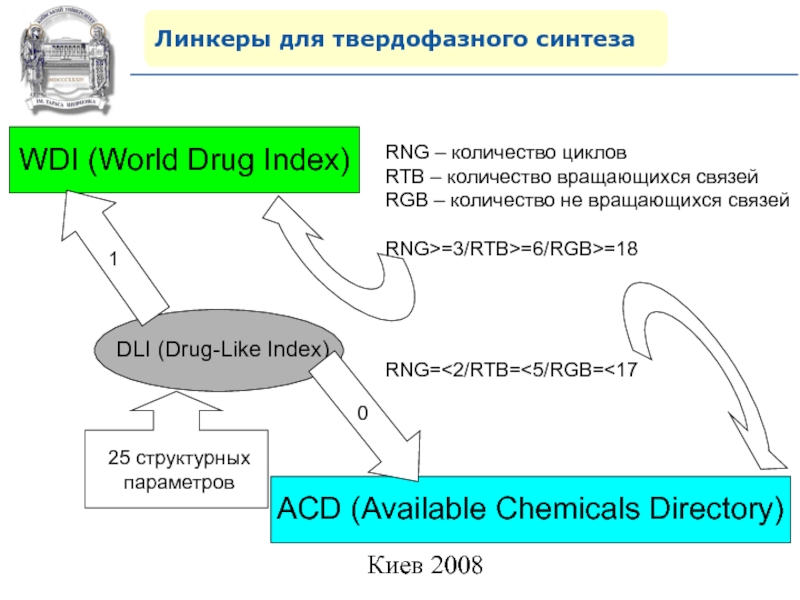
RNG – количество циклов
RTB – количество вращающихся
связей
RGB – количество не вращающихся связей
RNG>=3/RTB>=6/RGB>=18
RNG=
Слайд 91Молекулярное моделирование
Типы библиотек:
1) Первичная библиотека для скрининга. (Primary Screening Library)
Должна
удовлетворять правилу 4 (по возможности даже 3).
2) Таргетная (направленная) библиотека.
(Targeted Library)Должна удовлетворять правилу 5 (возможны некоторые послабления).
3) Фокусная библиотека. (Focus Library)
Построение QSAR, Heat-to-Lead оптимизация. ADME/PK-параметры (Absorption, Distribution, Metabolism, Excretion/ PharmacoKinetics) .
Слайд 92Молекулярное моделирование
Дискрипторы:
1) Одномерные (1D). (MW, ClogP, Hbond donor, Hbond acceptor,
и т.п.)
2) Двумерные (2D). (Структурные фрагменты)
3) Трехмерные (3D). (Конформации и
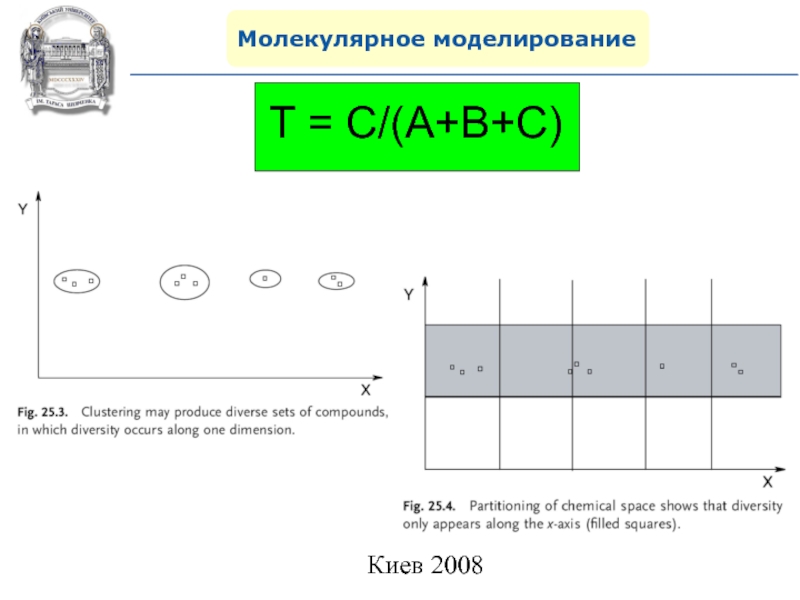
пространственное строение молекулы)Разнообразие (Diversity). Коефициент Танимото. (Tanimoto)
T – коефициент Танимото.
A – молекула в стринговом виде
B – другая молекула в стринговом виде,
C – общий фрагмент в А и B.
Слайд 94Молекулярное моделирование
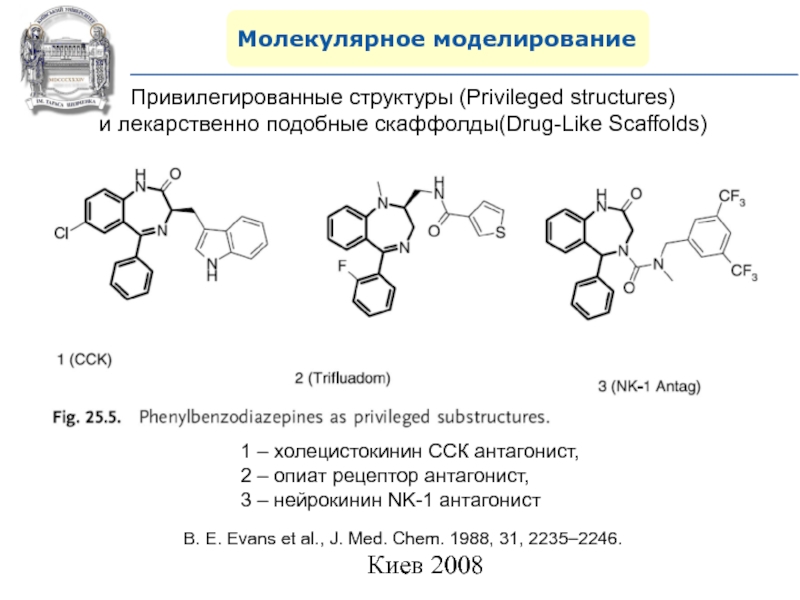
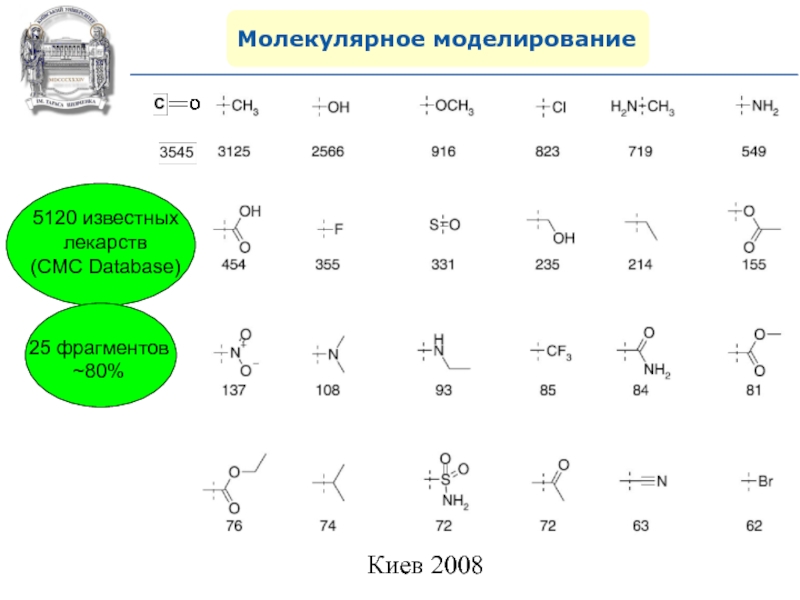
Привилегированные структуры (Privileged structures)
и лекарственно подобные скаффолды(Drug-Like Scaffolds)
B.
E. Evans et al., J. Med. Chem. 1988, 31, 2235–2246.
1
– холецистокинин ССК антагонист, 2 – опиат рецептор антагонист,
3 – нейрокинин NK-1 антагонист
Слайд 101Молекулярное моделирование
Ретросинтетический комбинаторный анализ
(RECAP ‘‘Retrosynthetic Combinatorial Analysis Procedure’’)
Слайд 102Молекулярное моделирование
Ретросинтетический комбинаторный анализ
(RECAP ‘‘Retrosynthetic Combinatorial Analysis Procedure’’)
Слайд 103Молекулярное моделирование
A. N. Shivanyuk,
S. V. Ryabukhin,
et al., Chemistry Today,
2007, 25, 6, 58-59.
Слайд 104Молекулярное моделирование
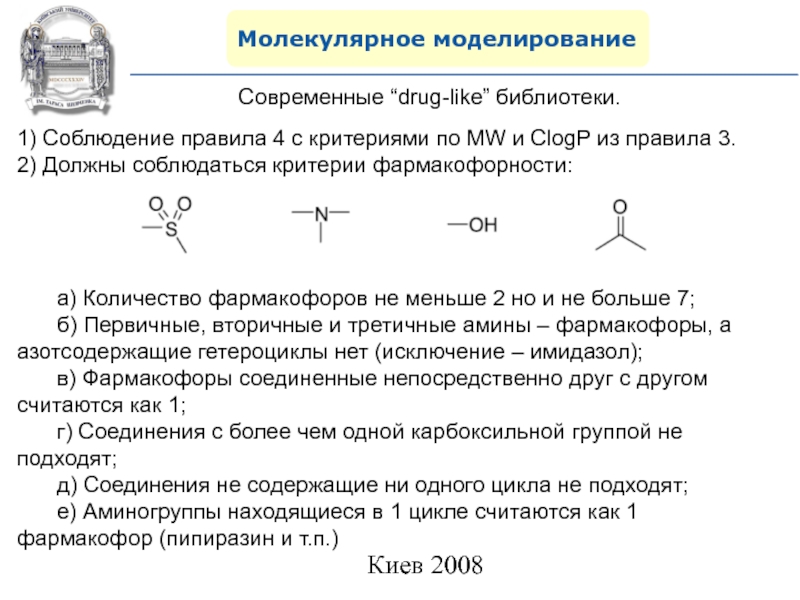
Современные “drug-like” библиотеки.
1) Соблюдение правила 4 с критериями по
MW и ClogP из правила 3.
2) Должны соблюдаться критерии
фармакофорности:а) Количество фармакофоров не меньше 2 но и не больше 7;
б) Первичные, вторичные и третичные амины – фармакофоры, а азотсодержащие гетероциклы нет (исключение – имидазол);
в) Фармакофоры соединенные непосредственно друг с другом считаются как 1;
г) Соединения с более чем одной карбоксильной группой не подходят;
д) Соединения не содержащие ни одного цикла не подходят;
е) Аминогруппы находящиеся в 1 цикле считаются как 1 фармакофор (пипиразин и т.п.)
Слайд 105Молекулярное моделирование
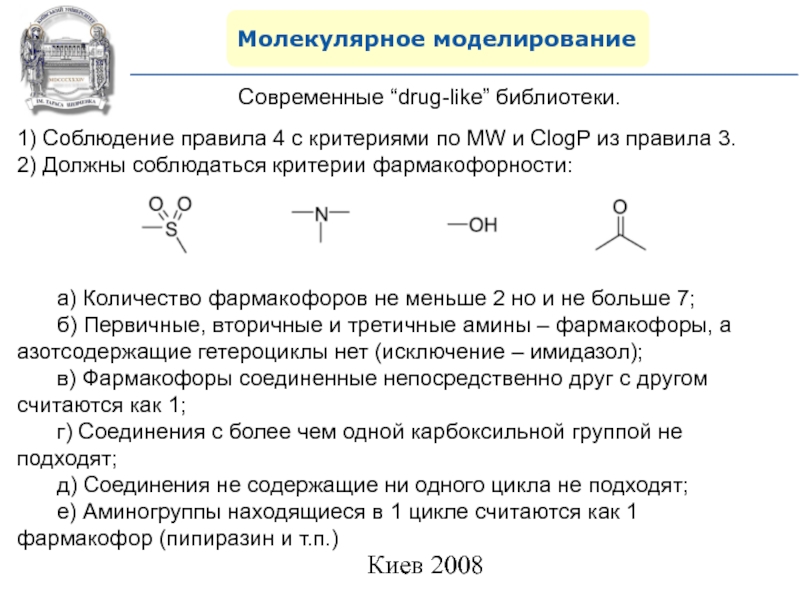
Современные “drug-like” библиотеки.
1) Соблюдение правила 4 с критериями по
MW и ClogP из правила 3.
2) Должны соблюдаться критерии
фармакофорности:а) Количество фармакофоров не меньше 2 но и не больше 7;
б) Первичные, вторичные и третичные амины – фармакофоры, а азотсодержащие гетероциклы нет (исключение – имидазол);
в) Фармакофоры соединенные непосредственно друг с другом считаются как 1;
г) Соединения с более чем одной карбоксильной группой не подходят;
д) Соединения не содержащие ни одного цикла не подходят;
е) Аминогруппы находящиеся в 1 цикле считаются как 1 фармакофор (пипиразин и т.п.)