Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Курс Биология опухолевой клетки (2019 г. ) Лекция 1 0 (часть 1) Онкогенные
Содержание
- 1. Курс Биология опухолевой клетки (2019 г. ) Лекция 1 0 (часть 1) Онкогенные
- 2. Вирус-ассоциированные опухоли у населения мира51015Доля смертности от
- 3. Для злокачественной трансформации инфицированных клеток необходимы
- 4. ДНК-содержащие
- 5. 51015Доля смертности от рака в мире51015Рак печениРак
- 6. Известно более 150 типов (5 групп)
- 7. Вирус папиллом человека (HPV)Функции вирусаСинтезДНК++++-/++Экспрессияпоздних генов++++--Stratum corneumStratum
- 8. Геном вируса папилломы человека (HPV) ДНК HPV,
- 9. Неконтролируемое размножение клеток,накопление дополнительных генетических измененийОнкобелки высокоонкогенных
- 10. Одновременная инактивация р53 и pRb продуктами
- 11. MAPK (Raf-Erk, p38, Jnk), PI3K-Akt,
- 12. Полиомавирус клеток Меркеля (Merkel cell polyomavirus,
- 13. Полиомавирус клеток Меркеля (Merkel cell polyomavirus,
- 14. Онкогены MCPyVДля MCPyV-негативных МКК характерны замены C>T,
- 15. Заболевания человека, ассоциированные с вирусом Эпштейна-Барр (EBV)Доброкачественная
- 16. Персистирует у 80-95% взрослого населения планеты.
- 17. Риск трансформации увеличен при каждой из 3-х
- 18. Слайд 18
- 19. Воздействие LMP1, LMP2 и EBNA2 на сигнальные путиAP-1activationp38MAPKATF-2activationLMP1LMP2EBNA2Alteration ofOct signaling
- 20. Герпесвирус человека, ассоциированныйс саркомой Капоши (KSHV/HHV-8)Инфицированность населения
- 21. 24TR13TR765abcdefgh20 т.п.н.Линейный геном HHV-8 содержит длинную уникальную
- 22. Белки HHV-8, гомологичные клеточным белкам: v-Bcl-2 –
- 23. HHV-8ПерсистентнаяинфекцияТрансформацияклетки, уходот иммунологи-ческого надзораОпухолевый ростРаспространениевируса, заражениеэндотелиоцитов Литическаяинфекция,репликациявируса
- 24. Онкогенные вирусыРетровирусыДНК-содержащиевирусыВносятвирусные онкогеныИнсерционныймутагенезАктивированныеклеточныепротоонкогеныСтимуляция размножения и миграции клеток,отмена
- 25. Канцерогенез при инфекции Helicobacter pyloriРак желудкаВпрыскивание белка
- 26. Курс «Биология опухолевой клетки»(2019 г.)Лекция 10 (часть 2)Ускользание опухолей от иммунологического надзораН.Л. Лазаревич
- 27. Злокачественные новообразования возникают врезультате
- 28. Иммунный ответ на опухоли1957 г. – BURNET
- 29. Доказательства существования специфическогопротивоопухолевого иммунитетаAdapted from R.Weinberg, The Biology of Cancer (© Garland Science 2007)T-cells
- 30. Механизмы индукции апоптоза цитотоксическими Т-лимфоцитами:Формирование и действие
- 31. Увеличение частоты ряда форм опухолей послепересадки органов
- 32. Опухоли отличаются по содержанию в них Т-клеток
- 33. Антигены опухолевых клеток, распознаваемые цитотоксическими Т-клетками1. Опухоль-специфические
- 34. Опухоль-специфические антигены (TSAs) –
- 35. Опухоль-ассоциированные антигены (TАAs)
- 36. Опухоль-ассоциированные антигены (TАAs) и
- 37. ГуморальныйиммунитетКлеточный иммунитетВ-клеткиПлазматическиеклеткиСекреция антителКонтролерыЭффекторыТH(хэлперы)Связываниеантигена,пролиферацияТreg(регулят.)ТC(цитотокс)Дендритные,макрофагиАнтиген-презентирующиеУбийствоклеток-мишенейУбийствоклеток-мишенейНейтрализация патогенаНеспецифический (врожденный)NK-клетки,макрофагиЦито-токсическиеТ-клеткиСпецифический (адаптивный)Fcрецепт.ВрожденноераспознаваниеКомплемент
- 38. NKNKпотенциальныеклетки-мишениПротивоопухолевый иммунный ответ у бестимусных мышей обеспечивают
- 39. Многогранная роль макрофагов в канцерогенезеВоспаление нормальных тканей,увеличение
- 40. Shankaran et al., Nature, 2001, 410:1107-1111; adapted
- 41. Prendergast, Immune escape as fundamental trait of cancer ..., Oncogene, 2008, 27:3889-3900
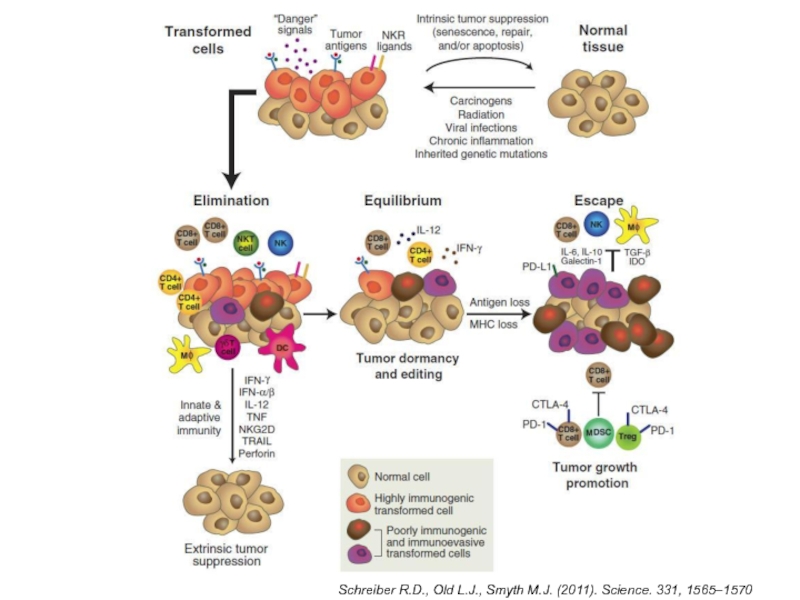
- 42. Schreiber R.D., Old L.J., Smyth M.J. (2011). Science. 331, 1565–1570
- 43. Как опухолевые клетки уходятот иммунологического надзора ?1.
- 44. Adapted from The Biology of Cancer (©
- 45. Ускользание от иммунного надзора:2. Создание защитного барьера,
- 46. Fas-LFas-LFas-LFasFas-LFasАпоптозАпоптозПовышение экспрессии Fas-L в неопластических клетках может
- 47. melanoma metastasisin lungУскользание от иммунного надзора:2. Создание
- 48. Ускользание от иммунного надзора:2. Создание защитного барьера
- 49. Курс «Биология опухолевой клетки»(2019 г.)Н.Л. ЛазаревичЛекция 11
- 50. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Курс «Биология опухолевой клетки»
(2019 г.)
Лекция 10 (часть 1)
Онкогенные вирусы человека
(продолжение)
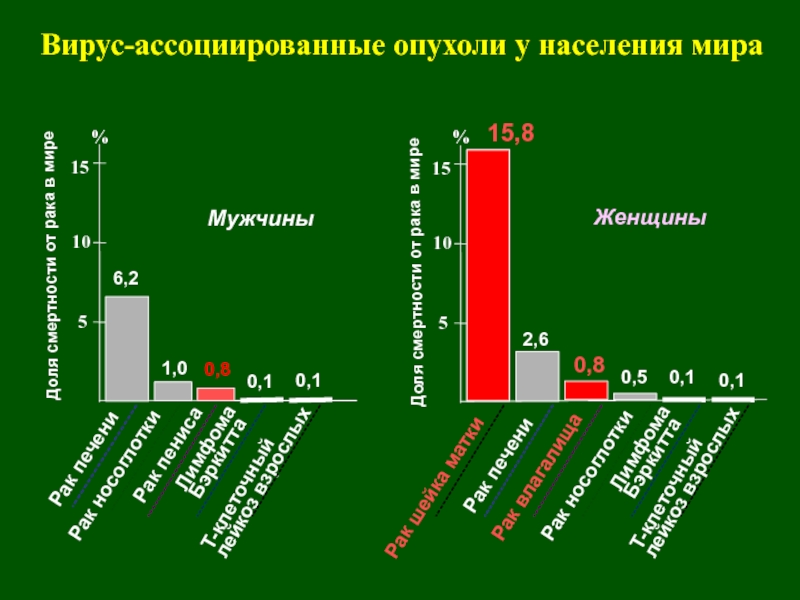
Слайд 2Вирус-ассоциированные опухоли у населения мира
5
10
15
Доля смертности от рака в мире
5
10
15
Рак
печени
Рак носоглотки
Рак пениса
Лимфома
Бэркитта
T-клеточный
лейкоз взрослых
6,2
%
%
1,0
0,8
0,1
0,1
15,8
2,6
0,8
0,5
0,1
0,1
Мужчины
Женщины
Доля смертности от рака в мире
Рак шейка
маткиРак печени
Рак влагалища
Рак носоглотки
Лимфома
Бэркитта
T-клеточный
лейкоз взрослых
Слайд 3 Для злокачественной трансформации инфицированных клеток необходимы дополнительные факторы и
условия, ведущие к отбору опухолевого клона клеток
Опухоль у инфицированных
лиц возникает, как правило, редко, примерно, 1 случай заболевания на десятки, сотни, а иногда и тысячи инфицированных лицПосле инфицирования до возникновения опухоли проходит длительный латентный период, длящийся годами и даже десятилетиями
У большинства инфицированных лиц возникновение опухоли не является обязательным событием, но они входят в группу риска
Особенности вирусного канцерогенеза у людей
Слайд 4 ДНК-содержащие
Новообразования
Вирус гепатита В (HBV)
Гепатоцеллюлярная карциномаВирус папилломы (HPV) Рак шейки матки и др.
Вирус Эпштейна-Барр (EBV) Лимфома Беркитта, рак носо-
глотки, лимфогранулематоз
Герпесвирус-8 (HHV-8/KSHV) Саркома Капоши и др.
Полиомавирус клеток Меркеля Карцинома клеток Меркеля
(MCPyV/HPyV5)
РНК-содержащие Новообразования
HTLV-1 Т-клеточный лейкоз взрослых
Вирус гепатита С (HСV) Гепатоцеллюлярная карцинома
Онкогенные вирусы человека
Слайд 55
10
15
Доля смертности от рака в мире
5
10
15
Рак печени
Рак носоглотки
Рак пениса
Лимфома
Бэркитта
T-клеточный
лейкоз взрослых
6,2
%
%
1,0
0,8
0,1
0,1
15,8
2,6
0,8
0,5
0,1
0,1
Мужчины
Женщины
Доля
смертности от рака в мире
Рак шейка матки
Рак печени
Рак влагалища
Рак носоглотки
Лимфома
Бэркитта
T-клеточный
лейкоз
взрослых Вирус-ассоциированные опухоли у населения мира
Слайд 6
Известно более 150 типов (5 групп) HPV, но лишь
некоторые из них (альфа-группа) поражают слизистый эпителий и увеличивают риск
возникновения опухолей. Высоко онкогенные - HPV16 и HPV18.HPV16 ответственен за 50% случаев рака шейки матки; HPV18, 31, 33, и 45 – за 20% случаев; другие типы – за часть остальных случаев (< чем в 5% раков шейки матки HPV не выявляется).
Другие новообразования – опухоли аногенитальной области (ануса, вульвы и влагалища) – 85-95%, рак ротоглотки – 50% и др.
У 90% женщин HPV инфекция исчезает самостоятельно через год после инфицирования под воздействием иммунной системы организма. У меньшинства возникают опухоли.
Вирус папилломы человека (HPV)
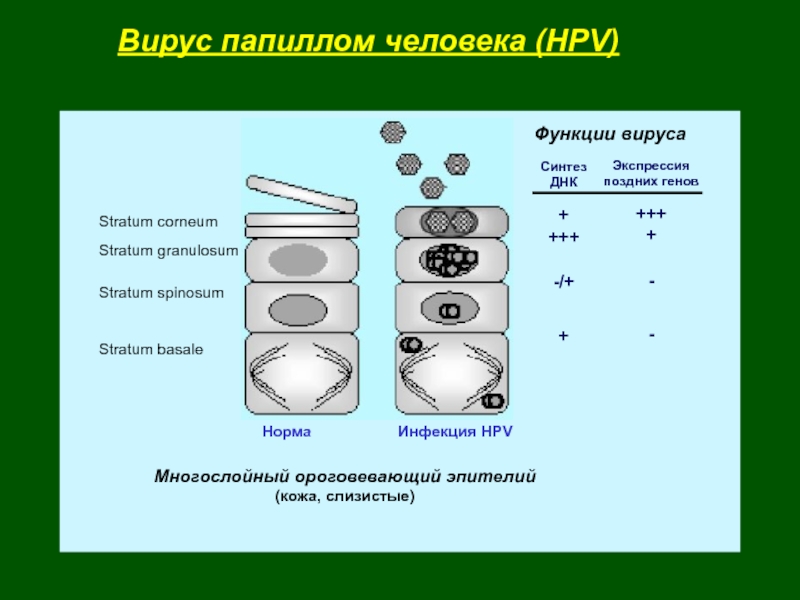
Слайд 7Вирус папиллом человека (HPV)
Функции вируса
Синтез
ДНК
+
+++
-/+
+
Экспрессия
поздних генов
+++
+
-
-
Stratum corneum
Stratum granulosum
Stratum spinosum
Stratum basale
Норма
Инфекция
HPVМногослойный ороговевающий эпителий
(кожа, слизистые)
Слайд 8Геном вируса папилломы человека (HPV)
ДНК HPV, ~8000 п.о., cодержит
9 ORF,
2 из которых (L1 и L2) кодируют
структурные белки вириона, а 7 других (Е1-Е7), т.н. ранние гены,
контролируют репродукцию вируса.
Онкогенный эффект HPV обусловлен экспрессией Е6, Е7 и, в меньшей степени, E5.
Эписомная форма (50-100 копий). На
поздних этапах малигнизации может
происходить интеграция ДНК HPV в
ДНК клетки может привести к
малигнизации.
интеграция
ДНК
клетки
ДНК
клетки
E6
E7
E1
E2
E4
E2
E5
L1
L2
Слайд 9Неконтролируемое размножение клеток,
накопление дополнительных генетических изменений
Онкобелки высокоонкогенных типов HPV
(HPV16, HPV18
и др.):
E6
Связывание и
инактивация
р53
Нарушение
контроля
чекпойнтов
и апоптоза;
мутагенез
E
6
E7
E5
Стимуляция
деления;
отмена реп-
ликативного
старения
Активация
генов
MYC, hTERT
Связывание и
инактивация
рRb, p107,
p130Отмена
негативного
контроля
входа в
S-фазу
Связывание и
инактивация
p21Cip1, p27Kip1
Усиление тирозинкиназной активности EGFR, стимуляция
МАР киназ
Инициация
митотических
циклов
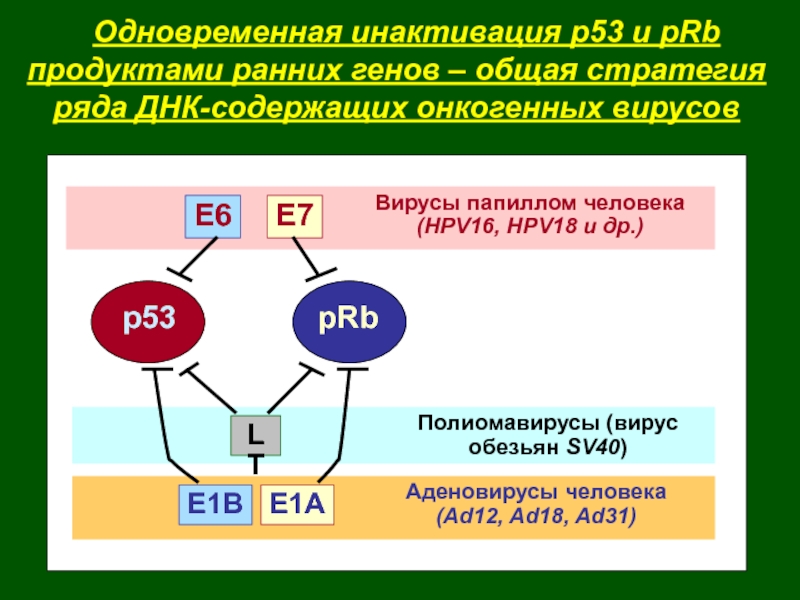
Слайд 10 Одновременная инактивация р53 и pRb
продуктами ранних генов –
общая стратегия ряда ДНК-содержащих онкогенных вирусов
Вирусы папиллом человека
(HPV16, HPV18 и
др.)p53
pRb
E6
E7
E1B
E1A
LT
Полиомавирусы (вирус обезьян SV40)
Аденовирусы человека
(Ad12, Ad18, Ad31)
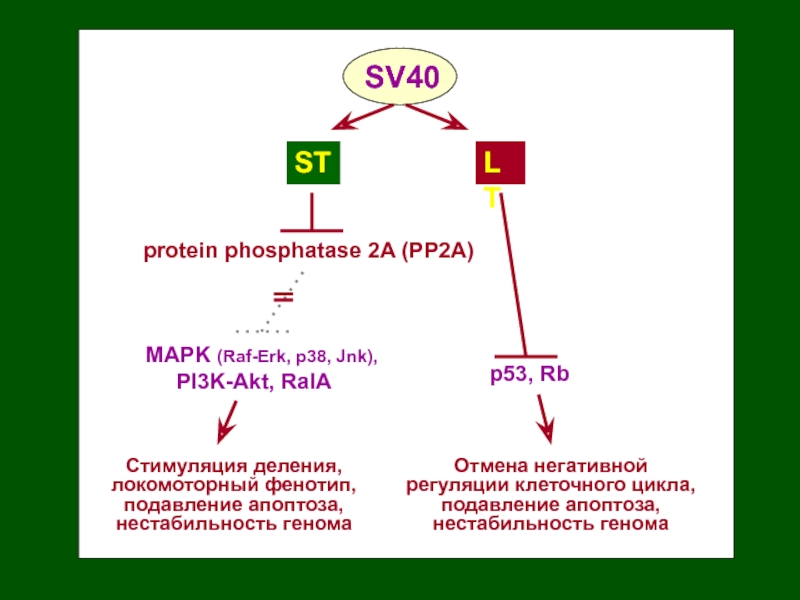
Слайд 11MAPK (Raf-Erk, p38, Jnk),
PI3K-Akt, RalA
ST
LT
p53, Rb
protein phosphatase
2A (PP2A)
SV40
Отмена негативной
регуляции клеточного цикла,
подавление апоптоза,
нестабильность генома
Стимуляция деления, локомоторный фенотип,
подавление
апоптоза,нестабильность генома
Слайд 12Полиомавирус клеток Меркеля
(Merkel cell polyomavirus, MCPyV)
Карцинома клеток Меркеля
(ККМ) - редкая злокачественная опухоль кожи нейроэндокрин-ного происхождения, описанная Cyril
Toker в 1972 году. До 1972 года такие опухоли относили к недифференцированному раку кожи.В 1978 году Tang и Toker предположили возникновение этих опухолей из клеток Меркеля (механорецепторы в нижних
слоях эпидермиса).
Хотя заболеваемость ККМ примерно в 30 раз ниже, чем заболеваемость меланомой кожи, смертность составляет 46%, что почти в 4 раза больше, чем при инвазивной меланоме (12,5%).
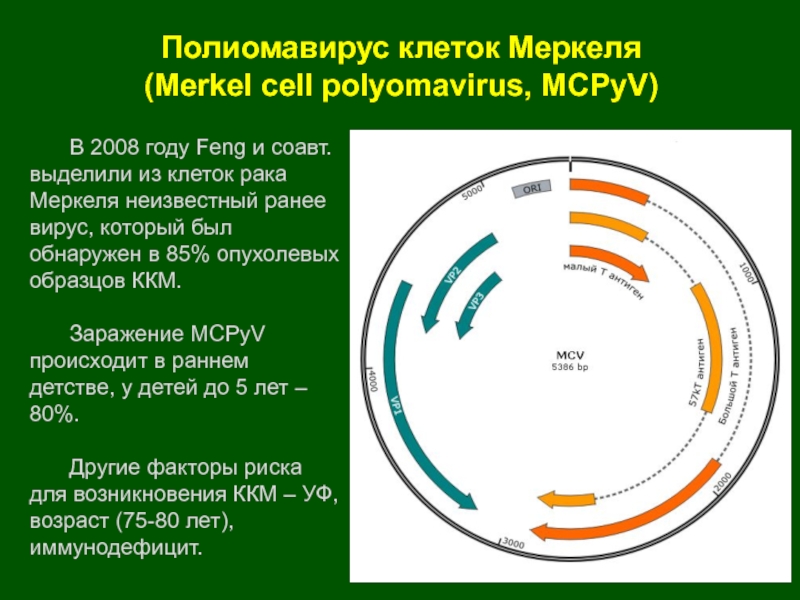
Слайд 13Полиомавирус клеток Меркеля
(Merkel cell polyomavirus, MCPyV)
В 2008 году
Feng и соавт. выделили из клеток рака Меркеля неизвестный ранее
вирус, который был обнаружен в 85% опухолевых образцов ККМ.Заражение MCPyV происходит в раннем детстве, у детей до 5 лет – 80%.
Другие факторы риска для возникновения ККМ – УФ, возраст (75-80 лет), иммунодефицит.
Слайд 14Онкогены MCPyV
Для MCPyV-негативных МКК характерны замены C>T, инактивирующие мутации генов
pRb, p53, системы ремоделирования хроматина и системы репарации ДНК
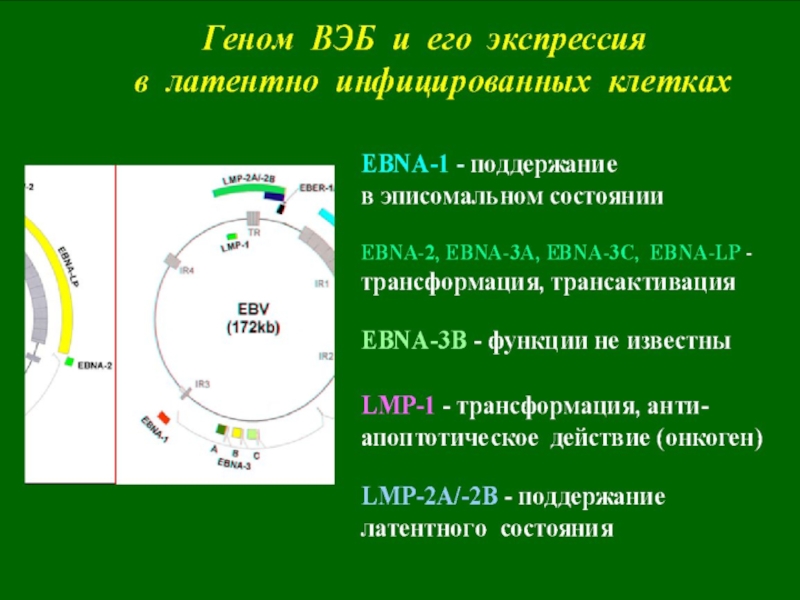
Слайд 15Заболевания человека, ассоциированные
с вирусом Эпштейна-Барр (EBV)
Доброкачественная реактивная инфекция
Инфекционный мононуклеоз
>99 Злокачественные новообразования
Лимфоидные
Лимфогрануломатоз (ЛГМ), смешанно-клеточный 70
ЛГМ, ассоциированный со СПИД >95
Лимфома Беркитта, Африканская >95
Лимфома Беркитта, Северо-американская 20
Лимфома Беркитта, СПИД-ассоциированная 30
Неходжкинская лимфома, СПИД-ассоциированная 40
Назальная Т/NK-клеточная лимфома >95
Раки
Рак носоглотки, Азия >95
Рак носоглотки, США 75
Рак желудка, Япония, США 6-16
% EBV-ассоциир.
Слайд 16 Персистирует у 80-95% взрослого населения планеты. Заражает B-лимфоциты, T/NK-клетки
и некоторые типы эпителиоцитов.
Инфицирование обычно происходит в раннем
детстве и протекает бессимптомно. При более позднем контакте у половины индивидуумов развивается инфекционный мононуклеоз. После первичного инфицирования EBV человек пожизненно становится носителем вируса. EBV – ДНК-содержащий вирус
(сем. герпесвирусов, род Lymphomacriptoviruses;
геном – 172 т.п.н.)
EBV nuclear antigens (EBNAs) and latent membrane proteins (LMPs)
Слайд 17Риск трансформации увеличен при каждой из 3-х форм латентной инфекции
(программы б-г),
Стратегии взаимодействия EBV c клеткой:
а) продуктивная литическая инфекция
(плазматические В-клетки, эпителиоциты ротоглотки;
экспрессируется 90 вирусных генов);
б) программа стимуляции пролиферации
(дифференцирующиеся В-клетки;
индуцируется экспрессией белков EBNA1-6, LMP1, LMP2);
в) программа «спасения вирусов»
(В-иммунобласты, T/NK-клетки, эпителиоциты;
экспрессируются EBNA1, LMP1, LMP2);
г) программа «сокрытия вируса»
(В-клетки памяти и эпителиоциты, уход от иммунологического распознавания и уничтожения зараженных клеток;
вирусные белки не экспрессируются, либо фенотипы
LMP2A+ или LMP2A+/EBNA1+)
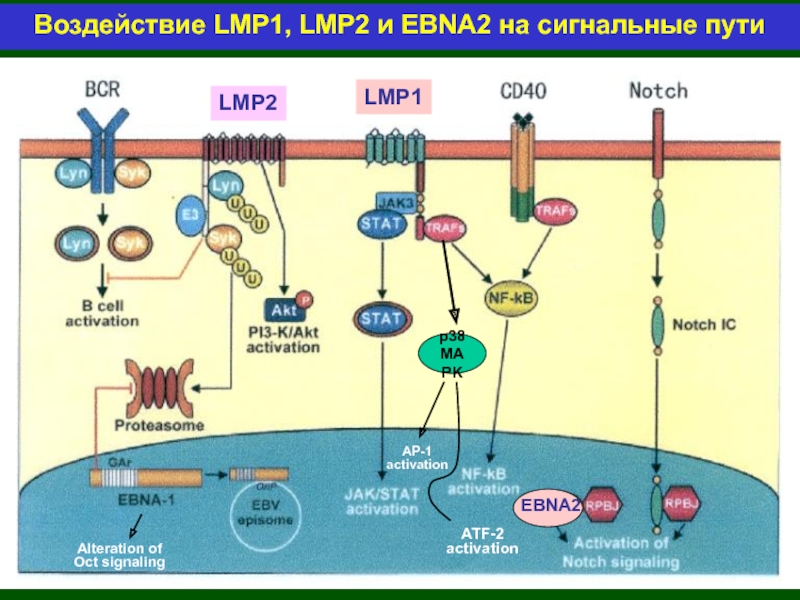
Слайд 19Воздействие LMP1, LMP2 и EBNA2 на сигнальные пути
AP-1
activation
p38
MAPK
ATF-2
activation
LMP1
LMP2
EBNA2
Alteration of
Oct signaling
Слайд 20Герпесвирус человека, ассоциированный
с саркомой Капоши (KSHV/HHV-8)
Инфицированность населения HHV-8 сильно варьирует
в разных географических областях:
регионы Африки и Средиземноморья –
большинство;страны Западной Европы и США – редко и ассоциирована
с отдельными группами (гомосексуалисты, больные
СПИДом и другими формами иммунодефицитов).
Вирус заражает эпителиоциты простаты, эндотелиоциты сосудов и кроветворные клетки. Передача инфекции в основном происходит половым путем.
Саркома Капоши – многофокусный неопластический процесс, возникающий из эндотелия лимфатических и кровеносных сосудов, главным образом дермы. Опухоль включает также размножающиеся периваскулярные фибробласты.
(подсемейство гамма-герпесвирусов, род радиновирусов)
Слайд 212
4
TR
1
3
TR
7
6
5
a
b
c
d
e
f
g
h
20 т.п.н.
Линейный геном HHV-8 содержит длинную уникальную область (LUR) (140.5
тысяч пар оснований, 81 ген)
Некоторые из генов LUR кодируют белки,
гомологичные известным белкам человека,участвующим в процессах канцерогенеза
Геном HHV-8 подразделяется на 7 блоковых областей (1-7), которые кодируют структурные белки и ферменты, участвующие в репликации клетки. Межблоковые области генома (а-h) кодируют уникальные вирусные белки
Слайд 22Белки HHV-8, гомологичные клеточным белкам:
v-Bcl-2 – гомолог анти-апоптотического белка
Bcl-2;
vFLIP – гомолог ингибитора прокаспазы-8 с-FLIP;
v-cyclin D – гомолог
циклина D2;vMIP-I, vMIP-II – гомологи хемокинов макрофагов MIP-I, MIP-II;
vIL6 – гомолог IL6;
vIRF – гомолог IRF-1 и IRF-2 (передают сигналы от интерферонов);
vGPCR – гомолог рецептора IL8
ORF K1 – трансмембранный гликопротеин;
Капошин (ORF K12)
Другие потенциально онкогенные белки HHV-8
Слайд 23HHV-8
Персистентная
инфекция
Трансформация
клетки, уход
от иммунологи-
ческого надзора
Опухолевый рост
Распространение
вируса, заражение
эндотелиоцитов
Литическая
инфекция,
репликация
вируса
Слайд 24Онкогенные вирусы
Ретровирусы
ДНК-содержащие
вирусы
Вносят
вирусные
онкогены
Инсерционный
мутагенез
Активированные
клеточные
протоонкогены
Стимуляция размножения и миграции клеток,
отмена негативного контроля пролиферации
подавление
апоптоза, генетическая нестабильность
Вносят
вирусные
онкогены
E6,LMP1,
E1B
E7, E1A
Изменение
транскрипции
клеточных
белков
Подавление
активности
р53
Гомологи/
имитаторы
клеточных
белков
Tах
Подавление
активности
рRb, p105, p130
T-SV40
vBcl2,vFLIP,
vCycD и др.
Слайд 25Канцерогенез при инфекции Helicobacter pylori
Рак желудка
Впрыскивание белка CagA:
Специфические эффекты
cтимуляция размножения
и миграции клеток, подавление
апоптоза, мутагенез
Хронический гастрит:
кислородные и азотные
радикалы
мутагенез,
стимуляция размножения
Неспецифические
эффекты H. pylori – грам-отрицательные бактерии, обитающие в желудке
(20-30% населения развитых стран и 50-70% - в слаборазвитых странах).
cвязывание Grb2
Ras-MAPK
NFkB BclX, IAPs, FLIP, IL1,
IL6, IL8, TNFα, Cox2, iNOS и др.
гастрин
Ключевую роль в играет белок CagA, кодируемый участком генома сagPAI (присутствует у ~60% штаммов). Рак развивается у 1-2% индивидуумов, инфицированных такими штаммами. Дополнительные факторы риска - генетическая предрасположенность (полиморфизмом генов определенных цитокинов), высокосолевая диета и др.
Слайд 26Курс «Биология опухолевой клетки»
(2019 г.)
Лекция 10 (часть 2)
Ускользание опухолей от
иммунологического надзора
Н.Л. Лазаревич
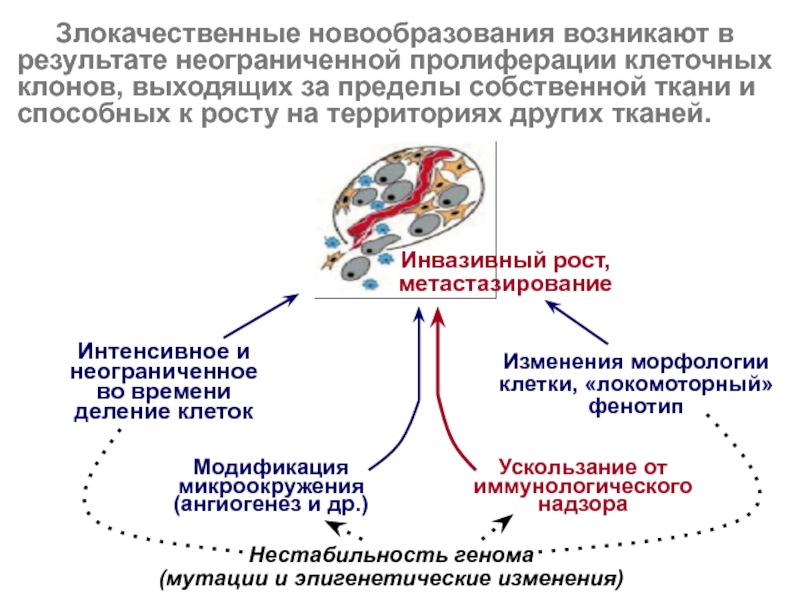
Слайд 27 Злокачественные новообразования возникают в
результате неограниченной пролиферации клеточных
клонов, выходящих за пределы собственной ткани и способных к росту
на территориях других тканей.Инвазивный рост, метастазирование
Нестабильность генома
(мутации и эпигенетические изменения)
Интенсивное и
неограниченное во времени деление клеток
Модификация
микроокружения
(ангиогенез и др.)
Изменения морфологии
клетки, «локомоторный» фенотип
Ускользание от иммунологического надзора
Слайд 28Иммунный ответ на опухоли
1957 г. – BURNET – концепция иммунологического
надзора
(tumour immunosurveillance):“... small accumulations of tumour cells may develop and, because of their possession of new antigenic potentialities, provoke an effective immunological reaction with regression of the tumour and no clinical hint of its existence”
ТС
Раковая
клетка
(апоптоз)
From The Biology of Cancer (© Garland Science 2007)
Слайд 29Доказательства существования специфического
противоопухолевого иммунитета
Adapted from R.Weinberg, The Biology of Cancer
(© Garland Science 2007)
T-cells
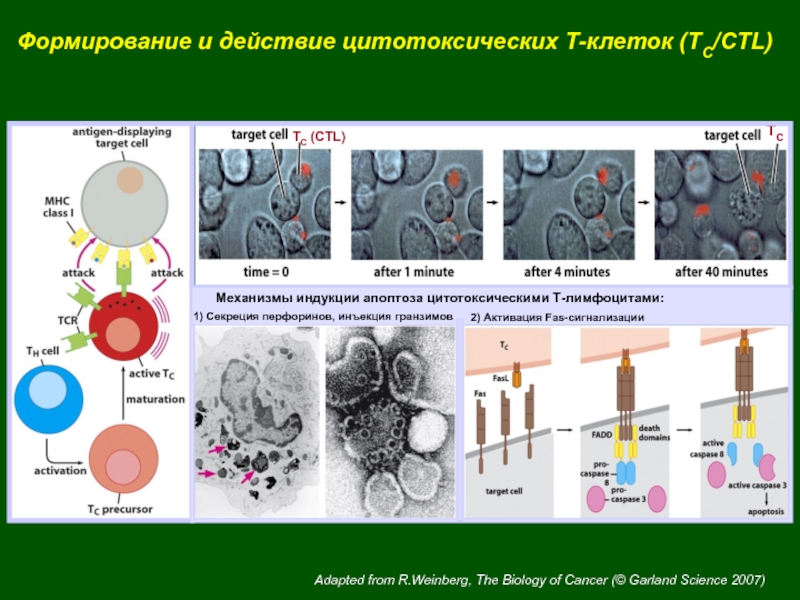
Слайд 30Механизмы индукции апоптоза цитотоксическими Т-лимфоцитами:
Формирование и действие цитотоксических Т-клеток (TC/CTL)
Adapted from R.Weinberg, The Biology of Cancer (© Garland Science
2007)1) Секреция перфоринов, инъекция гранзимов
2) Активация Fas-сигнализации
Слайд 31Увеличение частоты ряда форм опухолей после
пересадки органов и подавления иммунной
системы
Резко повышается риск развития вирус-ассоциированных опухолей:
саркома Капоши (HHV-8)
– 400-500 разрак влагалища и анальной области (HPV) – ~100 раз
лимфома Ходжкина (EBV) – 28-49 раз
рак печени (HBV, HCV) – 20-38 раз
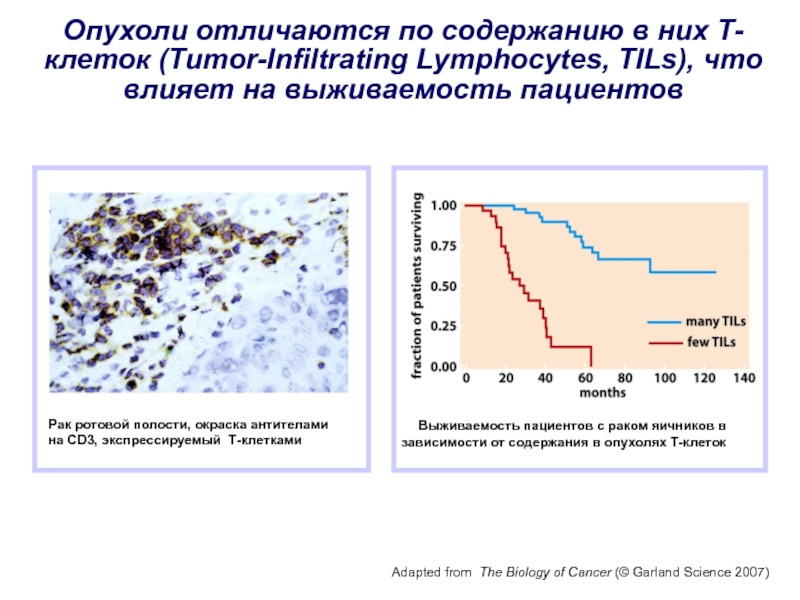
Слайд 32Опухоли отличаются по содержанию в них Т-клеток (Tumor-Infiltrating Lymphocytes, TILs),
что влияет на выживаемость пациентов
Рак ротовой полости, окраска антителами
на CD3,
экспрессируемый Т-клетками Выживаемость пациентов с раком яичников в
зависимости от содержания в опухолях Т-клеток
Adapted from The Biology of Cancer (© Garland Science 2007)
Слайд 33Антигены опухолевых клеток, распознаваемые цитотоксическими Т-клетками
1. Опухоль-специфические антигены (Tumor-Specific Antigens,
TSAs)
(для
мышей – Tumor-Specific Transplantation Antigens, TSTAs)2. Опухоль-ассоциированные антигены (Tumor-Associated Antigens, TAAs)
(для мышей – Tumor Associated Transplantation Antigens, TATAs)
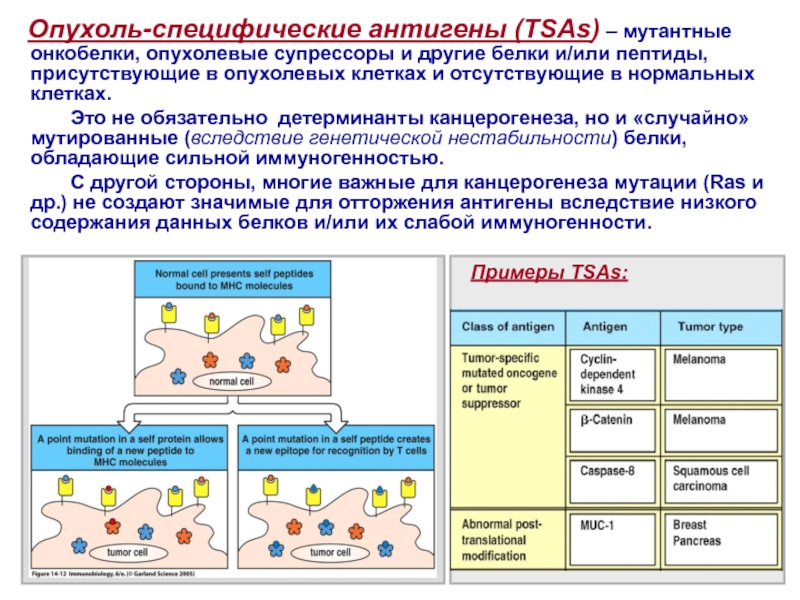
Слайд 34 Опухоль-специфические антигены (TSAs) – мутантные онкобелки, опухолевые
супрессоры и другие белки и/или пептиды, присутствующие в опухолевых клетках
и отсутствующие в нормальных клетках.Это не обязательно детерминанты канцерогенеза, но и «случайно» мутированные (вследствие генетической нестабильности) белки, обладающие сильной иммуногенностью.
С другой стороны, многие важные для канцерогенеза мутации (Ras и др.) не создают значимые для отторжения антигены вследствие низкого содержания данных белков и/или их слабой иммуногенности.
Примеры TSAs:
Слайд 35 Опухоль-ассоциированные антигены (TАAs) – присутствующие в
опухолевых клетках нормальные белки, к которым, в силу той или
иной причины, не развилась иммунотолератность (не распознаются как «свои»)Adapted from Immunobilology (© Garland Science 2005) and The Biology of Cancer (© Garland Science 2007)
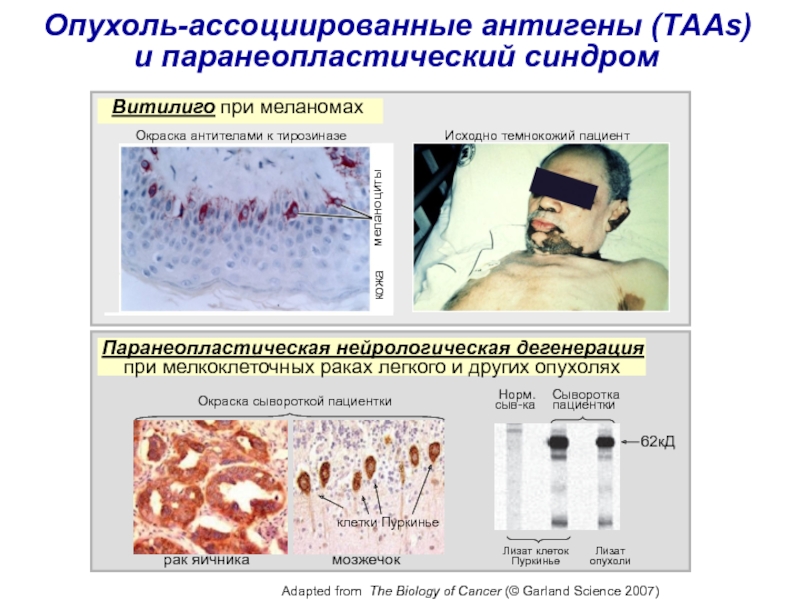
Слайд 36 Опухоль-ассоциированные антигены (TАAs) и паранеопластический синдром
рак яичника
мозжечок
клетки
Пуркинье
Окраска сывороткой пациентки
Лизат клеток
Пуркинье
Adapted from The Biology of Cancer (©
Garland Science 2007)Лизат
опухоли
Сыворотка
пациентки
Норм.
сыв-ка
62кД
Окраска антителами к тирозиназе
Исходно темнокожий пациент
Витилиго при меланомах
Паранеопластическая нейрологическая дегенерация
при мелкоклеточных раках легкого и других опухолях
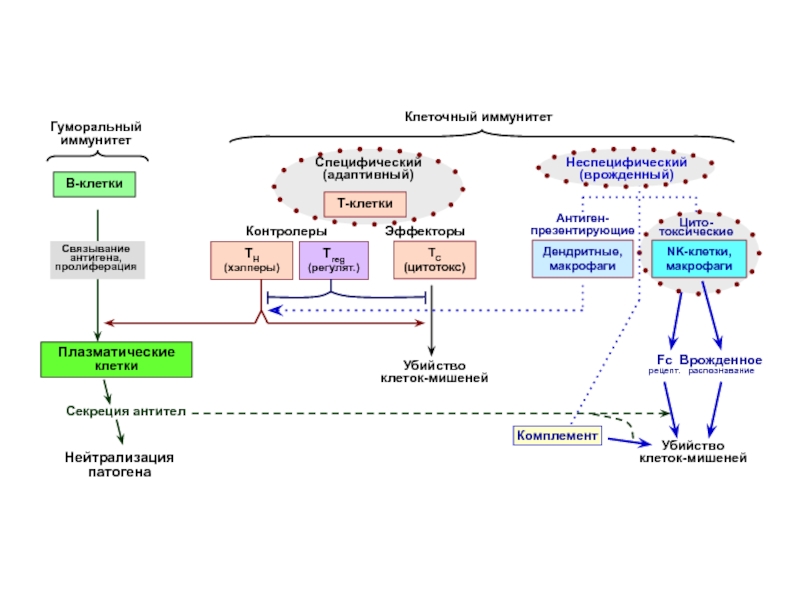
Слайд 37Гуморальный
иммунитет
Клеточный иммунитет
В-клетки
Плазматические
клетки
Секреция антител
Контролеры
Эффекторы
ТH
(хэлперы)
Связывание
антигена,
пролиферация
Тreg
(регулят.)
ТC
(цитотокс)
Дендритные,
макрофаги
Антиген-презентирующие
Убийство
клеток-мишеней
Убийство
клеток-мишеней
Нейтрализация патогена
Неспецифический (врожденный)
NK-клетки,
макрофаги
Цито-токсические
Т-клетки
Специфический (адаптивный)
Fc
рецепт.
Врожденное
распознавание
Комплемент
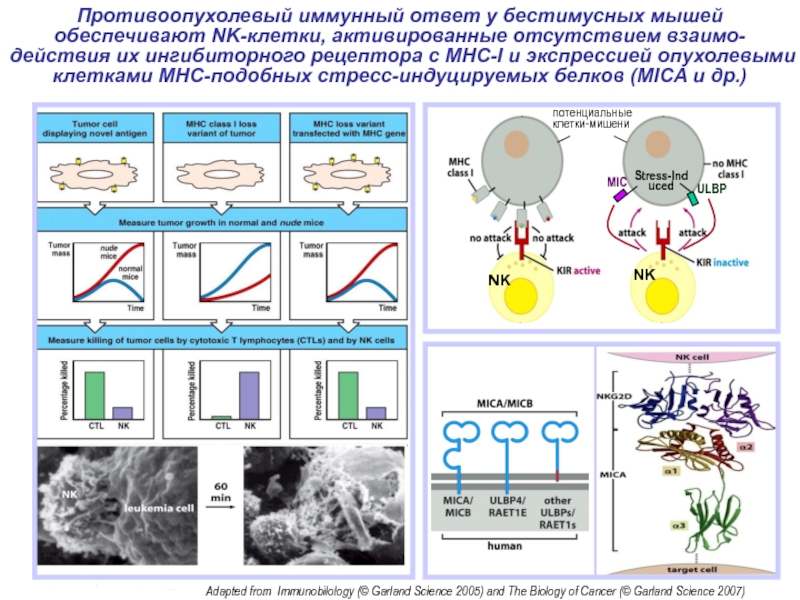
Слайд 38NK
NK
потенциальные
клетки-мишени
Противоопухолевый иммунный ответ у бестимусных мышей обеспечивают NK-клетки, активированные отсутствием
взаимо-действия их ингибиторного рецептора с MHC-I и экспрессией опухолевыми клетками
MHC-подобных стресс-индуцируемых белков (MICA и др.)Adapted from Immunobilology (© Garland Science 2005) and The Biology of Cancer (© Garland Science 2007)
Слайд 39Многогранная роль макрофагов в канцерогенезе
Воспаление нормальных тканей,
увеличение вероятности
возникновения опухоли
Моноцит
Sica et
al., Cancer Lett., 2008, 264:299–310
Стимуляция роста опухоли
ТАМ
Tumor-Associated
Macrophages
Противоопухолевый эффект
фагоцитоз опухолевых клеток
стимуляция
Т-клеток
Миграция
в опухольГипоксия, aктивация HIF-1
М1
макрофаг
М2
макрофаг
Папиллярный рак щитовидной железы
Регенерация тканей, заживление ран
Слайд 40Shankaran et al., Nature, 2001, 410:1107-1111; adapted from The Biology
of Cancer (© Garland Science 2007)
Эксперименты на мышах RAG2 -/-
указывают на «иммуноредактирование» (immunoediting) опухолевых клеток при развитии новообразованийОпухоли – 11/57
Опухоли – 30/52
У диких мышей не возникает сильно иммуногенных опухолей
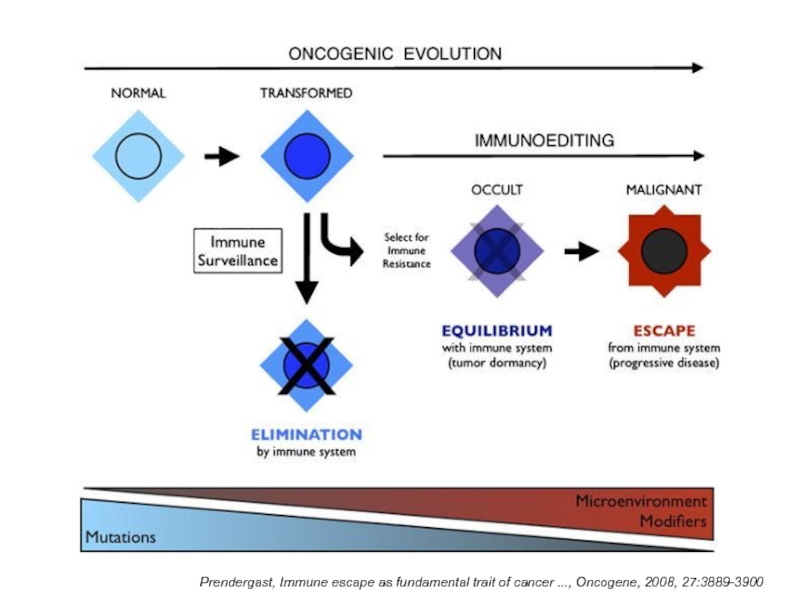
Слайд 43Как опухолевые клетки уходят
от иммунологического надзора ?
1. Понижение иммуногенности опухолевых
клеток
2. Инактивация иммуноцитов, создание защитного
барьера
3. Подавление внутриклеточных
реакций, ведущих к смерти клетки при ее взаимодействии с иммуноцитами,
антителами и белками комплемента (подавление апоптоза
и др. – лекция 4)
Слайд 44Adapted from The Biology of Cancer (© Garland Science 2007)
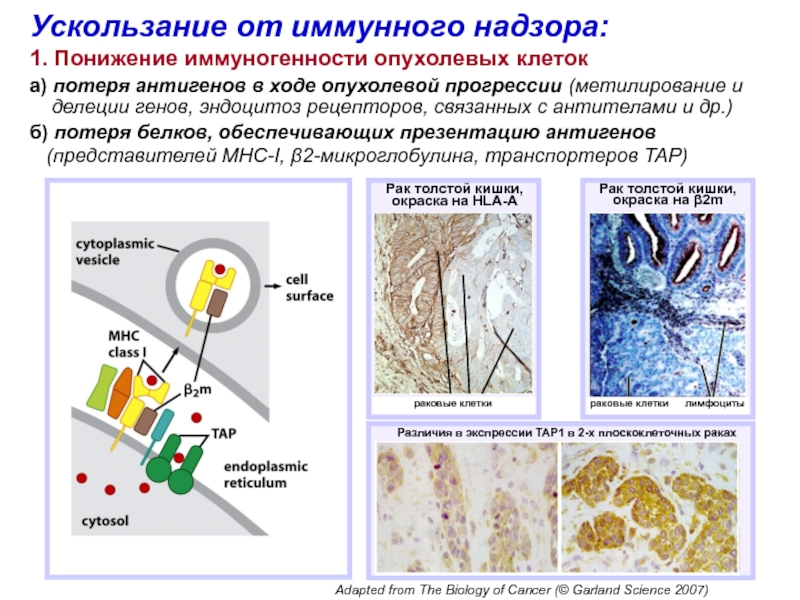
Ускользание
от иммунного надзора:
1. Понижение иммуногенности опухолевых клеток
а) потеря антигенов в
ходе опухолевой прогрессии (метилирование и делеции генов, эндоцитоз рецепторов, связанных с антителами и др.)
б) потеря белков, обеспечивающих презентацию антигенов
(представителей MHC-I, β2-микроглобулина, транспортеров TAP)
Рак толстой кишки,
окраска на HLA-A
Рак толстой кишки,
окраска на β2m
раковые клетки
лимфоциты
раковые клетки
Различия в экспрессии TAP1 в 2-х плоскоклеточных раках
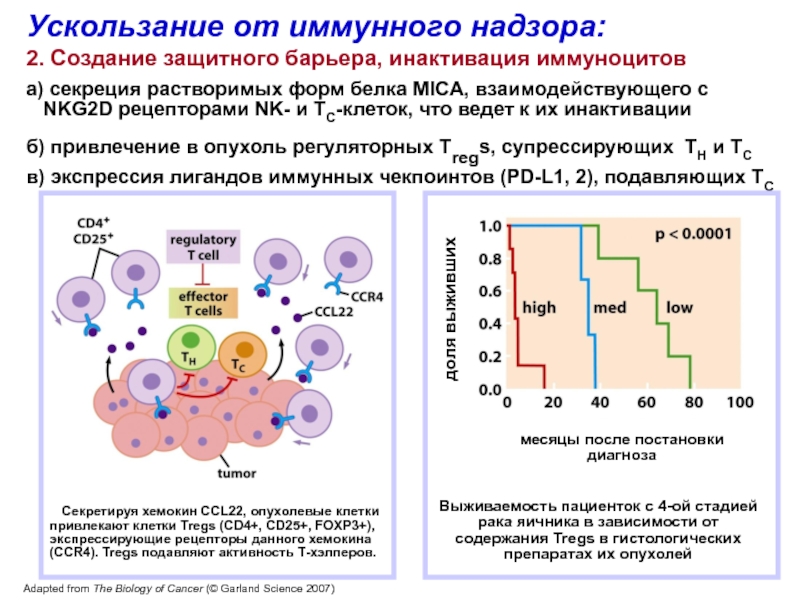
Слайд 45Ускользание от иммунного надзора:
2. Создание защитного барьера, инактивация иммуноцитов
а)
секреция растворимых форм белка MICA, взаимодействующего с
NKG2D
рецепторами NK- и TC-клеток, что ведет к их инактивацииб) привлечение в опухоль регуляторных Tregs, супрессирующих TH и TC
в) экспрессия лигандов иммунных чекпоинтов (PD-L1, 2), подавляющих TC
Секретируя хемокин CCL22, опухолевые клетки
привлекают клетки Tregs (CD4+, CD25+, FOXP3+),
экспрессирующие рецепторы данного хемокина
(CCR4). Tregs подавляют активность Т-хэлперов.
Выживаемость пациенток с 4-ой стадией рака яичника в зависимости от содержания Tregs в гистологических препаратах их опухолей
Adapted from The Biology of Cancer (© Garland Science 2007)
Слайд 46Fas-L
Fas-L
Fas-L
Fas
Fas-L
Fas
Апоптоз
Апоптоз
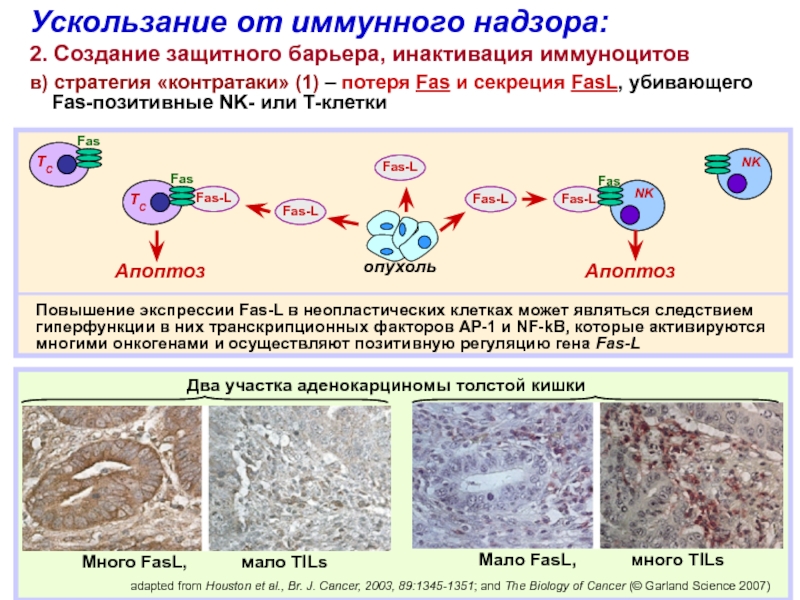
Повышение экспрессии Fas-L в неопластических клетках может являться следствием гиперфункции
в них транскрипционных факторов AP-1 и NF-kB, которые активируются многими
онкогенами и осуществляют позитивную регуляцию гена Fas-LNK
TС
Два участка аденокарциномы толстой кишки
adapted from Houston et al., Br. J. Cancer, 2003, 89:1345-1351; and The Biology of Cancer (© Garland Science 2007)
Много FasL, мало TILs
Мало FasL, много TILs
Fas
TС
Fas-L
NK
опухоль
Ускользание от иммунного надзора:
2. Создание защитного барьера, инактивация иммуноцитов
в) стратегия «контратаки» (1) – потеря Fas и секреция FasL, убивающего
Fas-позитивные NK- или Т-клетки
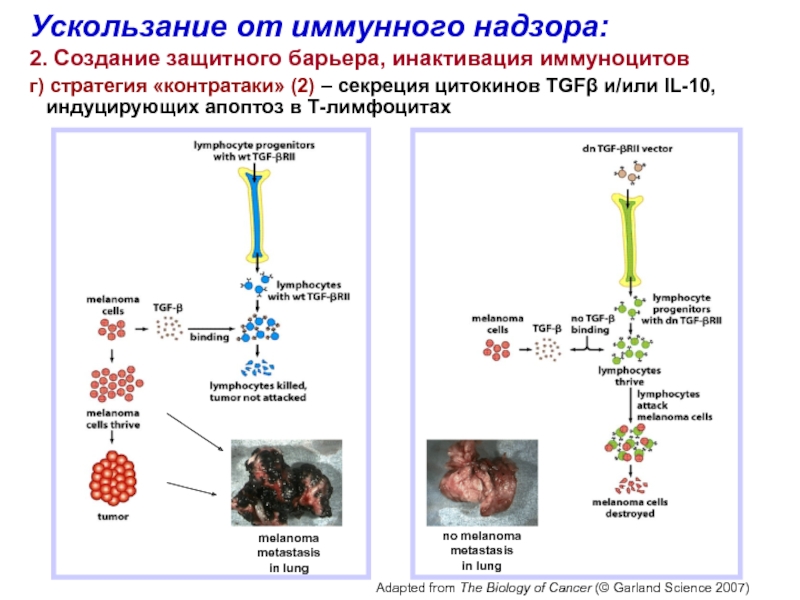
Слайд 47melanoma metastasis
in lung
Ускользание от иммунного надзора:
2. Создание защитного барьера, инактивация
иммуноцитов
г) стратегия «контратаки» (2) – секреция цитокинов TGFβ и/или
IL-10, индуцирующих апоптоз в Т-лимфоцитах
Adapted from The Biology of Cancer (© Garland Science 2007)
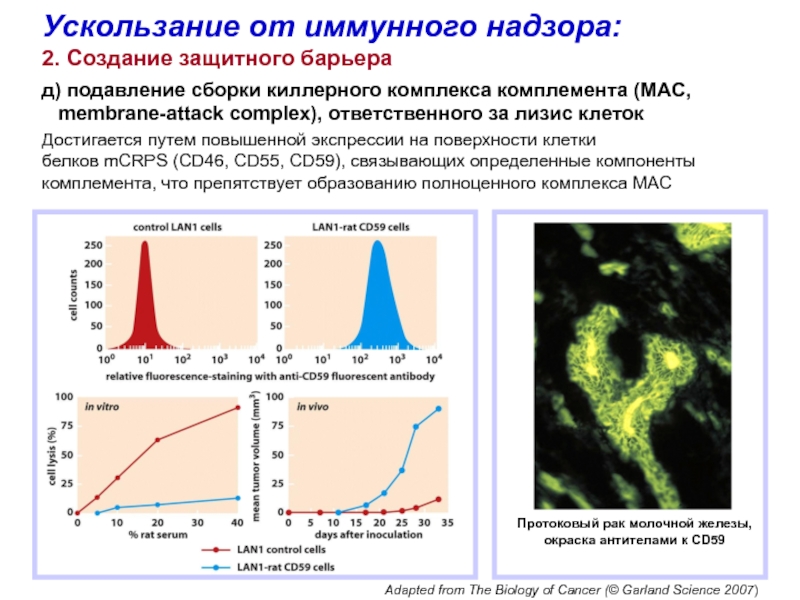
Слайд 48Ускользание от иммунного надзора:
2. Создание защитного барьера
д) подавление сборки
киллерного комплекса комплемента (MAC,
membrane-attack complex), ответственного за
лизис клетокДостигается путем повышенной экспрессии на поверхности клетки
белков mCRPS (CD46, CD55, CD59), связывающих определенные компоненты комплемента, что препятствует образованию полноценного комплекса MAC
Протоковый рак молочной железы,
окраска антителами к CD59
Adapted from The Biology of Cancer (© Garland Science 2007)