Слайд 1Л-5. Природные биоактивные соединения
Литература
1. Тюкавкина, Н.А. Биоорганическая химия: Учебник для
вузов / Н.А. Тюкавкина, Ю.И. Бауков. — М: Дрофа, 2004.
— 544 с.
2. Петров, А.А. Органическая химия: учебник для вузов / А.А. Петров, X.В. Вальян, А.Т. Трощенко. // Под ред. Стадничука М.Д. — 5-е изд., перераб. и доп. — СПб.: "Иван Федоров", 2002. — 624 с.
3. Травень, В.Ф. Органическая химия: Учебник для вузов: В 2 т. / В.Ф. Травень. - М: ИКЦ «Академкнига», 2004. - Т. 1. - 2004. - 727 с.; 2006. - Т. 2. - 2006. - 582 с.
4. Дрюк, В. Г. Курс органической химии / В.Г. Дрюк, М.С. Малиновский.— К.: Вища шк. Головное изд-во, 1987.— 400 с.
Вопросы
1. Углеводы. Биополимеры
1.1. Гликозиды 1.2. Крахмал, клетчатка
2. Аминокислоты. Биополимеры
2.1. Аминокислоты 2.2. Белки
3. Нуклеиновые кислоты. Биополимеры
3.1. Нуклеиновые кислоты 3.2. ДНК. РНК
3.3. Ферменты. Коферменты
Слайд 21. Углеводы. Биополимеры
Природные органические полимеры (биополимеры) составляют основу всех животных
и растительных организмов.
В растительном мире широко распространены полисахариды (целлюлоза, крахмал
и т.п.) и полиизопрены (натуральный каучук, гуттаперча, фрагменты липидов и т.п.).
Гликози́ды — органические соединения, молекулы которых состоят из двух частей:
углеводного (пиранозидного или фуранозидного) остатка;
не углеводного фрагмента (т. н. агликона).
В качестве гликозидов в более общем смысле могут рассматриваться и углеводы, состоящие из двух или более моносахаридных остатков.
Слайд 31.1. Гликозиды
Гликозиды представляют собой обширную группу органических веществ в растительном
(реже в животном) мире.
При кислотном, щелочном, ферментативном гидролизе они расщепляются на два или
несколько компонентов — агликон и углевод (или несколько углеводов).
Многие из гликозидов токсичны или обладают сильным физиологическим действием, например, гликозиды наперстянки, строфанта и другие.
Своё название гликозиды получили от греческих слов glykys — сладкий и eidos — вид, поскольку они при гидролизе распадаются на сахаристую и не сахаристую компоненты. В состав гликозидов входят углерод, водород, кислород, реже азот (амигдалин) и только некоторые содержат серу (синальбин, мирозин).
Слайд 41.1. Гликозиды
Гликозиды в чистом виде представляют собой нелетучие твердые вещества,
в большинстве случаев кристаллического строения. Они хорошо растворяются в воде
и спирте и обычно имеют горький вкус.
Химически гликозиды являются соединениями некоторых видов сахаров, чаще виноградного (глюкозы), со спиртами, кислотами, красящими и дубильными веществами и др.
Многие гликозиды так же, как и алкалоиды, сильно ядовиты. Для лечебных целей они применяются в очень небольших дозах.
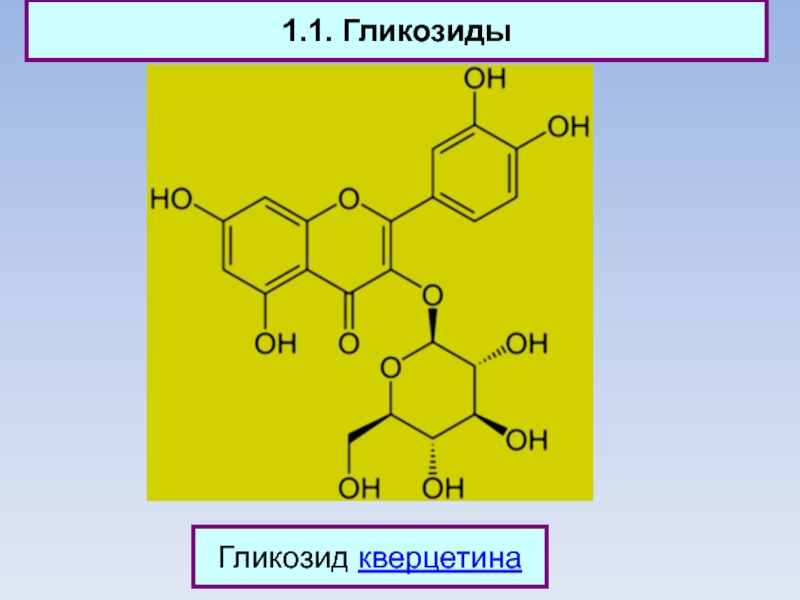
Слайд 51.1. Гликозиды
Гликозид кверцетина
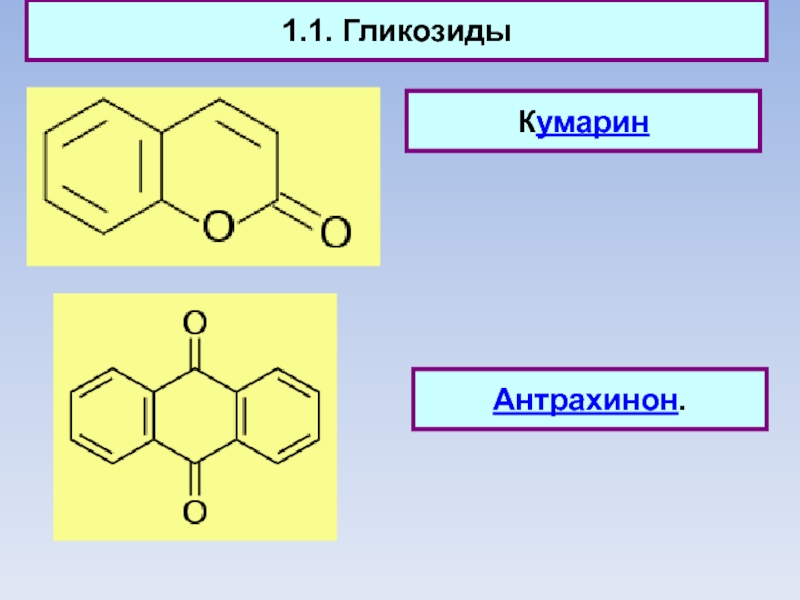
Слайд 61.1. Гликозиды
Кумарин
Антрахинон.
Слайд 71.1. Гликозиды
цианогенные или цианофорные гликозиды — образующие при гидролизе цианистоводородную кислоту;
например амигдалин, пруназин;
фенолгликозиды — содержащие фенольную группу или образующие её при гидролизе;
гликозиды группы кумарина. Гликозиды эти
широко распространены в природе; к ним относятся, к примеру, кумариновый гликозид, скиммин, эскулин, дафнин, фраксин. Все они при гидролизе распадаются на кумарин и сахар;
- оксиантрахиноновые гликозиды — широко распространены в природе; они большей частью окрашены в красный или жёлтый цвета. К ним относятся многие слабительные, например ревень, сенна, крушина, алоэ, содержащие производные оксиантрахинона. При гидролизе они распадаются на ди-, триоксиантрахиноны и сахар;
Слайд 81.1. Гликозиды
- Антрахинон - гликосинапиды — гликозиды, содержащие серу. Большей частью
они встречаются среди крестоцветных. При гидролизе они при участии фермента
мирозина образуют горчичное (эфирное) масло;
- сердечные гликозиды, содержащие в агликоне пергидро-циклопентано-фенантреновую структуру и характерный для данных гликозидов пятичленный (лактонный) цикл, наряду с ангулярной метильной или альдегидной группой при C10.
- цереброзиды, получаемые из мозгов животных; они являются d-галактозидами сфингозина;
- фитостеролины — являющиеся гликозидами стеринов (они широко распространены в природе, но мало исследованы).
Слайд 91.1. Гликозиды
Согласно другой классификации, в зависимости от природы атомов, формирующих
связь с агликоном, различают:
O-гликозиды: -O-HH-O-C6H11O5
C-гликозиды: -C-HH-O-C6H11O5
N-гликозиды: -N-HH-O-C6H11O5
S-гликозиды: -S-HH-O-C6H11O5
В зависимости от
химической природы агликона лекарственные O-гликозиды делятся на группы:
Цианогенные гликозиды
Сердечные гликозиды
Сапонины (тритерпеновые и стероидные соединения)
Антрагликозиды (антрацен)
Гликозиды-горечи
Слайд 101.1. Гликозиды
К сердечной группе относятся: дигитоксин (из листьев наперстянки), адонитоксин ицимарин (из травы адониса), конваллатоксин
и конвалламарин (из травы ландыша), строфантин (из семян строфанта).
Из растений
с гликозидами слабительного действия наибольшее значение имеют: жостер (в плодах содержатся рамноэмодин и другие гликозиды), ревень (содержит в корнях реин, реум-эмодин), крушина (в коре содержится франгулин и др.), сенна (в листьях находится алоэ-эмодин, реин и др.), алоэ (в сгущенном соке листьев содержится алоин и другие вещества).
К гликозидам относят также сапонины (содержатся в корнях истода, мыльнянки и др.), которые образуют с водой пену и употребляются внутрь в виде отваров как отхаркивающее.
Слайд 111.1. Гликозиды
Роль и значение гликозидов в растениях выяснена недостаточно. Хотя
гликозиды обладают различным химическим составом, соединения с меньшим молекулярным весом
значительно чаще встреча-ются в природе. Так, например, фазео-люнатин (или лимарин), содержащийся в фасоли, найден среди семейств лютиковых, лилейных, молочайных.
Ещё более распространены в природе гликозиды ароматической природы, являющиеся фенолами или эфирами фенолов, например арбутин, метиларбутин, кониферин. Близок кониферину и гесперидин, который можно рассматривать как халкон, «родственно» связанный с антоцианами и флавонами. Образование простейшего халкона можно рассматривать как конденсацию ацетофенона с бензальдегидом.
Слайд 121.1. Гликозиды
Роль и значение гликозидов в растениях выяснена недостаточно. Хотя
гликозиды обладают различным химическим составом, соединения с меньшим молекулярным весом
значительно чаще встреча-ются в природе. Так, например, фазео-люнатин (или лимарин), содержащийся в фасоли, найден среди семейств лютиковых, лилейных, молочайных.
Ещё более распространены в природе гликозиды ароматической природы, являющиеся фенолами или эфирами фенолов, например арбутин, метиларбутин, кониферин. Близок кониферину и гесперидин, который можно рассматривать как халкон, «родственно» связанный с антоцианами и флавонами. Образование простейшего халкона можно рассматривать как конденсацию ацетофенона с бензальдегидом.
Слайд 131.1. Гликозиды
Некоторые гликозиды, например семейства Loganiceae, содержат азот и представляют
как бы переход к алкалоидам.
В их состав входят пуриновые
и пиримидиновые производные, играющие важную роль во внутритканевых дыхательных процессах;
к ним относится и d-рибозид гуанина, известный под названием вернина.
Он обнаружен в ростках различных растений, в соке сахарной свеклы, в пыльце лесного ореха и сосны.
Слайд 141.2. Крахмал, клетчатка
Полисахариды - это природные высокомолекулярные углеводы, макромолекулы которых
состоят из остатков моносахаридов.
Основные представители - крахмал и целлюлоза -
построены из остатков одного моносахарида - глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n,
но совершенно различные свойства. Это обьясняется особенностями их пространственного строения.
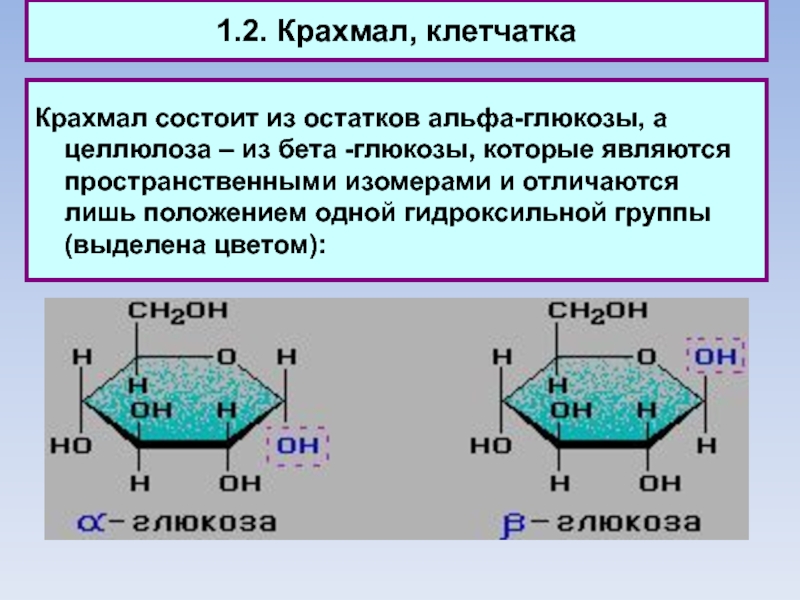
Слайд 151.2. Крахмал, клетчатка
Крахмал состоит из остатков альфа-глюкозы, а целлюлоза –
из бета -глюкозы, которые являются пространственными изомерами и отличаются лишь
положением одной гидроксильной группы (выделена цветом):
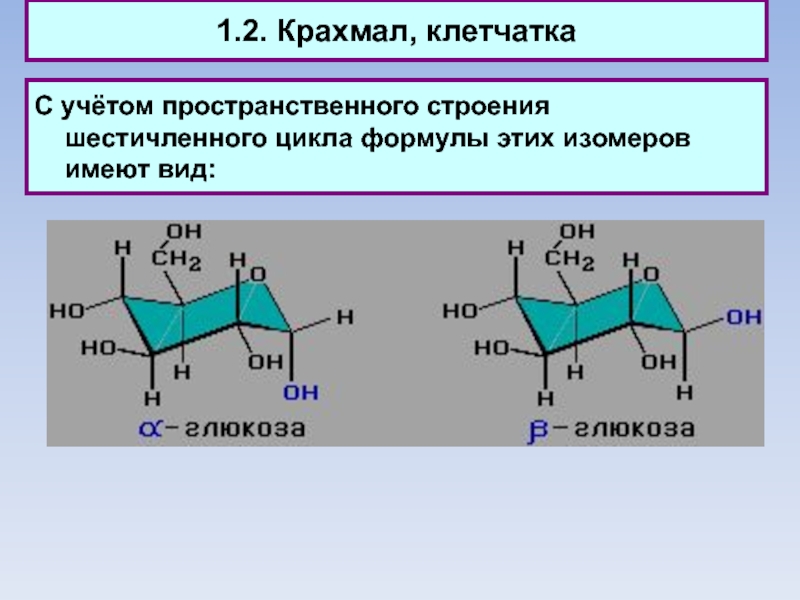
Слайд 161.2. Крахмал, клетчатка
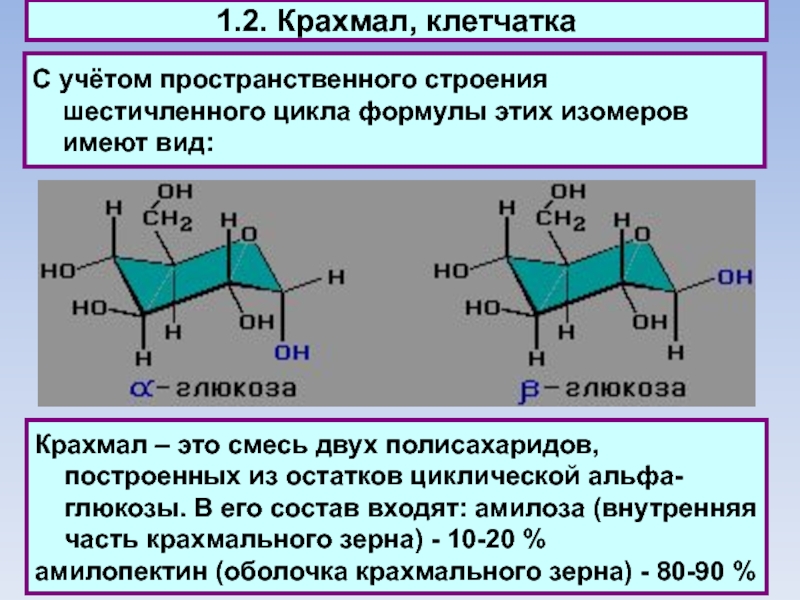
С учётом пространственного строения шестичленного цикла формулы этих
изомеров имеют вид:
Слайд 171.2. Крахмал, клетчатка
С учётом пространственного строения шестичленного цикла формулы этих
изомеров имеют вид:
Крахмал – это смесь двух полисахаридов, построенных
из остатков циклической альфа-глюкозы. В его состав входят: амилоза (внутренняя часть крахмального зерна) - 10-20 %
амилопектин (оболочка крахмального зерна) - 80-90 %
Слайд 181.2. Крахмал, клетчатка
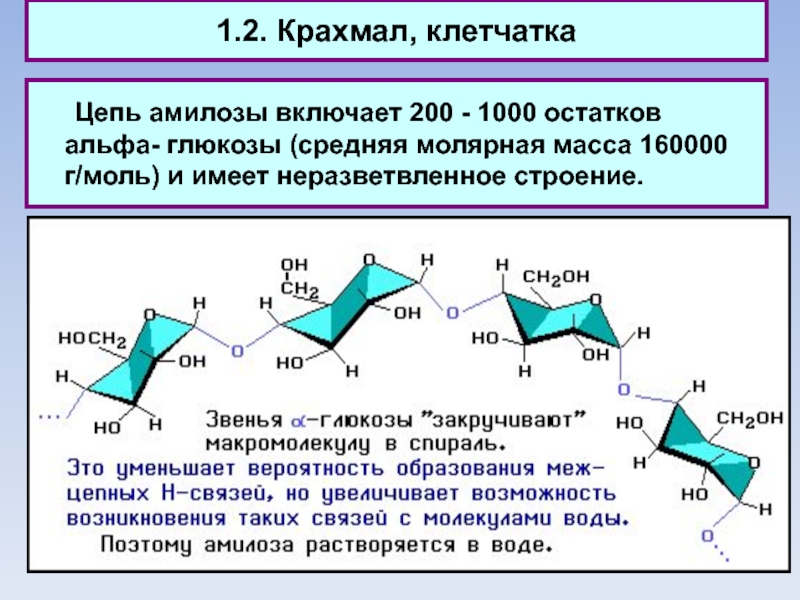
Цепь амилозы включает 200 - 1000 остатков альфа-
глюкозы (средняя молярная масса 160000 г/моль) и имеет неразветвленное строение.
Слайд 191.2. Крахмал, клетчатка
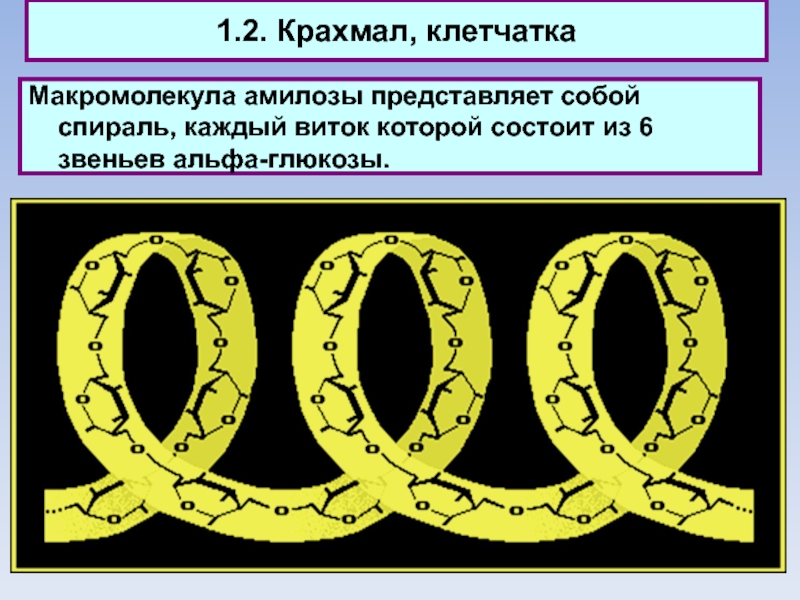
Макромолекула амилозы представляет собой спираль, каждый виток которой
состоит из 6 звеньев альфа-глюкозы.
Слайд 201.2. Крахмал, клетчатка
При взаимодействии амилозы с йодом в водном растворе
молекулы йода входят во внутренний канал спирали, образуя так называемое
соединение включения.
Это соединение имеет характерный синий цвет.
Данная реакция используется в аналитических целях для обнаружения как крахмала, так и йода (йод-крахмальная проба).
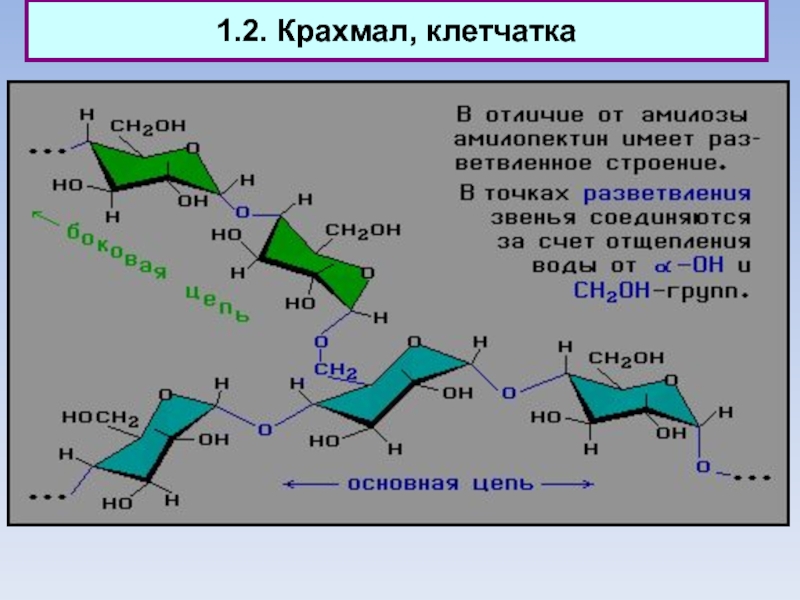
Амилопектин состоит из разветвлённых макромолекул, молярная масса которых достигает 1 - 6 млн. г/моль.
Подобно амилопектину построен гликоген (животный крахмал).
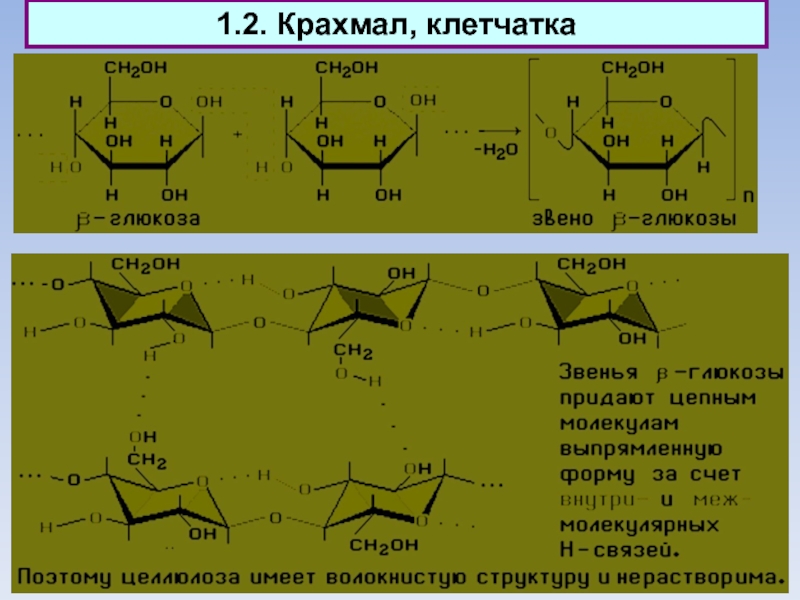
Слайд 221.2. Крахмал, клетчатка
Целлюлоза (клетчатка) - наиболее распространенный растительный полисахарид.
Этот биополимер
обладает большой механической прочностью и выполняет роль опорного материала растений,
образуя стенку растительных клеток. Используется в производстве волокон и бумаги. В большом количестве целлюлоза содержится в древесине и хлопке.
Цепи целлюлозы построены из остатков бета-глюкозы и имеют линейное строение.
Молярная масса целлюлозы - от 400000 до 2 млн. г/моль
Слайд 242.1. Аминокислоты
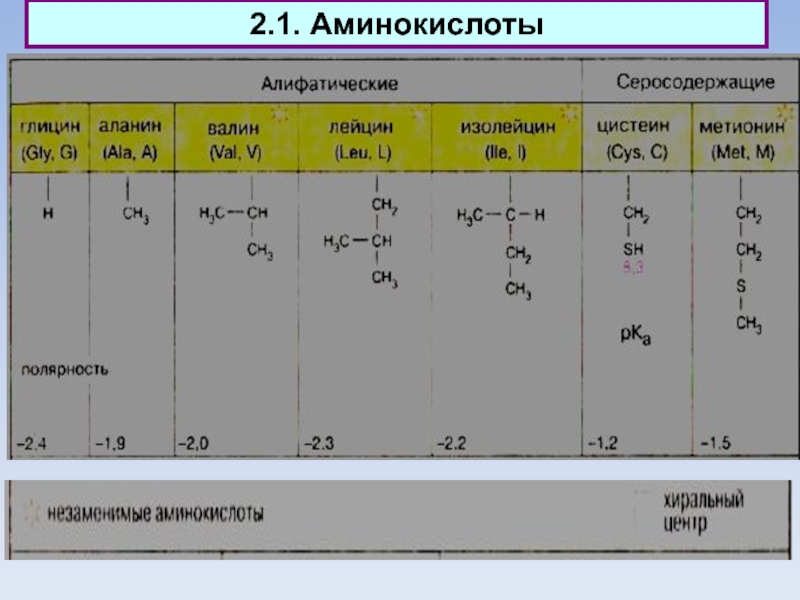
Протеино-генными называются 20 аминокислот, которые кодируются генетическим кодом и
включаются в белки в процессе трансляции.
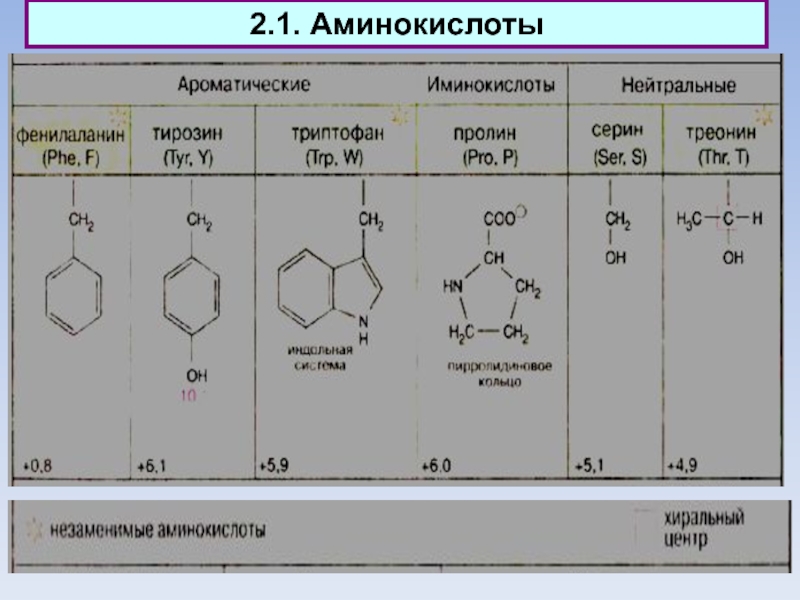
Ароматические аминокислоты содержат мезомерные (резонансно
стабилизированные) циклы. В этой группе лишь фенилаланин проявляет низкую низкую полярность. Тирозин и триптофан характеризуются заметной, а гистидин — даже высокой полярностью.
К алифатическим аминокислотам относятся глицин, аланин, валин, лейцин и изолейцин. Эти аминокислоты не несут в боковой цепи гетероатомов (N, О или S), циклических группировок и характеризуются отчётливо выраженной низкой полярностью.
Слайд 252.1. Аминокислоты
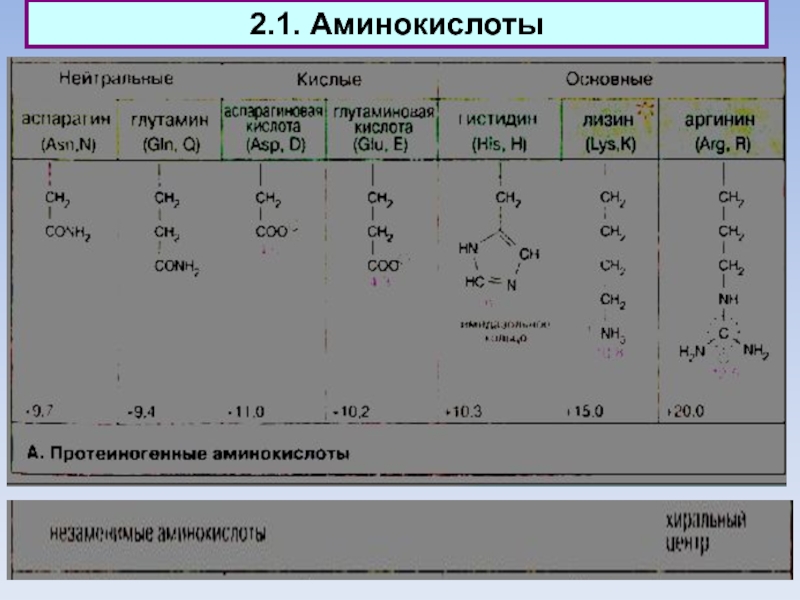
Нейтральные аминокислоты содержат гидроксильные (серин, треонин) или карбокс-амидные группы
(аспарагин, глутамин).
Хотя амидные группы не ионогенны, молекулы аспарагина и
глутамина высоко полярны.
Слайд 292.2. Белки
Белки являются основным органическим веществом, из которого построены клетки
животного организма (в растительных клетках белка содержится меньше).
Функции белков
в организме универсальны: ферментативная, структурная, рецепторная, сократительная, защитная, транспортная, регуляторная.
Белки (полипептиды) - биополимеры, построенные из остатков aльфа-аминокислот, соединённых пептидными (амидными) связями.
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации aльфа-аминокислот:
Слайд 302.2. Белки
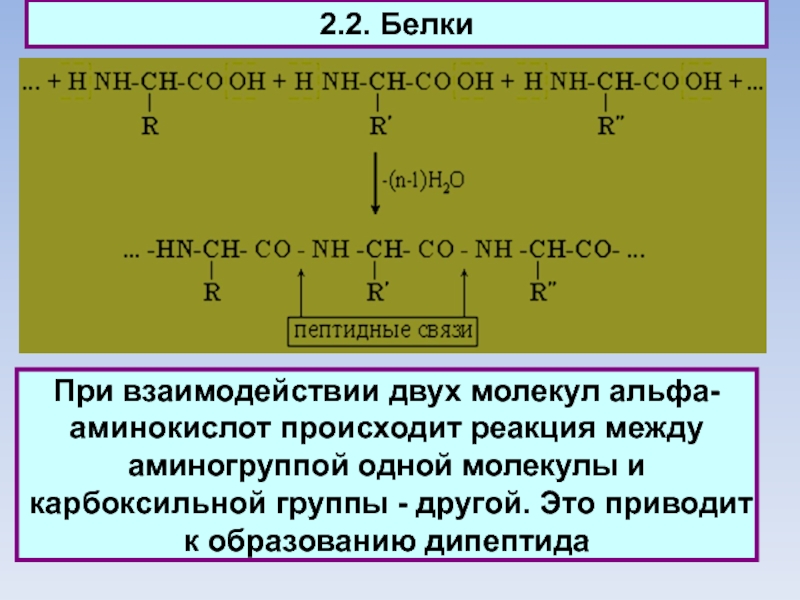
При взаимодействии двух молекул aльфа-аминокислот происходит реакция между аминогруппой
одной молекулы и карбоксильной группы - другой. Это приводит к
образованию дипептида
Слайд 312.2. Белки
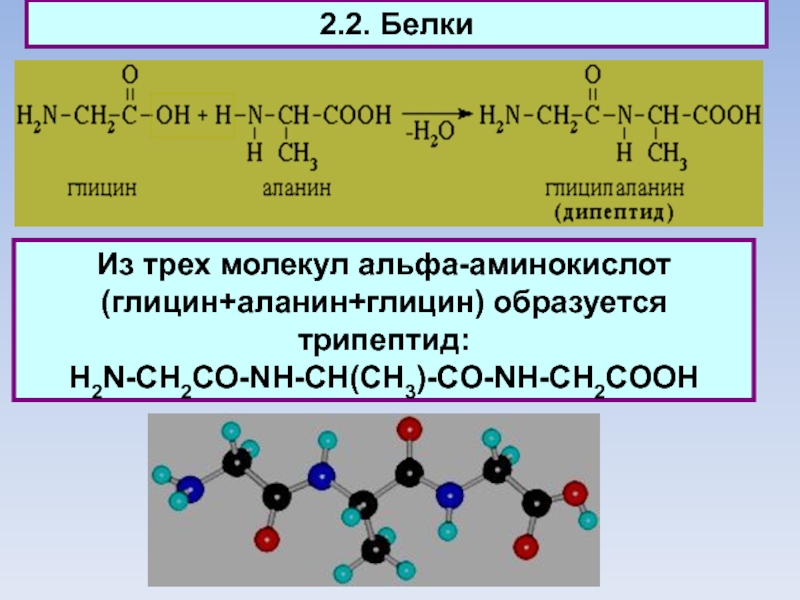
Из трех молекул aльфа-аминокислот (глицин+аланин+глицин) образуется трипептид:
H2N-CH2CO-NH-CH(CH3)-CO-NH-CH2COOH
Слайд 322.2. Белки
Аналогично происходит образование тетра-, пента- и полипептидов
Функции белков в
природе универсальны:
- каталитические (ферменты);
- регуляторные (гормоны);
- структурные (кератин
шерсти, фиброин шелка, коллаген);
- двигательные (актин, миозин);
- транспортные (гемоглобин);
- запасные (казеин, яичный альбумин);
- защитные (иммуноглобулины) и т.д.
Слайд 332.2. Белки
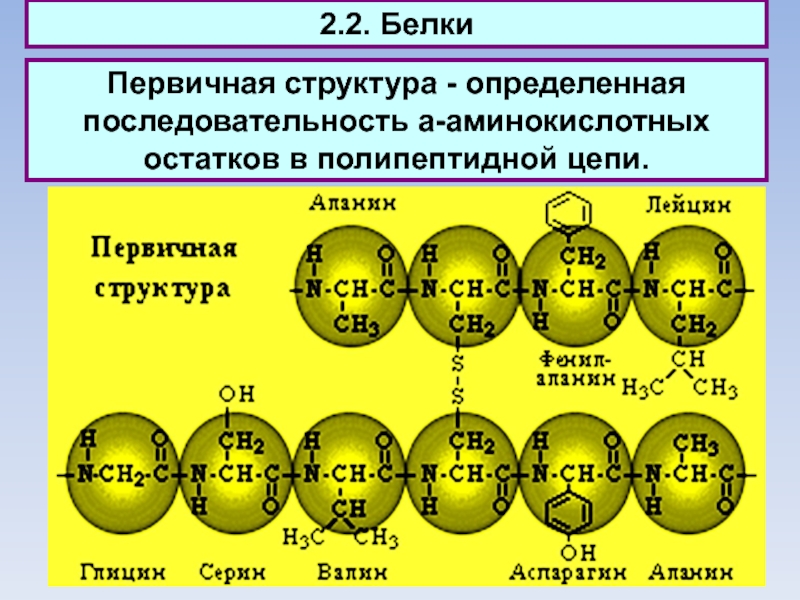
Первичная структура - определенная последовательность a-аминокислотных остатков в полипептидной
цепи.
Слайд 342.2. Белки
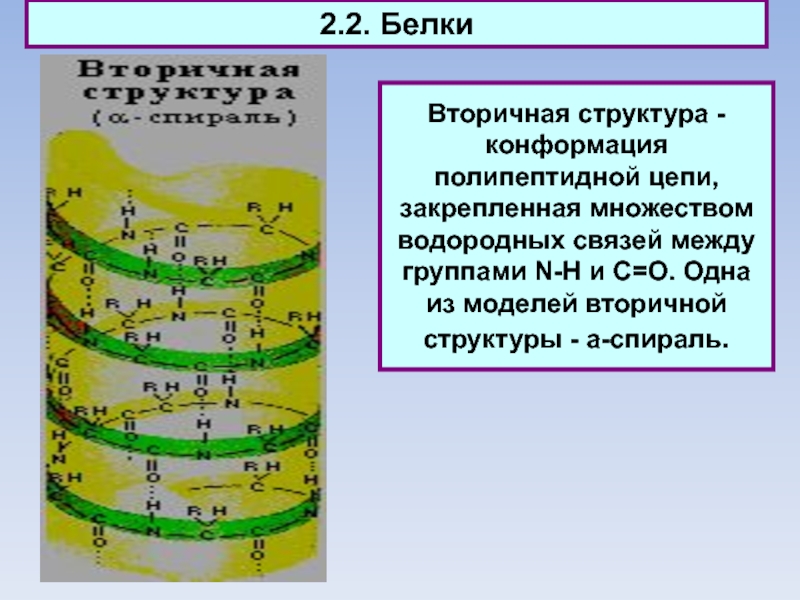
Вторичная структура - конформация полипептидной цепи, закрепленная множеством водородных
связей между группами N-H и С=О. Одна из моделей вторичной
структуры - a-спираль.
Слайд 352.2. Белки
Третичная структура - форма закрученной спирали в пространстве, образованная
главным образом за счет дисульфидных мостиков -S-S-, водородных связей, гидрофобных
и ионных взаимодействий.
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов.
Слайд 362.2. Белки
Четвертичная структура - агрегаты нескольких белковых макромолекул (белковые комплексы),
образованные за счёт взаимодействия разных полипептидных цепей.
Несмотря на многочисленность белков,
в их состав входят остатки лишь 22 a-аминокислот.
Слайд 373. Нуклеиновые кислоты. Биополимеры
Нуклеиновые кислоты осуществляют хранение, воспроизводство и реализацию
генетической информации, управляют точным ходом биосинтеза белков в клетках.
Нуклеиновые кислоты
(HK) - это биополимеры, макромолекулы которых состоят из многократно повторяющихся звеньев - нуклеотидов. Поэтому их называют также поли-нуклеотидами.
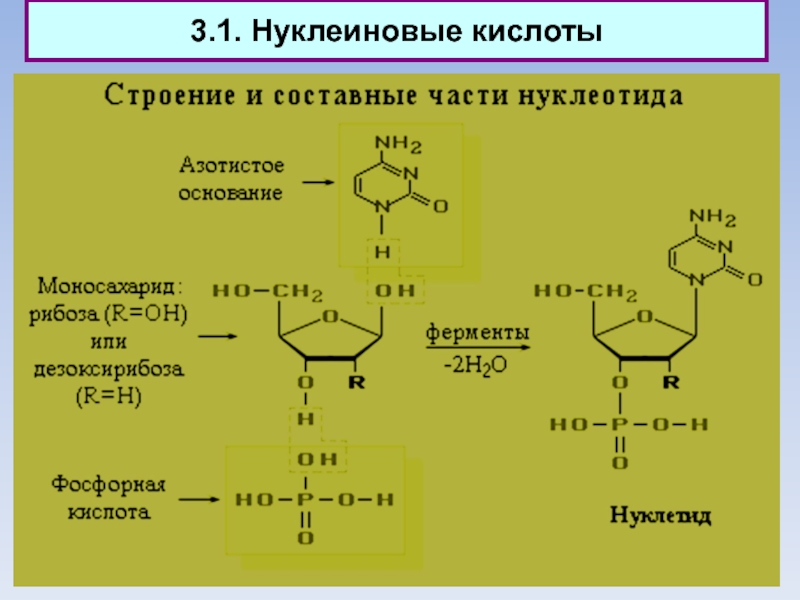
В состав нуклеотида - структурного звена нуклеиновых кислот - входят три составные части:
- азотистое основание - пиримидиновое или пуриновое;
- моносахарид - рибоза или 2-дезоксирибоза;
- остаток фосфорной кислоты.
Слайд 383. Нуклеиновые кислоты. Биополимеры
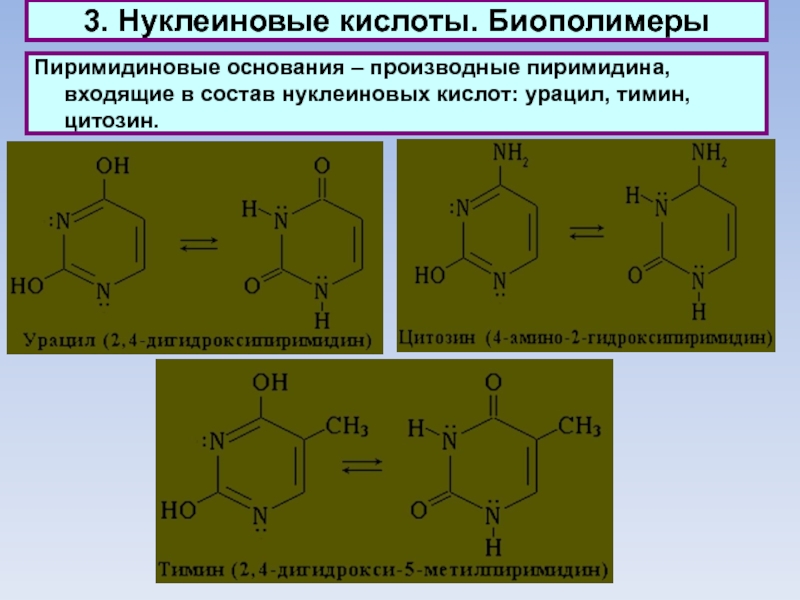
Пиримидиновые основания – производные пиримидина, входящие в
состав нуклеиновых кислот: урацил, тимин, цитозин.
Слайд 393. Нуклеиновые кислоты. Биополимеры
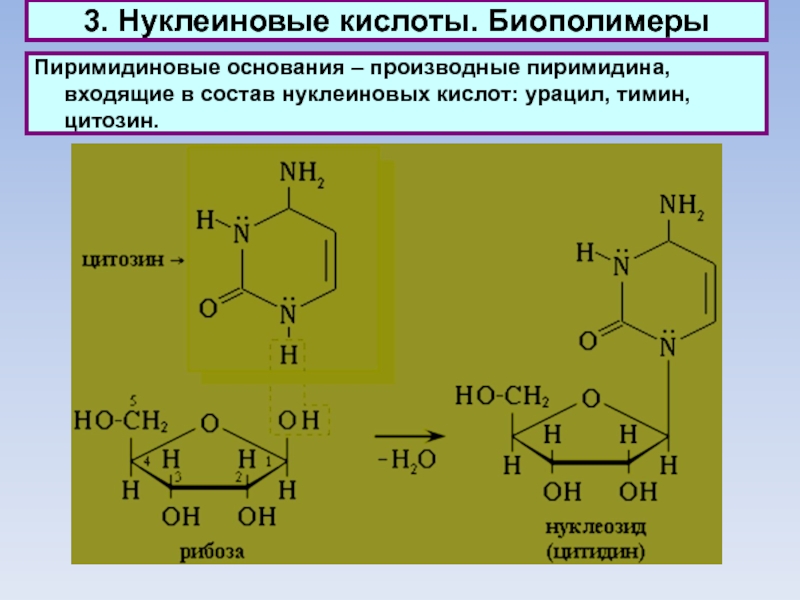
Пиримидиновые основания – производные пиримидина, входящие в
состав нуклеиновых кислот: урацил, тимин, цитозин.
Слайд 413.1. Нуклеиновые кислоты
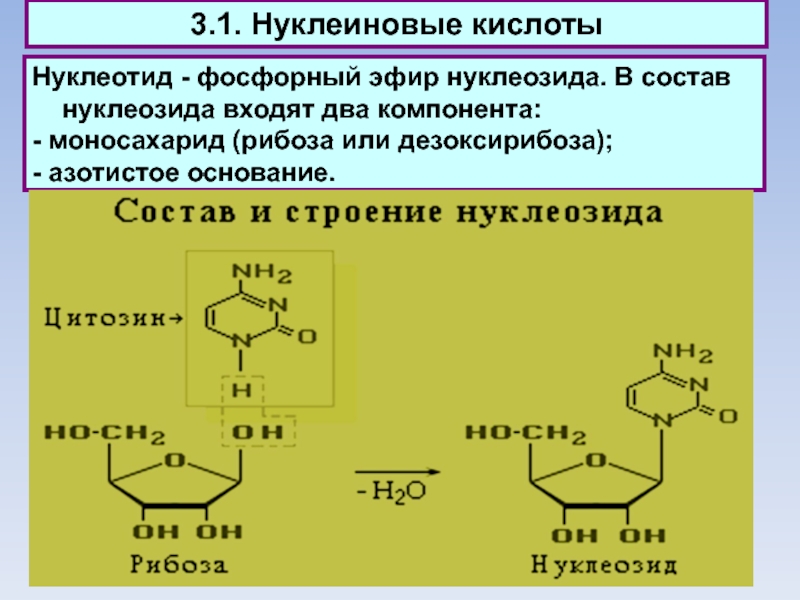
Нуклеотид - фосфорный эфир нуклеозида. В состав нуклеозида
входят два компонента:
- моносахарид (рибоза или дезоксирибоза);
- азотистое основание.
Слайд 423.2. ДНК. РНК
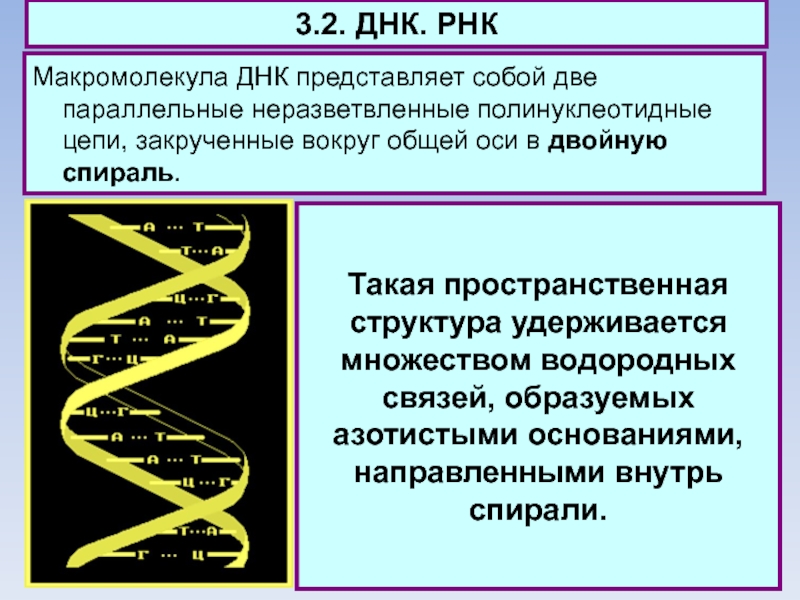
Макромолекула ДНК представляет собой две параллельные неразветвленные полинуклеотидные
цепи, закрученные вокруг общей оси в двойную спираль.
Такая пространственная структура
удерживается множеством водородных связей, образуемых азотистыми основаниями, направленными внутрь спирали.
Слайд 433.2. ДНК. РНК
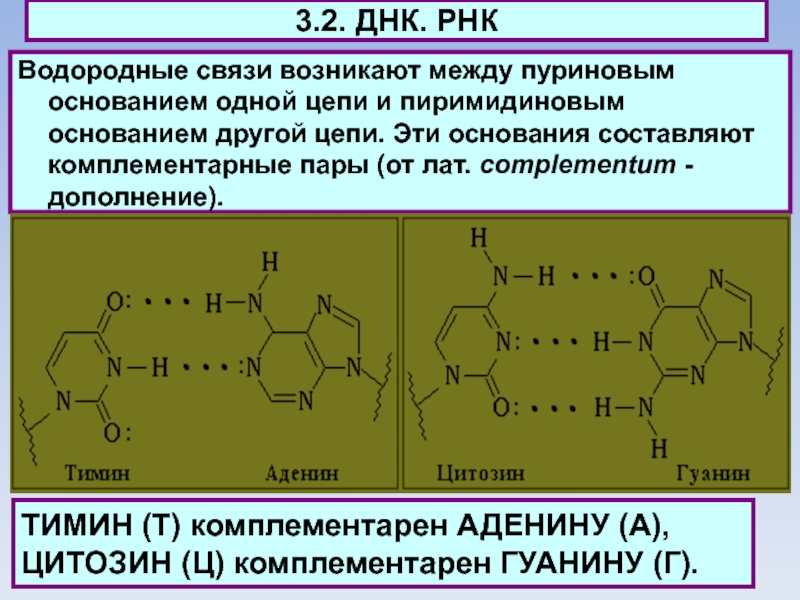
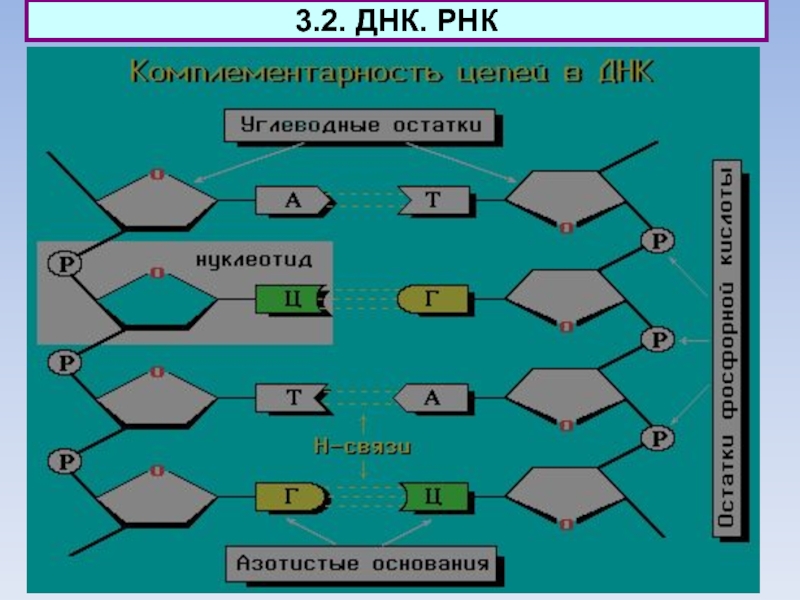
Водородные связи возникают между пуриновым основанием одной цепи
и пиримидиновым основанием другой цепи. Эти основания составляют комплементарные пары
(от лат. complementum - дополнение).
ТИМИН (Т) комплементарен АДЕНИНУ (А),
ЦИТОЗИН (Ц) комплементарен ГУАНИНУ (Г).
Слайд 453.2. ДНК. РНК
Способность ДНК не только хранить, но и использовать
генетическую информацию определяется следующими ее свойствами:
· молекулы ДНК способны
к репликации (удвоению), т.е. могут обеспечить возможность синтеза других молекул ДНК, идентичных исходным;
· молекулы ДНК могут направлять совершенно точным и определённым образом синтез белков, специфичных для организмов данного вида.
Слайд 463.2. ДНК. РНК
Способность ДНК не только хранить, но и использовать
генетическую информацию определяется следующими ее свойствами:
· молекулы ДНК способны
к репликации (удвоению), т.е. могут обеспечить возможность синтеза других молекул ДНК, идентичных исходным;
· молекулы ДНК могут направлять совершенно точным и определённым образом синтез белков, специфичных для организмов данного вида.
Слайд 473.3. Ферменты
Ферме́нты, или энзи́мы (от лат. fermentum, греч. ζύμη, ἔνζυμον
— закваска) — обычно белковые молекулы или молекулы РНК (рибозимы)
или их комплексы, ускоряющие (катализирующие) химические реакции в живых системах.
Слайд 483.3. Ферменты
Классификация ферментов по типу химических реакций):
1 класс –
оксидоредуктазы: катализируют окислительно-восстановительные процессы - (дегидрогеназы, оксидазы, цитохромы).
2 класс
– трансферазы: катализируют реакции переноса химических групп, название берут от группы, которую переносят (метилтрансферазы, сульфотрансферазы, аминотрансферазы, фосфотрансферазы, ацилтрансферазы).
3 класс – гидролазы: катализируют реакции гидролиза, т.е. расщепление субстрата с участи- ем воды (пептидазы, эстеразы, фосфатазы, гликозидазы).
Слайд 493.3. Ферменты
Классификация ферментов по типу химических реакций):
4 класс –
лиазы: катализируют реакции расщепления ковалентных связей между атомами C, O,
N, S негидролитическим путем (декарбоксилазы, альдолазы, дегидратазы).
5 класс – изомеразы: катализируют реакции изомеризации (эпимеразы, рацемазы, изомера- зы).
6 класс – лигазы: (синтетазы) катализируют реакции синтеза молекул за счет энергии АТФ (АТФ-синтаза, пируваткарбоксилаза).
Слайд 503.3. Ферменты
Клеточная организация ферментативной активности
Ферменты располагаются в субклеточных структурах (органеллах)
соответственно их функциям:
а) в ядре содержатся ферменты преобразования нуклеиновых
кислот;
б) во внутренней мембране митохондрий – ферменты дыхательной цепи;
в) в лизосомах – гидролазы;
г) в цитоплазме – ферменты гликолиза, синтеза жирных кислот;
д) в матриксе митохондрий – ферменты ЦТК, окислительного декарбоксилирования α-кетокислот, β– окисления жирных кислот;
е) плазматическая мембрана содержит ферменты транслоказы, которые переносят через мембрану ионы Nа+ , К+ , глюкозу, аминокислоты и т.д
Слайд 513.8. Гетероциклы
Алкалоиды
Производными пиридина и пиперидина являются некоторые представители большой группы
природных веществ основного характера — алкалоидов.
Алкалоиды содержатся в растительных
организмах и часто обладают сильным физиологическим и фармакологическим действием.
Слайд 523.8. Гетероциклы
Алкалоиды
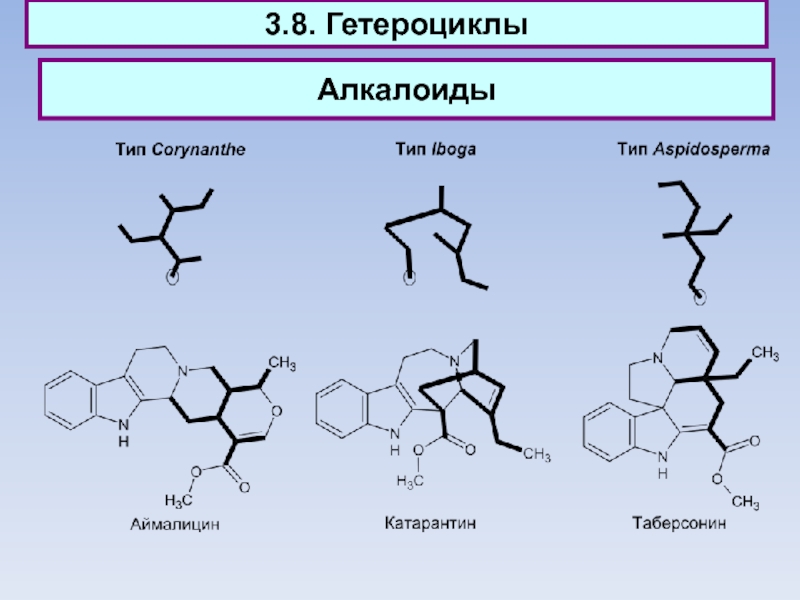
Большинство изученных алкалоидов имеет в своей основе более или
менее сложно построенные гетероциклические системы; они могут быть классифицированы по
природе гетеро-циклов:
1. Алкалоиды группы пиридина (кониин, никотин, анабазин).
2. Алкалоиды группы хинолина (хинин, цинхонин).
3. Алкалоиды группы изохинолина (папаверин, наркотин, курарин).
4. Алкалоиды группы фенантренизохинолина (морфин, кодеин, тебаин).
5. Алкалоиды группы конденсированных пирролидинпиперидиновых циклов, группы тропина (атропин, кокаин).
6. Алкалоиды группы пурина (кофеин, теобромин).
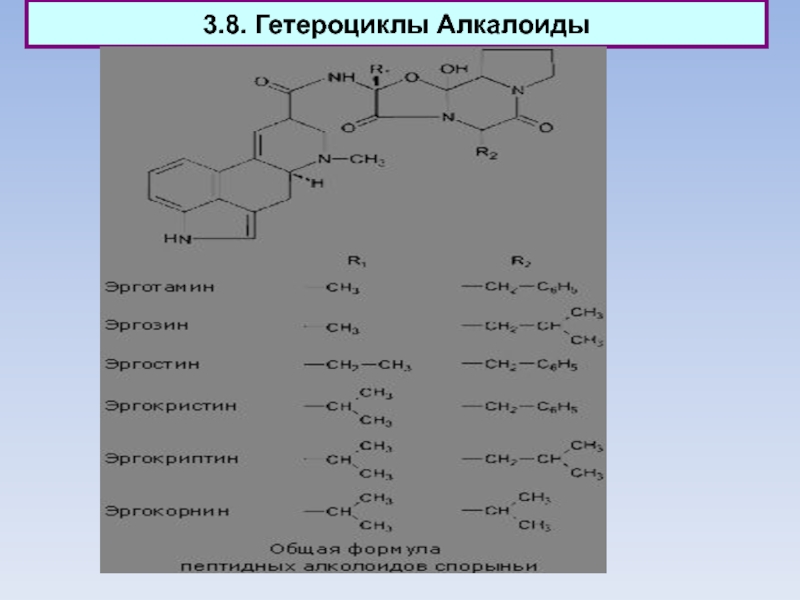
Слайд 553.8. Гетероциклы Алкалоиды
Сейчас известны сведения и выделено более 10 000
алкалоидов.
Основными источниками алкалоидов являются грибы и растения, (особенно богаты ими
растения из семейства бобовых, маковых, паслёновых, лютиковых, маревых, сложноцветных), а действуют на животных, поражая нервную и мышечную системы.
Химические основы их действия, в общем, понятны. Многие гормоны и медиаторы в организме животных — амины или пептиды, также производные аминокислот.
Это ацетилхолин, адреналин, норадреналин, серотонин, дофамин, эндорфины и другие.
Алкалоиды в химическом отношении похожи на них . Попав в тело животного или человека, они связываются с рецепторами, предназначенными для регуляторных молекул самого организма, и блокируют или запускают разнообразные процессы, например передачу сигнала (ацетилхолина) от нервных окончаний мышцам.
Слайд 563.8. Гетероциклы Алкалоиды
Атропин— антихолинергическое средство, алкалоид, содержащийся в различных растениях
семейства паслёновых: красавке, белене, разных видах дурмана и др.
Применяют атропин
при язвенной болезни желудка и двенадцатиперстной кишки, пилороспазме, холецистите, желчнокаменной болезни, при спазмах кишечника и мочевых путей, бронхиальной астме, для уменьшения секреции слюнных, желудочных и бронхиальных желез, при брадикардии, развившейся в результате повышения тонуса блуждающего нерва.
При болях, связанных со спазмами гладкой мускулатуры, атропин часто вводят вместе с анальгезирующими средствами (анальгин, промедол, морфин и др.).
В анестезиологической практике атропин применяют перед наркозом и операцией и во время операции для предупреждения бронхиоло- и ларингоспазма, ограничения секреции слюнных и бронхиальных желез и уменьшения других рефлекторных реакций и побочных явлений, связанных с возбуждением блуждающего нерва.
Слайд 573.8. Гетероциклы Алкалоиды
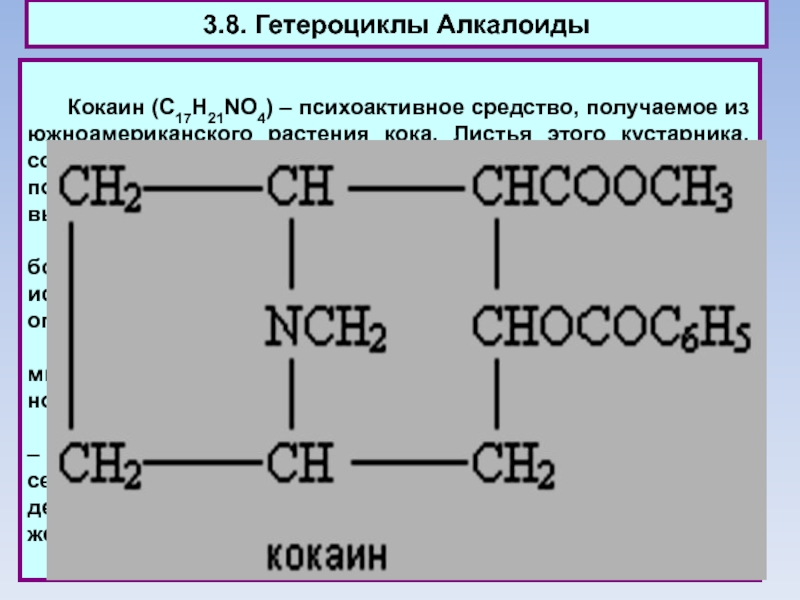
Кокаин (C17H21NO4) – психоактивное средство, получаемое из южноамериканского
растения кока. Листья этого кустарника, содержащие от 0,5 до 1%
кокаина, - Жевание листьев коки помогало индейцам древней империи инков переносить высокогорный климат.
Из-за уникальной способности одновременно блокировать болевые ощущения и уменьшать кровотечение кокаин все еще используют в медицинской практике при хирургических операциях в ротовой и носовой полости.
Воздействие на психику проявляется уже через несколько минут: человек чувствует прилив энергии, ощущает в себе новые возможности.
Физиологический эффект кокаина сходен с легким стрессом – незначительно повышается кровяное давление, учащаются сердцебиения и дыхание. Через некоторое время наступают депрессия и беспокойство, что приводит к необоримому желанию принять новую дозу, чего бы это ни стоило.
Слайд 583.8. Гетероциклы Алкалоиды
Морфин C17H19NO3 (из мака) и скополамин C17H21NO4 (из скополии и белладонны)
действуют успокаивающе на нервную систему.
Пилокарпин (из растения пилокарпус), в отличие от
атропина, суживает зрачки.
Стрихнин (из семян чилибухи) является сильнейшим ядом. Введенный в кровь в количестве хотя бы 0,01 г, он вызывает временный паралич окончаний двигательных нервов, а в больших дозах - смерть.
Хинин, добываемый из хинного дерева, обладает жаропонижающим действием и широко применяется при малярии.
Платифиллин (из крестовника широколистного) оказывает антиспазматическое действие и применяется при бронхиальной астме, язве желудка и двенадцатиперстной кишки и других заболеваниях.
Сальсолин (из солянки Рихтера) способствует понижению кровяного давления и применяется при гипертонии.
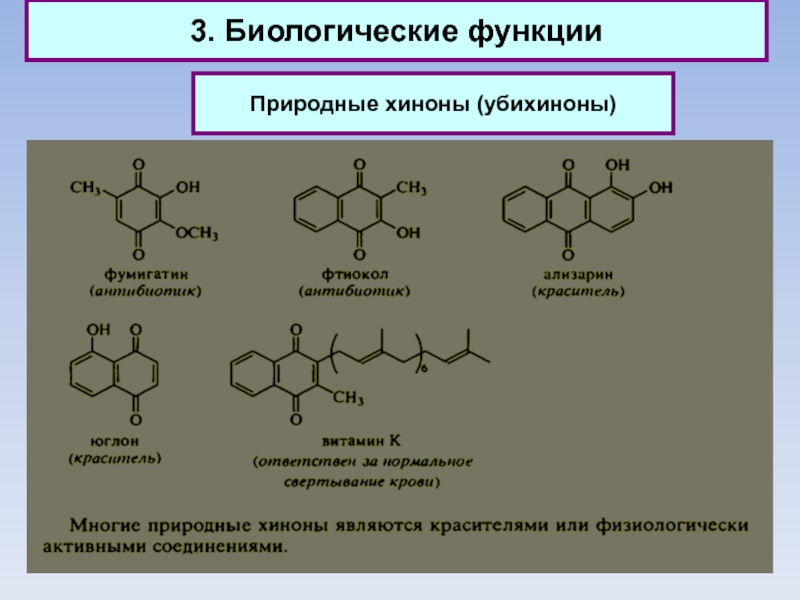
Слайд 603. Биологические функции
Природные хиноны (убихиноны)
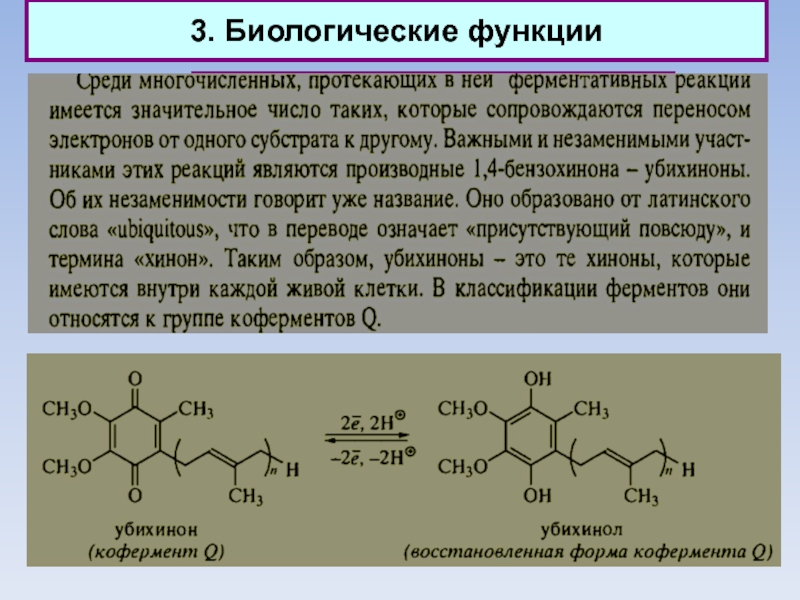
Слайд 613. Биологические функции
Природные хиноны (убихиноны)