Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лектор: ст. преподаватель каф. биологической химии Миронова Ксения
Содержание
- 1. Лектор: ст. преподаватель каф. биологической химии Миронова Ксения
- 2. Биохимия – образно говоря, наука о жизни.И
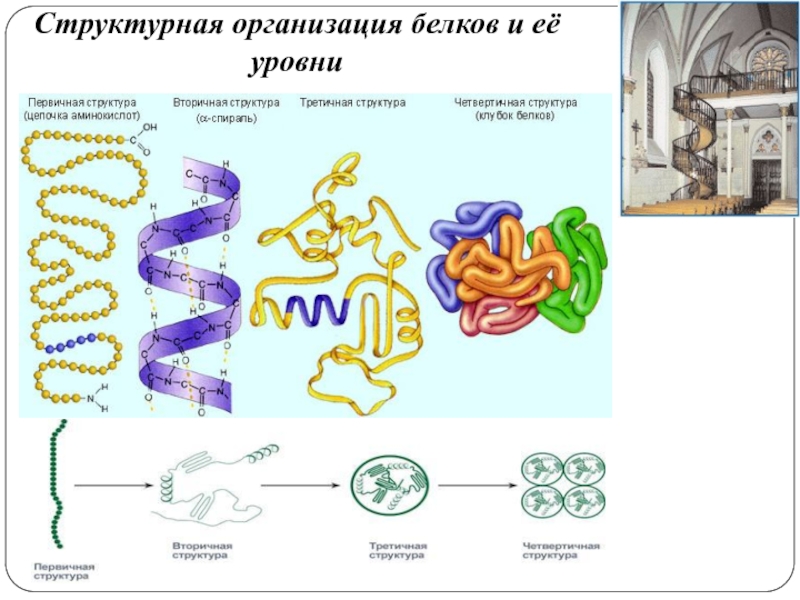
- 3. Структурная организация белков и её уровни
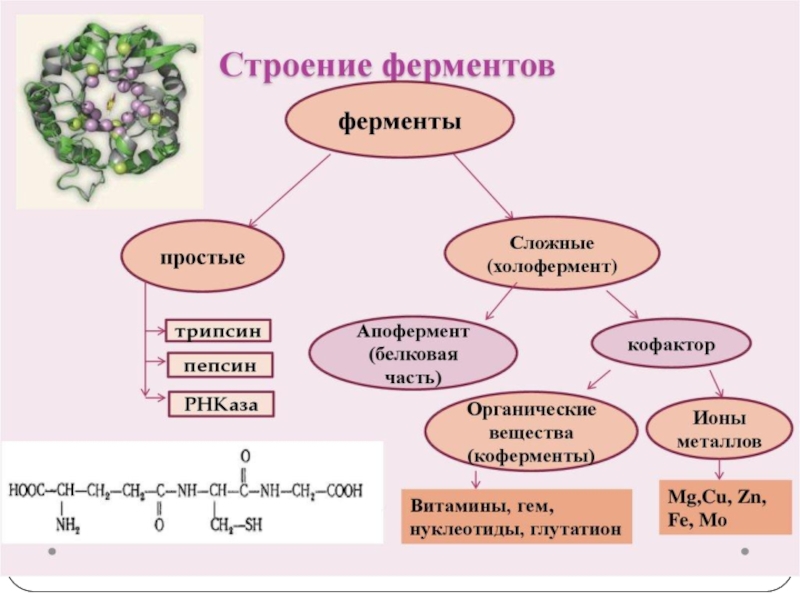
- 4. ФЕРМЕНТЫ или энзимы (Е) - биокатализаторы белковой
- 5. Свойства Е как хим. катализаторов:
- 6. Слайд 6
- 7. Строение ферментов (Е)Активный центр (АЦ) фермента участок
- 8. Свойства ферментов1. Термолабильность ( V от to
- 9. 3. Зависимость скорости реакции от концентрации фермента4. Зависимость скорости реакции от концентрации субстрата
- 10. Кинетика ферментативных реакций (Михаэлис, Ментен 1913 г.)
- 11. Классификация Е В 1961 г в Москве V
- 12. Слайд 12
- 13. Название Е1. Систематическое название – согласно современной
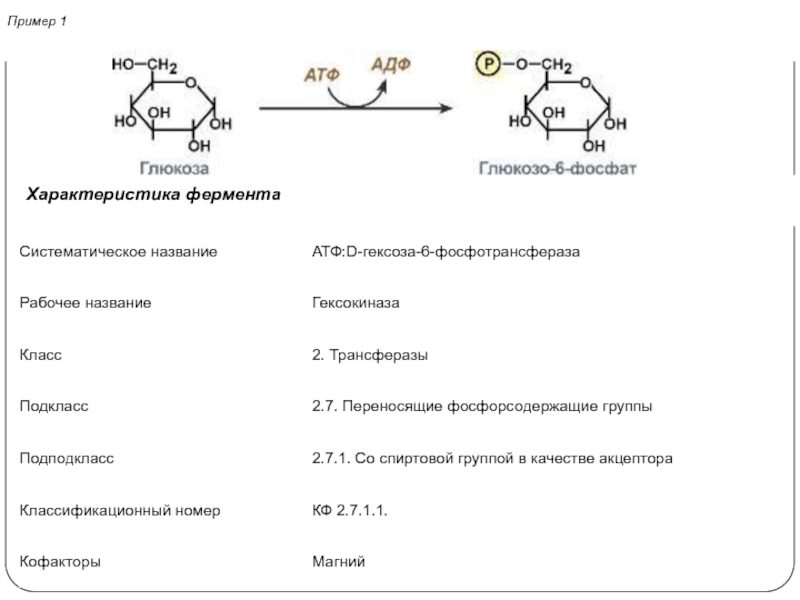
- 14. Пример 1Характеристика фермента
- 15. Слайд 15
- 16. Изоферменты Определение: группа белков, катализирующая одну реакцию,
- 17. Ферменты проявляют специфичностьСпецифичность, т.е. высокая избирательность действия
- 18. 1. Теория Фишера (модель "жесткой матрицы", "ключ-замок") – активный
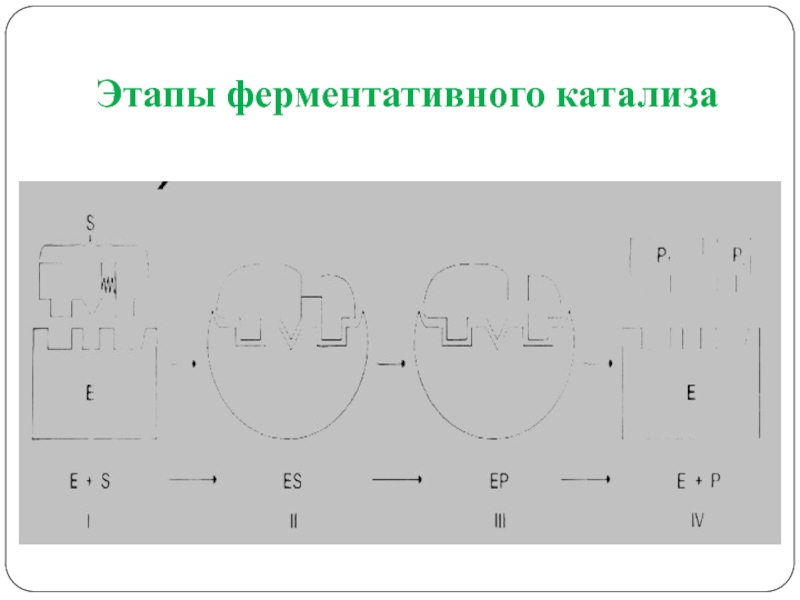
- 19. Этапы ферментативного катализа
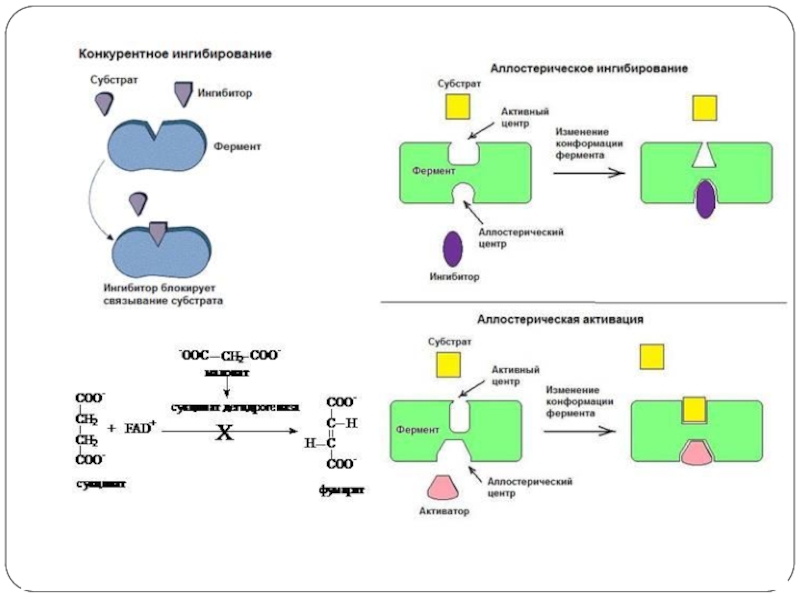
- 20. Регуляция активности ферментов Доступность субстрата или кофермента Изменение
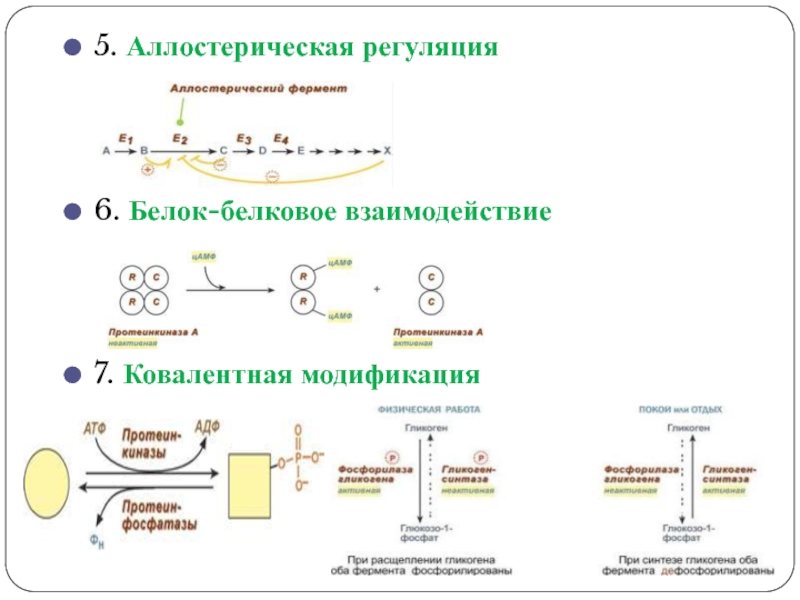
- 21. 5. Аллостерическая регуляция6. Белок-белковое взаимодействие7. Ковалентная модификация
- 22. Слайд 22
- 23. Слайд 23
- 24. Механизм необратимого ингибирования ацетилхолинэстеразыМеханизм необратимого ингибирования циклооксигеназыСходство
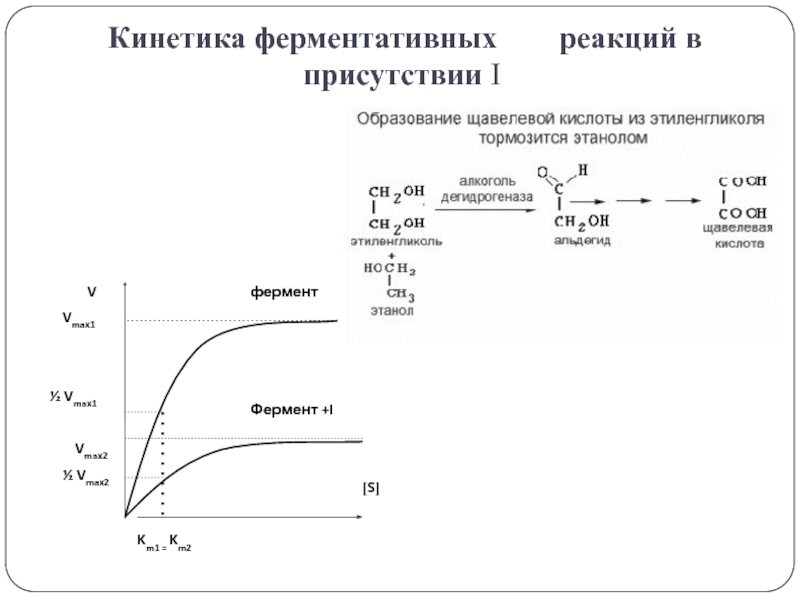
- 25. Кинетика ферментативных реакций в присутствии I
- 26. Ферменты в медицине: энзимодиагностика заболеваний;лечение: комплексы ферментов
- 27. Использование ферментов в медицине происходит по четырем направлениям:энзимодиагностика,энзимотерапия,использование ферментов в медицинских технологиях и промышленности.применение ингибиторов ферментов
- 28. ЭнзимотерапияЭнзимотерапия – это использование ферментов в качестве
- 29. Спасибо за внимание!Белок счастья
- 30. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Лектор:
ст. преподаватель каф. биологической химии
Миронова Ксения Александровна
E-mail: kseniya.chem@gmail.com
Биохимия
как наука.
Слайд 2Биохимия – образно говоря, наука о жизни.
И очень важно, что
основные химические вещества и важные метаболические процессы одинаковы и для
бактерий и для человека. Другими словами, основные принципы биохимии одинаковы для всех живых организмов.Слайд 4ФЕРМЕНТЫ или энзимы (Е) - биокатализаторы белковой природы, ускоряющие реакции
в клетке.
Лат. Fermentum –закваска, а энзим от греч.
Еп - в и zyme – дрожжиФерменты (Е) катализируют превращение веществ, кот. наз. - субстраты – (S), в продукт (Р).
Е Е
В общем виде: S Р А + В А--В
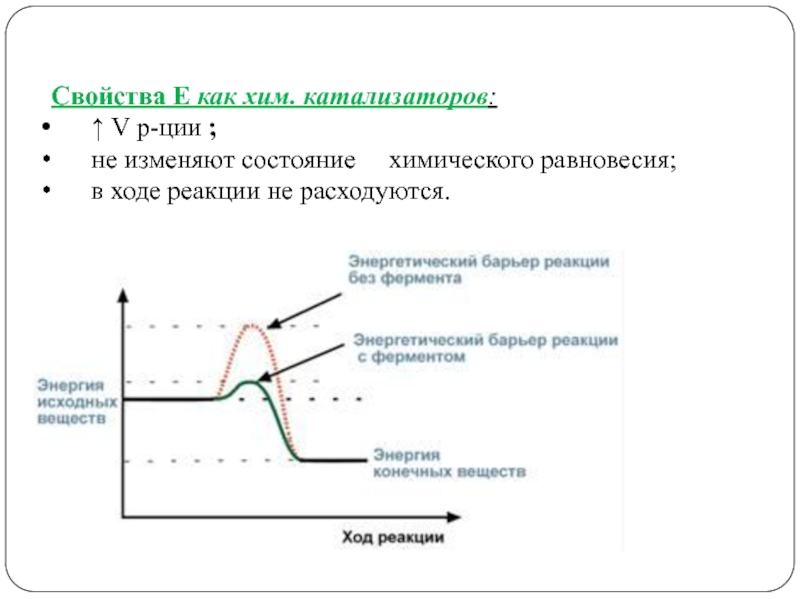
Слайд 5Свойства Е как хим. катализаторов:
↑ V р-ции ;
не изменяют состояние химического равновесия;
в ходе реакции не расходуются.
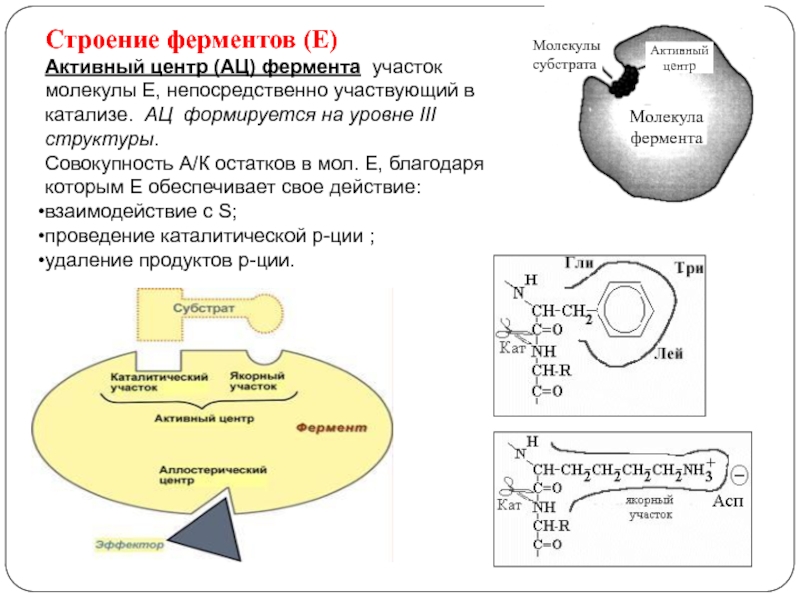
Слайд 7Строение ферментов (Е)
Активный центр (АЦ) фермента участок молекулы Е, непосредственно
участвующий в катализе. АЦ формируется на уровне III структуры.
Совокупность
А/К остатков в мол. Е, благодаря которым Е обеспечивает свое действие:взаимодействие с S;
проведение каталитической р-ции ;
удаление продуктов р-ции.
Молекулы субстрата
Активный центр
Молекула фермента
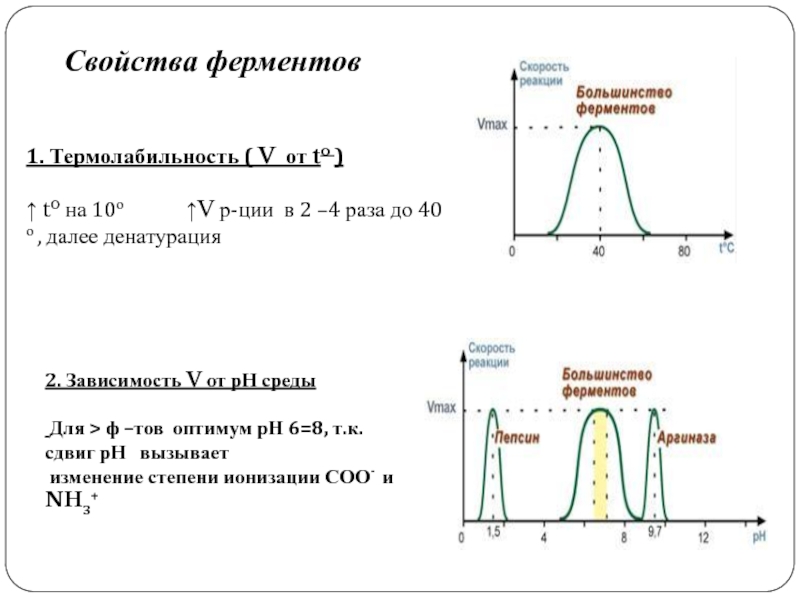
Слайд 8Свойства ферментов
1. Термолабильность ( V от to )
↑ to на
10о ↑V
р-ции в 2 –4 раза до 40 о , далее денатурация2. Зависимость V от рН среды
Для > ф –тов оптимум рН 6=8, т.к. сдвиг рН вызывает
изменение степени ионизации СОО- и NH3+
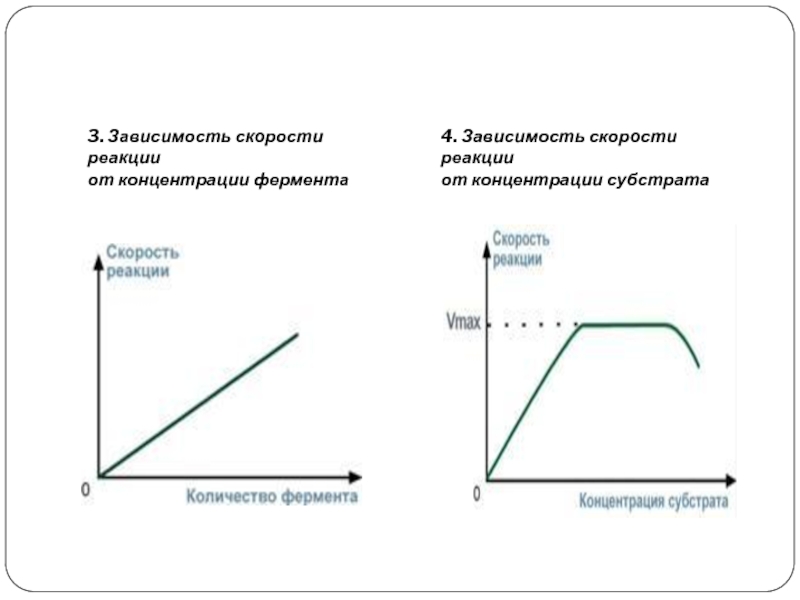
Слайд 93. Зависимость скорости реакции
от концентрации фермента
4. Зависимость скорости реакции
от концентрации
субстрата
Слайд 10Кинетика ферментативных реакций
(Михаэлис, Ментен 1913 г.)
Зависимость V от [
S] – кинетика ферментативной реакции
Km = [S], если скорость
реакции равна половине от максимальной скорости . Чем выше значение Км для ферментативной реакции, тем меньше активность фермента. При высоких значениях Км, сродство фермента к субстрату низкое.(Михаэлис и Ментен, 1913 г.)
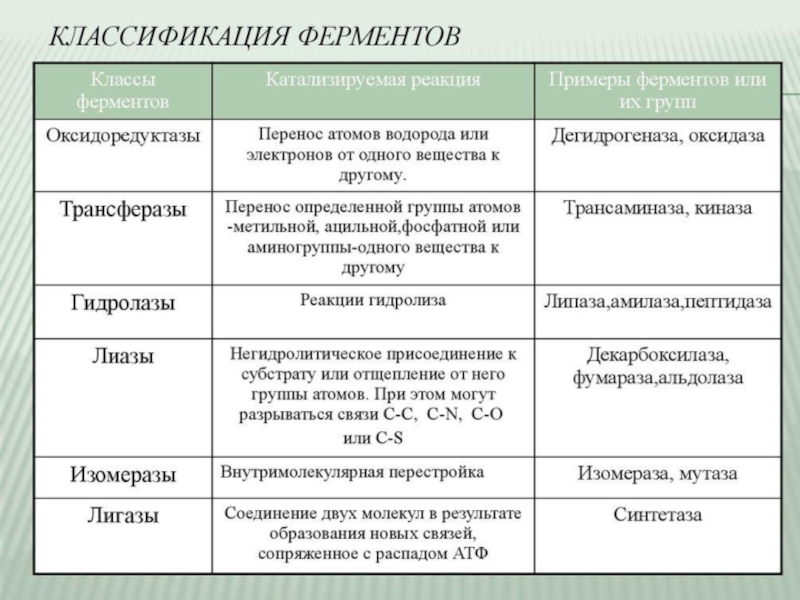
Слайд 11Классификация Е
В 1961 г в Москве V Международный биохимический союз
принял современную классификацию ферментов. В соответствии с этой классификацией все ферменты
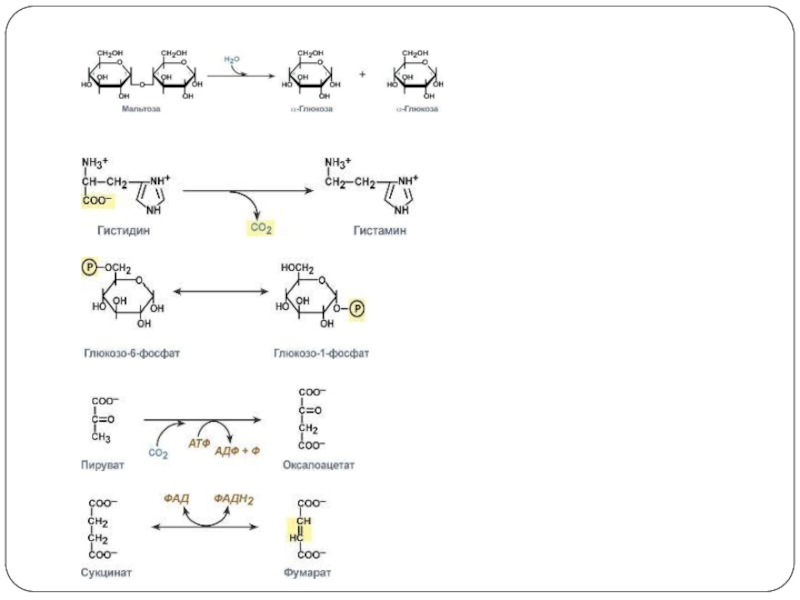
делятся:на классы – по типу катализируемой реакции,
каждый класс подразделяется на подклассы – по природе атакуемой химической группы,
подклассы делятся на подподклассы – по характеру атакуемой связи или по природе акцептора.
Выделяют 6 классов ферментов:
I класс – Оксидоредуктазы
II класс – Трансферазы
III класс – Гидролазы
IV класс – Лиазы
V класс – Изомеразы
VI класс – Лигазы
Слайд 13Название Е
1. Систематическое название – согласно современной классификации. Часто такое
название длинно и сложно для использования, поэтому как производное систематического
названия у многих ферментов имеется одно или несколько рабочих названий.2. Тривиальное название – название, сложившееся исторически. Например, пепсин, трипсин. Для некоторых Е (чаще для гидролаз) к названию субстрата добавляется окончание "-аза" – уреаза, амилаза, липаза. Тем не менее и у таких Е имеется систематическое название.
Например, алкогольдегидрогеназа имеет номер КФ 1.1.1.1. – это оксидоредуктаза, действует на ОН-группу донора с НАД в качестве акцептора с первым порядковым номером в своем подподклассе; лактатдегидрогеназа – КФ 1.1.1.27, действует на ОН-группу донора с НАД в качестве акцептора с порядковым номером 27 в своем подподклассе
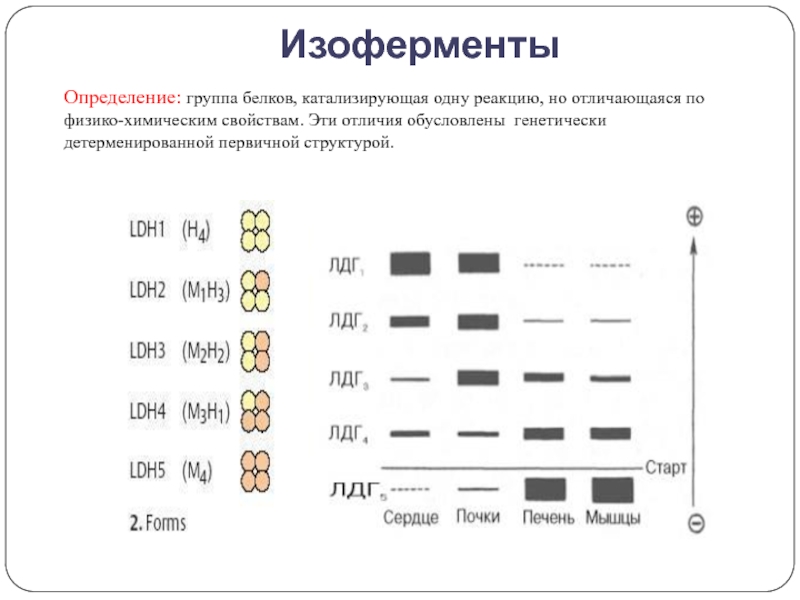
Слайд 16Изоферменты
Определение: группа белков, катализирующая одну реакцию, но отличающаяся по физико-химическим
свойствам. Эти отличия обусловлены генетически детерменированной первичной структурой.
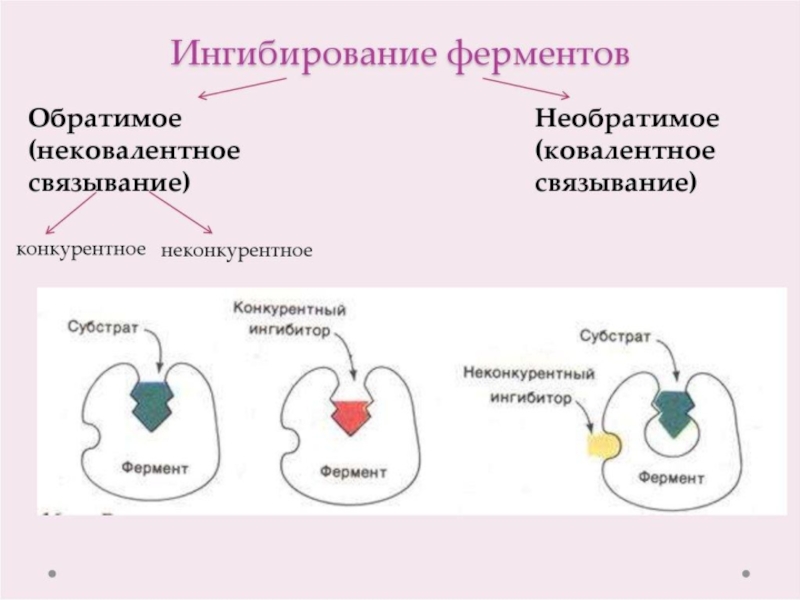
Слайд 17Ферменты проявляют специфичность
Специфичность, т.е. высокая избирательность действия ферментов, основана на комплементарности структуры
субстрата и активного центра фермента.
1. Стереоспецифичность – катализ только одного из стереоизомеров,
например:2. Абсолютная специфичность – фермент производит катализ только одного вещества. Например, расщепление мочевины уреазой.
3. Групповая специфичность – катализ субстратов с общими структурными особенностями, т.е. при наличии определенной связи или химической группы, например, наличие ОН-группы: алкогольдегидрогеназа окисляет до альдегидов одноатомные спирты (этанол, метанол, пропанол).
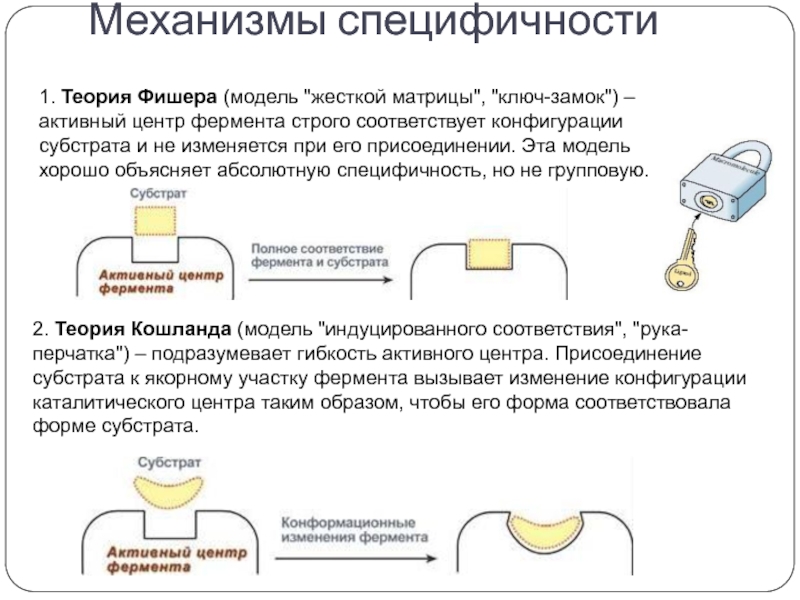
Слайд 181. Теория Фишера (модель "жесткой матрицы", "ключ-замок") – активный центр фермента строго
соответствует конфигурации субстрата и не изменяется при его присоединении. Эта
модель хорошо объясняет абсолютную специфичность, но не групповую.Механизмы специфичности
2. Теория Кошланда (модель "индуцированного соответствия", "рука-перчатка") – подразумевает гибкость активного центра. Присоединение субстрата к якорному участку фермента вызывает изменение конфигурации каталитического центра таким образом, чтобы его форма соответствовала форме субстрата.
Слайд 20Регуляция активности ферментов
Доступность субстрата или кофермента
Изменение количества хотя бы одного
из субстратов прекращает или начинает реакцию.
2. Компартментализация
Компартментализация – это сосредоточение
ферментов и их субстратов в одном компартменте.3. Изменение количества фермента (токсические субстраты этанол, барбитураты стимулируют в печени синтез "своего" изофермента цитохрома Р450, который окисляет и обезвреживает эти вещества).
4. Частичный протеолиз проферментов
Подобный механизм защищает внутриклеточные структуры от повреждений.
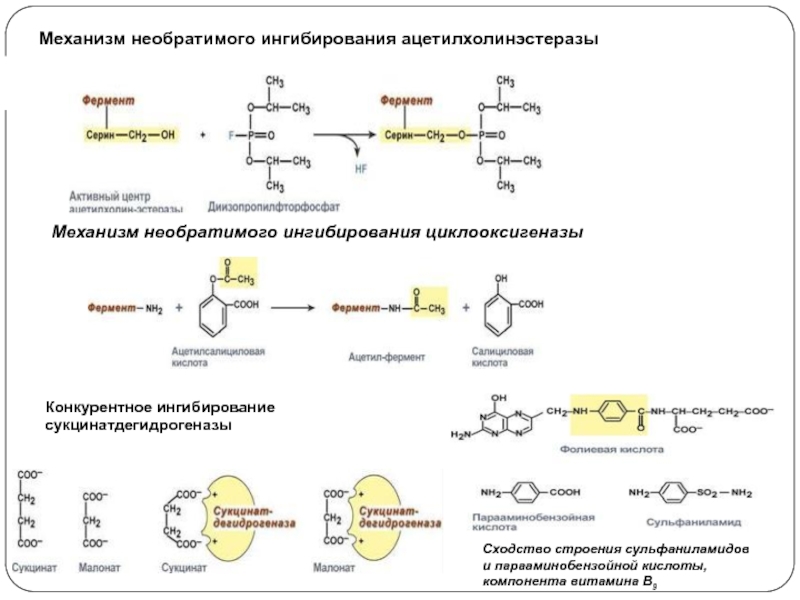
Слайд 24Механизм необратимого ингибирования ацетилхолинэстеразы
Механизм необратимого ингибирования циклооксигеназы
Сходство строения сульфаниламидов
и парааминобензойной
кислоты, компонента витамина В9
Конкурентное ингибирование сукцинатдегидрогеназы
Слайд 26Ферменты в медицине:
энзимодиагностика заболеваний;
лечение: комплексы ферментов желудочно-кишечного тракта (Фестал, Панзинорм
форте, Мезим форте, Энзистал и т.п.) , фермент гиалуронидаза нужна
организму для обратимого изменения проницаемости межклеточного вещества для рассасывания рубцов, тромбов , Цитохром с – фермент, участвующий в процессах тканевого дыхания. Его применяют при асфиксии новорожденных, астматических состояниях, сердечной недостаточности, различных видах гепатита и т.п. и др;фармпрепараты регулируют активность Е => изменяют метаболизм клетки;
в молекулярной генетике (изучение генома, генные рекомбинации)
Слайд 27Использование ферментов в медицине происходит по четырем направлениям:
энзимодиагностика,
энзимотерапия,
использование ферментов в
медицинских технологиях и промышленности.
применение ингибиторов ферментов
Слайд 28Энзимотерапия
Энзимотерапия – это использование ферментов в качестве лекарственных средств.
Самыми распространенными
ферментативными препаратами являются комплексы ферментов желудочно-кишечного тракта (Фестал, Панзинорм форте, Мезим форте,
Энзистал и т.п.), содержащие пепсин, трипсин, амилазу и т.п., и используемые для заместительной терапии при нарушениях переваривания веществ в желудочно-кишечном тракте.Тканевой фермент гиалуронидаза нужна организму для обратимого изменения проницаемости межклеточного вещества, в основе которого находится гиалуроновая кислота. Лекарственную форму гиалуронидазы – лидазу – вводят для размягчения рубцов, появления подвижности в суставах, рассасывания гематом.
Цитохром с – белок, участвующий в процессах тканевого дыхания. Его применяют при асфиксии новорожденных, астматических состояниях, сердечной недостаточности, различных видах гепатита и т.п.
Рибонуклеаза и дезоксирибонуклеаза входят в состав глазных капель для лечения вирусных конъюнктивитов. При нанесении на рану они разжижают гной, при ингаляциях уменьшают вязкость слизи, деполимеризуя нуклеиновые кислоты в мокроте.
Трипсин ингалируют при бронхолегочных заболеваниях для разжижения густой и вязкой мокроты.
Фицин используется в фармацевтической промышленности в качестве добавки к зубным пастам для удаления зубного налета.
Коллагеназу применяют для ускорения отторжения некротизированных тканей, для очистки трофических язв. Весьма широко применяются в настоящее время ингибиторы протеаз (контрикал, гордокс) при панкреатитах – состояниях, когда происходит активирование пищеварительных ферментов в протоках и клетках поджелудочной железы.
Ингибиторы холинэстеразы (физостигмин, прозерин) приводят к накоплению нейромедиатора ацетилхолина в синапсах и показаны при миастении, двигательных и чувствительных нарушениях при невритах, радикулитах, психогенной импотенции.
Препараты, содержащие ингибиторы моноаминоксидазы (наком, мадопар), повышают выработку нейромедиаторов катехоламинов в ЦНС при лечении паркинсонизма. Подавление активности моноаминооксидазы (разрушающей катехоламины) сохраняет нормальную передачу сигналов в нервной системе.
Ингибиторы ангиотензинпревращающего фермента (каптоприл, эналаприл и т.п.) используются как антигипертензивное средство и вызывают расширение периферических сосудов, уменьшение нагрузки на миокард, снижение артериального давления.
Аллопуринол – ингибитор ксантиноксидазы, фермента катаболизма пуринов, требуется для снижения образования мочевой кислоты и подавления развития гиперурикемии и подагры.
Ингибиторы гидроксиметилглутарил-SКоА-редуктазы (ловастатин, флувастатин, аторвастатин) применяются для снижения синтеза холестерола при атеросклерозе, заболеваниях сердечно-сосудистой системы, дислипопротеинемиях.
Ингибитор карбоангидразы (ацетазоламид) используется как мочегонное средство при лечении глаукомы, отеков, эпилепсии, алкалозах и горной болезни.



![Лектор:
ст. преподаватель каф. биологической химии
Миронова Ксения Кинетика ферментативных реакций (Михаэлис, Ментен 1913 г.) Зависимость V от [ Кинетика ферментативных реакций (Михаэлис, Ментен 1913 г.) Зависимость V от [ S] – кинетика ферментативной реакции Km](/img/tmb/4/338710/7855de66592f6d6399a44c2f45224700-800x.jpg)