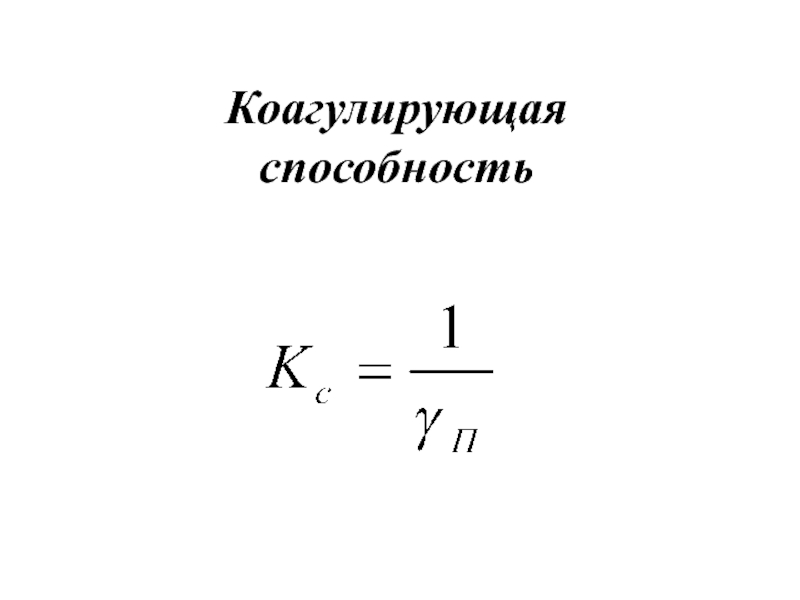Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЛЕКЦИЯ 9
Содержание
- 1. ЛЕКЦИЯ 9
- 2. Степень дисперсности – это величина, обратная размеру (L) дисперсных частиц[D] = [см-1]
- 3. Классификация дисперсных систем по степени дисперсности
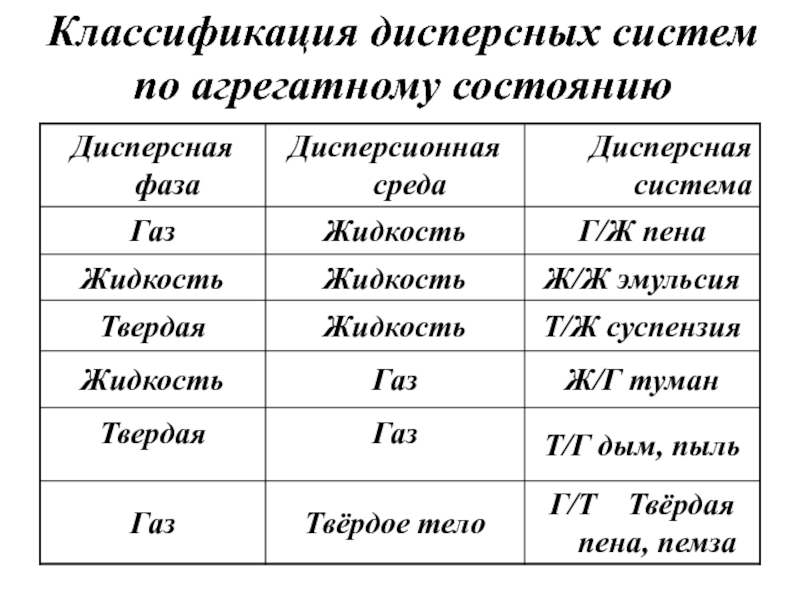
- 4. Классификация дисперсных систем по агрегатному состоянию
- 5. Дым (т. в-во/ г)Туман (ж/г)Пена (г/ж)Пористый шоколад(г/тв.в-во)Минералы(тв. в-во/тв. в-во) Суспензии
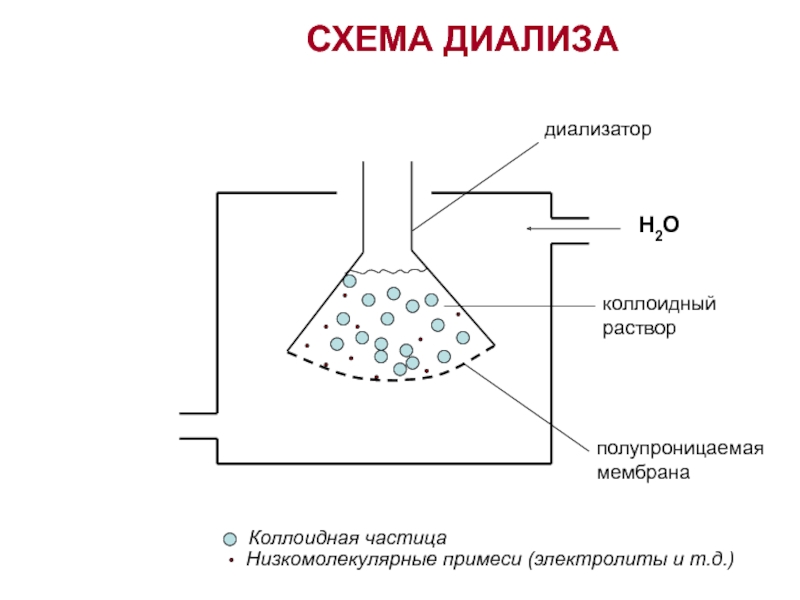
- 6. диализаторполупроницаемаямембранаколлоидныйрастворКоллоидная частицаНизкомолекулярные примеси (электролиты и т.д.)СХЕМА ДИАЛИЗА
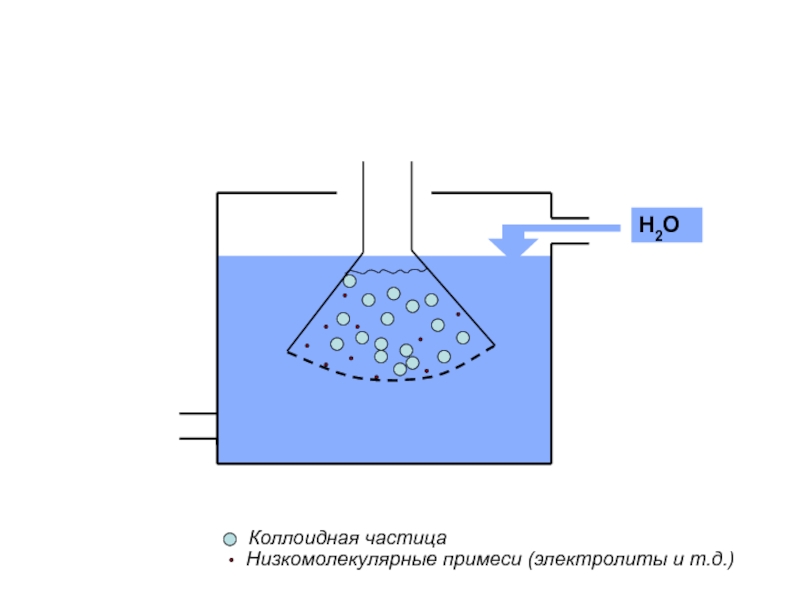
- 7. Слайд 7
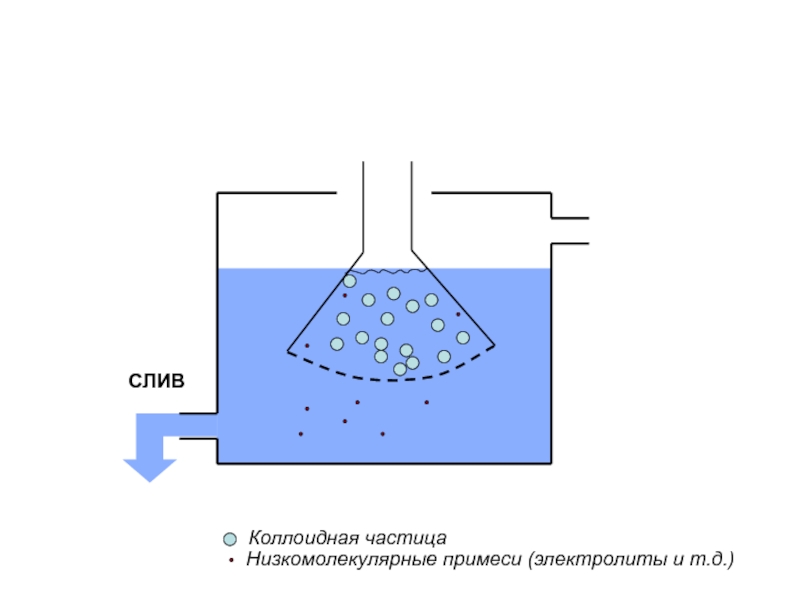
- 8. СЛИВ
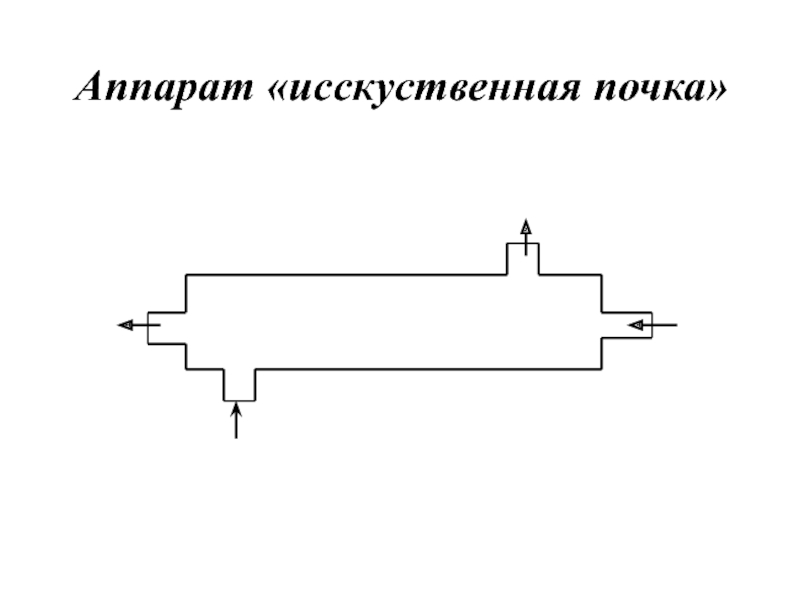
- 9. Аппарат «исскуственная почка»
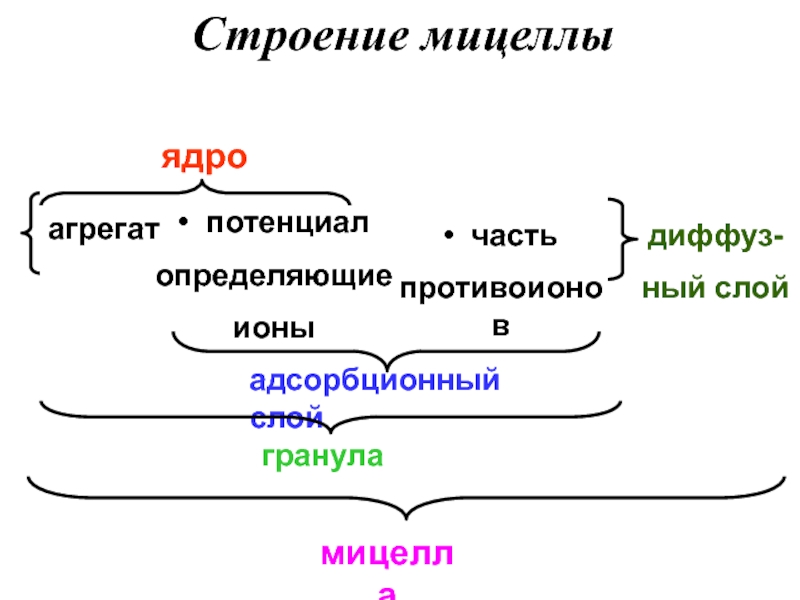
- 10. Строение мицеллыядродиффуз-ный слойагрегат• потенциалопределяющиеионы • частьпротивоионов адсорбционный слойгрануламицелла
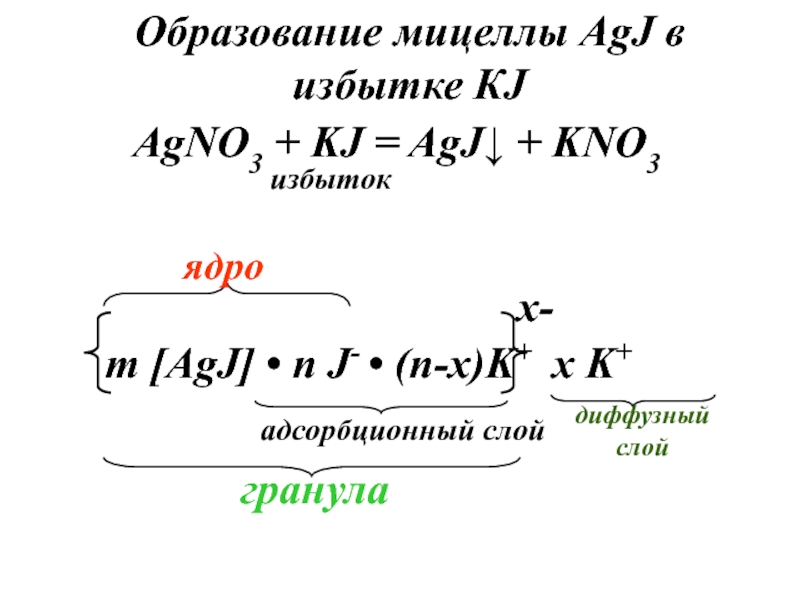
- 11. Образование мицеллы AgJ в избытке КJAgNO3 + KJ = AgJ↓ + KNO3избыток
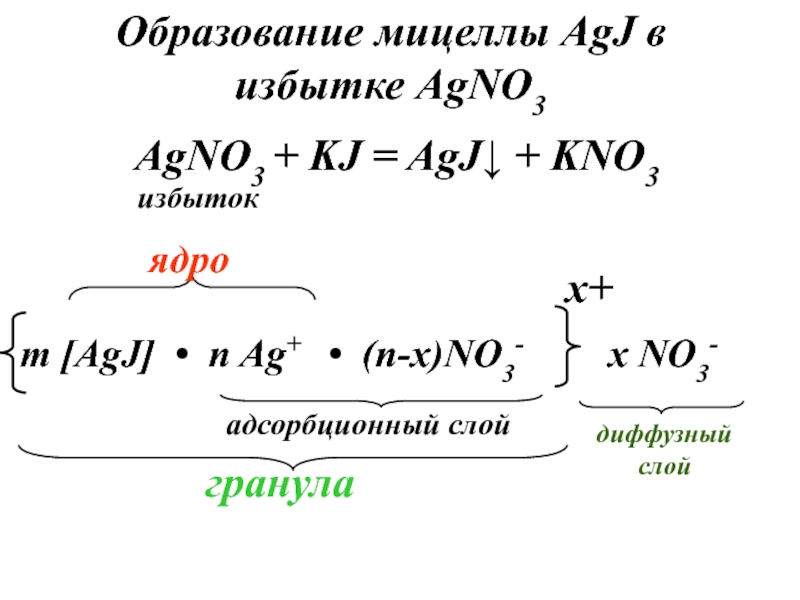
- 12. Образование мицеллы AgJ в избытке AgNO3AgNO3 + KJ = AgJ↓ + KNO3избыток
- 13. Электрокинетический потенциалη – вязкость среды (Н×с/м2);l -
- 14. Е – приложенная разность потенциалов (В);τ - время (с)
- 15. Порог коагуляции (γП) – это минимальное количество
- 16. γ - порог коагуляции (моль/л);С – концентрация
- 17. Правило Шульце-ГардиКоагуляцию вызывают ионы с зарядом, противоположным
- 18. Na+ < Mg2+ < Al3+Li+ < Na+ < K+коагулирующая способность увеличивается
- 19. Коагулирующая способность
- 20. Скачать презентанцию
Степень дисперсности – это величина, обратная размеру (L) дисперсных частиц[D] = [см-1]

![ЛЕКЦИЯ 9 Степень дисперсности – это величина, обратная размеру (L) дисперсных частиц[D] = [см-1] Степень дисперсности – это величина, обратная размеру (L) дисперсных частиц[D] = [см-1]](/img/tmb/4/325387/9f760bac9242a5742a6e7a475086947b-800x.jpg)