Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лимфомы
Содержание
- 1. Лимфомы
- 2. В основе гемобластозов лежат соматические мутации на
- 3. ЛимфопоэзВ-лимфоциты – регуляция гуморального иммунитетаТ-лимфоциты
- 4. Из фолликулов развиваются нодулярные лимфомы, лимфома Беркитта.Из
- 5. Общие признаки лимфомУровень поражения (мутации) – унипотентная
- 6. Виды лимфомЛимфогранулематозНеходжкинские лимфомы
- 7. История вопроса1832 - Т.Hodgkin - первое
- 8. Заболеваемость ЛГМ1 пик - 15-36 лет (максимум
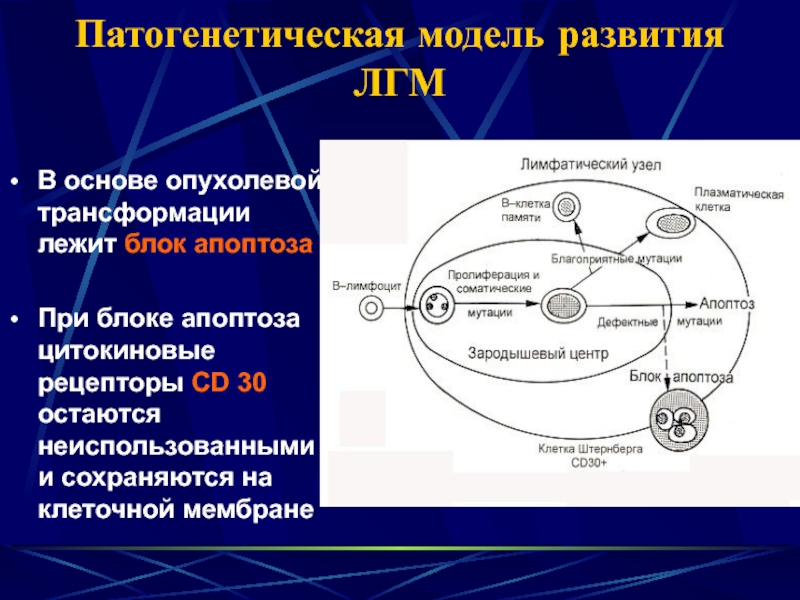
- 9. Патогенетическая модель развития ЛГМВ основе опухолевой трансформации
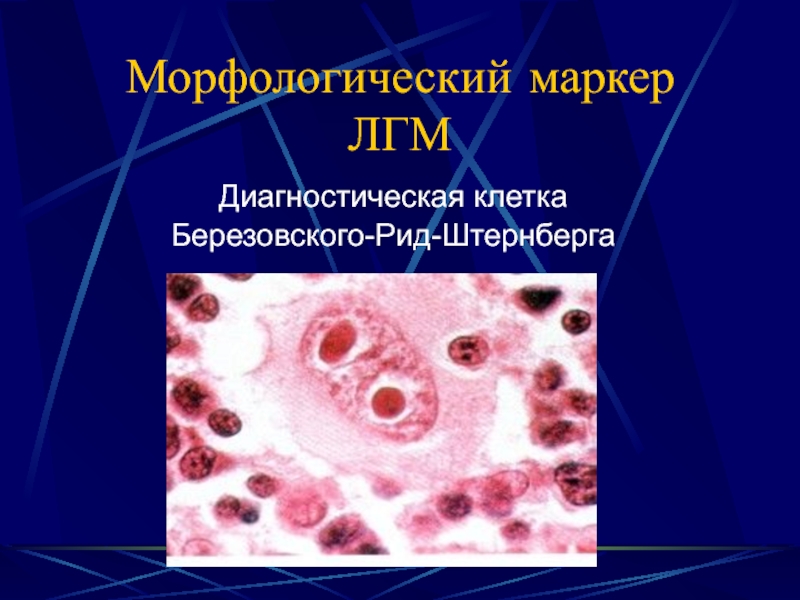
- 10. Морфологический маркер ЛГМДиагностическая клеткаБерезовского-Рид-Штернберга
- 11. Гистологические варианты ЛГМ R.J.Lukes, J.J.Butler, E.D.Hicks, 1966Лимфоидное
- 12. Клиника ЛГМПоражение лимфатических узловПоражение других лимфоидных органовОрганное поражениеОбщие симптомы
- 13. Поражение лимфатических узловЧастота поражения периферических лимфоузлов
- 14. Органное поражение при ЛГМСелезенка - 25%Легкие -
- 15. Общие симптомы при ЛГМ 46%ЛихорадкаПроливные ночные поты ПохуданиеКожный зуд
- 16. Клиническая классификация ЛГМ (Анн-Арбор, 1971)
- 17. Клиническая классификацияА – отсутствие общих симптомовБ –
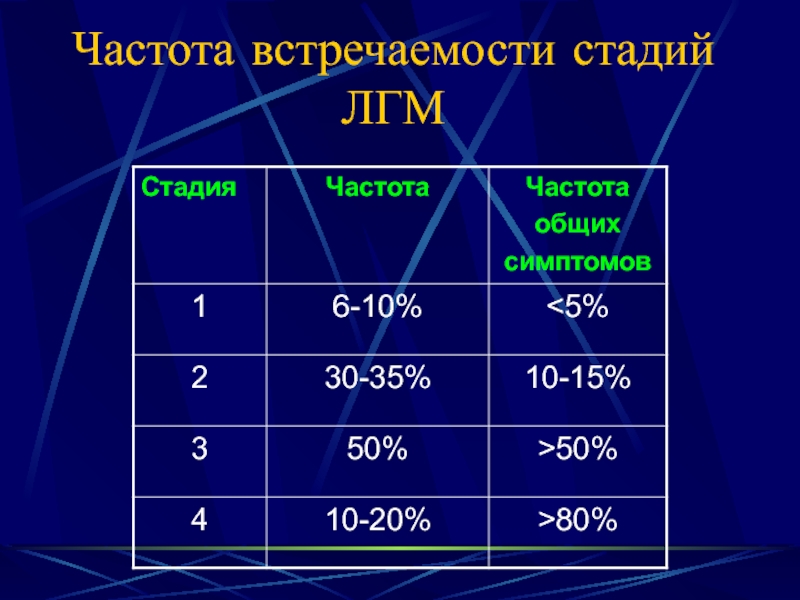
- 18. Частота встречаемости стадий ЛГМ
- 19. Первичная диагностика ЛГМОбщий и биохимический кровиRg-исследование легких
- 20. Изменения гемограммыАбсолютный нейтрофилез со сдвигом влевоУмеренная эозинофилияЛимфоцитопенияУскоренное
- 21. Показатели биологической активностиСОЭ > 30 мм\часГаптоглобин >1,5г\лЦерулоплазмин
- 22. Уточняющая диагностикаКТ грудной полостиКТ брюшной полостиСтернальная пункцияТрепан-биопсия
- 23. Прогностические факторы рискаСтадия заболевания (наиболее неблагоприятны Б-варианты)Формы
- 24. Лечение ЛГМ: Комбинированное химиолучевоеПервый этап –
- 25. Варианты ПХТ
- 26. Интенсификация лечения больных с неблагоприятными факторамиСокращение интервалов
- 27. Выживаемость больных при ЛГМПолная ремиссия 60-90%20-летняя выживаемость
- 28. Заболеваемость НХЛСредний возраст 60-65 летЗаболеваемость в 15-20
- 29. Этиология НХЛ Генетически обусловленный иммунодефицит:
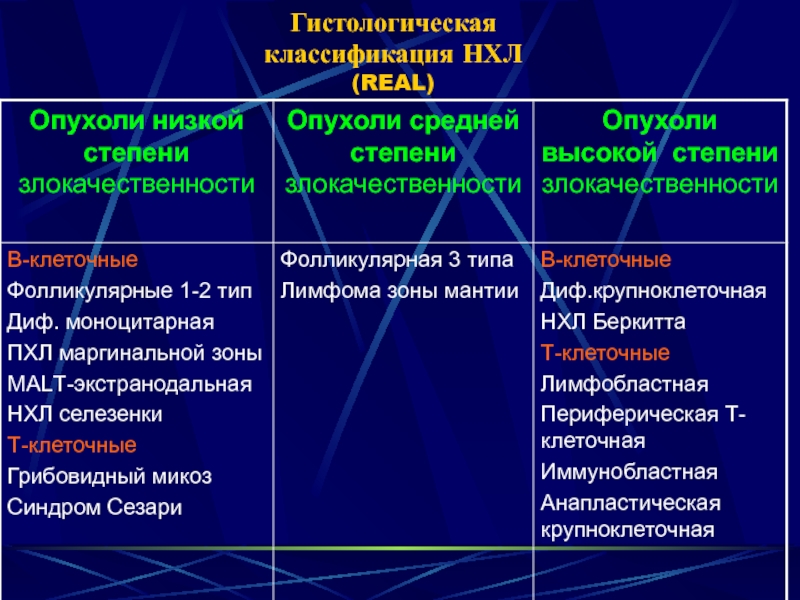
- 30. Гистологическая классификация НХЛ (REAL)
- 31. Слайд 31
- 32. Опухоли низкой степени злокачественности30-40%Медленное течениеДлительная выживаемость (5-летняя
- 33. Опухоли высокой степени злокачественностиБыстрое прогрессированиеВыживаемость – месяцыУмеренно
- 34. МALT-лимфомаАссоциирована с инфицированием Heliobakter pylori.Обычно- локальное экстранодальное
- 35. Фолликулярная лимфомаНаиболее частый вариант НХЛ с благоприятным
- 36. Диффузная В-крупноклеточная лимфомаНаиболее частый вариант НХЛ высокой
- 37. Лимфома БеркиттаЯвляется В-клеточной лимфомой высокой степени злокачественности.Связь
- 38. Первичные кожные лимфомыТ-клеточные - 82% (грибовидный микоз)
- 39. Диагностика НХЛ Диагностика
- 40. Факторы прогноза Стадия заболевания 3 и 4Гистологическая формаИммунофенотип опухоли Уровень ЛДГПоражение костного мозга
- 41. Лечение НХЛПолихимиотерапия Основной метод. Применяется
- 42. Лечение Т-клеточных НХЛ Длительный непрерывный курс
- 43. Лечение В-клеточных НХЛКороткие циклы высокодозной ПХТ
- 44. Скачать презентанцию
В основе гемобластозов лежат соматические мутации на уровне полипотентных или унипотентных клеток под влиянием мутагенов.Гемобластоз может первично поражать либо костный мозг, либо внекостномозговую лимфоидную ткань.Лейкоз – поражение костного мозгаЛимфомы – поражение
Слайды и текст этой презентации
Слайд 1Определение
Злокачественные лимфомы - это новообразования лимфоидной ткани, которые могут первично
возникать в центральных органах иммуногнеза, лимфатических узлах или экстранодально.
Слайд 2
В основе гемобластозов лежат соматические мутации на уровне полипотентных или
унипотентных клеток под влиянием мутагенов.
Гемобластоз может первично поражать либо костный
мозг, либо внекостномозговую лимфоидную ткань.Лейкоз – поражение костного мозга
Лимфомы – поражение внекостномозговой лимфоидной ткани
Слайд 3Лимфопоэз
В-лимфоциты –
регуляция гуморального иммунитета
Т-лимфоциты –
регуляция клеточного иммунитета
NK-клетки –
регуляция спонтанной клеточной
цитотоксичностиСлайд 4
Из фолликулов развиваются нодулярные лимфомы, лимфома Беркитта.
Из паракортикальной зоны развиваются
Т-клеточные лимфомы.
Из медуллярного вещества развиваются хр.лимфолейкозы, парапротеинемические злокачественные лимфомы.
Из синусов
развиваются гистиоцитомы.Слайд 5Общие признаки лимфом
Уровень поражения (мутации) – унипотентная клетка-предшественник В- или
Т-лимфоцитов,
либо полипотентная клетка-предшественник лимфопоэза.
Первичный опухолевый
рост вне костного мозга.Отсутствие на начальных этапах изменений в периферической крови.
Возможность поражения костного мозга в виде нодулярной пролиферации и с выходом в кровь клеток, составляющий морфологический субстрат опухоли (лейкемизация).
Преобладание в клинической картине синдрома тканевой пролиферации, нередко с развитием локальной симптоматики (компрессия, язвенные поражения и др.).
Слайд 7История вопроса
1832 - Т.Hodgkin - первое описание 7 случаев
1890
- С.Я.Березовский - дал полную хар-ку
заболевания, описал типичные клетки 1898 - K.Sternberg - подробное описание клеток,
хар-ка заболевания
1902 - D.Reed - описание типичных клеток
1856 - S .Wilks – “Hodgkin’s disease”
1904 - “Лимфогранулематоз”
1998 - “Hodgkin’s lymphoma”
Слайд 8Заболеваемость ЛГМ
1 пик - 15-36 лет (максимум 20-25 лет)
2 пик
- после 55 лет
Дети - 10% от
всех заболевшихСлайд 9Патогенетическая модель развития ЛГМ
В основе опухолевой трансформации лежит блок апоптоза
При
блоке апоптоза цитокиновые рецепторы СD 30 остаются неиспользованными и сохраняются
на клеточной мембранеСлайд 11Гистологические варианты ЛГМ
R.J.Lukes, J.J.Butler, E.D.Hicks, 1966
Лимфоидное преобладание
7-10 %
Склеронодулярный
30-45%
Смешанно-клеточный
30-45%Лимфоидное истощение (ретикулярный, диффузный фиброз)
7-10%
У молодых,чаще женщин – нодулярный склероз
У старших – смешанно-клеточный вариант
У пожилых – лимфоидное истощение
Слайд 12Клиника ЛГМ
Поражение лимфатических узлов
Поражение других лимфоидных органов
Органное поражение
Общие симптомы
Слайд 13Поражение лимфатических узлов
Частота поражения периферических лимфоузлов
90%
Шейно-надключичные –70%
Подмышечные 3%
Медиастинальные
15%Паховые 4%
Забрюшинные
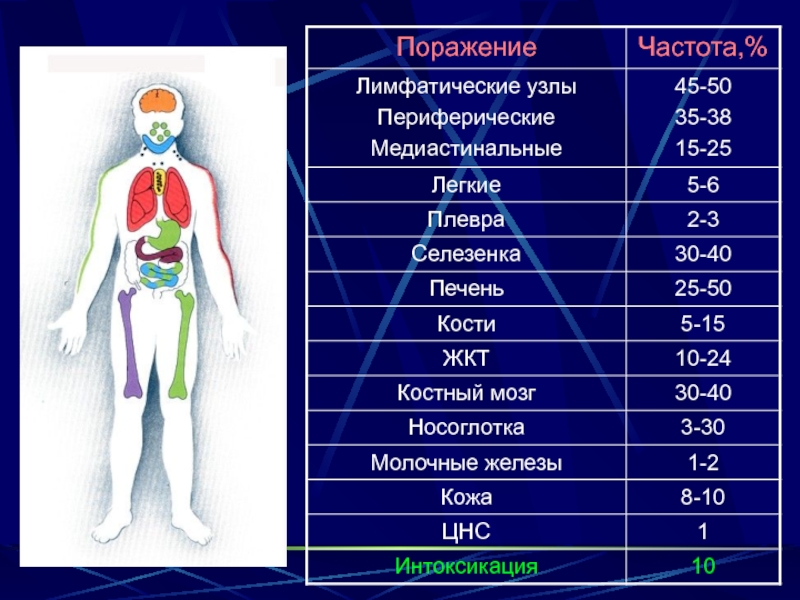
Слайд 14Органное поражение при ЛГМ
Селезенка - 25%
Легкие - 20-30%
Печень - 10-12%
Кости – 14-20%
Костный мозг – 10-12%
Кожа – обычно
паранеоплазииЦНС - редко
ЖКТ – 3%
Щитовидная и молочные железы 1-3%
Вилочковая железа- 3%
Слайд 17Клиническая классификация
А – отсутствие общих симптомов
Б – наличие одного или
нескольких общих симптомов:
Похудание более 10% за 6 месяцев
Температура свыше 38ºПрофузные ночные поты
Слайд 19Первичная диагностика ЛГМ
Общий и биохимический крови
Rg-исследование легких в 2-х проекциях
УЗИ
брюшной полости
Морфологическая верификация диагноза:
пункционная биопсияэксцизионная биопсия
Слайд 20Изменения гемограммы
Абсолютный нейтрофилез со сдвигом влево
Умеренная эозинофилия
Лимфоцитопения
Ускоренное СОЭ
Может
быть:Лейкоцитоз или лейкопения
Тромбоцитоз или тромбоцитопения
Нормохромная анемия
Слайд 21Показатели биологической активности
СОЭ > 30 мм\час
Гаптоглобин >1,5г\л
Церулоплазмин >400мг\л
Альфа-2-глобулин >10г\л
Фибриноген >4г\л
Щелочная
фосфатаза >1,3ммоль\л
Отсутствие изменений или изменение 1 показателя –”a” подстадия
Увеличение 2
и более показателей – “б” подстадияСлайд 22Уточняющая диагностика
КТ грудной полости
КТ брюшной полости
Стернальная пункция
Трепан-биопсия подвздошной кости
Скелетография
Сцинтиграфия костей
с 99Tс
Сцинтиграфия лимфоузлов с 67Ga
Лапаротомия со спленэктомией
Нижняя прямая лимфография
Слайд 23Прогностические факторы риска
Стадия заболевания (наиболее неблагоприятны Б-варианты)
Формы лимфоидного истощения и
смешанно-клеточный вариант.
Массивность поражения:
- Размеры периферических л\узлов>10см
- Увеличение средостения >1\3 диаметра грудной клетки-поражение 3 и более зон л\узлов
СОЭ >30 мм\ч в Б-подстадии и
>50 мм\ч в А-подстадии
5. Экстранодальное поражение
Массивное поражение селезенки (наличие 4 и более очагов или диффузное поражение)
Возраст старше 60 лет
Мужской пол
Вовлечение костного мозга
Слайд 24Лечение ЛГМ:
Комбинированное химиолучевое
Первый этап –
полихимиотерапия
Второй этап –
лучевая терапия(СОД 30 - 40 Гр)
Третий этап –
полихимиотерапия
Слайд 25Варианты ПХТ
1 линия
DOPP+ АБ
MOРР
COPP+АБ
АВVD
2 линия
CEP
IEP
Лечение проводится 2-х недельными циклами с 2-х недельными перерывами.
Всего проводится 3-6 курсов, затем – лучевая терапия.
Слайд 26Интенсификация лечения больных с неблагоприятными факторами
Сокращение интервалов между курсами лечения.
Непрерывная ПХТ с облучением в сниженных дозах зон массивного
исходного поражения и\или остаточных опухолевых масс.Применение колониестимулирующих факторов
Г-КСФ (G-CSF), ГМ-КСФ(GM-CSF).
Высокодозная ПХТ под защитой аутотрансплантации костного мозга или стволовых клеток.
Слайд 27Выживаемость больных при ЛГМ
Полная ремиссия 60-90%
20-летняя выживаемость у больных с
полной ремиссией >60%
Большинство рецидивов возникает на протяжении 3-4 лет
Слайд 28Заболеваемость НХЛ
Средний возраст 60-65 лет
Заболеваемость в 15-20 лет в 10
раз ниже,чем в 75 лет
Чаще болеют мужчины
Слайд 29Этиология НХЛ
Генетически обусловленный иммунодефицит:
Атаксия- телеангиоэктазия
С-м Вискотта-Олдрича
Х-сцепленный
лимфопролифератив-ный синдром
Аутоиммунные болезни:
Ревматоидный артрит
Синдром Фелти
Тиреоидит Хасимото
Приобретенный иммунодефицит:ВИЧ-инфекция
Иммуносупрессивная терапия
Вирусные инфекции:
Вирус Эпштейн-Барр (EBV)
Слайд 32Опухоли низкой степени злокачественности
30-40%
Медленное течение
Длительная выживаемость (5-летняя >80%, медиана 7-10
лет)
Умеренная чувствительность к ХТ
Невозможность излечения при стандартной ХТ
Средний возраст 50-55
летОбычно-генерализованная лимфаденопатия+ спленомегалия
Поражение костного мозга у 75% больных
Большая частота 4 стадии
Слайд 33Опухоли высокой степени злокачественности
Быстрое прогрессирование
Выживаемость – месяцы
Умеренно и высокочувствительны к
ХТ
М.б излечены стандартными схемами ПХТ (у 80% больных)
Результаты лечения зависят
от прогностических факторов5-летняя выживаемость:
от 14% при лимфомах мантии
до 78% при анапластических крупноклеточных лимфомах
Слайд 34МALT-лимфома
Ассоциирована с инфицированием Heliobakter pylori.
Обычно- локальное экстранодальное поражение
желудок – 50%
легкие – 12%паращитовидные железы – 6%
щитовидная железа – 3%
У 1\3 больных в момент диагностики – 4 стадия,нередко с поражением костного мозга.
Благоприятный прогноз:
полная ремиссия - 70%
5-летняя выживаемость – 86%
10-летняя выживаемость – 80%
Слайд 35Фолликулярная лимфома
Наиболее частый вариант НХЛ с благоприятным прогнозом у взрослых.
Средний
возраст 55 лет
Длительная генерализованная лимфаденопатия и спленомегалия
Отсутствие общей симптоматики
Поражение
костного мозга у 75% больныхПрогрессирование ведет к трансформации опухоли в иммунобластную крупноклеточную или мелкоклеточную с неизвитыми ядрами.
5-летняя выживаемость -70%
10-летняя выживаемость - 15%
Слайд 36Диффузная В-крупноклеточная лимфома
Наиболее частый вариант НХЛ высокой степени злокачественности
Может быть
первичной или явиться следствием трансформации зрелоклеточных лимфом.
У 1\3 –1 или
2 стадия заболеванияу 2-3 – диссеминированные формы
Частое поражение экстралимфатических зон:
мягкие ткани
молочные железы.
Крайне неблагоприятный прогноз:
медиана выживаемости у нелеченных больных <1 года
в 1-2 стадии – излечение у 80%
Слайд 37Лимфома Беркитта
Является В-клеточной лимфомой высокой степени злокачественности.
Связь с инфицированием вирусом
Эпштейн-Барра.
В 80% - в Африке и Новой Гвинее, в 20%
спорадическая.Имеет очень короткое время удвоения клеток.
Своеобразие клиники:
- поражение лицевого скелета и орбиты (при эндемии)
-нехарактерна лимфаденопатия
-поражение ЖКТ и забрюшинных л\у (при спорадических случаях)
-поражение костного мозга у 20%
-поражение ЦНС в 2\3 случаев (менингиты, поражение зрительного и лицевого нерва у 30%)
Слайд 38Первичные кожные лимфомы
Т-клеточные - 82% (грибовидный микоз)
В-клеточные -
18%
Медленное развитие (5 лет и более)
Прогрессирование проявляется
лимфаденопатией, чаще
периферической, позже абдоминальной и медиастинальной, затем -органное поражение.Общая выживаемость- 65-70%
Слайд 39Диагностика НХЛ
Диагностика аналогична ЛГМ
Дополнительно:
Уровень
ЛДГИммунофенотипирование
ФГДС
Колоноскопия
Люмбальная пункция
Консультация отолариноголога
Консультация невропатолога
Консультация офтальмолога
КТ головного мозга
Слайд 40Факторы прогноза
Стадия заболевания 3 и 4
Гистологическая форма
Иммунофенотип опухоли
Уровень
ЛДГ
Поражение костного мозга
Слайд 41Лечение НХЛ
Полихимиотерапия
Основной метод. Применяется как самостоятельно, так
и в сочетании с другими.
2. Хирургический метод
Как
самостоятельный метод применяется очень редко, при изолированном поражении ЖКТ3. Лучевая терапия
Высокоэффективна, но дает кратковременный эффект
Слайд 42Лечение
Т-клеточных НХЛ
Длительный непрерывный курс лечения (99 недель)
Основные препараты –винкристин,
АБ, L-аспарагиназа, антиметаболиты.
Различия в программе зависят только от стадии заболевания.
Поддерживающая
терапия в течение 1,5 лет.Слайд 43Лечение
В-клеточных НХЛ
Короткие циклы высокодозной ПХТ в течение 6 месяцев.
Основные
препараты –метотрексат, циклофосфан, цитозар, вепезид.
Схемы ПХТ зависят от массы опухоли,
объема операции, уровня ЛДГ.Отсутствие поддерживающей химиотерапии.