Слайд 2
Липидозы (lipidoses) — группа заболеваний, характеризующихся нарушением липидного обмена и имеющих
преимущественно наследственный характер. Большинство Л. относится к болезням накопления, которые
обусловлены отложением аномально больших количеств нерасщепленных продуктов жирового обмена в различных органах и тканях, что приводит к значительному нарушению их функции. В основе Л. лежит полная или частичная недостаточность лизосомальных ферментов, участвующих в обмене липидов и обусловленная наследственным дефектом соответствующего гена. Большинство Л. наследуется по аутосомно-рецессивному типу, исключение составляет болезнь Фабри, которая наследуется по Х-сцепленному, рецессивному типу.
Липидозы включают:
липопротеинемии, связанные с нарушением обмена липопротеидов.
гликолипидозы, обусловленные нарушением обмена гликолипидов.
Слайд 3
К липидозам относятся:
ганглиозидозы — GM1-ганглиозидоз (тип I, II, III), GM2-ганглиозидоз
(тип I, II, ювенильный, хронический тип);
болезнь Ниманна — Пика;
болезнь
Гоше; болезнь Фабри;
липогранулематоз Фарбера;
болезнь Вулмена;
болезнь I-клеток;
псевдогурлевскую полидистрофию;
метахроматическую лейкодистрофию;
болезнь Краббе.
Слайд 4
Ганглиозидозы — группа заболеваний, обусловленных нарушением катаболизма ганглиозидов — сложных гликолипидов, углеводная
часть молекулы которых содержит остаток сиаловой кислоты. Выделяют несколько типов
ОМ, и ОМ; ганглиозидозов. В основе их развития лежит метаболический дефект расщепления ганглиозидов в результате недостаточности специфических лизосомальных гидролаз.
Слайд 5
GM2-ганглиозидозы — большая фенотипически вариабельная группа заболеваний, в основе которых лежит
дефицит гексозаминидазы А и В. Подразделяются на инфантильную, ювенильную и взрослую
формы. Тип наследования всех типов — аутосомно-рецессивный.
Существует трехлокусная модель, объясняющая молекулярно-генетические основы GM2-ганглиозидозов. Мутация гена гексозаминидазы А (a-локус хромосомы 15q) лежит в основе болезни Тея — Сакса и ювенильного GM2-ганглиозидоза. Мутация в b-локусе 5-й хромосомы проявляется недостаточностью гексозаминидазы А и В и обусловливает GM2-ганглиозидоза тип II (болезни Сандхоффа).
Слайд 6
GM1-ганглиозидоз тип I (генерализованный семейный ганглиозидоз, нейровисцеральный липидоз, недостаточность b-галактозидазы)
характеризуется аутосомно-рецессивно наследуемой недостаточностью фермента GM1-b-галактозадазы. Активность этого фермента в
головном мозге, печени и фибробластах кожи больного снижена до 0,1% нормы. В основе болезни лежит мутация структурного гена, кодирующего мономерный полипептид A1GM1-b-галактозидазы и локализованного на коротком плече 3-й хромосомы (p12q21). При этом дефекте нарушено отщепление концевой галактозы от GM1-ганглиозида, который откладывается в больших количествах в сером веществе головного мозга и печени.
Слайд 7 Клиника
GM1-ганглиозидоз обнаруживается при рождении или
вскоре после него. Отмечаются плохой аппетит, слабость сосания и крика,
недостаточная прибавка в весе, отечность нижних конечностей, мышечная гипотония и малая активность ребенка (спокоен, большую часть времени спит). Гепатоспленомегалия наблюдается с первых месяцев жизни. Часто встречаются дорсолюмбальный сколиоз, нерезкое увеличение размеров суставов, укорочение и утолщение пальцев (брахидактилия). Рентгенографически определяется множественный дизостоз. Характерны частые бронхопневмонии. Развиваются клонико-тонические судороги, Примерно у 50% больных с рано развившимся GM1-ганглиозидозом наблюдаются вишнево-красные пятна на глазном дне в области желтого пятна, образовавшиеся в результате отложения ганглиозидов в клетках сетчатки. Если ребенок дожил до 6 месяцев, то у него формируется характерный внешний вид (выступающие лобные бугры, запавшая переносица, большие низко расположенные ушные раковины, гипертрофия десен, макроглоссия, отек лица). К 8-9 месяцам ребенок не сидит, не ползает, его движения некоординированы, мышечная гипотония сменяется гипертонусом, повышаются сухожильные рефлексы. К концу первого года жизни отмечаются глухота, слепота, спастическая тетраплегия, отсутствие реакции на окружающее, в терминальной стадии развивается децеребрационная ригидность.

Слайд 8 Диагностика
Диагноз GM1-ганглиозидоза подтверждается
при определении активности b-галактозидазы в лейкоцитах и культивируемых фибробластах. GM1-ганглиозидоз
тип I следует дифференцировать с мукополисахаридозом тип I — синдром Гурлер, болезнью Ниманна — Пика и I-клеточной болезнью. GM1-ганглиозидоз тип I проявляется в более раннем возрасте, чем синдром Гурлер и болезнь Ниманна — Пика. Для последней характерны помутнение роговицы, поражение костей, менее выраженное изменение черт лица.
На вскрытии обнаруживают расширение желудочков мозга и его атрофию в результате гибели нейронов. Гистологически выявляются пенистые гистиоциты в костном мозге, печени, селезенке, лимфатических узлах и др.
Слайд 9
Лечение:
Специфическая терапия отсутствует. Разрабатываются методы заместительной терапии b-галактозидазой (очищенной или
инкапсулированной в липосомах).
Исход:
Дети с GM1-ганглиозидозом обычно погибают в возрасте 2—3 лет
от рецидивирующей бронхопневмонии.
Слайд 10
GM1 ганглиозидоз тип II (ювенильный системный липидоз, болезнь Дерри) фенотипически отличается
от GM1-ганглиозидоза тип I обычно более поздним началом (после первого
года жизни), медленным прогрессированием, минимальным поражением костной ткани и отсутствием поражения внутренних органов. Описано немногим более 20 случаев заболевания. В результате дефицита b-галактозидазы уровень накопления GM1-ганглиозидов в сером веществе головного мозга в 10 раз превышает норму.
Слайд 11
Клиника:
В течение первого года жизни ребенок развивается нормально. К
концу первого года возникают атаксия и дизартрия, появляются сходящееся косоглазие,
мышечная гипотония, которую вскоре сменяет спастический тетрапарез. Отмечается быстрый регресс приобретенных навыков, пропадает интерес к окружающему, развиваются летаргия, судорожный синдром, трудно поддающийся лечению.
Диагностика:
Диагноз ставят на основании определения активности Р-галактозидазы. Дифференциальный диагноз необходимо проводить с метахроматической лейкодистрофией и юношеским GM2-ганглиозидозом, он основан на определении активности специфических ферментов.
Исход:
Продолжительность жизни больных GM1-ганглиозидозом II типа — от 3 до 10 лет. Больные погибают от рецидивирующих бронхолегочных инфекций.
Слайд 12
GM1-ганглиозидоз тип III проявляется прогрессирующей дизартрией на втором десятилетии жизни.
Развиваются атаксия и спастические параличи, деменция, которые медленно прогрессируют, судороги
бывают редко, зрение не страдает.
Слайд 13
GM2-ганглиозидоз тип I (амавротическая идиотия Тея — Сакса, болезнь Тея — Сакса)
встречается преимущественно среди евреев-ашкенази, частота гетерозиготных носителей гена среди этой
этнической группы составляет 1: 27.
Нарушение расщепления GM2-ганглиозидов в результате недостаточности фермента гексозаминидазы А приводит к его накоплению в головном мозге, в меньшей степени — во внутренних органах. Цитоплазма нейронов переполняется GM2-ганглиозидом, в результате чего происходит центральная демиелинизация. Если в норме в ткани головного мозга GM2-ганглиозид присутствует в следовых количествах, то при болезни Тея — Сакса он составляет 6—12% сухой массы. На поздних стадиях вследствие пролиферации астроцитов развивается мегалоэнцефалия. Одновременно в головном мозге резко снижается количество цереброзида и сульфатида.
Слайд 14
В течение первых 4—6 месяцев жизни ребенок развивается нормально, начинает сидеть,
ползать, улыбаться. Отмечается повышенная реакция на внешние раздражители (шум, свет) —
от испуга до миоклонических судорог. К 6 месяцам возникает мышечная гипотония. Со второго года жизни быстро прогрессирует нарушение моторного и интеллектуального развития. Появляются трудности кормления из-за нарушения глотания. Развиваются генерализованные атонические параличи. После 11/2 лет прогрессируют глухота, слепота, судороги, мышечный тонус повышается до появления спастических параличей вплоть до децеребрационной ригидности. У многих больных описывают «кукольное» лицо: бледная кожа, легкий румянец, длинные ресницы, хорошие волосы. В 90% случаев на глазном дне определяется симптом вишневой косточки. Больные дети умирают на втором году жизни.
Слайд 15
GM2-ганглиозидоз тип II (болезнь Сандхоффа, амавротическая идиотия Сандхоффа) по клинической
и патологоанатомической картине идентичен болезни Тея — Сакса. Встречается не только
в еврейских популяциях. В основе его лежит дефицит фермента гексозаминидазы А и В.
Как и при GM2-ганглиозидозе I типа характерно набухание нейронов с концентрическими слоями цитоплазматических включений, но при типе II выше концентрация аспалоганглиозида GM2 в нервной ткани, а также гликосфинголипида в мезенхимальных тканях внутренних органов, что проявляется незначительной гепатомегалией. Дифференциальный диагноз с GM2-ганглиозидозом I типа возможен лишь после исследования мутантных ферментов.
Слайд 16
Ювенильный GM2-ганглиозидоз. В основе его развития лежит дефицит фермента гексозаминидазы
А. Этническая избирательность отсутствует. Первые симптомы появляются в возрасте 2—6 лет,
основные проявления — атаксия и дизартрия. Позднее развиваются атетоидные движения конечностей и спастические параличи, прогрессирующие до децеребрационной ригидности. Слепота появляется на поздних стадиях болезни, симптом вишневой косточки на глазном дне отсутствует. Также не описаны гепатоспленомегалия, «кукольное» лицо, костные деформации. Дифференциальный диагноз проводят с другими типами GM2-ганглиозидозов и лейкодистрофиями на основании биохимических и молекулярно-генетических исследований. Больные ювенильным GM2-ганглиозидозом умирают в возрасте 5—15 лет вследствие повторных пневмоний.
Слайд 17
GM2-ганглиозидоз, хронический тип проявляется в возрасте от 4 до 16 лет медленно
прогрессирующим нарушением походки. В дальнейшем повышается мышечный тонус, развиваются полая
стопа, легкая атаксия, дизартрия, мышечная атрофия проксимальных частей конечностей. При этой форме ганглиозидоза интеллект не снижается. В лейкоцитах значительно снижена, а в культуре фибробластов отсутствует активность гексозаминидазы А; GM2-ганглиозиды в повышенной концентрации обнаруживаются в клетках головного мозга, особенно в субкортикальной области.
Болезнь Ниммана — Пика
Впервые описана в 1914 г. немецким педиатром Ниманном
(A. Niemann), а в 1926 г. немецкий патологоанатом Пик (L. Pick) доказал по данным гистологического исследования нозологическую самостоятельность этой патологии.
Болезнь Ниманна — Пика объединяет группу сфингомиелолипидозов, характеризующихся накоплением сфингомиелина вследствие снижения активности фермента сфингомиелиназы, катализирующего гидролиз сфингомиелина с образованием фосфорилхолина и церамидных остатков.
Слайд 20
Тип А (классическая инфантильная форма, острая нейропатическая форма) наблюдается наиболее
часто. Заболевание проявляется после рождения и характеризуется поражением внутренних органов
и ц.н.с. Уже в 3 месяца отмечаются трудности вскармливания, гипотрофия, а в 6 месяцев выявляется гепатоспленомегалия. Как правило, печень увеличивается раньше, чем селезенка. Дети истощены, характерны большой выступающий живот и тонкие конечности. Из неврологических нарушений отмечаются мышечная гипотония, угнетение сухожильных рефлексов, отсутствие реакции на окружающее, остановка моторного развития, затем утрата уже приобретенных навыков. Рано снижается слух. Кожа приобретает коричневато-желтую окраску из-за нарушения обмена сфингомиелина. Примерно в 50% случаев выявляется вишнево-красное пятно в области желтого пятна сетчатки. Также описаны помутнение роговицы, коричневое прокрашивание передней капсулы хрусталика. Больные дети умирают обычно на третьем году жизни.
Слайд 21
При типе В (висцеральная форма, хроническая форма без вовлечения нервной
системы) основные клинические проявления развиваются позже, чем при типе А.
Спленомегалия появляется в возрасте 2—6 лет, позднее поражаются печень и легкие (больные подвержены частым инфекциям дыхательных путей). Симптоматика поражения ц.н.с. отсутствует, напротив, в ряде случаев отмечены высокие интеллектуальные способности. Продолжительность жизни не снижена.
Тип С (подострая, юношеская форма, хроническая нейропатическая форма) проявляется в 1—2 года и характеризуется нейровисцеральными нарушениями. Сначала появляется гепатоспленомегалия (менее выражена по сравнению с типами А и В), может наблюдаться холестаз. Неврологические симптомы развиваются на фоне поражения внутренних органов, отмечаются мышечная гипотония, повышение глубоких сухожильных рефлексов, которые сменяются спастическим параличом, а также интенционный тремор, умеренная атаксия, судороги. Большинство больных погибает в возрасте 5—15 лет.
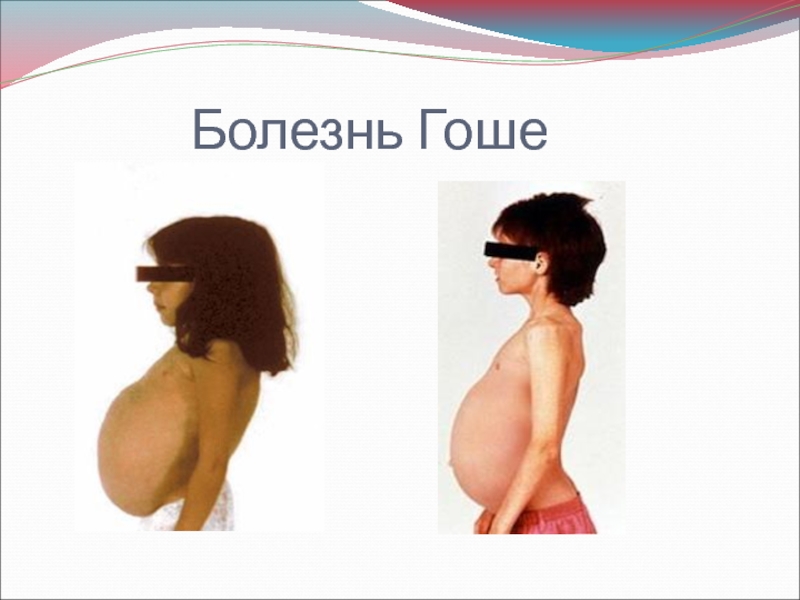
Слайд 22Болезнь Гоше
глюкоцереброзидный липидоз, глюкоцереброзидоз — одно из наиболее частых наследственных нарушений
гликолипидного обмена. Предполагают, что в основе болезни Гоше лежат аллельные
мутации генов, кодирующих глюкоцереброзидазу — фермент, катализирующий гидролитическое отщепление глюкозы от глюкоцереброзида, который накапливается в различных органах и тканях. Впервые больного с этой патологией описал французский дерматолог Гоше (Ph. Ch. Е. Gaucher) в 1882 г.
Слайд 24
Тип I (хронический, или взрослый, нейропатический) характеризуется развитием спленомегалии вскоре
после рождения. В ряде случаев возможны явления гиперспленизма с тромбоцитопенией,
анемией, лейкопенией, повышенная кровоточивость. Чуть позже обнаруживается гепатомегалия. Костные нарушения включают приступы болей в костях, длящиеся днями и неделями, переломы, расширение части бедренной кости и асептический некроз ее головки. В основе этих симптомов лежат сильное расширение костномозговой полости и увеличение массы клеток, накапливающих глюкоцереброзид. Возможна инфильтрация макрофагами легких и сердца, приводящая к легочной гипертензии и предрасположенности к развитию пневмонии. У некоторых больных в более старшем возрасте отмечается желто-коричневая пигментация кожи лица и нижних конечностей. Часто обнаруживают желто-коричневые участки утолщения роговицы. Неврологическая симптоматика отсутствует. Больные доживают до среднего возраста, хотя продолжительность жизни сильно варьирует. Течение заболевания медленное прогрессирующее.
Слайд 25
Тип II (острый инфантильный, острый нейропатический) может развиваться сразу после
рождения и до 18 месяцев (в основном в 3 месяца). Начальные проявления —
слабый крик, вялое сосание, отсутствие рефлекса Моро, гепатоспленомегалия. У детей выявляется косоглазие, затрудняется глотание, голова находится в положении ретрофлексии. К 9 месяцам развиваются спастические параличи с повышенными сухожильными рефлексами, клонусом и ригидностью мышц. В редких случаях отмечаются судороги. Все более прогрессирующие бульбарные нарушения приводят к смерти ребенка в результате повторных пневмоний в возрасте от 1 месяца до 2 лет (средний возраст — 9 месяцев).
III тип (ювенильный, или подострый, нейропатический) проявляется на втором году жизни спленомегалией. Гепатомегалия выражена умеренно. За этим следует «период молчания» длительностью от 3 до 7 лет, затем возникают явные неврологические нарушения. Неврологические симптомы (косоглазие, спастические параличи, атаксия, судороги) выражены не резко. Смерть обычно наступает через 2 года после появления неврологических нарушений.
Слайд 26Болезнь Фабри
диффузная универсальная ангиокератома, наследственный дистонический липидоз — врожденный дефект катаболизма
гликосфинголипидов с преобладанием поражения почек. Описана впервые в 1898 г. английским
дерматологом Андерсоном (Anderson) и немецким дерматологом Фабри (Fabry).
Болезнь Фабри обусловлена недостаточностью лизосомной гидролазы — a-галактозидазы А, наследуется по Х-сцепленному рецессивному типу, в связи с чем клиническая симптоматика проявляется у лиц мужского пола. Ген a-галактозидазы А локализован на длинном плече Х-хромосомы Xq22 ® q24.
Слайд 28
У гомозиготных мужчин заболевание проявляется в детском возрасте или у
подростков так называемыми кризами Фабри, характеризующимися мучительной обжигающей болью в
ладонях и стопах Приступы болей могут длиться несколько дней, сопровождаться небольшой лихорадкой и повышением СОЭ. Иногда ошибочно диагностируется ревматизм. Акропарастезии с возрастом становятся более частыми и тяжелыми. В детском возрасте отмечаются характерные для болезни Фабри поражения кожи — ангиокератомы (телеангиэктазии или маленькие поверхностные ангиомы), которые локализуются симметрично на бедрах, спине, ягодицах, наружных половых органах, в области коленных суставов и пупка. Ангиокератомы могут быть плоскими или несколько возвышающимися над поверхностью кожи, от темно-красного до голубовато-черного цвета, не бледнеют при надавливании. Характерен гипо- или ангидроз кожи. Возможно также поражение слизистой оболочки ротовой полости и конъюнктивы. Наблюдаются расширение и извилистость сетчатки и конъюнктивы, помутнение роговицы.
Слайд 29
С возрастом увеличивается накопление сфингогликолипидов и гликопротеида в органах сердечно-сосудистой
системы и почках. Появляются симптомы стенокардии, поражаются клапаны сердца (митральная
недостаточность и стеноз аорты), развиваются гипертрофия левого желудочка, инфаркт миокарда.
Наблюдаются протеинурия, снижение фильтрационной способности почек. Возможно развитие хронической почечной недостаточности. Артериальная гипертензия (по-видимому, почечного происхождения) усиливает нарушения со стороны сердца и способствует поражению мозговых сосудов. Цереброваскулярные проявления включают тромбоз, аневризмы, иногда кровоизлияния, что приводит к возникновению судорог, гемиплегии, афазии; возможен психоз. Изменения со стороны желудочно-кишечного тракта характеризуются тошнотой, рвотой, диареей, болями в животе. Отмечаются деформация дистальных межфаланговых суставов, асептический некроз головки бедренной и таранной костей, выраженный остеопороз позвонков. Возможны гипохромная микроцитарная анемия, задержка роста и полового созревания. Смерть наступает от уремии или сосудистых поражений сердца и головного мозга обычно на 4-м десятилетии жизни.
У гетерозиготных женщин симптомы заболевания могут отсутствовать, у большинства носительниц гена болезни Фабри наблюдаются кожные проявления и помутнение роговицы, иногда симптомы болезни выражены так же, как у мужчин.

Слайд 30
Болезнь Краббе (глобоидно-клеточная лейкодистрофия) — быстро прогрессирующее демиелинизирующее дегенеративное заболевание ц.н.с.
Тип наследования — аутосомно-рецессивный. В основе болезни лежит снижение активности фермента
галактозилцерамид-b-галактозидазы, который в норме расщепляет галактоцереброзид до церамида и галактозы. В головном мозге, печени, селезенке, почках, лейкоцитах, фибробластах накапливаются галактоцереброзид и его производное психозин. Количество последнего повышается в 10—100 раз, что оказывает токсическое воздействие на олигодендроглиальные клетки, формирующие миелиновую оболочку. В зонах демиелинизации вокруг мелких кровеносных сосудов белое вещество содержит большое количество глобоидных гистиоцитов (макрофагов). Уменьшение олигодендроглиальных клеток сопровождается глиозом. Периферические нервы подвергаются аксональной дегенерации с накоплением пенистых гистиоцитов.
Слайд 31
Как правило, первые клинические симптомы появляются на четвертом месяце жизни.
Отмечаются повышенная возбудимость и мышечная гипертония. Верхние и нижние конечности
у больных детей находятся в разогнутом состоянии, кулаки сжаты. Вскоре становится заметной задержка психомоторного развития. Позднее развиваются миоклонические судороги, генерализованная двигательная реакция на слуховые раздражители, спастический тетрапарез, повышение глубоких сухожильных рефлексов, при исследовании глазного дна выявляют атрофию зрительных нервов. Проявления периферической нейропатии встречаются лишь в отдельных случаях. В последующем развиваются характерные глубокие умственные расстройства, вялый тетрапарез, снижаются сухожильные рефлексы, мышечная гипертония сменяется гипотонией. Больные умирают в возрасте от 7 месяцев до 3 лет.
Диагноз основан на клинической картине, повышении содержания белка в цереброспинальной жидкости, выявлении снижения активности галактозилцерамид-b-галактозидазы. Дифференциальный диагноз проводят с другими формами лейкодистрофии на основании биохимического анализа. Специфическое лечение не разработано. Возможна пренатальная диагностика болезни Краббе путем исследования в культивируемых амниотических клетках активности галактозилцерамид-b-галактозидазы.