Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лучевая терапия рака ротоглотки
Содержание
- 1. Лучевая терапия рака ротоглотки
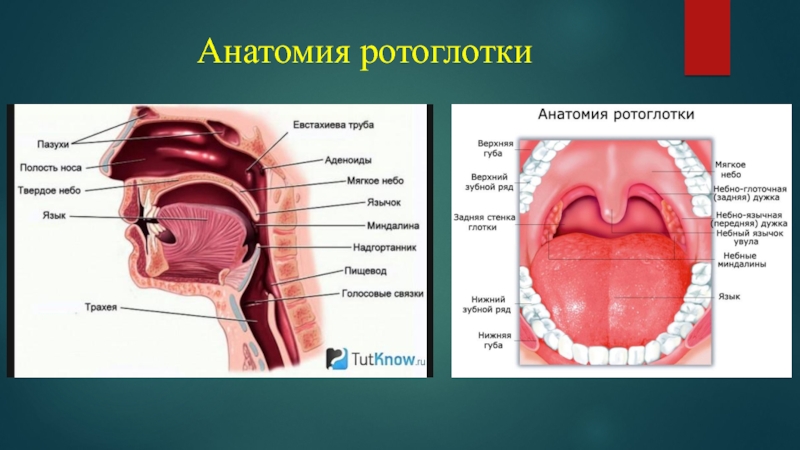
- 2. Анатомия ротоглотки
- 3. Слайд 3
- 4. Слайд 4
- 5. Различие в TNM классификации в отношении N+Для
- 6. Стратегия лечения больных раком ротоглоткиТ1-2,N0-1T3-4,N0-1Любая T,N2-3Трансоральная или
- 7. T1-2,N0-1ЛТТрансоральная или открытая резекция +СШЛАЭ+ крайДругие неблагоприятные
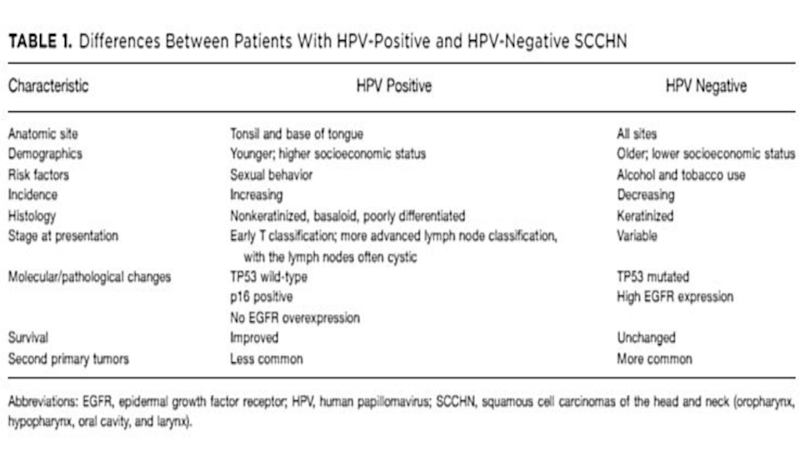
- 8. Клинические аспекты ВПЧ-позитивного ракаЧасто диагностируют на ранней
- 9. Методы лечения рака ротоглотки 1.Хирургическое лечение: transoral
- 10. Лучевая терапия самостоятельная При сравнении ЛТ и
- 11. Самостоятельная ЛТ у ВПЧ +Материалы и методы:156
- 12. Самостоятельная ЛТ у ВПЧ -
- 13. EORTC 22931 (2004 г) Адьювантная ХЛТ
- 14. Пациенты с раком ротоглотки (T1-T3) проведено хирургическое
- 15. Адъювантная ХЛТ у ВПЧ -29 пациентов МРР
- 16. Показания к адъювантной ХЛТ Послеоперационная ХЛТ:
- 17. Stein Lybak ,Per Gunnar Liavaa, Odd R. Monge, Jan Olofsson.Август 2010 гhttps://www.ncbi.nlm.nih.gov/pubmed/20803151Ретроспективный анализ
- 18. ПОЛТ у ВПЧ +Phase II Randomized Trial
- 19. ПОЛТ у ВПЧ -RTOG 1221: Phase IIНаличие
- 20. Показания к ПОЛТ при факторах риска рецидива:
- 21. Химиолучевая терапия рака ротоглотки
- 22. Показания к ХЛТ самостоятельной Рак ротоглотки III-IV стадии.
- 23. ХЛТ у ВПЧ +RTOG-1016 PHASE III
- 24. ХЛТ у ВПЧ -Крупное рандомизированное исследование, сравнивающее
- 25. Слайд 25
- 26. Индукционная ПХТ
- 27. ECOG 1308 ИХТ у ВПЧ +Результат:2 летняя
- 28. ИХТ у ВПЧ -
- 29. Показания к ИХТ местно-распространённый рак ротоглотки при невозможности проведения одновременной химиолучевой или лучевой терапии.
- 30. 1.Дефицит массы тела до начала специального лечения
- 31. Несмотря на различие в биологическим свойствах опухолей
- 32. Принципы лечения пациентов с раком ротоглоткиВозможности хирургического
- 33. 2D планирование Гриницы боковых противолежащих полей:Верхняя:
- 34. Слайд 34
- 35. GTV 70p: опухоль, видимая при осмотре, по
- 36. CTV высокого рискаCTV низкого риска
- 37. Критерии включения лимфоузлов в клинический объём
- 38. Одностороннее облучение лимфоузловFinally, patients with well-lateralized T1-T2
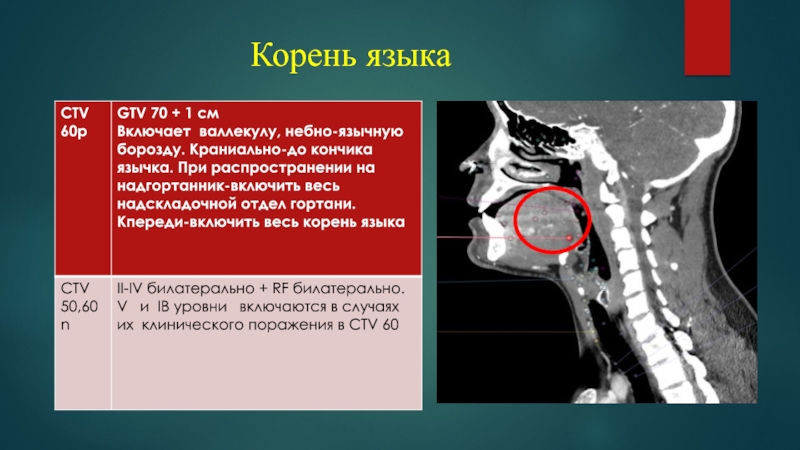
- 39. Корень языка
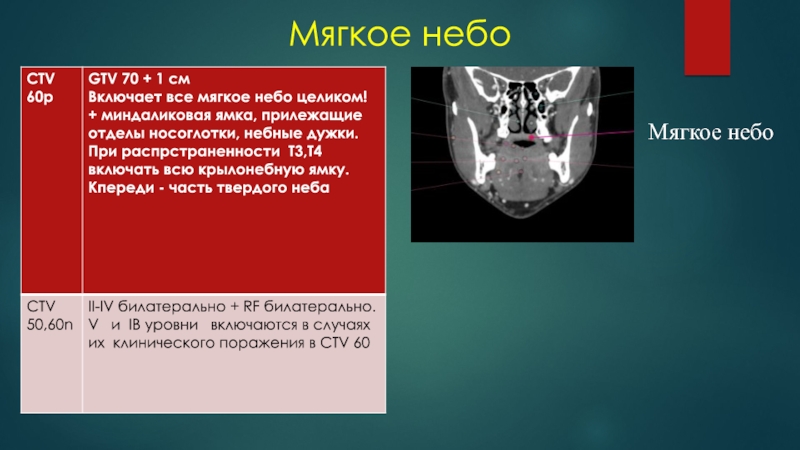
- 40. Мягкое небоМягкое небо
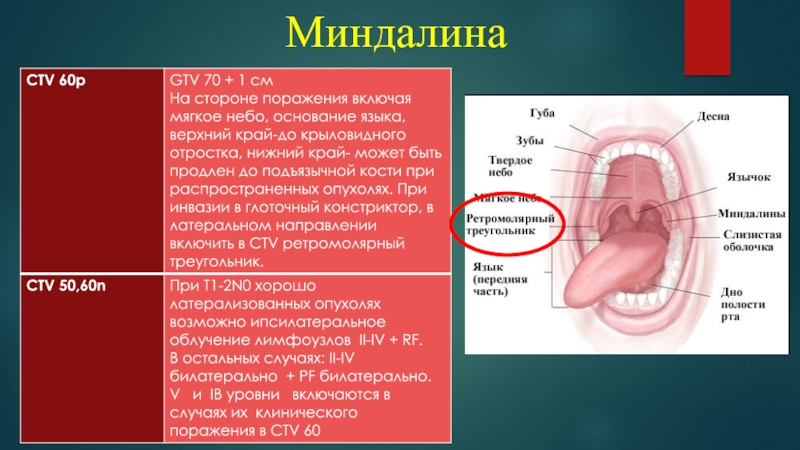
- 41. Миндалина
- 42. Целевые объемы и дозы адъювантной лучевой терапии
- 43. Органы риска/толерантные дозы
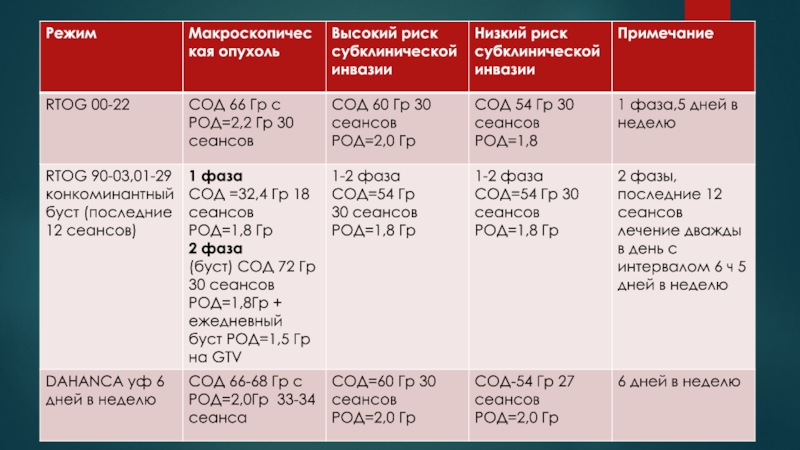
- 44. Режим фракционирования Традиционное фракционирование: 2,0Гр 5 дней
- 45. Слайд 45
- 46. IMRT технология
- 47. Оценка эффекта после завершения ЛТ или ХЛТ
- 48. Спасибо за внимание !!!
- 49. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Лучевая терапия рака ротоглотки
Челябинский Областной Клинический Центр
Онкологии и Ядерной Медицины
М.МСлайд 5Различие в TNM классификации в отношении N+
Для р16 (-) рака
Для
р16 (+) рака
(AJCC 8 TH ED., 201 )
Слайд 6Стратегия лечения больных раком ротоглотки
Т1-2,N0-1
T3-4,N0-1
Любая T,N2-3
Трансоральная или открытая резекция опухоли
При
положительном крае резекции или наличии ЭКР :попытка повторной резекции, при
невозможности-ЛТ или ХТДля N1
ЛТ+ ХТ
конкурентная ХТ +ЛТ
Индукционная ХТ, далее-ЛТ ,либо ХТ
Конкурентная ХТ+ЛТ
Либо
Индукционная ХТ с последующей ЛТ
При наличии неблагоприятных факторов в виде + края резекции и ЭКР : ЛТ+ХТ, либо только ЛТ
Трансоральная либо открытая резекция+СЛАШ: объем СШЛАЭ определяемся категорией N и мо;ет быть одно и двусторонней
Слайд 7T1-2,N0-1
ЛТ
Трансоральная или открытая резекция +СШЛАЭ
+ край
Другие неблагоприятные факторы
Ре-резекция
ХТ или ЛТ
T3-4,N0-1
Конкурирующая
ХТ+ЛТ
Индукционная ХТ ,далее-ЛТ+ХТ,либо только ХТ
Любая Т,,N2-3
Резекция +СШЛАЭ
N2-3 Билатеральная
N1 односторонняя
+ край
или ЭКРХТ
Слайд 8Клинические аспекты ВПЧ-позитивного рака
Часто диагностируют на ранней стадии, когда опухоль
имеет небольшие размеры с тенденцией к региональному метастазированию
Снижение среднего
возраста постановки диагноза для вирус-позитивных больных до 59,8 года по сравнению с ВПЧ-негативными пациентами, средний возраст которых на момент постановки диагноза составляет 66,6 Обладают повышенной радиочувствительностью
Уменьшение агрессивности лечения у больных ВПЧ-позитивной формой рака: использование ингибиторов EGFR, снижение суммарной дозы лучевой терапии в общей схеме химиолучевой терапии с цисплатином либо замена химиолучевой терапии оперативным вмешательством с менее интенсивной адъювантной терапией
Слайд 9Методы лечения рака ротоглотки
1.Хирургическое лечение:
transoral robotic surgery (TORS),
transoral laser microsurgery (TLM)
2.ЛТ
3.ХТ
4.ХЛТ
5.Адьювантная ЛТ
6.Адьювантная ХТ
Слайд 10Лучевая терапия самостоятельная
При сравнении ЛТ и хирургического лечения пациентов
с T1-2 N0-2 без ЭКР
Вывод: ЛТ обеспечивает более высокое качество
жизни пациентов, более лучшие функциональные результаты по сравнению с ТОРС. 3 фаза клинических исследований будет посвящена особенностям ТОРС в зависимости от статуса.Слайд 11Самостоятельная ЛТ у ВПЧ +
Материалы и методы:
156 пациентов с ВПЧ
+ пролечены только ЛТ
Изучалось влияние ВПЧ статуса на БРВ,
выживаемость без метастазов и ОВРезультатаы:
наличие ВПЧ коррелировало с увеличением БРВ
(5-year actuarial values 58% v 28%; P = .0005), выживаемостью без метастазов (72% v 34%; P = .0006), и ОВ (62% v 26%; P = .0003) по сравнению с ВПЧ –
ВЫВОД: наличие ВПЧ + статуса влияет на ответ на ЛТ и ОВ, увеличивая ОВ по сравнению с ВПЧ -
Слайд 13EORTC 22931 (2004 г)
Адьювантная ХЛТ
128 пациентов с раком ротоглотки
pT3–4, pT1-2N2-3 с вовлечением л/у IV–V , или T1-2N0-1 с
ЭКР, + краем, ЛВИ или ПНИ.Рандомизация на
1.послеоперационную ЛТ 66 Гр ( стандартное фракционирование )
2. и послеоперационная ЛТ+ Цисплатин 100 мг/м2 через 3 недели.
ХЛТ улучшила 5-летную OВ (40 → 53) и БРВ(69 → 82%).
Вывод: Добавление ХТ к ЛТ у прооперированных пациентов вне зависимости от ВПЧ статуса улучшает ОВ.
Слайд 14
Пациенты с раком ротоглотки (T1-T3) проведено хирургическое лечение в объеме
TORS и СШЛАЭ. Пациенты имели неблагоприятные факторы риска ( наличие
ЭКР, положительный край резекции и др.)Методика ЛТ: IMRT,средняя доза составила на первичный очаг 66 Гр
Результаты:
3-летняя БРВ 81.9 % в группе ХЛТ и 88.9% в группе лучевой терапии. Показатели ОВ оказались сравнимы.
Выводы:
У ВПЧ + не имеет преимуществ в отношении ОВ проведение ХЛТ, однако БРВ выше при применении ХЛТ.
Адьювантная ХЛТ у ВПЧ +
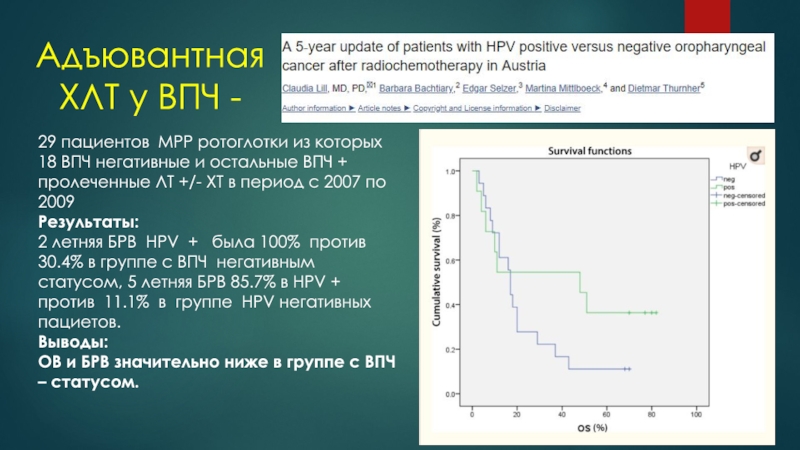
Слайд 15Адъювантная ХЛТ у ВПЧ -
29 пациентов МРР ротоглотки из которых
18 ВПЧ негативные и остальные ВПЧ + пролеченные ЛТ +/-
ХТ в период с 2007 по 2009Результаты:
2 летняя БРВ HPV + была 100% против 30.4% в группе с ВПЧ негативным статусом, 5 летняя БРВ 85.7% в HPV + против 11.1% в группе HPV негативных пациетов.
Выводы:
ОВ и БРВ значительно ниже в группе с ВПЧ – статусом.
Слайд 16Показания к адъювантной ХЛТ
Послеоперационная ХЛТ:
1. Наличие позитивного
края резекции
2. Прорастание опухолью капсулы ЛУ (ЭКР)
3. Метастазы в ЛУ IV или V уровней4. рN1 + сочетание ≥ 2 факторов: периневральная и сосудистая инвазия, рТ3, рТ4.
Слайд 17
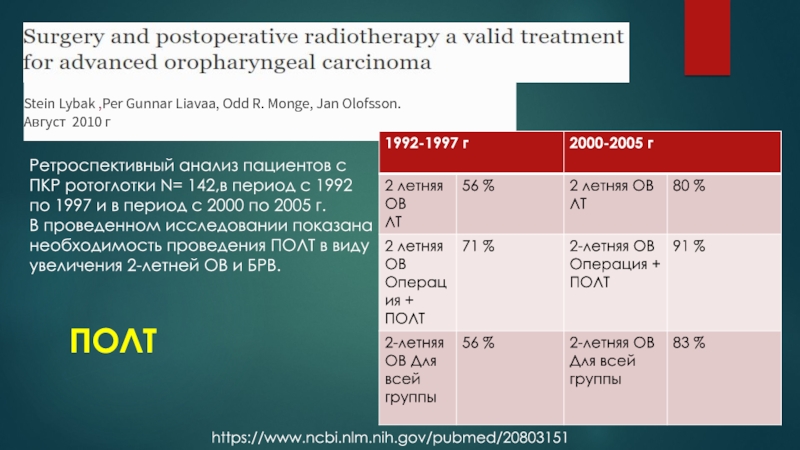
Stein Lybak ,Per Gunnar Liavaa, Odd R. Monge, Jan Olofsson.
Август 2010 г
https://www.ncbi.nlm.nih.gov/pubmed/20803151
Ретроспективный анализ пациентов с ПКР
ротоглотки N= 142,в период с 1992 по 1997 и в
период с 2000 по 2005 г.В проведенном исследовании показана необходимость проведения ПОЛТ в виду увеличения 2-летней ОВ и БРВ.
ПОЛТ
Слайд 18ПОЛТ у ВПЧ +
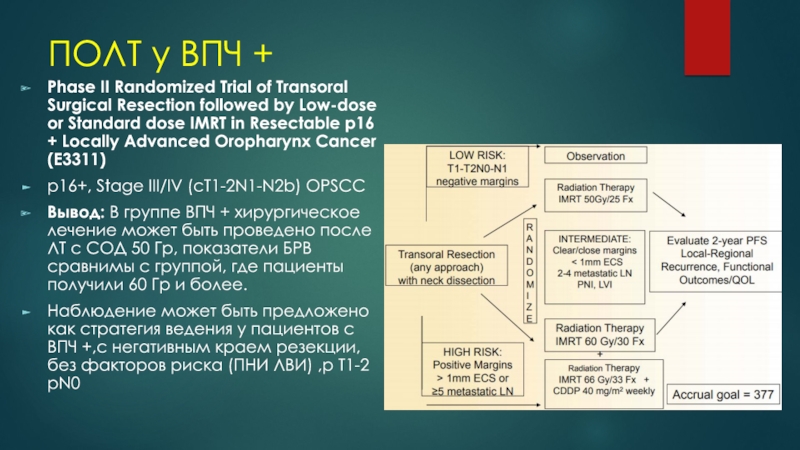
Phase II Randomized Trial of Transoral Surgical
Resection followed by Low-dose or Standard dose IMRT in Resectable
p16 + Locally Advanced Oropharynx Cancer (E3311)p16+, Stage III/IV (cT1-2N1-N2b) OPSCC
Вывод: В группе ВПЧ + хирургическое лечение может быть проведено после ЛТ с СОД 50 Гр, показатели БРВ сравнимы с группой, где пациенты получили 60 Гр и более.
Наблюдение может быть предложено как стратегия ведения у пациентов с ВПЧ +,с негативным краем резекции, без факторов риска (ПНИ ЛВИ) ,р T1-2 pN0
Слайд 19ПОЛТ у ВПЧ -
RTOG 1221: Phase II
Наличие хирургического лечения в
группе ВПЧ – операбельных больных позволило улучшить выживаемость без прогрессирования
на 15 % по сравнению с контрольной группой.Вывод: у ВПЧ – хирургическое лечение как на первичном очаге, так и на лимфоузлах, должно присутствовать в планировании лечения.
Слайд 20Показания к ПОЛТ
при факторах риска рецидива:
рТ4,
положительный и близкий
край резекции (˂ 5 мм),
рN2-3,
рТ3 рN1,
рN1 + периневральная инвазия (ПНИ)
и или лимфоваскулярная инвазия (ЛВИ).Примечание: Послеоперационную ЛТ начинают через 4-6 недель после операции при условии заживления послеоперационной раны и восстановления питания.
Слайд 23ХЛТ у ВПЧ +
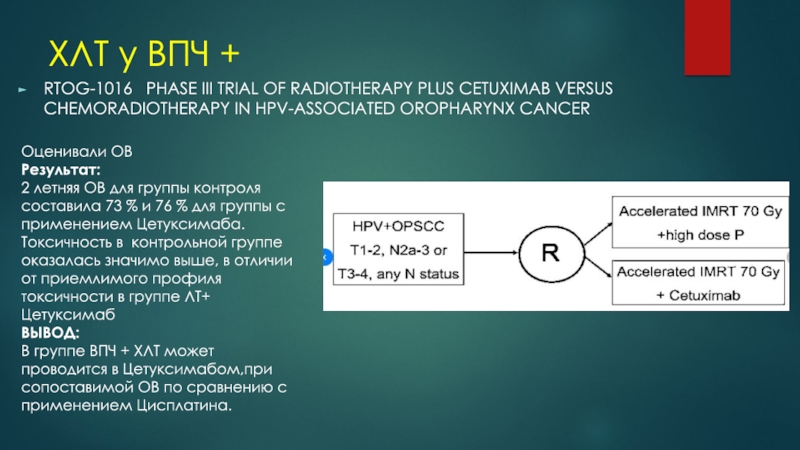
RTOG-1016 PHASE III TRIAL OF RADIOTHERAPY
PLUS CETUXIMAB VERSUS CHEMORADIOTHERAPY IN HPV-ASSOCIATED OROPHARYNX CANCER
Оценивали ОВ
Результат:
2
летняя ОВ для группы контроля составила 73 % и 76 % для группы с применением Цетуксимаба.Токсичность в контрольной группе оказалась значимо выше, в отличии от приемлимого профиля токсичности в группе ЛТ+ Цетуксимаб
ВЫВОД:
В группе ВПЧ + ХЛТ может проводится в Цетуксимабом,при сопоставимой ОВ по сравнению с применением Цисплатина.
Слайд 24ХЛТ у ВПЧ -
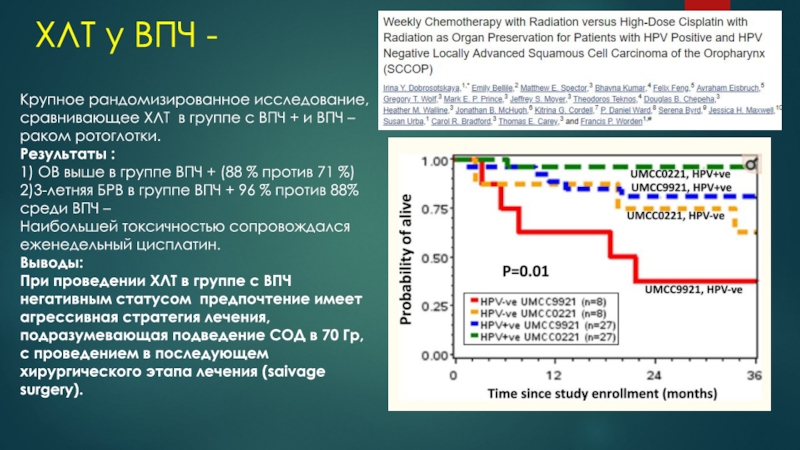
Крупное рандомизированное исследование, сравнивающее ХЛТ в группе
с ВПЧ + и ВПЧ – раком ротоглотки.
Результаты :
1) ОВ
выше в группе ВПЧ + (88 % против 71 %)2)3-летняя БРВ в группе ВПЧ + 96 % против 88% среди ВПЧ –
Наибольшей токсичностью сопровождался еженедельный цисплатин.
Выводы:
При проведении ХЛТ в группе с ВПЧ негативным статусом предпочтение имеет агрессивная стратегия лечения, подразумевающая подведение СОД в 70 Гр, с проведением в последующем хирургического этапа лечения (saivage surgery).
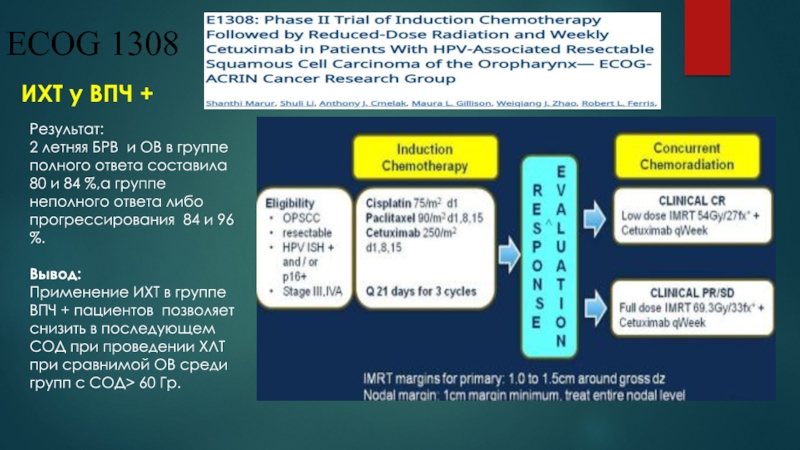
Слайд 27ECOG 1308
ИХТ у ВПЧ +
Результат:
2 летняя БРВ и ОВ
в группе полного ответа составила 80 и 84 %,а группе
неполного ответа либо прогрессирования 84 и 96 %.Вывод:
Применение ИХТ в группе ВПЧ + пациентов позволяет снизить в последующем СОД при проведении ХЛТ при сравнимой ОВ среди групп с СОД> 60 Гр.
Слайд 29Показания к ИХТ
местно-распространённый рак ротоглотки при невозможности проведения
одновременной химиолучевой или лучевой терапии.
Слайд 301.Дефицит массы тела до начала специального лечения является неблагоприятным фактором
2.
ВПЧ позитивный статус является фактором, способствующим потере веса даже при
использовании назогастрального зонда. Однако в данном исследовании нет пояснений, каков именно механизм влияния ВПЧ позитивного статуса на более раннюю необходимость привлечения нутритивной поддержки. Косвенно указано, что ВПЧ + пациенты имели большее количество мукозитов 3-4 степени, и мукозиты развивались в более раннем периоде лечения, чем у ВПЧ негативных.3.При лечении с помощью только ЛТ потребность в использовании назогастрального зонда появлялась на 4-5 неделе лечения, при ХЛТ на 3й.
Нутритивная поддержка
Слайд 31Несмотря на различие в биологическим свойствах опухолей ВПЧ + и
ВПЧ - , протокол предписания доз на объем не изменился.
На сегодняшний день существует множество клинических исследований, согласно которым стратегия «дезинтенсификации» лечения применима к ВПЧ + пациентам, однако нет рандомизированнных исследований, которые бы доказали эффективность данной стратегии.В перспективе для ДЛТ может быть разработан более дифференцированный протокол лечения с учетом ВПЧ статуса.
все хорошо, но…
Слайд 32Принципы лечения пациентов с раком ротоглотки
Возможности хирургического лечения опухолей данной
локализации ограничены высоким риском функциональных дефектов. Методом выбора является лучевая
терапия (ЛТ) и химиолучевая терапия (ХЛТ). При этом первичная опухоль зачастую более чувствительная к облучению, чем регионарные метастазы, что в ряде случаев определяет необходимость регионарной лимфаденэктомии при поражении регионарных лимфатических узлов (ЛУ) и излечении первичной опухоли.Значимым прогностическим фактором является наличие ВПЧ в опухоли
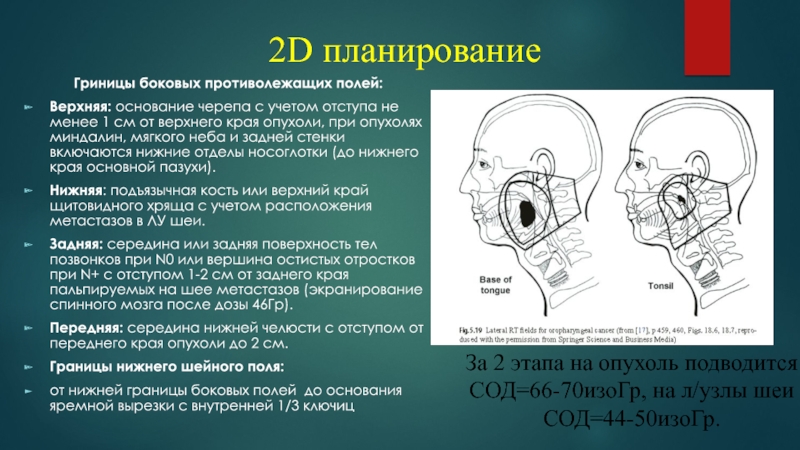
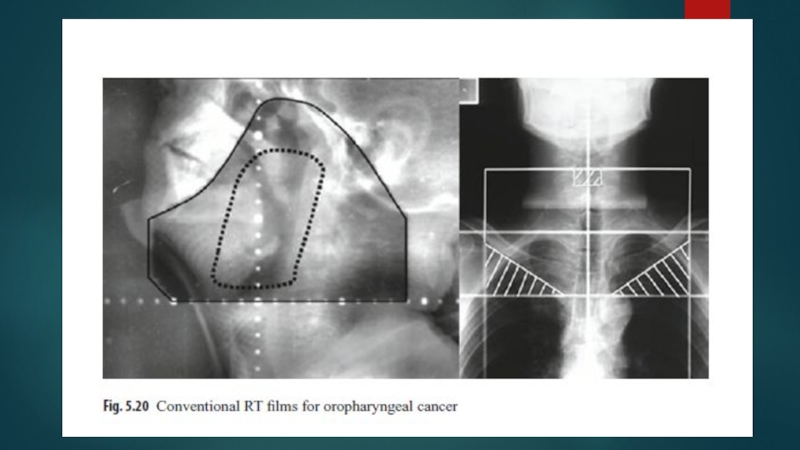
Слайд 33 2D планирование
Гриницы боковых противолежащих полей:
Верхняя: основание черепа с
учетом отступа не менее 1 см от верхнего края опухоли,
при опухолях миндалин, мягкого неба и задней стенки включаются нижние отделы носоглотки (до нижнего края основной пазухи).Нижняя: подъязычная кость или верхний край щитовидного хряща с учетом расположения метастазов в ЛУ шеи.
Задняя: середина или задняя поверхность тел позвонков при N0 или вершина остистых отростков при N+ с отступом 1-2 см от заднего края пальпируемых на шее метастазов (экранирование спинного мозга после дозы 46Гр).
Передняя: середина нижней челюсти с отступом от переднего края опухоли до 2 см.
Границы нижнего шейного поля:
от нижней границы боковых полей до основания яремной вырезки с внутренней 1/3 ключиц
За 2 этапа на опухоль подводится СОД=66-70изоГр, на л/узлы шеи СОД=44-50изоГр.
Слайд 35GTV 70p: опухоль, видимая при осмотре, по данным инструментальных методов
исследования.
GTV 70n: л/у диаметром > 1 см, с некротическими изменениями,
с патологическим накоплением контраста.CTV 70р: = GTV 70 + 5 мм, в ситуациях, когда нет четкой визуализации границ опухоли
PTV 70: CTV 70рn +3-5 мм
PRV для OAR: 3-5 мм
Предписание доз и отступы для 3D- CRT
Слайд 38Одностороннее облучение лимфоузлов
Finally, patients with well-lateralized T1-T2 tonsillar cancer and
N0-N1 nodal category should receive unilateral RT.
Unilateral RT may also
be considered in patients with lateralized (<1 cm of soft palate extension but no tongue involvement) T1-T2 N0-N1 tonsillar cancer with no clinical or radiograph evidence of extracapsular extension, again provided patients understand the relative benefits of unilateral treatment vs risk for contralateral nodal recurrence.Слайд 44Режим фракционирования
Традиционное фракционирование: 2,0Гр 5 дней в неделю (предпочтительно
при непрерывной ЛТ и ХЛТ).
Динамическое (ускоренное фракционирование): подведение 3 фракций
по 4,0Гр за один сеанс в день или два сеанса в день по 2,0Гр с интервалом 4 – 6 часов в первые 3 дня лечения или по пятницам (предпочтительно при СПЛИТ-курсах).Слайд 47Оценка эффекта после завершения ЛТ или ХЛТ
Результаты лечения оцениваются через
2-3 месяца после завершения ЛТ на основании визуального осмотра, эндоскопического
обследования и УЗИ.При подозрении на наличие остаточной опухоли в области первичного очага или регионарных метастазов обязательна биопсия для верификации.
При верификации остаточной опухоли решается вопрос о хирургическом лечении.
При сN2-3 и полном клиническом ответе на ЛТ или ХЛТ, через 3 месяца после завершения лечения необходимо ПЭТ-КТ, при наличии очагов повышенной метаболической активности в регионарных ЛУ выполняется регионарная лимфодиссекция.