Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
№ 3 лекция. БАЗ- дың заманауи, ғылыми классификациясы Лекция жоспары: БАЗ- дың
Содержание
- 1. № 3 лекция. БАЗ- дың заманауи, ғылыми классификациясы Лекция жоспары: БАЗ- дың
- 2. БАЗ-дың заманауи, ғылыми классификациясы анионактивтіКатионактивтібейионогендіамфолитті
- 3. Анионактивті БАЗГидрофобды көмірсутекті бөлігімен байланысқан теріс ионға
- 4. Анионактивті БАЗГидрофобды көмірсутекті бөлігімен байланысқан теріс ионға
- 5. 3) Алкилсульфонаттар және алкиларилсульфонаттар
- 6. 1) Жоғары май қышқылдары жуғыш әсері С8
- 7. 2) Алкилсульфаттар – заманауи жуғыш заттардың құрамына
- 8. 3) Алкил- и алкиларилсульфонаттар өте жақсы жуғыш
- 9. Натрий алкилбензольсулфаттарын алу;Натрий алкилсульфонаттарын алу;Натрий алкилсульфаттарын алу
- 10. Алкилдеу. Сульфонолды алудың негізгі екі әдісі бар:
- 11. Колонна ығыстыру принципі бойынша жұмыс істейді: хлор
- 12. Слайд 12
- 13. Алкилдеу нәтижесінде түзілген қосылыстардың алкил тізбегінде бензол
- 14. Алкилдеу реакциясында қолданылатын алюминий хлориді негізгі реакция
- 15. Алкилбензолды күкірт қышқылы мен олеум көмегімен сульфирлеу
- 16. Процестің конверсиясы – 98%, реация лезде өтеді,
- 17. Алкилбензолды күкірттің сұйық триоксиді мен диоксиді қоспасымен
- 18. Слайд 18
- 19. Алкилбензолсульфонаттардың хлорсыз өндірісінде шикізат ретінде сұйық немесе
- 20. Бензолды алкендермен алкилдеу реакциясын:
- 21. Алкендерден сульфонолды өндіру технологиясының ерекшелігі алкилаттар мен
- 22. Алкилбензолдардың мақсаттағы фракциясы 7- бағанадан кейін сульфураторға
- 23. Сульфонолға қойылатын негізгі техникалық талаптар:Натрий алкилбензолсульфонаты 35-40%(мас.)
- 24. Скачать презентанцию
БАЗ-дың заманауи, ғылыми классификациясы анионактивтіКатионактивтібейионогендіамфолитті
Слайды и текст этой презентации
Слайд 1№3 лекция. БАЗ-дың заманауи, ғылыми классификациясы
Лекция жоспары:
БАЗ-дың заманауи, ғылыми
классификациясы:
Слайд 3Анионактивті БАЗ
Гидрофобды көмірсутекті бөлігімен байланысқан теріс ионға және қарсы ион
– катионға диссоцияланады.
Анионды БАЗ-дар өздерінің жақсы жуғыштық қасиетіне, техникалық көрсеткіштеріне
және арзандығына байланысты СЖЗ кеңінен қолд. СЖЗ өндірісінде натрийдің алкилбензолсульфонаттары, алкилсульфонаттары, алкилсульфаттары қолд. АБАЗ-дарды алудың негізгі тәсілдеріне майлы спирттерді сульфаттау; алкилбензолдарды, олефиндерді және т.б. Көмірсутектерді күкірт қышқылымен, олеуммен (SO3 әртүрлі мөлшерде) сульфирлеп, сілті ерітінділерімен бейтараптау жатады.Слайд 4
Анионактивті БАЗ
Гидрофобды көмірсутекті бөлігімен байланысқан теріс ионға және қарсы ион
– катионға диссоцияланады.
Құрылысы бойынша 4 топқа бөлінеді:
Жоғары май қышқылдары
(карбон қышқылдары) және олардың тұздары RCOONa;алкилсульфаттар а) R-CH2-OSO3Na
б)
Слайд 53) Алкилсульфонаттар және
алкиларилсульфонаттар
R-CH2-OSO2Na
R-Ar-OSO2Na
4) Басқа гидрофильді топтары
бар бар БАЗ - фосфаттар, фосфонаттар, тиосульфаттар, сульфамидтер және т.б.Слайд 61) Жоғары май қышқылдары жуғыш әсері С8 басталып, мах –
С11-С17 көтерілгенше дейін жоғарылайды. С20 қолданылмайды, себебі Na тұздарының ерігіштігі
төмендейді. -СООН – әлсіз полярлы топ болғандықтан, бірнеше кемшіліктері бар:а) кермектілігі жоғары суда жумайды (Mg, Ca жуғыш әсерін төмендетеді);
б) сілтілік ерітінділерде ғана жуады, сондықтан жібек және синтетикалық маталарды жууда қолданбайды.
Қасиетін жасарту үшін қосымша топтар, көбінесе полипептидті, еңгізеді.
Мысалы: ламепон – RCONHR1(CONHR2)COOМе
Mg, Ca тұздарына және бейтарап ерітінділерде тұрақты.
Слайд 72) Алкилсульфаттар – заманауи жуғыш заттардың құрамына кіреді, Mg, Ca
тұздары жақсы ериді. Мах – С12 – С18.
Екіншілік алкилсульфаттардың жуғыш
қабілеті төмен және сульфотоптын орналасуына тәуелді, тізбек шетіне жақын орналасқан сайын жуғыш қабілеті жоғарылайды. Слайд 83) Алкил- и алкиларилсульфонаттар өте жақсы жуғыш заттар, олардың Mg,
Ca тұздары суда жақсы ериді, қышқыл орталарда да жуғыш әсер
көрсетеді.Артықшылықтары:
ерігіштігі, термиялық тұрақтылығы және төмен су тартқыш қабілеті, сондықтан оларды ұнтақ түрінде өндіреді.
Жаңа қасиеттерге иелендіру үшін олардың құрамына функционалды топтарды еңгізеді: эфирлік немесе амидті.
Слайд 9Натрий алкилбензольсулфаттарын алу;
Натрий алкилсульфонаттарын алу;
Натрий алкилсульфаттарын алу
Слайд 10Алкилдеу. Сульфонолды алудың негізгі екі әдісі бар: хлорлы және хлорсыз.
Сульфонолдарды хлорлы әдіс бойынша алудың бірінші сатысында С10-С14 фракциясының қаныққан
көмірсутектерін газ тәрізді хлормен хлорлайды:R-CH3 + Cl2 →R-CH2Cl + HCl
R-CH2 -CH3 + Cl2 →R-CHCl-CH3 + HCl
Слайд 11Колонна ығыстыру принципі бойынша жұмыс істейді: хлор перфорацияланған түтік бойымен
колоннаның төменгі жағына түседі, көмірсутетер де төмен беріледі, ал реакциялық
масса жоғарыдан шығарылады. Реакция жылулығы тоңазытқыш арқылы циркуляцияланатын реакциялық массаның көмегімен шығарылады. Колоннадағы температура 30 °С-ге жуық шамада сақталады. Хлорлаудан кейін алкилхлоридтер бензолды алкилдеу сатысына түседі:R-CH2 Cl + C6 H6 (AlCl3)→R-CH2-C6 H5 + HCl
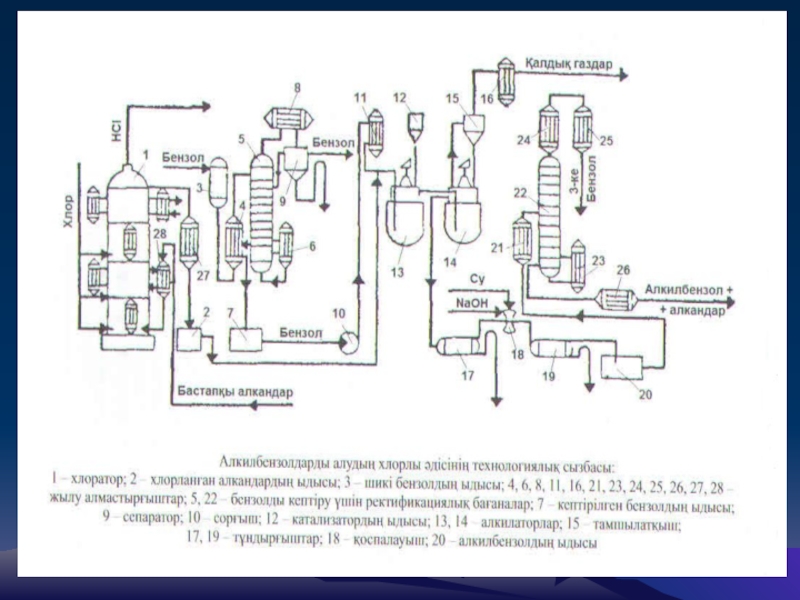
Алкилбензолды алудың хлорлы әдісінің технологиялық сызбанұсқасы:
Слайд 13
Алкилдеу нәтижесінде түзілген қосылыстардың алкил тізбегінде бензол сақинасы әртүрлі орналасады.
Бензол тізбектің ортасында орналасқан алкилбензолдардың түзілуін катализатордың әсерінен жүретін алкил
топтарының изомерленуі қамтамасыз етеді:R-CH2 Cl + C6 H6 →R-CH2-C6 H5 + HCl
R-CHCl-R/ + C6 H6 →R-CH-(C6 H5)-R/ + HCl
Бензолды алкилдеу кезінде бензолмен дихлоралкандардың әрекеттесуінен – дифенилалкандар, сонымен қатар монохлоралкандар мен алкилбензолдан диалканбензолдар түзілуі ықтимал.
R-CHCl-R/ + R//- CH-(C6 H5)-R/// →RCHR/- C6 H5-R//CHR/// + HCl
монохлоралкан алкилбензол диалкилбензол
Слайд 14Алкилдеу реакциясында қолданылатын алюминий хлориді негізгі реакция үшін жақсы катализатор
бола тұрып, қосымша реакциялардың да жүруін қамтамасыз етеді. Оңтайлы температура
10-160С-ден аспау керек, ал катализатордың мөлшері реакцияланатын массаның 15% -на жуық шаманы құрайды.Алкилдеу үшін катализаторды арнайы дайындайды: оны қыздыра отырып, алкилбензолда ерітеді., одан кейін хлорсутекпен қанықтырады. Түзілген 2R-C6H5 . AlCl3.HCl комплексін алкилдеу катализаторы ретінде қолданады.
Алкилбензолды сульфирлеу үшін әдетте күкірт қышқылы, олеум немесе күкірт триоксиді қолданылады.
Слайд 15Алкилбензолды күкірт қышқылы мен олеум көмегімен сульфирлеу келесі реакциялар бойынша
жүреді:
RC6 H5 + H2SO4
→ RC6 H4 SO3H + H2O2RC6 H5 + H2SO4 .SO3 → 2RC6 H4 SO3H + H2O
Реакция жылдамдығы алкил радикалының ұзаруымен өсіп, қоспадағы су мөлшерінің артуымен азаяды, содан сульфирлеу терең өту үшін суды байланыстыратын сульфирлеуші агенттің артық мөлшерін алған жөн. Бірақ сульфирлеуші агент мөлшерінің артуымен ластанған күкірт қышқылы мен реакциялық массаны нейтралдауға кететін сілті мөлшері арта түседі. Сондықтан оған қарағанда перспективті сульфирдеуші агент болып SO3 табылады. алкилбензолдың күкірт триоксидімен сульфирленуі қайтымсыз реакция, себебі реакциялық қоспада су болмайды:
RC6 H5 + SO3 → RC6 H4 SO3H.
Слайд 16Процестің конверсиясы – 98%, реация лезде өтеді, бірақ нәтижесінде қосымша
өнімдер – сульфон қышқылдарының ангидридтері түзіліп, олардың мөлшері күкірт триоксидінің
артық мөлшерінде және температураның артуымен өседі. Сульфон қышқылдары ангидридтерін сумен бірге қыздырса, олар алкилбензолсульфон қышқылдарына айналады:2RC6 H5 +3SO3 → (RC6 H4 SO2)2О + H2SO4
(RC6 H4 SO2)2О + H2O→ 2RC6 H4 SO3H
Әдетте сульфирлеу реакциясын реагенттердің нақты мольдік қатынасы мен төмен температурада (реакция зонасые біркелкі суыту арқылы) жүргізеді. Нейтрализацияның алдында арнайы аппаратта сульфон қышқылдарының ангидридтерін бұзады.
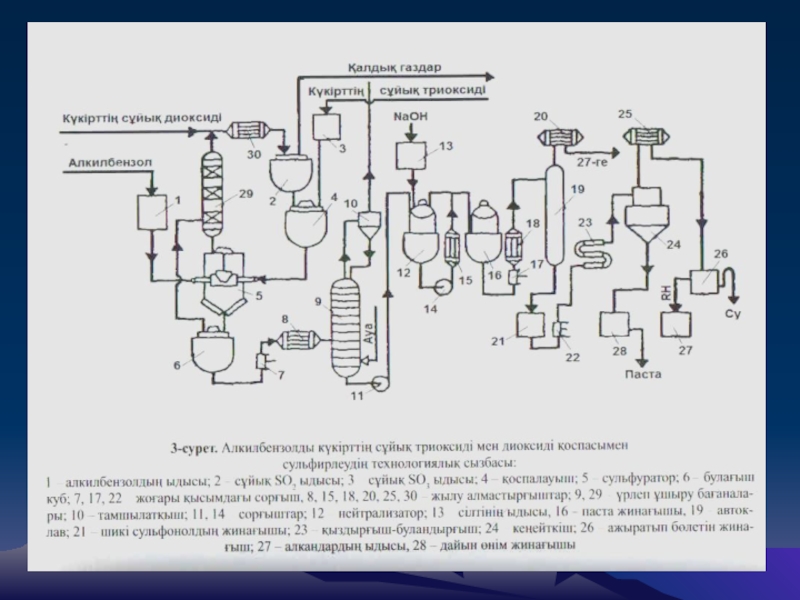
Слайд 17Алкилбензолды күкірттің сұйық триоксиді мен диоксиді қоспасымен сульфирлеу реакцияны төмен
температурада жүргізуге мүмкіндік туғызады, яғни тотығу прцестері мен қызу ықтималдығы
азаяды(бірақ сульфирлеу тереңдігінің азаю мүмкіндігі жойылмайды). Бұл әдістің тағы бір артықшылығы сульфирлеу реакциясы гомогенді ортада өтеді және күкірт диоксиді алкилбензолдар үшін еріткіш болып табылады. Реакцияларға қажет еріткіштің мөлшерін реакция жылулуғын толығымен шығаруға шағып есептейді (3-сурет).Слайд 19Алкилбензолсульфонаттардың хлорсыз өндірісінде шикізат ретінде сұйық немесе қатты парафиндердің крекинг
нәтижесінде алынатын С10-С14 фракциядағы алкендер қолданылады. Крекинг өнімдеріне 15-20% (мас)
қаныққан және 80-85% (мас) қанықпаған көмірсутектер кіреді. Қанықпаған көмірсутектердің басым бөлігін түзу сызықты алкендер-1 құрайды. С10-С14 фракциядағы алкиндер-1 шығымы 35%(мас) тең.Алкилбензолсульфонаттардың өндірісіндегі алкендер-1 AlCl3 катализаторындағы этиленнің олигомеризациясы арқылы алынады. Нәтижесінде көміртек атомдарының жұп санымен анықталатын алкендердің қоспасы түзіліп, ондағы С10-С14 фракциясы 50%(мас)-ды құрайды. Алкилбензосульфонаттар өндірісінде алкендерді шикізат ретінде қолданудың артықшылығы олардың құрамында қаныққан көмірсутектердің болмауында, яғни сульфатталмаған қосылыстарды бөліп шығару процесінің жеңілденуінде.
Слайд 20Бензолды алкендермен алкилдеу реакциясын:
AlCl3
С6Н6
+ R-CH=CH2 C6H5-CHRCH3 жалпы түрде келтіруге болады.
Өндірісте катализатор ретінде алкилхлоридтермен алкилдеу процесіндегідей құрамда ерігіш комплекс күйіндегі алюмийний хлоридін қолданады.
Алкилдеу кезінде негізгі реакциямен қатар α-олефиндердің изомерленуі мен полимерленуі, полиалкилдеу және т.б. реакциялары жүреді. Бұл реакциялардың нәтижесінде негізгі өнім- моноалкилбензолсульфонаттармен қатар диалкилбензолсульфонаттар түзілуі мүмкін және мұндай қосымша өнімдер соңғы өнімнің түсін нашарлатады.
Слайд 21Алкендерден сульфонолды өндіру технологиясының ерекшелігі алкилаттар мен мақсаттағы фракцияны бөліп
алу сатысының аппаратуралық жабдықталуы болып табылады (4-сурет). Хлорсыз тәсілмен сульфонолды
алудың технологиялық сызбанұсқасыСлайд 22Алкилбензолдардың мақсаттағы фракциясы 7- бағанадан кейін сульфураторға (9) түседі. Күкірт
қышқылымен периодтық сульфаттау тиімсіз болып табылады, себебі реакция қатаң жағдайда
жүргізіліп, күкірт қышқылының үлкен шамадағы артық мөлшерін талап етеді. Оған қарағанда үздіксіз тәсіл экономикалық тиімдірек: сульфаттау температурасы- 30-40˚С, тереңдігі- 96-98 %.Сульфаттаудан кейінгі сатысы- күкірт қышқылының артық мөлшерін бөліп алу. Сульфоқышқылдар күкірт қышқылының 70-75%-дық ерітіндісінде ерімейтін болғандықтан, реакция өнімдерін сумен сұйытып, жоғарғы қабатын, яғни сульфоқышқылдарды қышқыл гудроннан бөліп алады. Әрі қарай нейтрализациялайды.
Слайд 23Сульфонолға қойылатын негізгі техникалық талаптар:
Натрий алкилбензолсульфонаты 35-40%(мас.) болуы керек;
БАЗ-ға есептегенде
сульфатталмаған қосылыстар 3,5%-дан аспау керек;
Натрий сульфаты 5%-дан аспау керек;
БАЗ-ға есептегенде
жоғары молекулалық сульфоқышқылдар кем дегенде 80% болуы керек;Молекулалық массасы 320-330 болу керек;
1%-дық ерітіндінің рН көрсеткіші 7,5-9,5 болуы керек.
Сульфонолдың 1 тоннасын алу үшін 0,4 т бензол, 0,9 т алкен-1, 0,03 т алюминий хлориді, 0,27 т күкірт триоксиді, 0,15 т натрий гидроксиді кетеді.