Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Непредельные углеводороды
Содержание
- 1. Непредельные углеводороды
- 2. Классификация
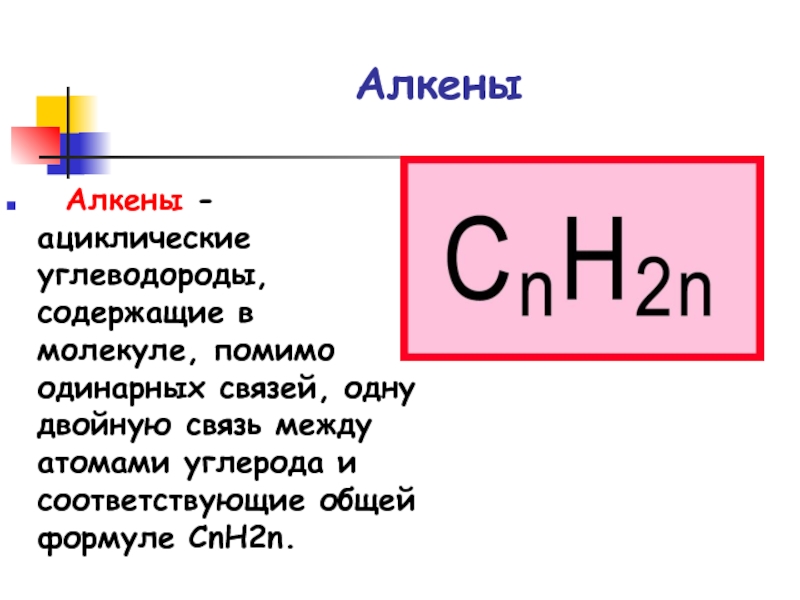
- 3. Алкены Алкены - ациклические углеводороды, содержащие
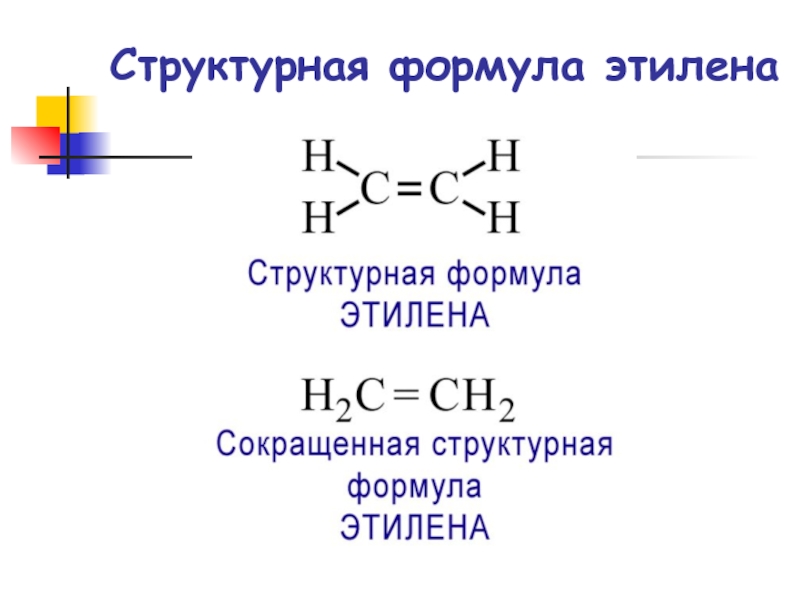
- 4. Структурная формула этилена
- 5. Изомерия и номенклатура
- 6. Номенклатура алкенов
- 7. Алкены. Номенклатура 1)
- 8. Алкены. Номенклатура 2) в
- 9. Алкены. Номенклатура 3) Углеводородные
- 10. Алкены. Номенклатура2-метилбутен-2 2,5-диметилгексен-2
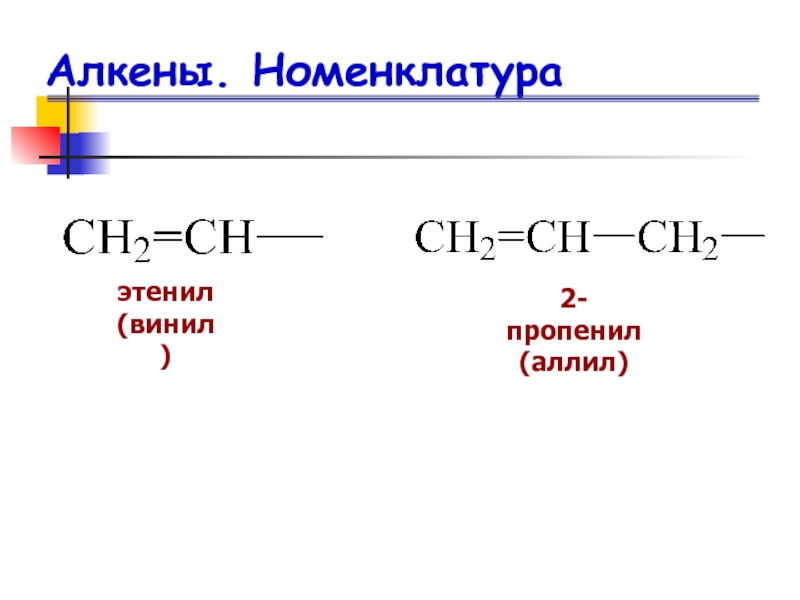
- 11. Алкены. Номенклатураэтенил(винил) 2-пропенил(аллил)
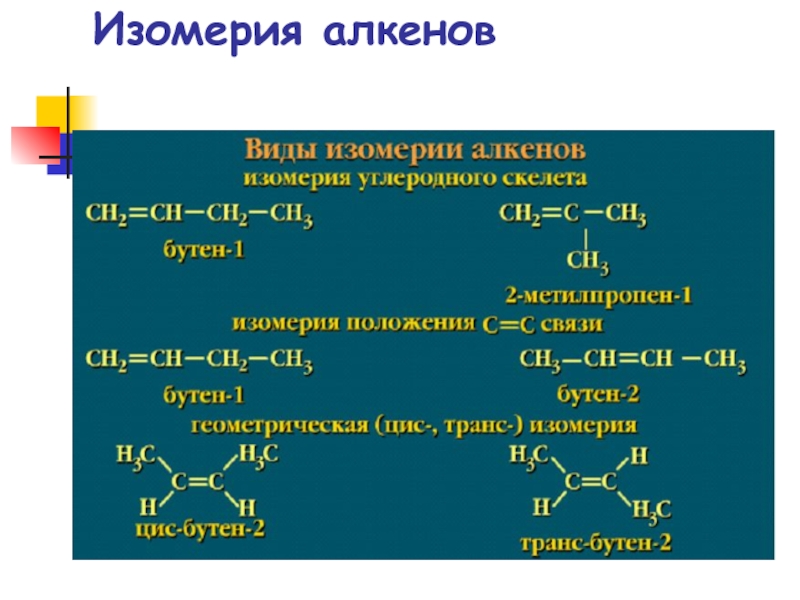
- 12. Изомерия алкенов
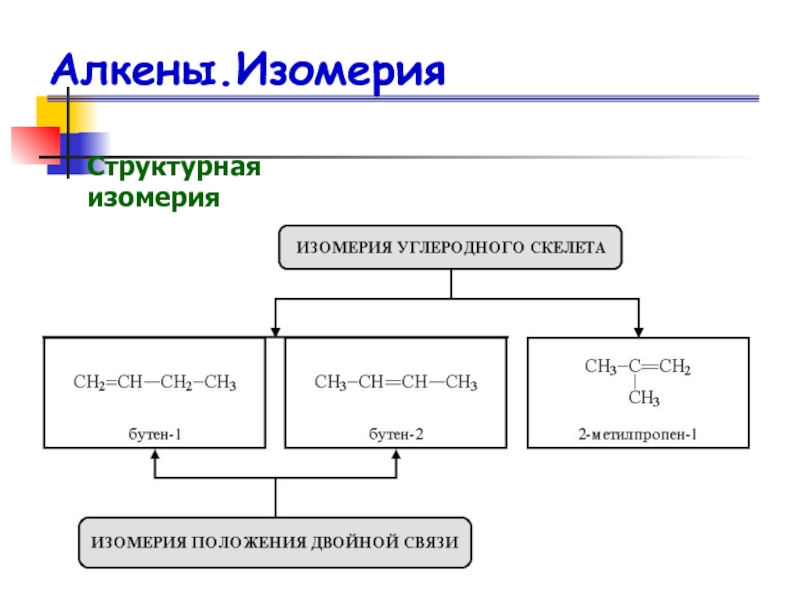
- 13. Алкены.ИзомерияСтруктурная изомерия
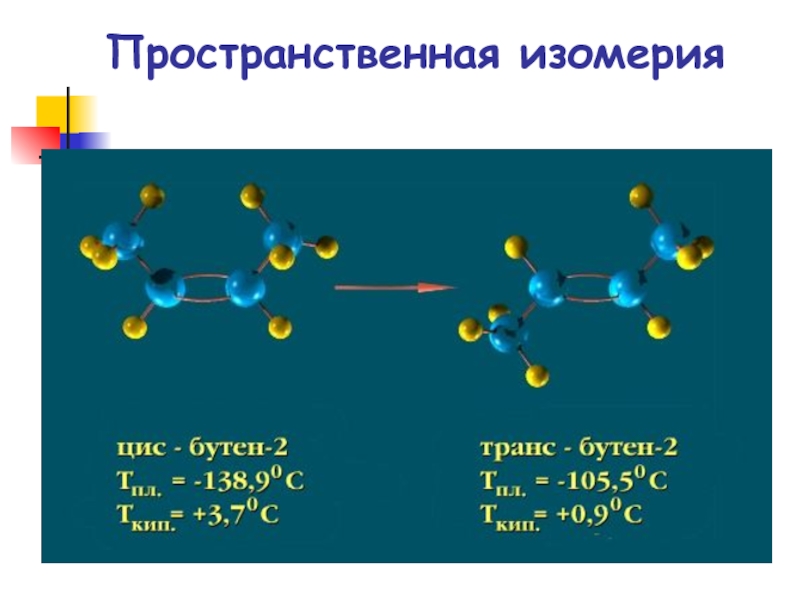
- 14. Пространственная изомерия
- 15. Пространственная изомерия
- 16. Пространственная изомерияПространственная изомерия Цис- и транс-изомеры бутена-2
- 17. Пространственная изомерияПространственная изомерия цис-бутен-2Ткип=4С транс-бутен-2Ткип=1С
- 18. Пространственная изомерия
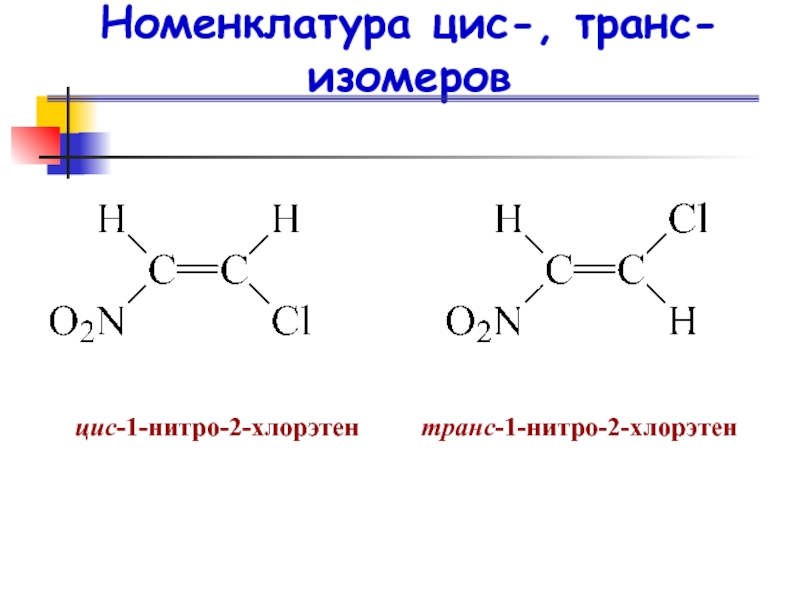
- 19. Номенклатура цис-, транс-изомеров
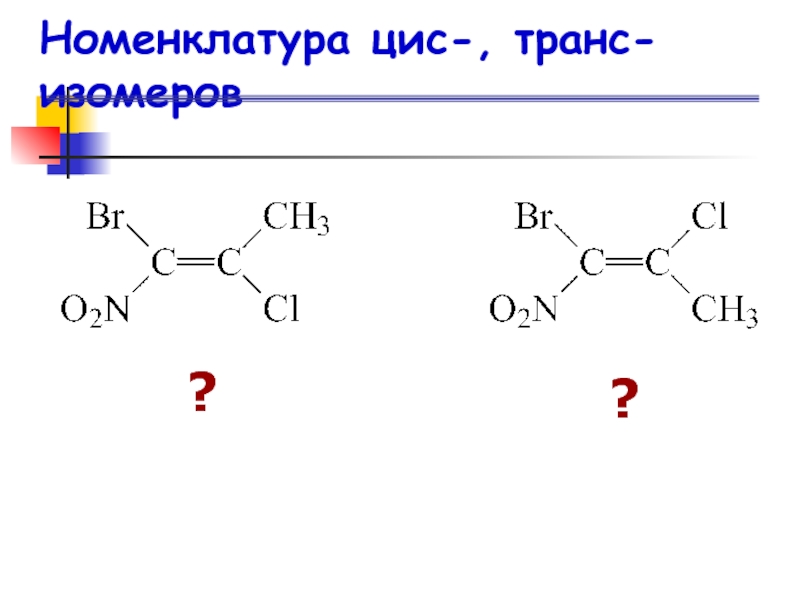
- 20. Номенклатура цис-, транс-изомеров ??
- 21. Номенклатура цис-, транс-изомеров Система Кана–Ингольда–Прелога Прелог Владимир(23.07.1906–07.01.1998) (Швейцария)Ингольд Кристофер (28.10.1893–8.10.1970) (Великобритания)Роберт Сидни Кан(9.06.1899-15.09.1981) (Великобритания)?
- 22. Номенклатура цис-, транс-изомеров 1. Используя систему
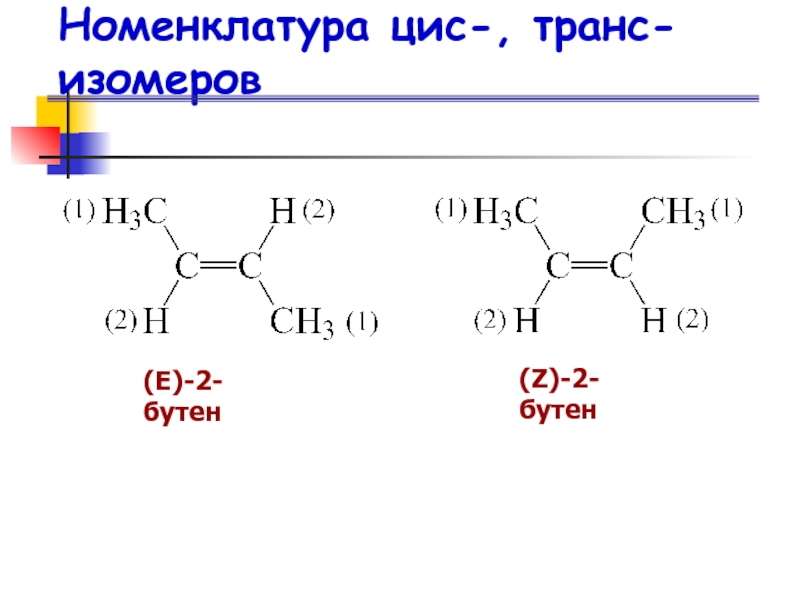
- 23. Номенклатура цис-, транс-изомеров (Е)-2-бутен (Z)-2-бутен
- 24. Номенклатура цис-, транс-изомеров (Е)-1-бром-1-нитро-2-хлорпропен (Z)-1-бром-1-нитро-2-хлорпропен
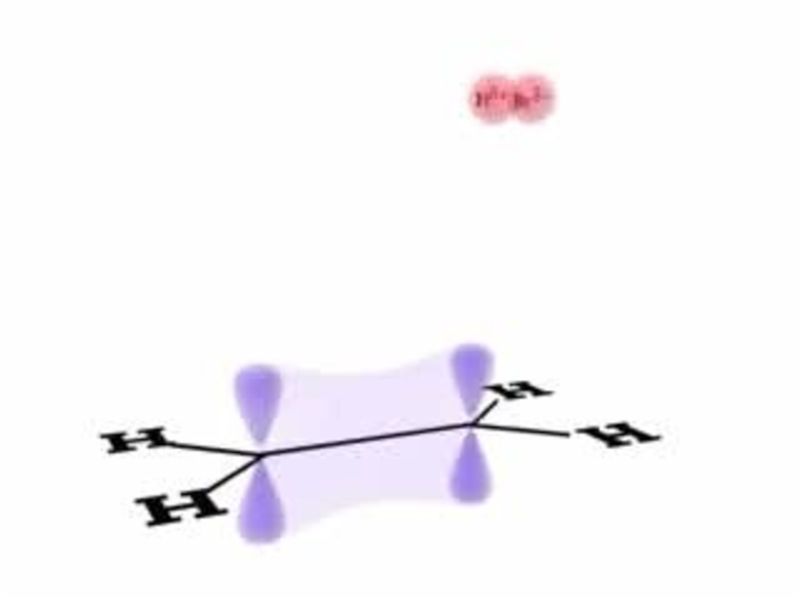
- 25. Строение алкенов
- 26. Модель молекулы этилена
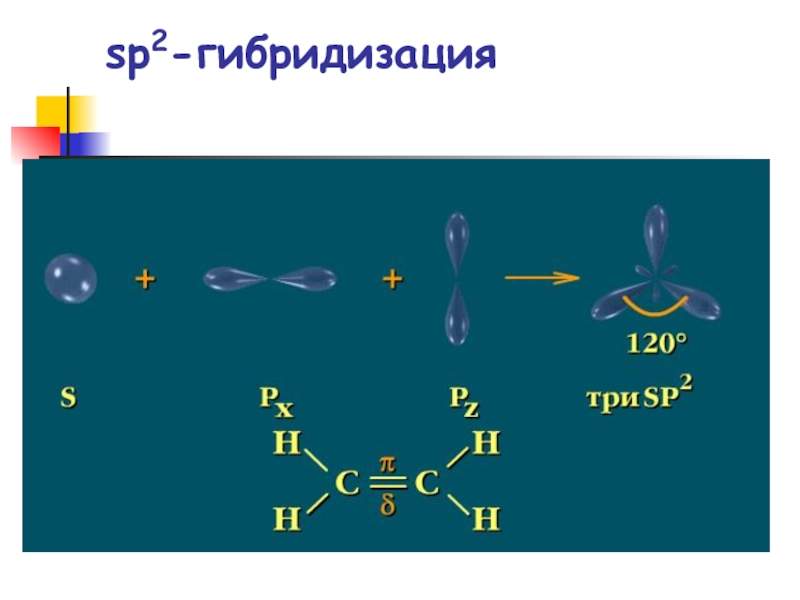
- 27. sp2-гибридизация
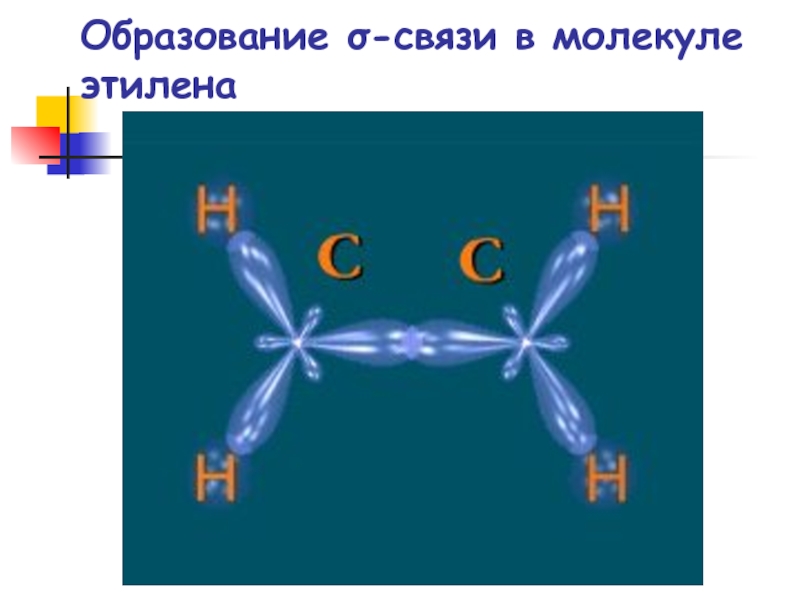
- 28. Образование σ-связи в молекуле этилена
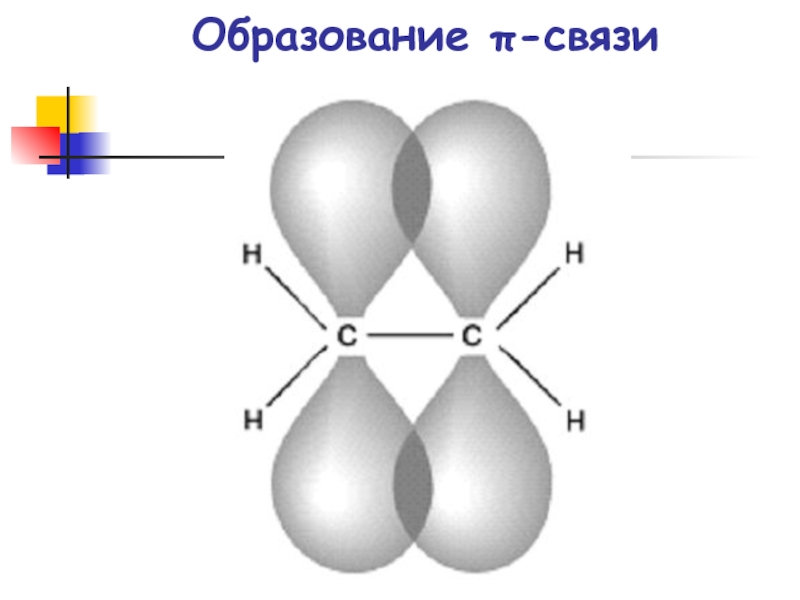
- 29. Образование π-связи
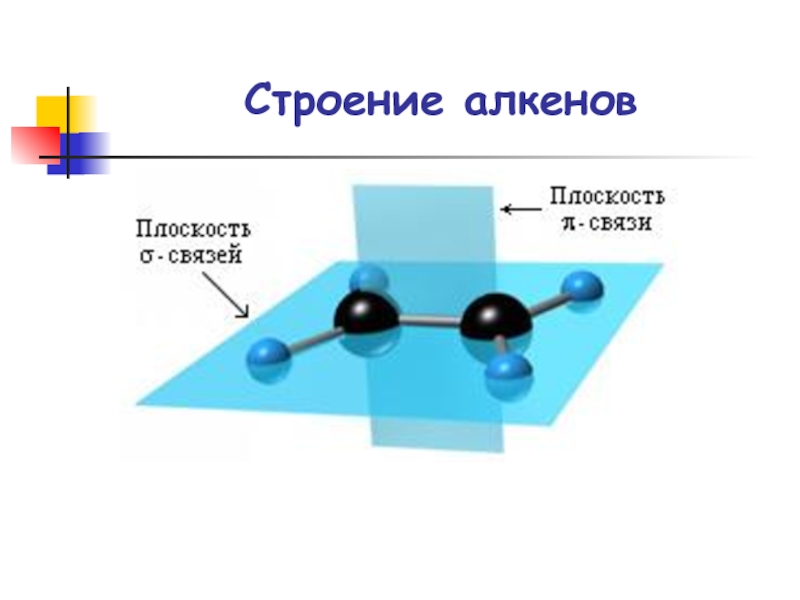
- 30. Строение алкенов
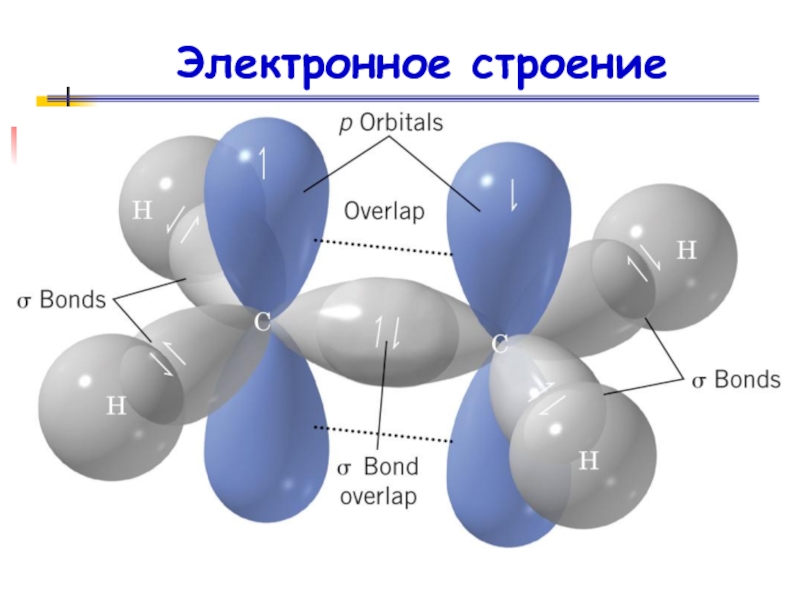
- 31. Электронное строение
- 32. Слайд 32
- 33. Нахождение в природе Этилен и его
- 34. Способы получения алкенов
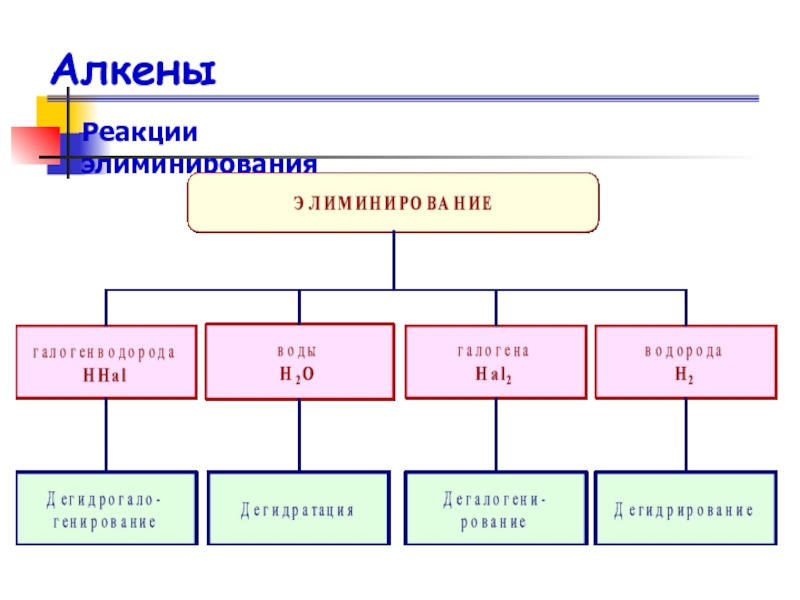
- 35. АлкеныРеакции элиминированияЭлиминирование — это отщепление двух атомов
- 36. АлкеныРеакции элиминирования
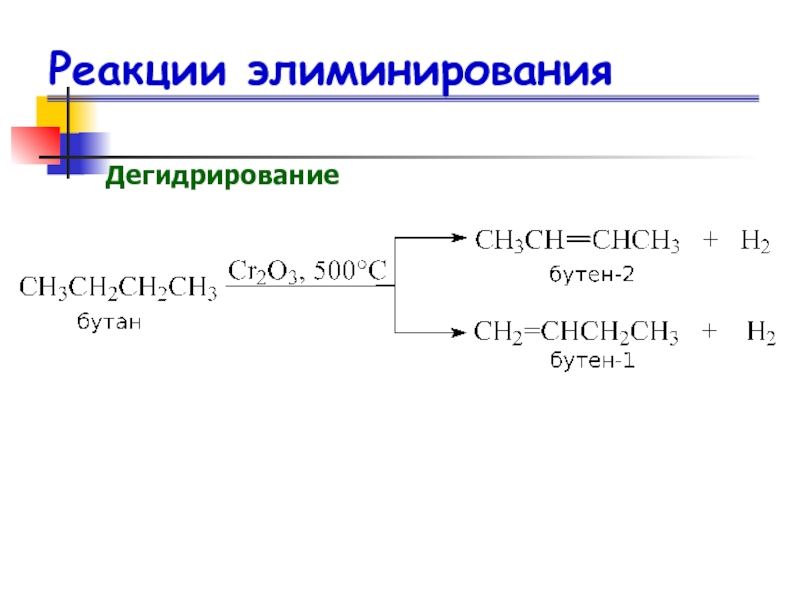
- 37. Дегидрирование алканов
- 38. Реакции элиминированияДегидрирование
- 39. Дегидрогалогенирование хлорпроизводных
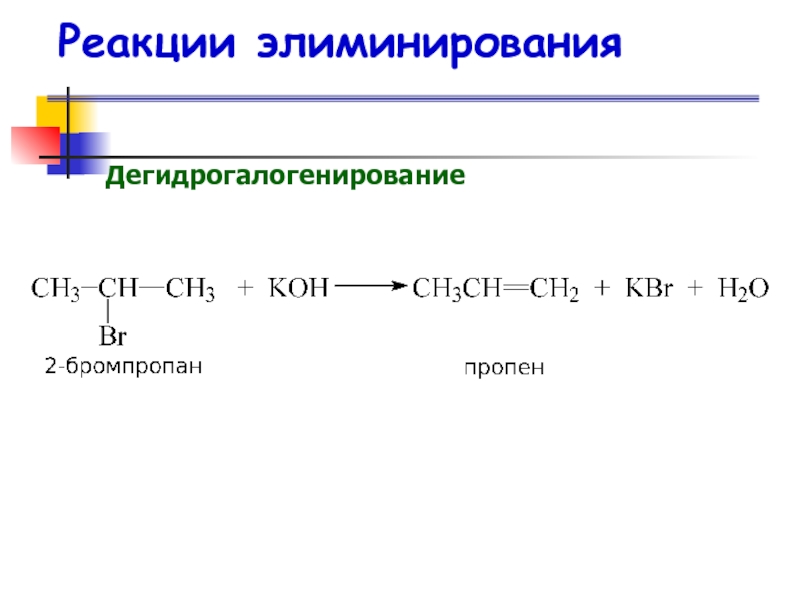
- 40. Реакции элиминирования Дегидрогалогенирование
- 41. Реакции элиминирования Дегидрогалогенирование Правило ЗайцеваВ случае нессиметричных
- 42. ЗАЙЦЕВ Александр Михайлович (Россия)(2.VII.1841 - 1.IX.1910)
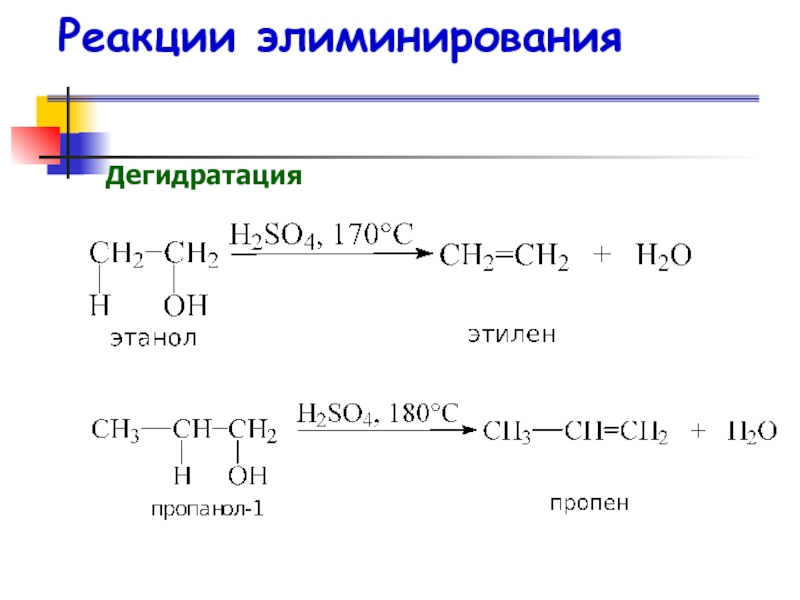
- 43. Дегидратация спиртов
- 44. Реакции элиминирования Дегидратация
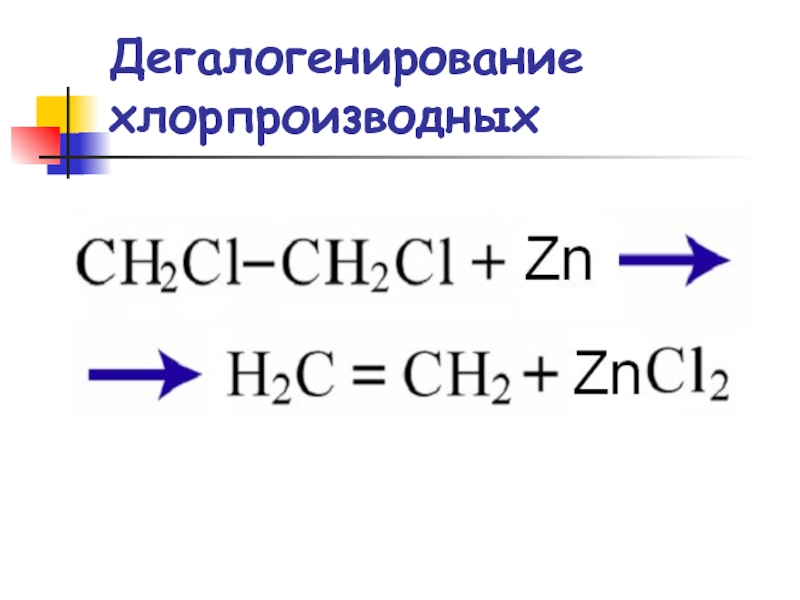
- 45. Дегалогенирование хлорпроизводных
- 46. Реакции элиминирования Дегалогенирование
- 47. Пиролиз алканов
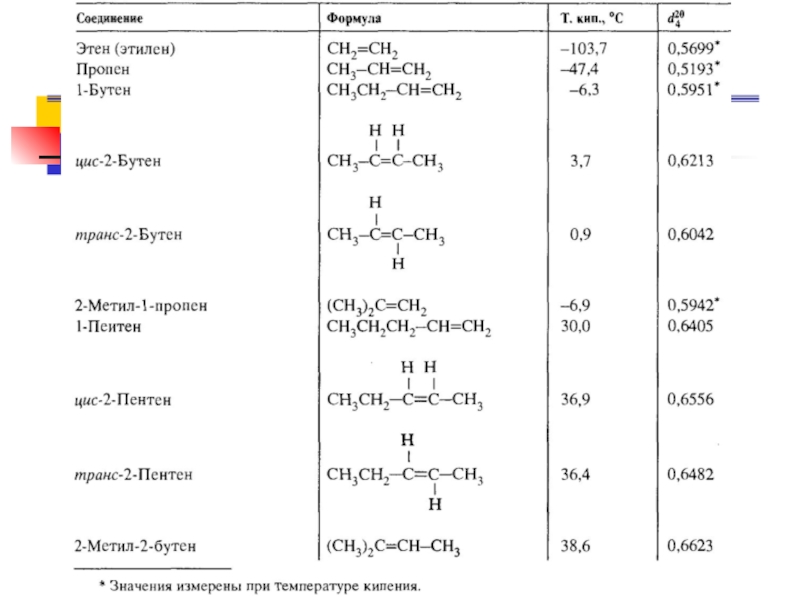
- 48. Физические свойства алкенов Алкены обладают более
- 49. Слайд 49
- 50. Химические свойства
- 51. Общая характеристика реакционной способности алкенов
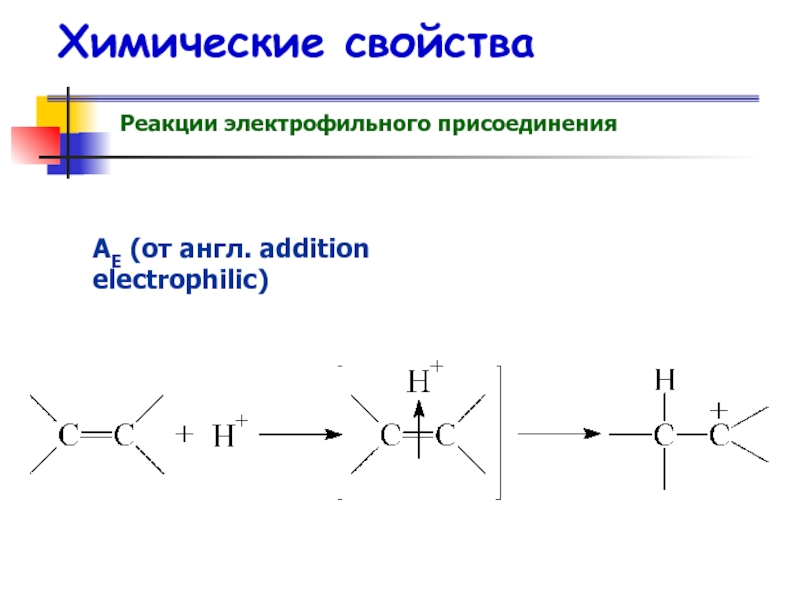
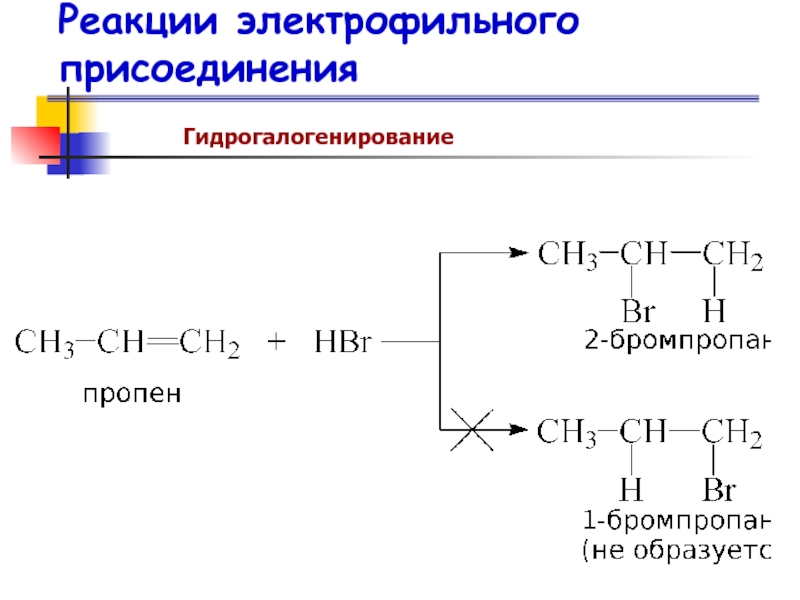
- 52. Химические свойства Реакции электрофильного присоединения АE (от англ. addition electrophilic)
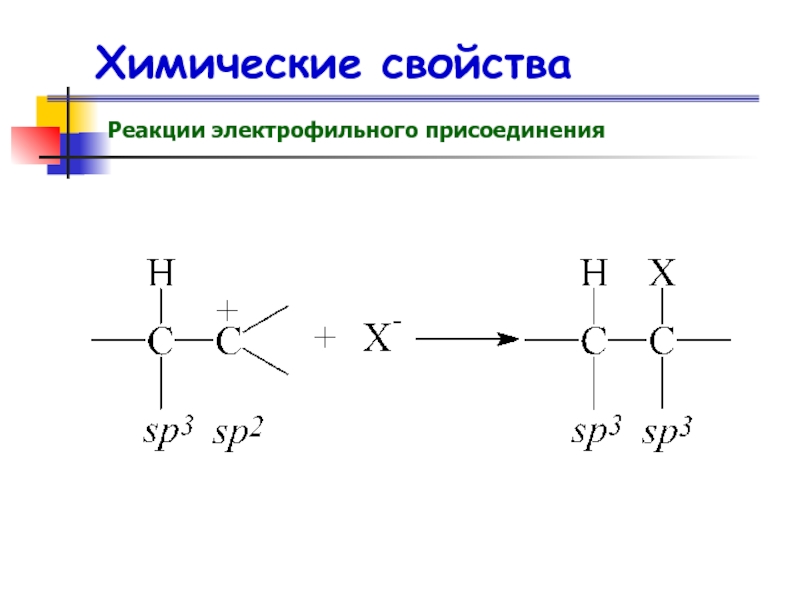
- 53. Химические свойства Реакции электрофильного присоединения
- 54. Химические свойстваРеакции электрофильного присоединения
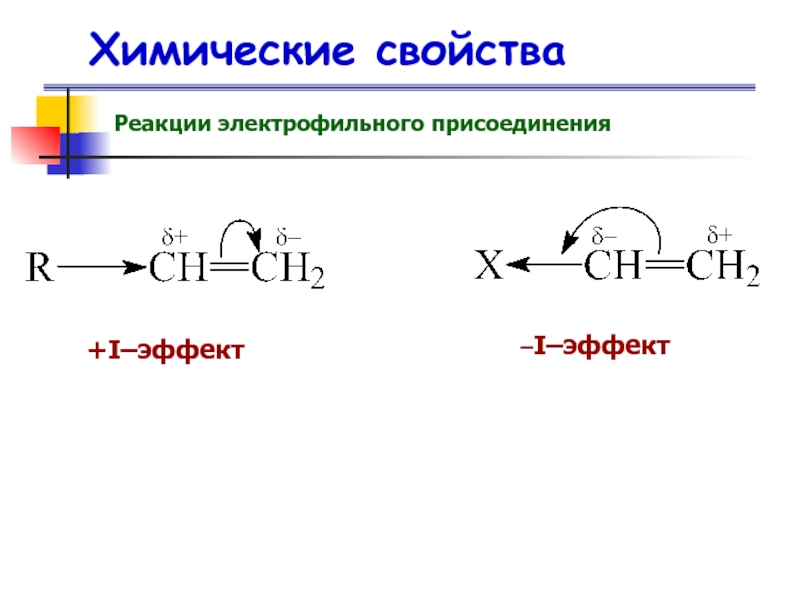
- 55. Химические свойстваРеакции электрофильного присоединения +I–эффект –I–эффект
- 56. Реакции присоединения
- 57. Гидрирование этилена
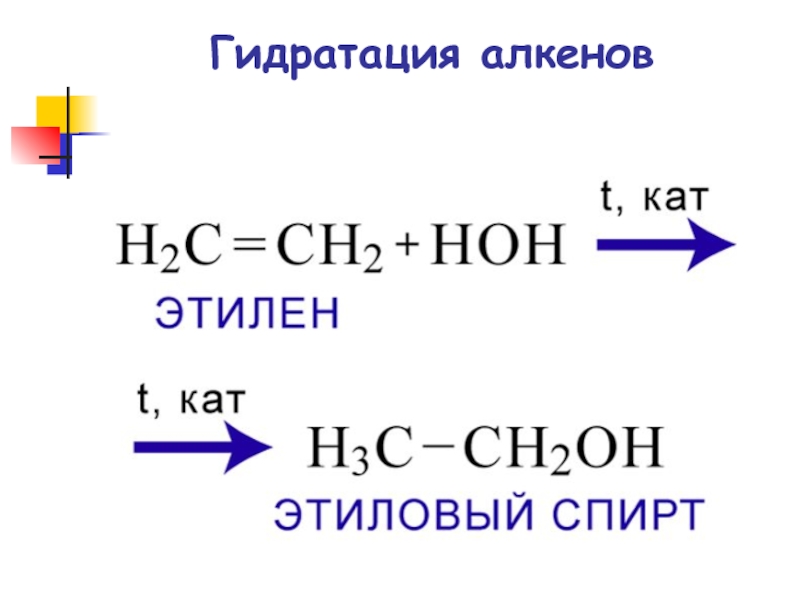
- 58. Гидратация алкенов
- 59. Галогенирование алкенов
- 60. Реакции электрофильного присоединения Галогенирование
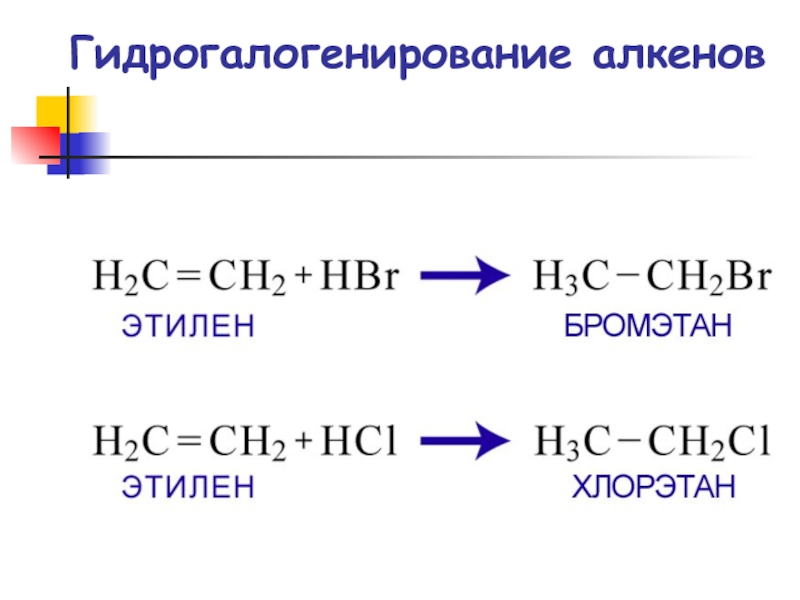
- 61. Гидрогалогенирование алкенов
- 62. Реакции электрофильного присоединения Гидрогалогенирование
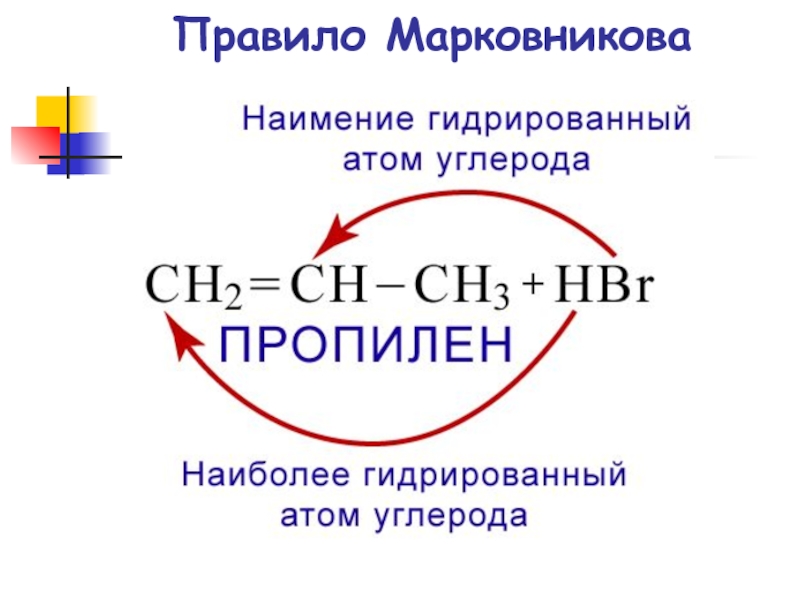
- 63. Правило Марковникова
- 64. Владимир Васильевич Марковников 1837 – 1904 гг.
- 65. Слайд 65
- 66. Механизм реакции гидрогалогенирования
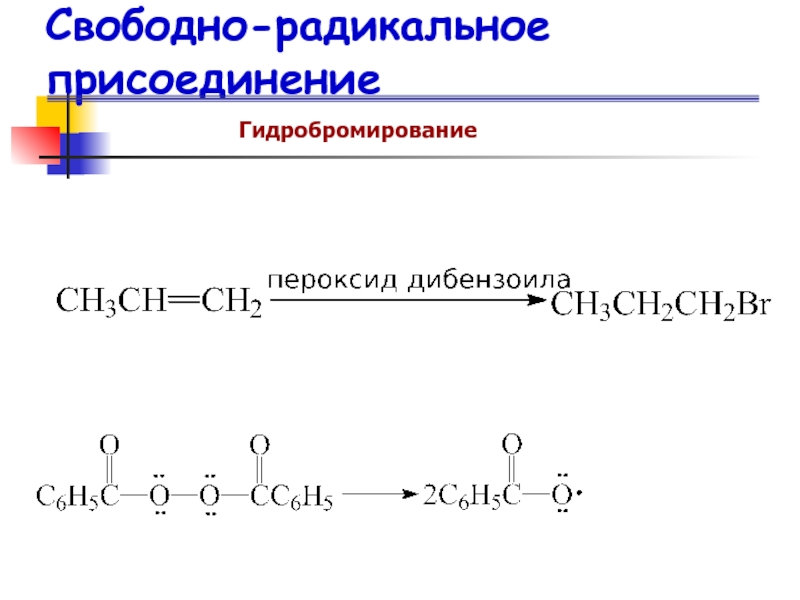
- 67. Свободно-радикальное присоединение Гидробромирование
- 68. Свободно-радикальное присоединениеГидробромированиеПрисоединение HBr против правила Марковникова происходит
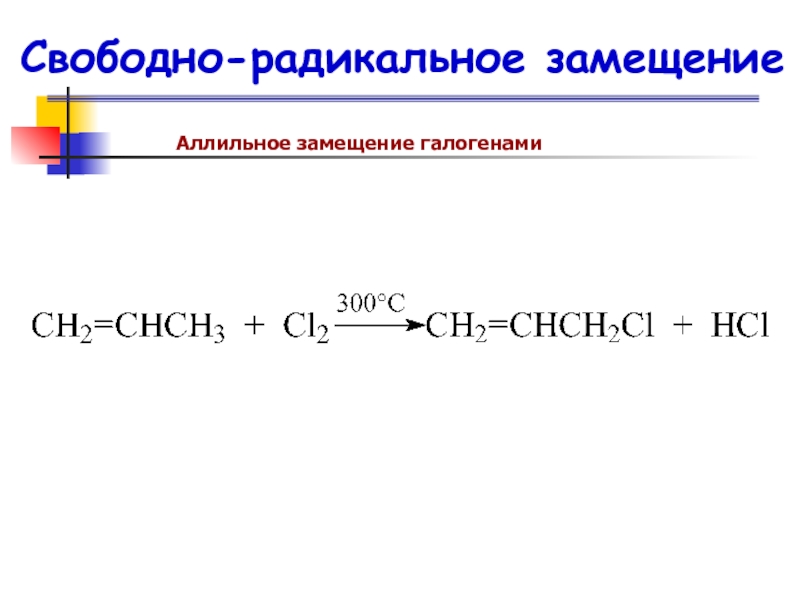
- 69. Свободно-радикальное замещениеАллильное замещение галогенами
- 70. Реакции окисления, полимеризации
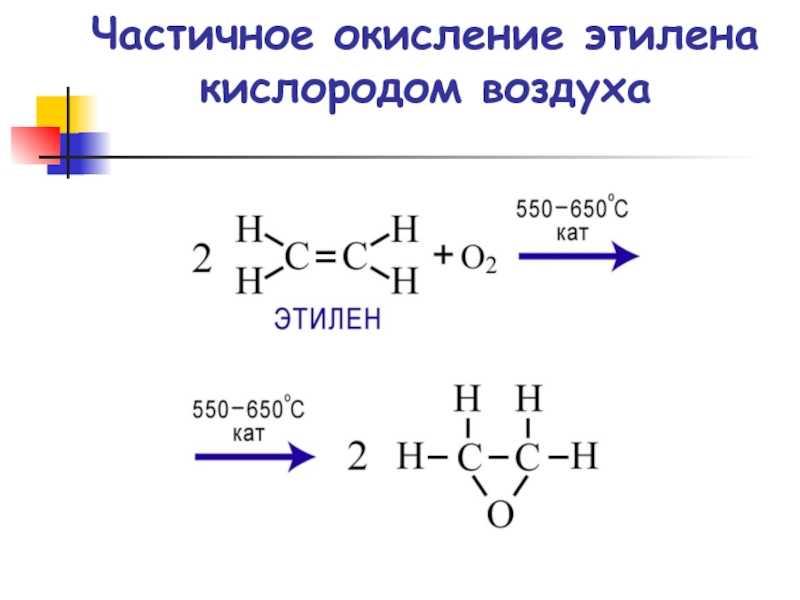
- 71. Частичное окисление этилена кислородом воздуха
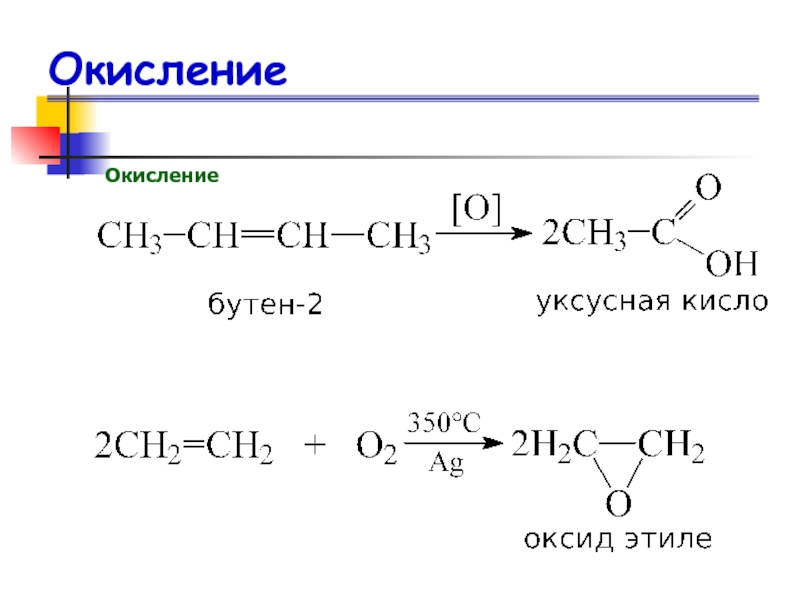
- 72. ОкислениеОкисление
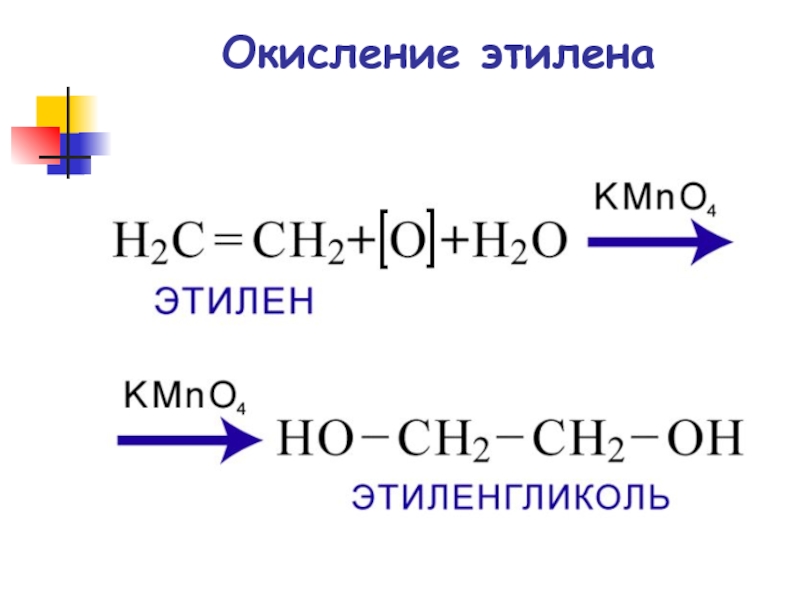
- 73. Окисление этилена
- 74. ОкислениеОкислениеОкисление по ВагнеруВАГНЕР Егор Егорович (9.XII.1849 – 27.XI.1903)
- 75. Слайд 75
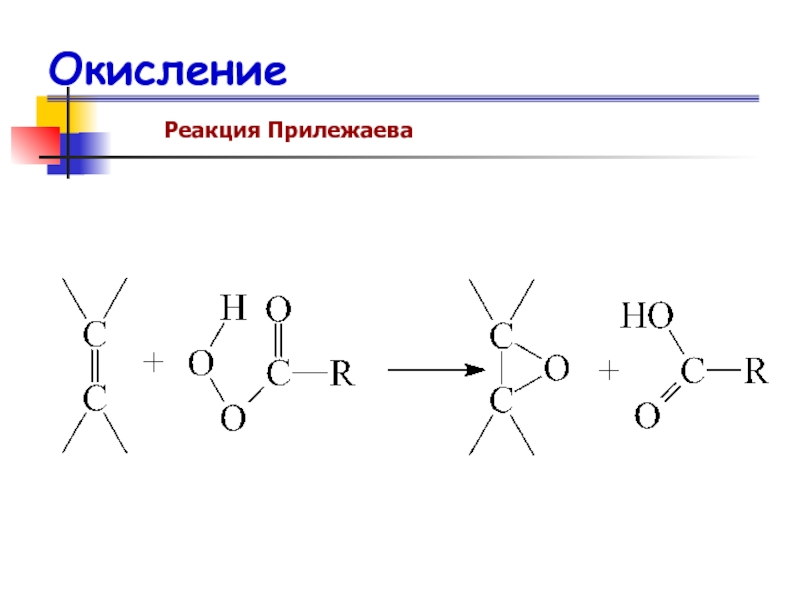
- 76. ОкислениеРеакция Прилежаева
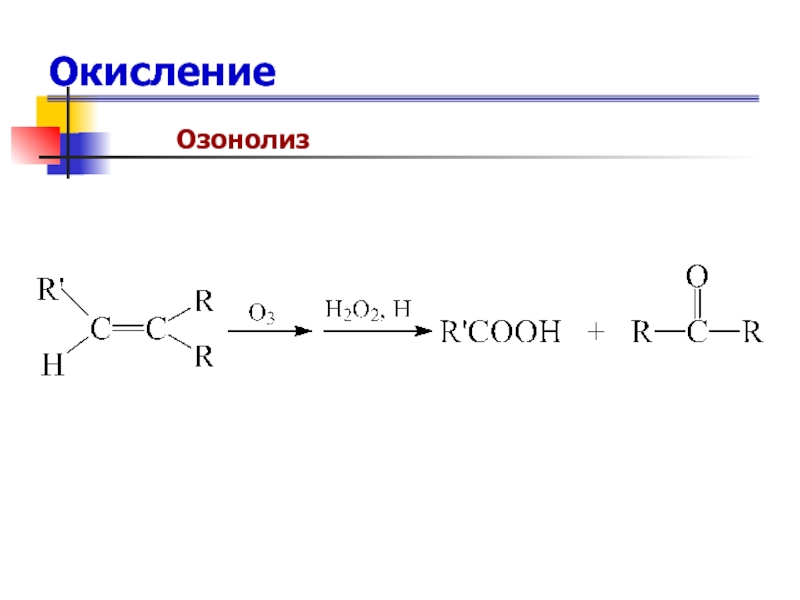
- 77. ОкислениеОзонолиз
- 78. ОкислениеОзонолиз
- 79. Горение этилена
- 80. Слайд 80
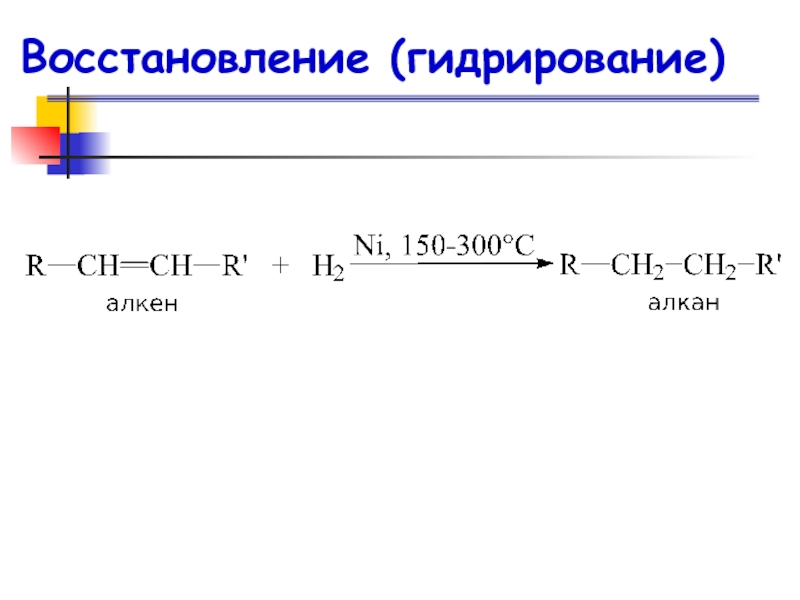
- 81. Восстановление (гидрирование)
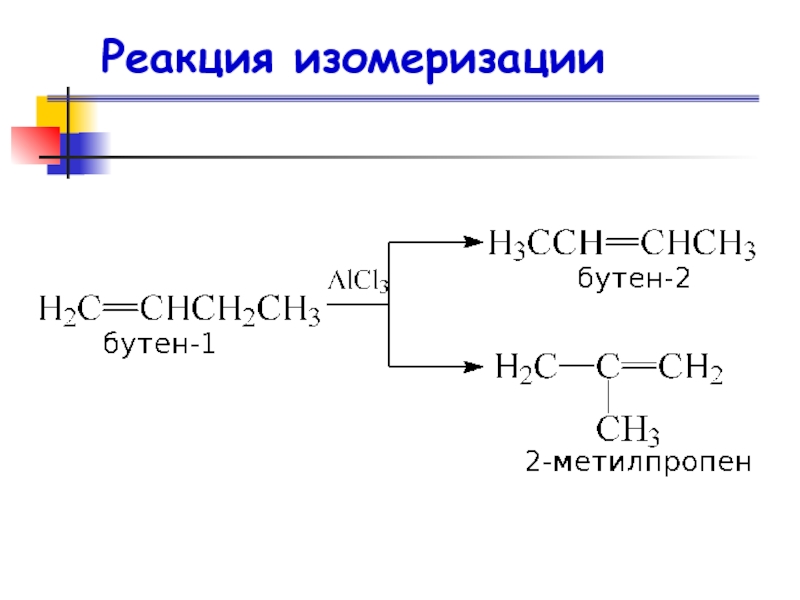
- 82. Реакция изомеризации
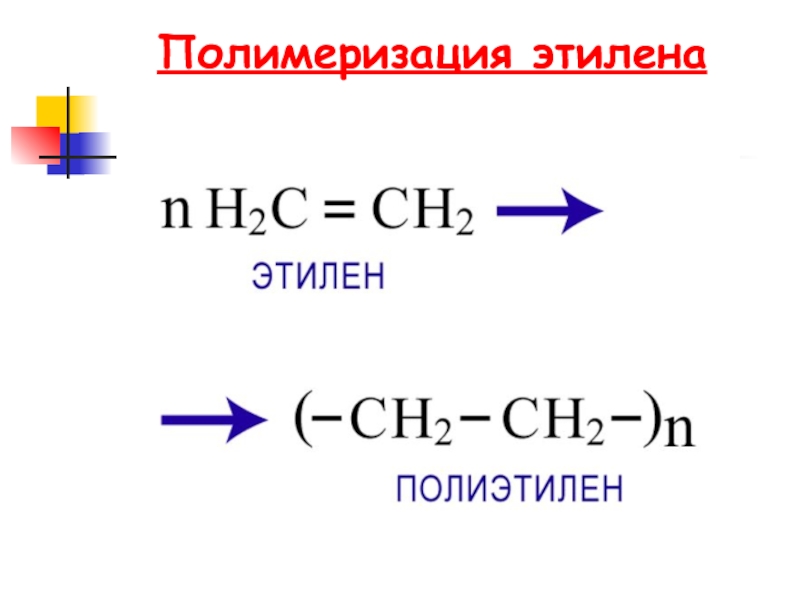
- 83. Полимеризация этилена
- 84. Реакция полимеризацииРеакция полимеризации — это последовательное присоединение
- 85. Реакция полимеризации
- 86. Реакция полимеризацииполиэтиленполипропилен
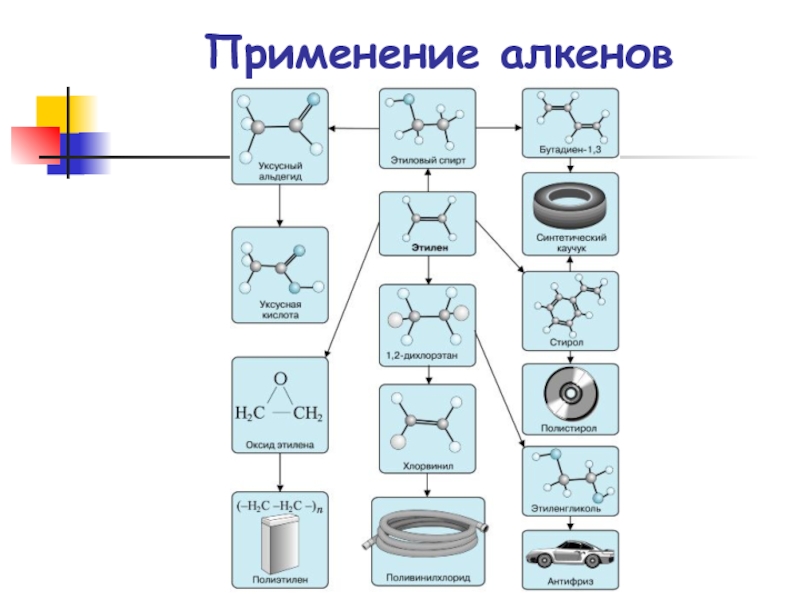
- 87. Применение алкенов
- 88. ЗадачиТест 1Тест 2Тест 3Тест 4Тест 5
- 89. Скачать презентанцию
Слайды и текст этой презентации
Слайд 7Алкены. Номенклатура
1) в алкенах с
неразветвленной цепью нумерацию производят с того конца, ближе к которому
находится двойная связь. В названии алкана, соответствующего этой родоначальной структуре, суффикс -ан заменяется на –ен.этилен
пропилен
гексен-2
Слайд 8Алкены. Номенклатура
2) в случае разветвления главной
считается цепь, включающая двойную связь, даже если эта цепь и
не является самой длинной. Нумерация производится таким образом, чтобы атом углерода, от которого начинается двойная связь, получил наименьший номер2-этилпентен-1
Слайд 9Алкены. Номенклатура
3) Углеводородные заместители обозначаются префиксом.
Положение их указывается цифрой, соответствующей номеру того атома углерода, у
которого находится заместитель. Заместители перечисляются в алфавитном порядке. В случае нескольких одинаковых углеводородных заместителей перед их названием ставится умножительная приставка ди-, три- и т. д.Слайд 17Пространственная изомерия
Пространственная изомерия
цис-бутен-2
Ткип=4С
транс-бутен-2
Ткип=1С
Слайд 21Номенклатура цис-, транс-изомеров
Система Кана–Ингольда–Прелога
Прелог Владимир
(23.07.1906–07.01.1998)
(Швейцария)
Ингольд Кристофер
(28.10.1893–8.10.1970)
(Великобритания)
Роберт Сидни Кан
(9.06.1899-15.09.1981)
(Великобритания)
?
Слайд 22Номенклатура цис-, транс-изомеров
1. Используя систему Кана–Ингольда–Прелога, определяют сначала относительное
старшинство заместителей, связанных с двойной связью, и дают им номера
по старшинству 1 или 2.2. Если две наиболее старшие группы расположены по одну сторону от плоскости -связи, то конфигурация заместителей обозначается символом Z, если же эти группы находятся по разные стороны от плоскости -связи, то конфигурация обозначается символом Е.
Слайд 24Номенклатура цис-, транс-изомеров
(Е)-1-бром-1-нитро-
2-хлорпропен
(Z)-1-бром-1-нитро-
2-хлорпропен
Слайд 33Нахождение в природе
Этилен и его гомологи в очень
небольшом количестве встречаются в природном газе, а также нефти. Олефины,
образуются при крекинге нефти, при сухой перегонке дерева и каменного угля.Слайд 35Алкены
Реакции элиминирования
Элиминирование — это отщепление двух атомов или групп атомов
от соседних атомов углерода с образованием между ними -связи.
Слайд 41Реакции элиминирования
Дегидрогалогенирование
Правило Зайцева
В случае нессиметричных алкилгалогенидов отщепление атома водорода
происходит от наименее гидрогенизированного атома углерода.
Слайд 48Физические свойства алкенов
Алкены обладают более резким запахом. По
ρ легче воды, плохо растворяются в воде. Некоторые алкены
обладают физиологической, биологической активностью.Слайд 51Общая характеристика реакционной способности алкенов
Алкены достаточно
химически активны. Причиной этого является наличие в их молекулах π-связи.
Считается, что π-связь является менее прочной, чем σ-связь по энергии, более поляризуемой и пространственно доступной для атаки различных реагентов. Поэтому наиболее характерными реакциями для алкенов являются реакции присоединения, протекающие за счет разрыва π-связи и образования двух новых σ-связей.Слайд 52Химические свойства
Реакции электрофильного присоединения
АE (от англ. addition electrophilic)
Слайд 64Владимир Васильевич Марковников 1837 – 1904 гг.
Русский химик-органик. Исследования посвящены теоретической органической химии, органическому синтезу и
нефтехимии. Исследования спиртов, карбоновых кислот послужили основой его учения о взаимном влиянии атомов как главном содержании теории химического строения. В 1869 г. сформулировал правило о направлении реакций замещения, отщепления, присоединения по двойной связи и изомеризации в зависимости от химического строения (правило Марковникова).Слайд 68Свободно-радикальное присоединение
Гидробромирование
Присоединение HBr против правила Марковникова происходит следующим образом: Br
(а не Н) реагирует в первую очередь с -системой и
быстрее всего образуется наиболее стабильный радикал.«Перекисный эффект» или эффект Хараша.