Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Непредельные углеводороды: этилен
Содержание
- 1. Непредельные углеводороды: этилен
- 2. Вспомним:Что изучает органическая химия?- Что такое органические вещества?- Какой класс веществ вами изучен?
- 3. «Верно-неверно» о метане:1) молекула содержит 4 атома
- 4. Проверка:Верно: 1, 4, 5, 6, 7;Неверно: 2, 3, 8.
- 5. Мнение психологов: Человек, который успешно изучает химию,
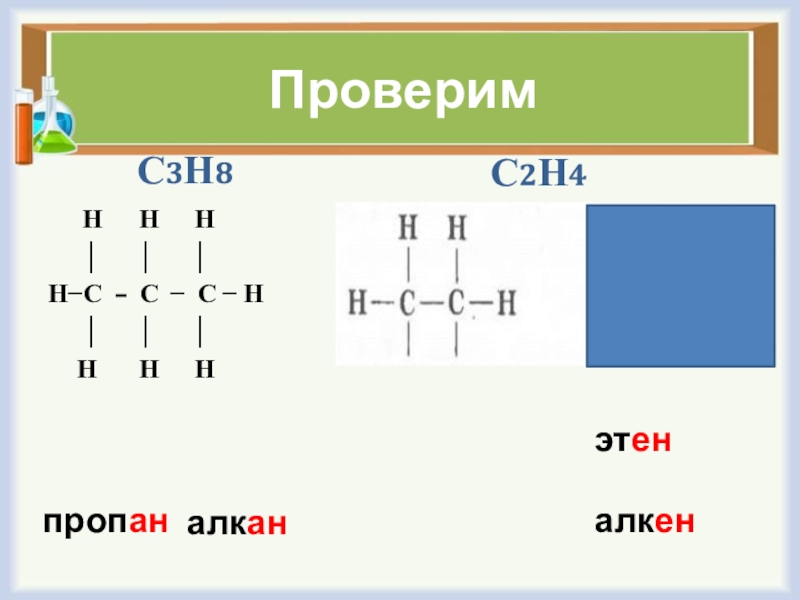
- 6. Задание:Составить развернутые структурные формула следующих веществ: С3Н8 и С2Н4.
- 7. Проверим С3Н8
- 8. История открытия этилена1669 г. немецкий ученый Иоганн
- 9. История открытия этилена1795 г. голландский химик И.
- 10. Непредельные углеводороды олефины (маслородный)Алкены
- 11. 1860 г. А. М. Бутлеровустановил, что в
- 12. Слайд 12
- 13. Гомологический рядэтилен (международное название — этен)
- 14. Сделайте вывод: Как отличается состав этиленового углеводорода от состава предельного с тем же числом углеродных атомов?
- 15. Алкан → алкен + Н2(дегидрирование)
- 16. Физические свойства По
- 17. Химические свойства Для алкенов
- 18. 2) Гидрирование. Легко присоединяют водород в
- 19. 4)Реакция полимеризации. Реакцией полимеризации называется
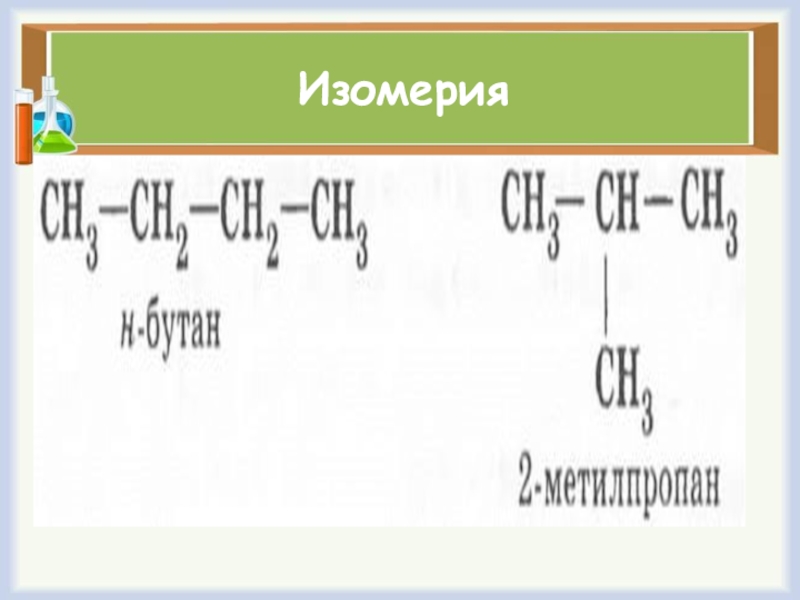
- 20. ИзомерияВспомните определение явления изомерии и поясните его на примере бутана.
- 21. Изомерия алкенаКакие виды изомерии определили?
- 22. Закрепление1.Выпишите отдельно формулы предельных и этиленовых углеводородов и назовите вещества: С5Н10; С2Н2;СН4;С2Н6; С3Н4;C4H10;С2Н2; C6H6
- 23. Непредельный углеводородПредположите,в какие реакции будут вступать непредельные углеводороды.
- 24. Применение этиленаВ 1938 г. в России (тогда
- 25. Слайд 25
- 26. Домашнее заданиеПараграф 34
- 27. Скачать презентанцию
Вспомним:Что изучает органическая химия?- Что такое органические вещества?- Какой класс веществ вами изучен?
Слайды и текст этой презентации
Слайд 2Вспомним:
Что изучает органическая химия?
- Что такое органические вещества?
- Какой класс
веществ вами изучен?
Слайд 3«Верно-неверно» о метане:
1) молекула содержит 4 атома водорода
2) является непредельным
углеводородом
3) атом углерода в молекуле соединён с атомами водорода двойной
связью4) вступает в реакцию замещения с хлором
5) не вступает в реакции присоединения с бромоводородом
6) нерастворим в воде
7) при сгорании выделяется большое количество теплоты
8) реагирует с водородом
Слайд 5Мнение психологов:
Человек, который успешно изучает химию, обладает логическим мышлением,
но тот, кто разобрался в органической химии – обладает колоссальной
логикой…Слайд 8История открытия этилена
1669 г.
немецкий ученый Иоганн Иохим Бехер
Нагревая этиловый
спирт с серной кислотой, получил неизвестный ранее газ, названный «газ
Бехера»Слайд 9История открытия этилена
1795 г.
голландский химик И. Дейман
установил, что «газ
Бехера»
состоит из
углерода и водорода,
при взаимодействии
с хлором превращается в маслянистую жидкость (1,2-дихлорэтан)Слайд 111860 г.
А. М. Бутлеров
установил, что в этилене на
два атома углерода приходится четыре атома водорода.
Слайд 13Гомологический ряд
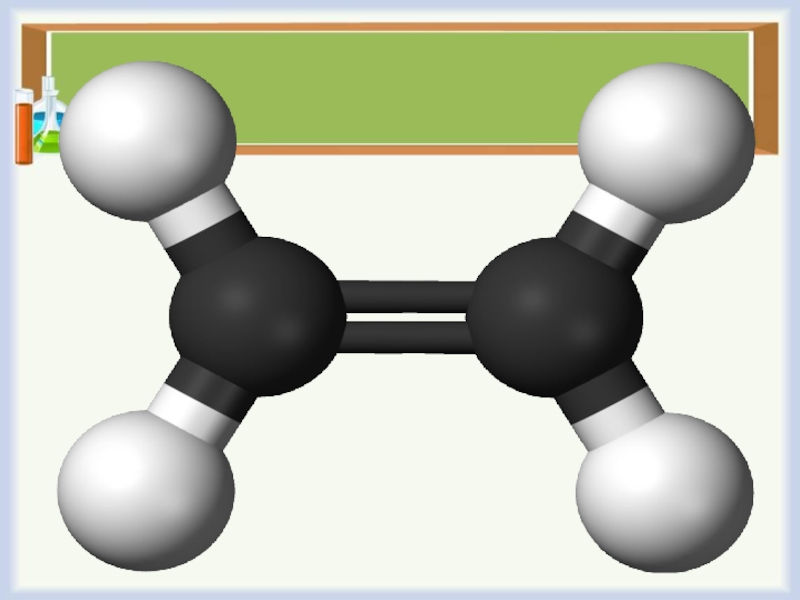
этилен (международное название — этен)
СН2=СН2
пропилен ( международное название – пропен) СН2=СН СН3
Запишите 2 последующих у/ в .
( С4, С5). Назовите их.
4. Составьте общую формулу класса алкенов.
CnH2n
Слайд 14Сделайте вывод:
Как отличается состав этиленового углеводорода от состава предельного
с тем же числом углеродных атомов?
Слайд 16Физические свойства
По физическим свойствам этиленовые углеводороды
близки к алканам. При нормальных условиях углеводороды C2–C4 – газы,
C5–C15 – жидкости, высшие представители – твердые вещества. Температура их плавления и кипения, а также плотность увеличиваются с ростом молекулярной массы. Все они легче воды, плохо растворимы в ней, однако растворимы в органических растворителях.Слайд 17Химические свойства
Для алкенов наиболее типичными являются
реакции присоединения.
1) обесцвечивание бромной воды.
H2C=CH2 + Br2 → BrCH2–CH2BrПриведенная реакция - обесцвечивание алкеном бромной воды является качественной реакцией на двойную связь.
Слайд 18 2) Гидрирование. Легко присоединяют водород в присутствии катализаторов (Pt,
Pd, Ni) образуя предельные углеводороды.
CH3–CH=CH2 +
H2 ––Ni→ CH3–CH2–CH33) Горение.
При сжигании в кислороде алкены дают
углекислый газ и воду.
H2C=CH2 + 3O2 → 2CO2 + 2H2O
Слайд 194)Реакция полимеризации.
Реакцией полимеризации называется процеcc соединения нескольких
молекул низкомолекулярного вещества с образованием высокомолекулярного соединения (полимера) .
Полимеризация
алкенов происходит при нагревании, при повышенном давлении, при участии катализаторовnH2C=CH2 →(- H2C-CH2 - )n
этилен полиэтилен