Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОБМІН РЕЧОВИН ТА ЕНЕРГІЇ (МЕТАБОЛІЗМ)
Содержание
- 1. ОБМІН РЕЧОВИН ТА ЕНЕРГІЇ (МЕТАБОЛІЗМ)
- 2. Обмін речовин (метаболізм) – сукупність всіх хімічних
- 3. Хімічні речовини, що беруть участь в обміні
- 4. Метаболізм забезпечує: 1. Розвиток 2. Життєдіяльність 3.
- 5. Метаболізм складається з анаболізму (процеси синтезу) і катаболізму (процеси розпаду речовин)
- 6. Слайд 6
- 7. Основа обміну речовинАсиміляція (анаболізм):хімічні перетворення, що приводять
- 8. Ці процеси взаємопов'язані і направлені на безперервне
- 9. Живі клітини постійно потребують органічні і неорганічні
- 10. Із багаточисельних метаболітів виділяють 3 найбільш важливих
- 11. Слайд 11
- 12. Ні вуглеводи, ні жири, ні білки не
- 13. Макроергічні сполуки- це сполуки, що містять макроергічні
- 14. Центральне місце серед макроергічних сполук займає АТФ
- 15. Структура АТФ
- 16. Аденозинтрифосфорна кислота (АТФ)
- 17. АТФ – універсальна «енергетична валюта» всіх живих
- 18. В клітині молекула АТФ використовується протягом 1
- 19. Біологічне окиснення може відбуватися кількома шляхами:-
- 20. Біологічне окиснення Це сукупність окисно-відновних процесів у
- 21. Функції біологічного окиснення:Енергетичне забезпечення процесів життєдіяльності: підтримання
- 22. Окиснення органічних речовин Оксигеном до СО2 і Н2О називається тканинним диханням або біологічним окисненням.
- 23. Тканинне дихання відбувається за участі ланцюгу перенесення
- 24. Слайд 24
- 25. Слайд 25
- 26. Уперше мітохондрії (МХ) були виявлені у вигляді
- 27. Дихальний ланцюгСукупність ферментів, що здійснюють транспорт електронів
- 28. В ЛПЕ приймають участь 4 групи ферментів
- 29. Слайд 29
- 30. Слайд 30
- 31. Слайд 31
- 32. Слайд 32
- 33. Піридинзалежні дегідрогенази (двохкомпонентні)Специфічний білок (апофермент) + кофермент
- 34. NAD - залежна дегідрогеназа каталізує реакції окиснення
- 35. Слайд 35
- 36. Флавінзалежні дегідрогенази (двохкомпонентні)Специфічний білок (апофермент) + кофермент
- 37. Слайд 37
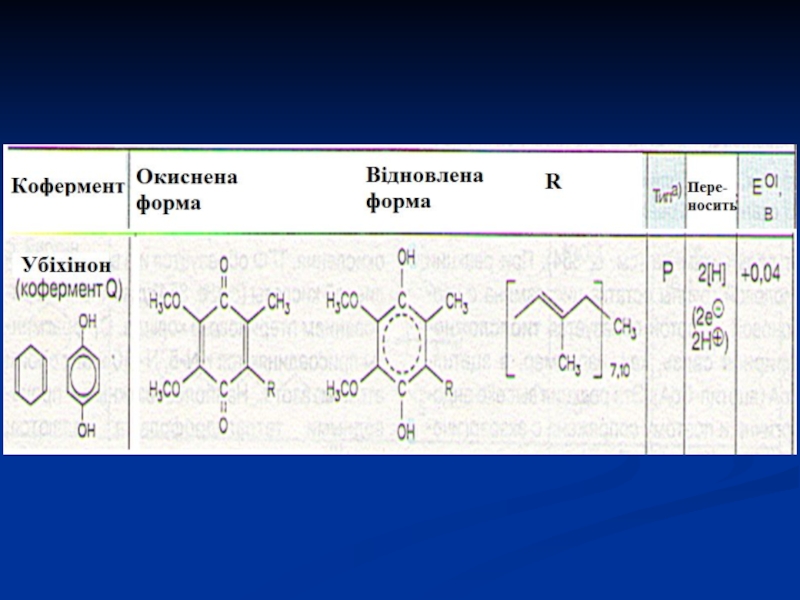
- 38. УБІХІНОН або коензим Q – проміжний переносник
- 39. Слайд 39
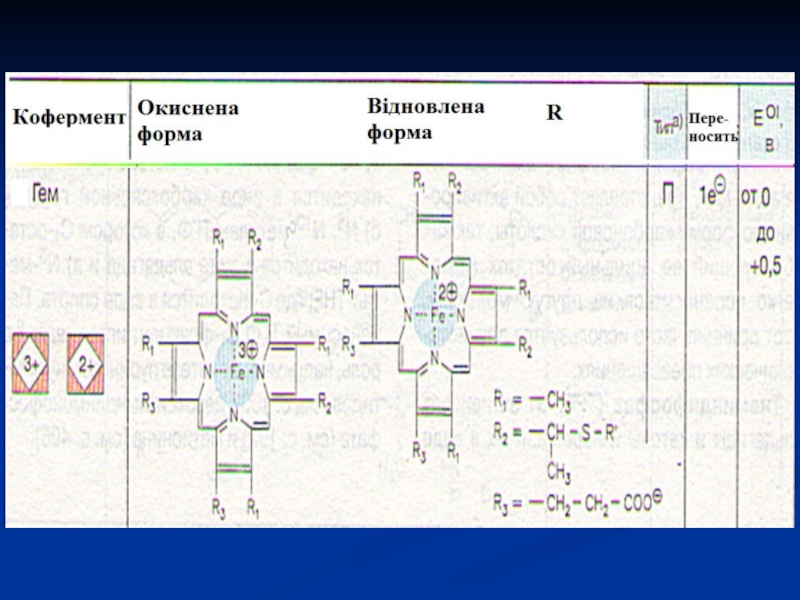
- 40. Цитохроми Відносяться до гемвмісних хромопротеїнів. Їх простетичною
- 41. Слайд 41
- 42. В природі існують сімейства цитохромів (в, с,
- 43. Редокс-потенціалНапрямок потоку електронів при спряженні однієї окисної
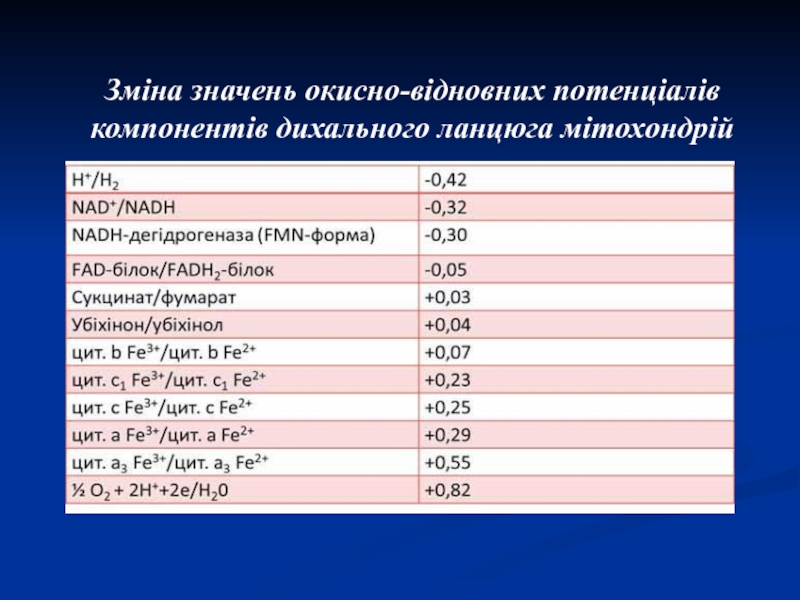
- 44. Зміна значень окисно-відновних потенціалів компонентів дихального ланцюга мітохондрій
- 45. Ендогенна водаУбіхінон передає на систему цитохромів тільки
- 46. Інгібітори дихального ланцюгу Речовини, що блокують
- 47. Окисне фосфорилуванняСинтез АТФ з АДФ відбувається в
- 48. Слайд 48
- 49. створюється протонний градієнт, при якому концентрація протонів
- 50. В дихальному ланцюгу можна виділити
- 51. Енергія електрохімічного потенціалу використовується для синтезу АТФ,
- 52. АТФ-синтазаСкладається з 2-х білкових комплексів. Гідрофобний комплекс
- 53. Для синтезу 1 моля АТФ з АДФ
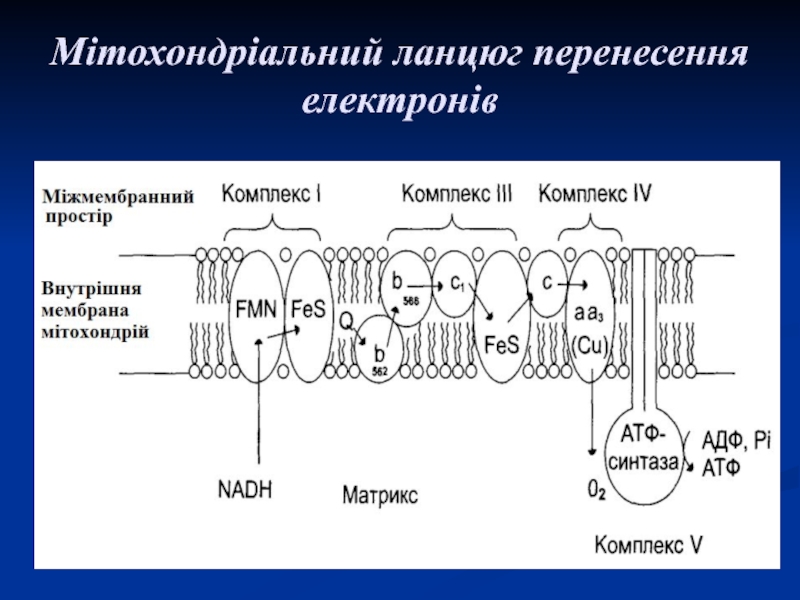
- 54. Мітохондріальний ланцюг перенесення електронів
- 55. В НАД-залежних реакціях при окисненні 1 моля
- 56. Роз'єднання дихання і фосфорилуванняДеякі хімічні речовини (протонофори)
- 57. В результаті роз'єднання кількість АТФ зменшується, а
- 58. МІКРОСОМАЛЬНЕ ОКИСНЕННЯЦе ще один тип біологічного окиснення,
- 59. До ферментів
- 60. ФУНКЦІЇ МІКРОСОМАЛЬНОГО ОКИСНЕННЯ: Окиснення речовин циклічної структури,
- 61. Утворення пероксиду водню. При тканинному диханні можливе
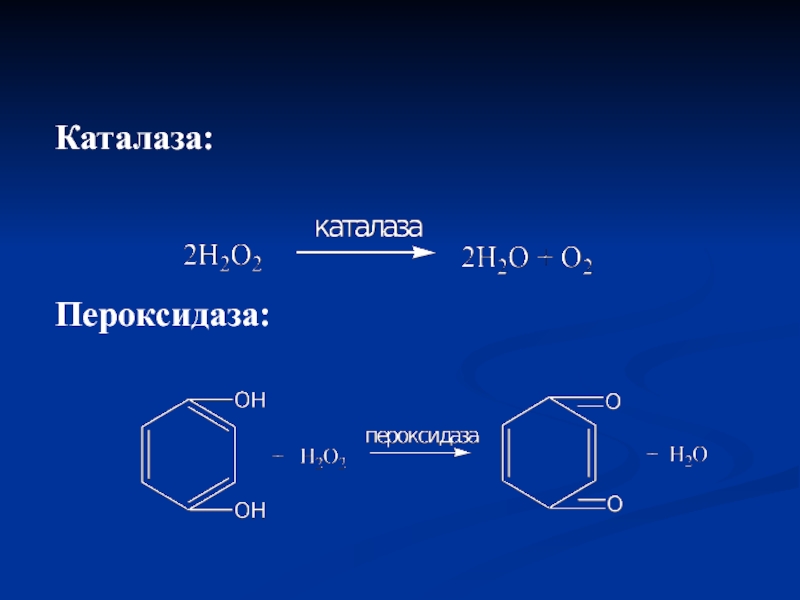
- 62. Каталаза:Пероксидаза:
- 63. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Обмін речовин (метаболізм) – сукупність всіх хімічних реакцій і всіх
видів перетворень речовин та енергії в організмі.
Слайд 3Хімічні речовини, що беруть участь в обміні речовин називаються метаболітами.
Поза клітиною майже всі ці перетворення проходили б дуже повільно
і не направлено.Впорядковані послідовності хімічних реакцій, що проходять з високою продуктивністю, так звані метаболічні шляхи, можливі тільки завдяки присутності в клітині специфічних ферментів.
Слайд 4Метаболізм забезпечує: 1. Розвиток 2. Життєдіяльність 3. Самовідтворення організмів 4. Зв'язок з оточуючим середовищем 5.
Адаптацію до змін зовнішніх умов
Слайд 5Метаболізм складається з анаболізму (процеси синтезу) і катаболізму (процеси розпаду
речовин)
Слайд 7Основа обміну речовин
Асиміляція (анаболізм):
хімічні перетворення, що приводять до використання органічних
речовин, які надходять із зовнішнього середовища для синтезу специфічних білків,
НК, ліпідів, полісахаридів та ін.Супроводжуються поглинанням енергії (ендергонічні)
Дисиміляція (катаболізм):
процеси розпаду органічних речовин до кінцевих продуктів – води, СО2, амоніаку, сечовини, сечової кислоти.
Супроводжуються
виділенням енергії (екзергонічні)
Слайд 8Ці процеси взаємопов'язані і направлені на безперервне поновлення живого матеріалу
і забезпечення його необхідною енергією.
Організм тварин і людини – відкрита
система, яка потребує притоку енергії ззовні.Слайд 9Живі клітини постійно потребують органічні і неорганічні речовини, а також
хімічну енергію, яку вони отримують переважно з АТФ (АТР).
Всі
організми ділять на автотрофні та гетеротрофні. Автотрофні організми, до яких належать рослини і більшість мікроорганізмів, можуть синтезувати органічні молекули з неорганічних попередників (CO2), наприклад, за рахунок фотосинтезу.
Гетеротрофи, наприклад тварини та гриби, залежать від одержання органічних речовин з їжею.
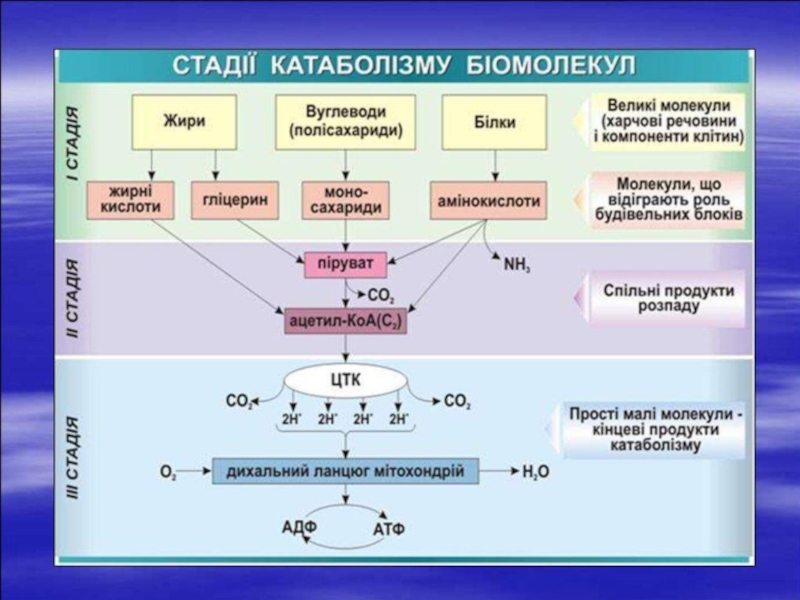
Слайд 10Із багаточисельних метаболітів виділяють 3 найбільш важливих – піруват (ПВК),
ацетил-КоА і гліцерин.
Вони є ланкою, що зв'язує між собою
метаболізм білків, вуглеводів та ліпідів.Кінцевими продуктами розпаду органічних речовин у тварин є диоксид Карбону (CO2), вода (H2O) та амоніак (NH3). Амоніак перетворюється в сечовину і в такій формі виводиться з організму.
Слайд 12
Ні вуглеводи, ні жири, ні білки не можуть безпосередньо бути
«паливом» для клітинних процесів.
Клітини тварин можуть використовувати тільки енергію розриву
хімічних зв'язків!Вона може передаватися з однієї частини клітини в іншу і використовуватися економно.
Слайд 13Макроергічні сполуки
- це сполуки, що містять макроергічні (багаті на енергію)
фосфатні зв'язки.
В результаті їх гідролізу виділяється більше 5 ккал/моль
енергії.Знаком ~ (тильда) позначають макроергічний зв'язок.
До макроергів відносять: АТФ, УТФ, ЦТФ, ГТФ, ТТФ,
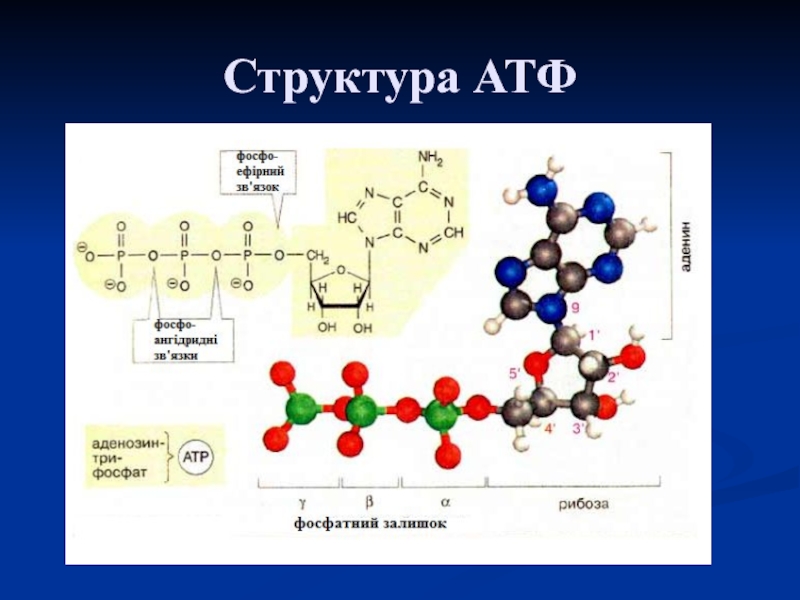
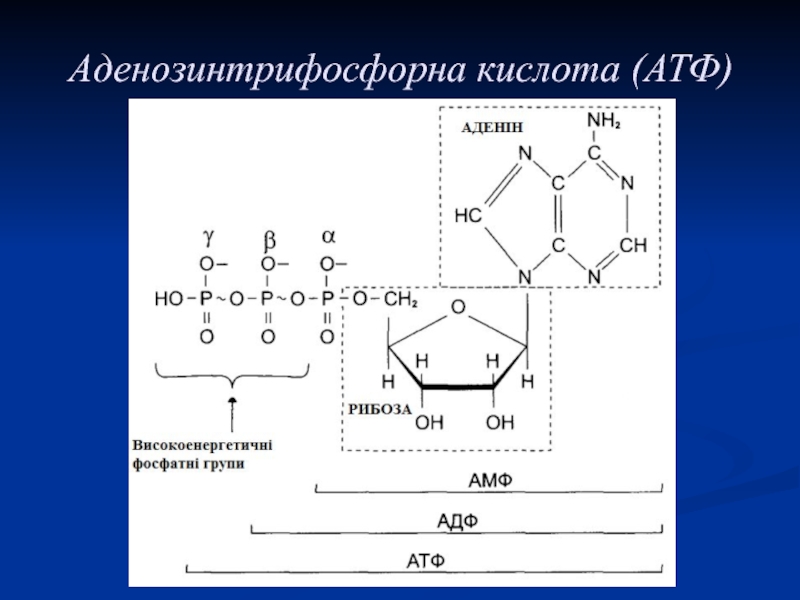
Слайд 14Центральне місце серед макроергічних сполук займає АТФ – молекула, багата
енергією, оскільки вона містить 2 фосфоефірних зв'язки.
В результаті
гідролізу АТФ перетворюється в АДФ і ортофосфат (Р). При цьому виділяється 7,3 ккал/моль вільної енергії.
Слайд 17АТФ – універсальна «енергетична валюта» всіх живих організмів.
АТФ мобільна,
потрапляє в любу частину клітини, де вона може підлягати гідролізу
з виділенням вільної енергії.В залежності від глибини гідролізу АТФ в якості кінцевого продукту може утворитися АДФ або АМФ.
Слайд 18В клітині молекула АТФ використовується протягом 1 хвилини після її
утворення.
У людини кількість АТФ, рівне за величиною масі його
тіла, використовується протягом 24 годин.Клітина повинна мати надійний механізм поповнення АТФ і продукції тепла.
Синтез АТФ у клітині може здійснюватися двома шляхами:
Субстратне фосфорилування, під час якого відбувається безпосередня передача молекули активного фосфату на АДФ від більш енерговмісних сполук.
Окисне фосфорилування, яке відбувається в мітохондріях і спряжене з тканинним диханням.
Слайд 19Біологічне окиснення
може відбуватися кількома шляхами:
- відщеплення від субстратів атомів
Гідрогену і електронів (дегідрування):
на внутрішній мембрані мітохондрій;
Енергія: АТФ
+ тепло; Ф-ція: забезпечення процесів біоокиснення.
- приєднання до субстрату Оксигену (оксигенація):
в мікросомах;
тепло;
знезараження чужорідних сполук, токсинів. Синтез органічних речовин.
Слайд 20Біологічне окиснення
Це сукупність окисно-відновних процесів у біологічних об'єктах, які відбуваються
в клітинах організму в період внутрішньоклітинного обміну та мають важливу
роль в забезпеченні організму енергією і метаболітами.Слайд 21Функції біологічного окиснення:
Енергетичне забезпечення процесів життєдіяльності: підтримання температури тіла, хімічні
синтези, електричні процеси, механічна робота.
Усунення кінцевих і шкідливих продуктів обміну
речовин.Знезараження чужорідних сполук.
Синтез ключових метаболітів.
Регуляція обміну речовин шляхом змінення співвідношення окиснених і відновлених форм коферментів (НАД ⁄ НАД·Н).
Слайд 22Окиснення органічних речовин Оксигеном до СО2 і Н2О називається тканинним
диханням або біологічним окисненням.
Слайд 23Тканинне дихання відбувається за участі
ланцюгу перенесення електронів (ЛПЕ)
або дихального ланцюгу,
який утворений окисно-відновними ферментами, локалізованими в ліпідному
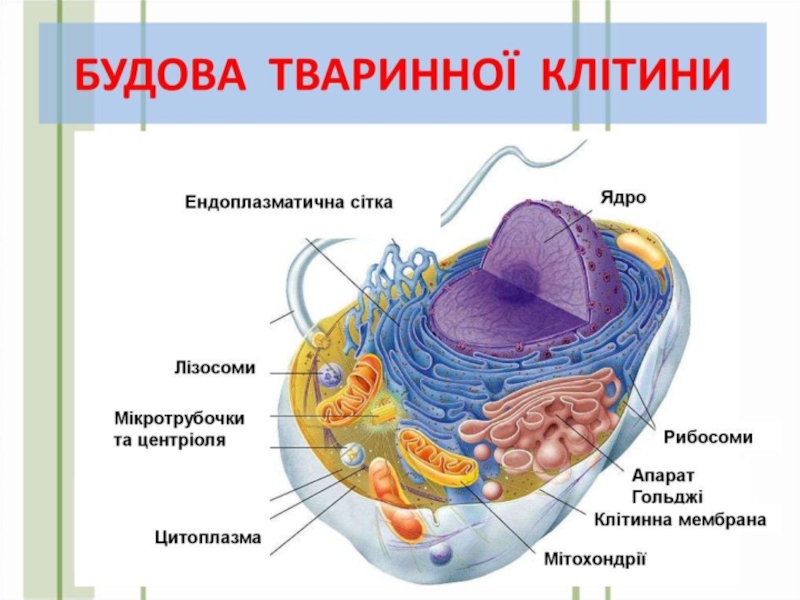
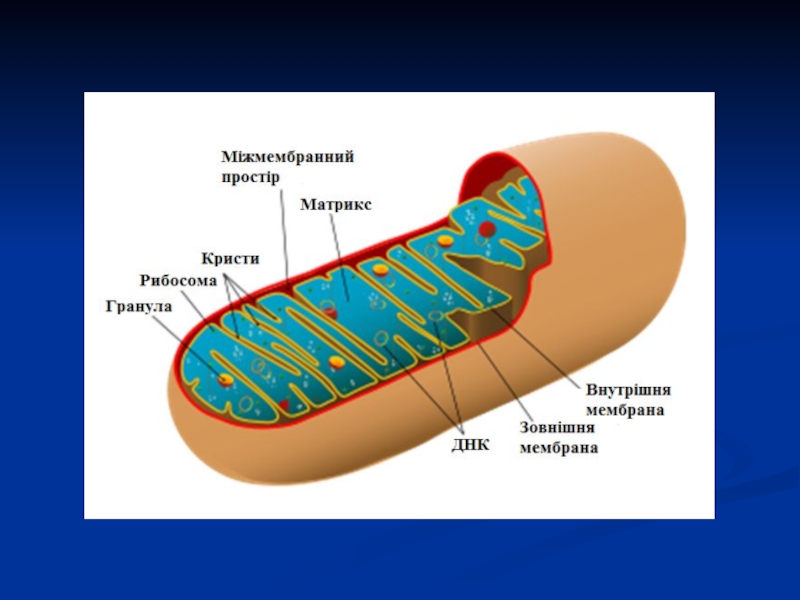
шарі внутрішньої мембрани мітохондрій.Слайд 26 Уперше мітохондрії (МХ) були виявлені у вигляді гранул у м'язових
клітинах (1850 р.). Кількість МХ у клітинах мінлива. Їх особливо
багато у клітинах з великою потребою у кисні. Залежно від того, в яких ділянках клітини відбувається споживання енергії, МХ здатні переміщуватись туди по цитоплазмі.МХ мають дві замкнені, ізольовані мембрани: внутрішню та зовнішню, які розділені водним міжмембранним простором.
Простір між крістами внутрішньої мембрани МХ заповнений напіврідкою гелеподібною масою – матриксом, що складається на 50% з білка. Матрикс містить ферменти: циклу Кребса, β-окиснення жирних кислот (основні постачальники субстратів окиснення), окиснення амінокислот та піруватдегідрогеназний комплекс ферментів.
На відміну від інших внутрішньоклітинних органоїдів МХ мають свій геном, тому в матриксі також знаходяться ферменти автономного мітохондріального синтезу ДНК, РНК, білків тощо.
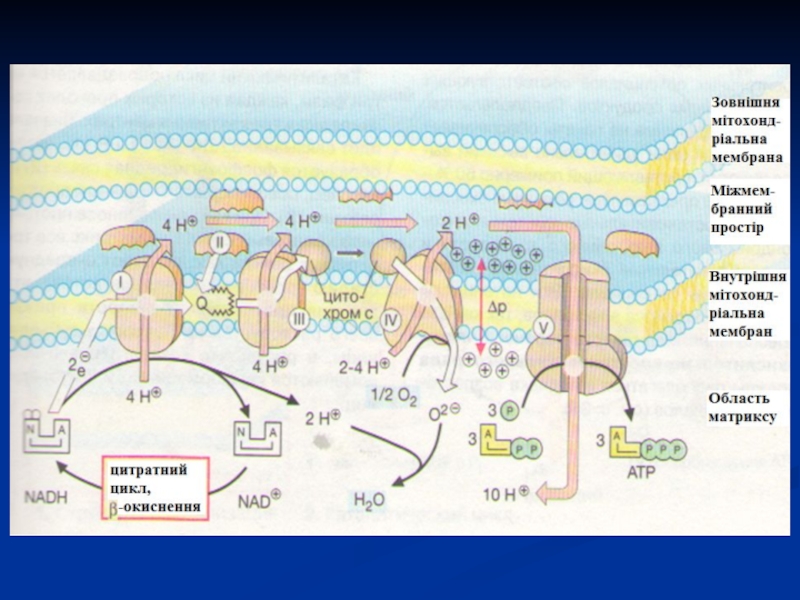
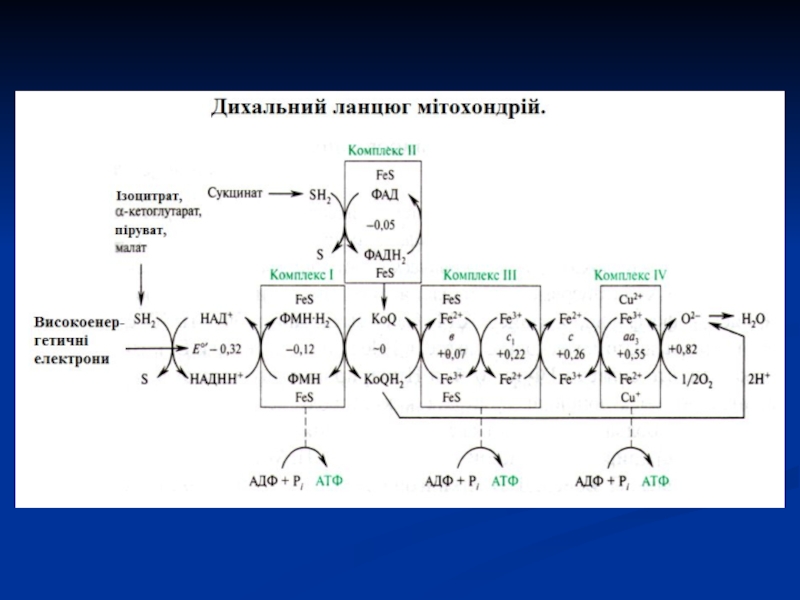
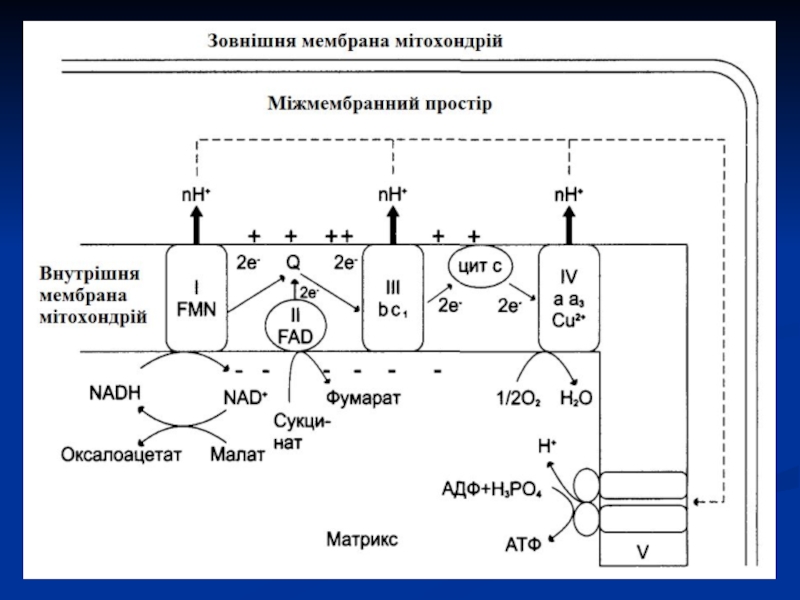
Слайд 27Дихальний ланцюг
Сукупність ферментів, що здійснюють транспорт електронів від речовини, що
окиснюється, на О2 називається дихальним ланцюгом або ланцюгом перенесення електронів
(ЛПЕ).Перенесення електронів в дихальному ланцюгу забезпечується різницею потенціалів між окремими ланками цього ланцюгу.
Послідовний рух електронів в дихальному ланцюгу супроводжується ступінчатим вивільненням хімічної енергії, яка акумулюється в макроергічних зв'язках АТФ.
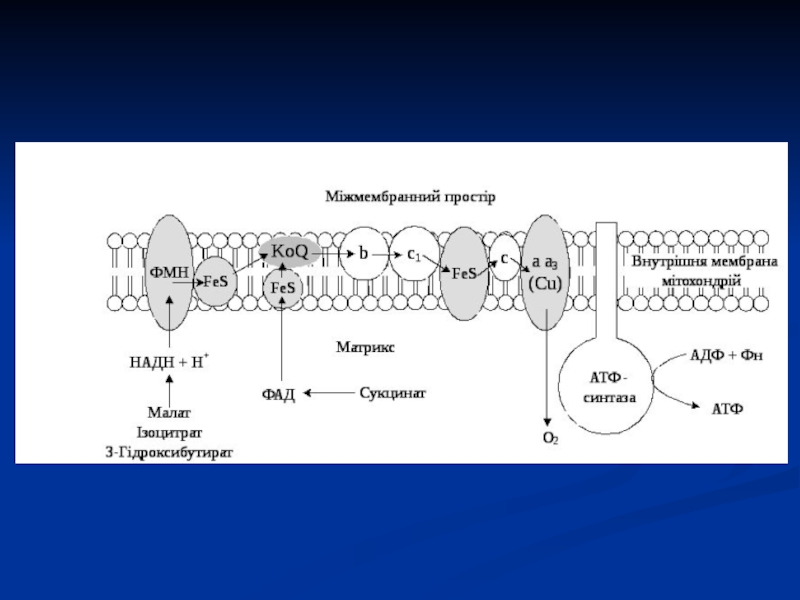
Слайд 28В ЛПЕ приймають участь
4 групи ферментів класу оксидоредуктаз:
піридинзалежні дегідрогенази,
флавінзалежні дегідрогенази,
убіхінон або коензим Q;
цитохромні системи (в, с,
а), представлені комплексом гемінових ферментів і цитохромоксидаза (а3).Всі 4 групи коферментів сприяють перенесенню протонів і електронів від органічних речовин, що окиснюються, на Оксиген.
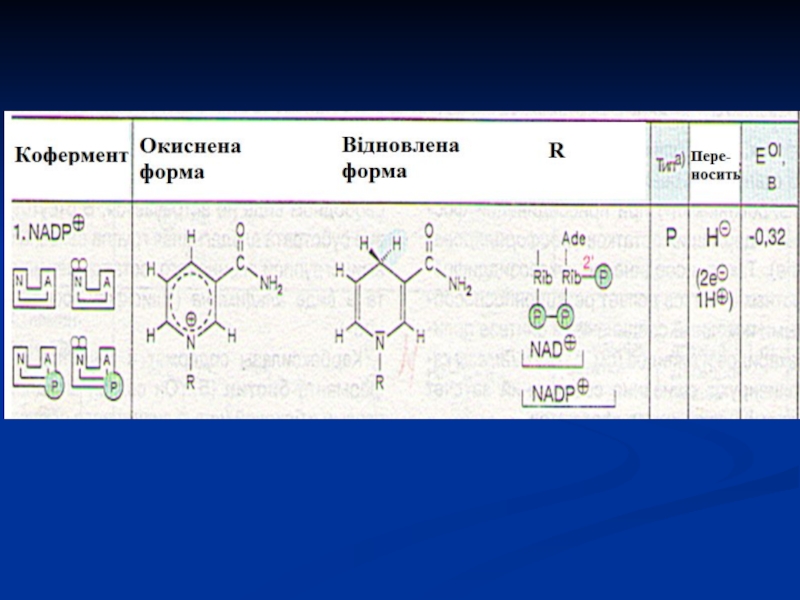
Слайд 33Піридинзалежні дегідрогенази (двохкомпонентні)
Специфічний білок (апофермент) + кофермент НАД або НАДФ.
Є універсальними акцепторами Гідрогену для багатьох субстратів (спиртів, альдегідів і
т.д.).Відбираючи від субстрату атоми Гідрогену, вони відновлюються, а субстрати окиснюються.
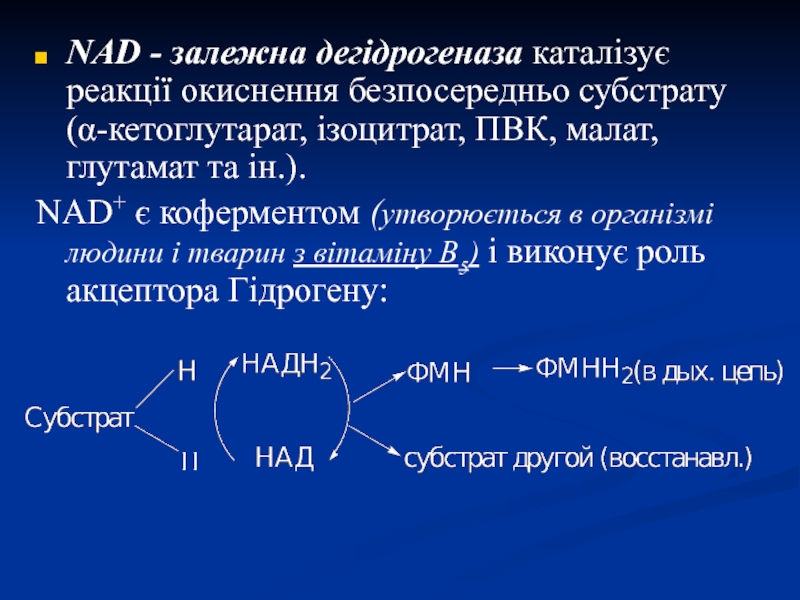
Слайд 34NAD - залежна дегідрогеназа каталізує реакції окиснення безпосередньо субстрату (α-кетоглутарат,
ізоцитрат, ПВК, малат, глутамат та ін.).
NAD+ є коферментом (утворюється
в організмі людини і тварин з вітаміну В5) і виконує роль акцептора Гідрогену: Слайд 36Флавінзалежні дегідрогенази (двохкомпонентні)
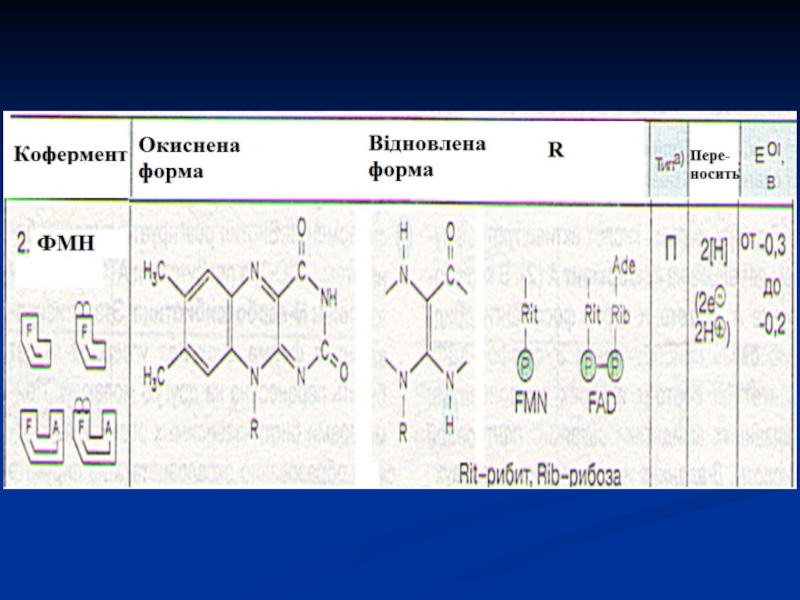
Специфічний білок (апофермент) + кофермент ФМН або ФАД.
Флавінові
коферменти щільно зв'язані з апоферментами (на відміну від піридинзалежних дегідрогеназ).
Ці
коферменти утворюються в організмі людини з вітаміну В2.Окиснюють відновлені субстрати (сукцинат, ацил-КоА, α-гліцерофосфат).
Слайд 38УБІХІНОН або коензим Q – проміжний переносник атомів Гідрогену, тобто
електронів і протонів в мітохондріальній мембрані, окиснює відновлену форму флавінових
ферментів.Слайд 40Цитохроми
Відносяться до гемвмісних хромопротеїнів. Їх простетичною групою є гем,
у якого атом заліза має здатність легко приєднувати (відновлюватися) і
віддавати (окиснюватися) електрони.Слайд 42В природі існують сімейства цитохромів (в, с, а), які відрізняються
між собою величиною електричного потенціалу, який збільшується в напрямку в
→ с → аа3. В такому порядку електрони в ланцюгу цитохромів послідовно передаються від в до а3.Цитохроми називають проміжними переносниками електронів
(між дегідрогеназами і О2).
Слайд 43Редокс-потенціал
Напрямок потоку електронів при спряженні однієї окисної системи з іншою
визначається їх стандартними окисно-відновними потенціалами або редокс-потенціалами (Е0).
Слайд 45Ендогенна вода
Убіхінон передає на систему цитохромів тільки електрони, а протони
(Н+) надходять в середовище, де взаємодіють з відновленим О2, утворюється
вода, що називається ендогенною:2Н+ + 1⁄2О2 → Н2О.
Утворюється в результаті окиснення вуглеводів, білків та ліпідів (100г ліпідів при окисненні дають організму 107 г води).
Верблюд в пустелі використовує жирові відкладення в горбах для одержання ендогенної води.
Слайд 46Інгібітори дихального ланцюгу
Речовини, що блокують певні етапи цього
процесу.
Для НАД-залежної дегідрогенази:
- ротенон – високотоксична
сполука, що міститься в деяких водоростях та є отрутою для риб; - амітал – лікарський препарат з групи барбітуратів.
Для убіхінону – антиміцин А, токсичний антибіотик.
Для цитохромоксидази – ціанід, СО, Н2S. Ціанід є найбільш токсичним для людини, він приєднується до Fe3+ цитохромоксидази і блокує перенесення електронів до кисню.
Слайд 47Окисне фосфорилування
Синтез АТФ з АДФ відбувається в результаті окисного фосфорилування,
яке сполучене з процесом біологічного окиснення (тканинного дихання).
Цей процес
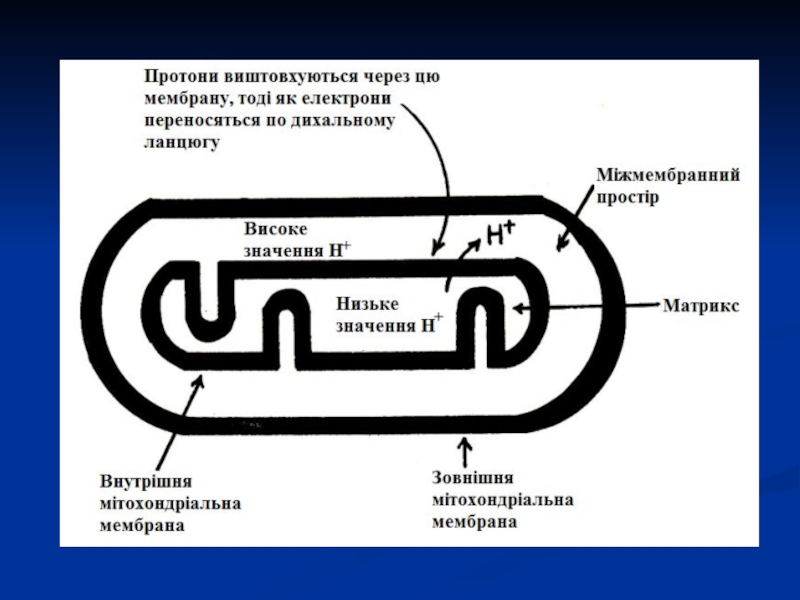
був відкритий Енгельгардтом.Слайд 49створюється протонний градієнт, при якому концентрація протонів у міжмембранному просторі
більше, а рН менше, ніж у матриксі.
з'являється різниця потенціалів
по обидві сторони мембрани: негативний заряд на внутрішній стороні і позитивний – на зовнішній. Разом вони утворюють електрохімічний потенціал - джерело енергії для синтезу АТФ. Слайд 50В дихальному ланцюгу можна виділити
3 ділянки, в яких перенесення електронів
супроводжується зниженням вільної енергії.Ці ділянки називають пунктами сполучення дихання і фосфорилування.
Кількість енергії, що тут виділяється, приблизно така, яка є необхідною для синтезу АТФ з АДФ і фосфату:
АДФ + Н3РО4 ↔ АТФ
Слайд 51Енергія електрохімічного потенціалу використовується для синтезу АТФ, якщо протони повертаються
в матрикс через іонні канали АТФ-синтази.
АТФ-синтаза (Н-АТФаза) – інтегральний білок
внутрішньої мембрани мітохондрій. Він розташований безпосередньо поблизу дихального ланцюга. Підвищення концентрації протонів у міжмембранному просторі активує АТФ-азу.
Слайд 52АТФ-синтаза
Складається з 2-х білкових комплексів.
Гідрофобний комплекс занурений в мембрану.
Він є основою, яка фіксує АТФ-азу в мембрані. Складається з
декількох субодиниць, що утворюють канал, по якому протони переносяться в матрикс.Другий комплекс виступає в мітохондріальний матрикс. Він складається з 9 субодиниць, в яких і відбувається синтез АТФ.
Слайд 53Для синтезу 1 моля АТФ з АДФ необхідно
7,5 ккал енергії,
що є рівносильним різниці редокс-потенціалів 0,15-0,22 V.
Така енергія вивільнюється
при переході електронів:- від НАД до ФМН (1 комплекс),
- від цитохрому в до цитохрому с (3 комплекс),
- від цитохромоксидази аа3 до О2 (4 комплекс).
Слайд 55В НАД-залежних реакціях при окисненні 1 моля субстрату утворюється 3
АТФ,
у ФАД-залежних реакціях – 2 АТФ,
у випадку окиснення аскорбінової
кислоти–1АТФЗагальна кількість АТФ в організмі 30-50 г, але кожна молекула АТФ в клітині може «жити» менше хвилини.
Збільшення концентрації АДФ негайно приводить до прискорення дихання і фосфорилування.
Слайд 56Роз'єднання дихання і фосфорилування
Деякі хімічні речовини (протонофори) можуть переносити протони
або інші іони (іонофори) з міжмембранного простору через мембрану в
матрикс, минаючи протонні канали АТФ-синтази.В результаті зникає електрохімічний потенціал і припиняється синтез АТФ.
Це явище називається роз'єднанням дихання і фосфорилування.
Слайд 57В результаті роз'єднання кількість АТФ зменшується, а АДФ збільшується. Швидкість
окиснення НАДН і ФАДН2 підвищується, збільшується і кількість кисню, що
поглинається, але енергія виділяється тільки у вигляді теплоти.Приклади роз'єднуючих агентів:
дикумарол (антикоагулянт);
білірубін (метаболіт гему);
тироксин (гормон щитоподібної залози).
Всі вони проявляють свою дію тільки за умови високої концентрації.
Слайд 58МІКРОСОМАЛЬНЕ ОКИСНЕННЯ
Це ще один тип біологічного окиснення, який відбувається в
мікросомах (переважно в печінці і надниркових залозах) і пов'язаний з
безпосереднім включенням Оксигену в сполуку, яка окиснюється.В мікросомальному окисненні, на відміну від мітохондріального, Оксиген використовується не з енергетичною, а з «пластичною» метою.
Слайд 59 До ферментів мікросомального окиснення відтносяться
МОНООКСИГЕНАЗИ і ДИОКСИГЕНАЗИ.
Монооксигенази (гідроксилази) при окисненні речовини включають 1 атом
Оксигену. Диоксигенази каталізують реакції окиснення з включенням в молекулу 2 атомів молекули кисню.
Слайд 60ФУНКЦІЇ МІКРОСОМАЛЬНОГО ОКИСНЕННЯ:
Окиснення речовин циклічної структури, які не можуть окиснюватися
шляхом дегідрування (триптофан, гомогентизинова кислота та ін.);
Синтез стеринів (холестерин, жовчні
кислоти, гормони кіркової речовини надниркових залоз, статеві гормони);Метаболізм лікарських препаратів, а також знезараження токсичних речовин.
Слайд 61Утворення пероксиду водню.
При тканинному диханні можливе утворення пероксиду водню (Н2О2),
який є сильним окисником сульфгідрильних груп ферментів. Він токсичний для
клітин.В процесі еволюції утворився ряд ферментів, які його розщеплюють, в тому числі КАТАЛАЗА, що міститься в еритроцитах, в печінці та інших тканинах.