Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОБЩИЕ ВОПРОСЫ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
Содержание
- 1. ОБЩИЕ ВОПРОСЫ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
- 2. Н. Н. Бурденко (1946): «Стремление удалить инфекцию
- 3. Антимикробные средства относятся к лекарственным препаратам,
- 4. Отличительные особенности антибиотиков как лекарственных средствМишень действия
- 5. Классификация антибактериальных препаратов
- 6. История1906г – противосифилитический антибиотик сальварсан1936г – первый
- 7. Слайд 7
- 8. Антибиотикорезистентность - способность микроорганизмов сохранять жизнедеятельность на фоне применения терапевтических доз антибактериальных препаратов.
- 9. АнтибиотикорезистентностьПРИРОДНАЯОтсутствие у микроорганизма мишени для действия препаратаЯвляется
- 10. Факторы, способствующие росту антибиотикорезистентности Использование антибиотиков
- 11. Источники развития резистентностиМикробная клетка делится каждые 20
- 12. История развития резистентности стафилококков1885- открытие стафилококков1941- бензилпенициллин
- 13. Модификация мишени – MRSA (ORSA)Все β-
- 14. Основные антистафилококковые препаратыMSSAОксациллинЦефазолинЦефуроксимАмоксициллин/клавуланатМакролидыФторхинолоныMRSAВанкомицинЛинезолид (Зивокс)Даптомицин (Кубицин)Цефтаролин (Зинфоро)
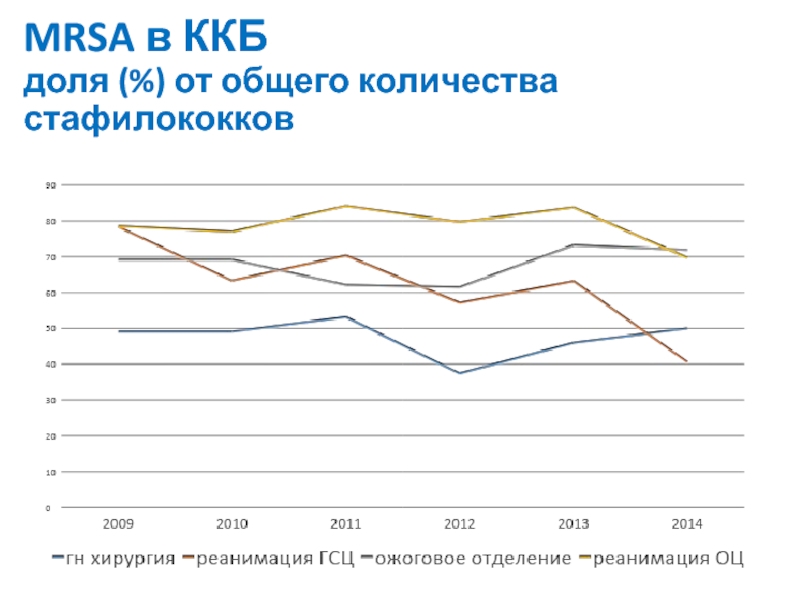
- 15. MRSA в ККБ доля (%) от общего количества стафилококков
- 16. Основной путь передачи MRSA- контактный Мытье рукИзоляция
- 17. Проблемные нозокомиальные возбудителиГлобальная проблема полирезистентных микроорганизмов в
- 18. Распространение полирезистентных микроорганизмов в ЛПУ ЕвропыMRSAVREK.pneu Ceph-R K.pneu Carb-R P.aerug Carb-R EARS-net, 2011
- 19. Распространенность БЛРС среди Enterobacteriaceae * S.K. Bouchillon
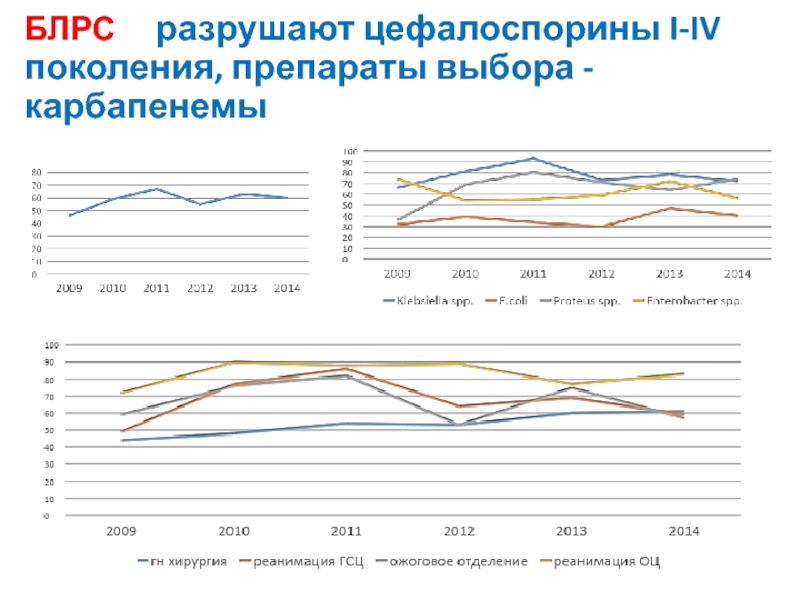
- 20. БЛРС разрушают цефалоспорины I-IV поколения, препараты выбора - карбапенемы
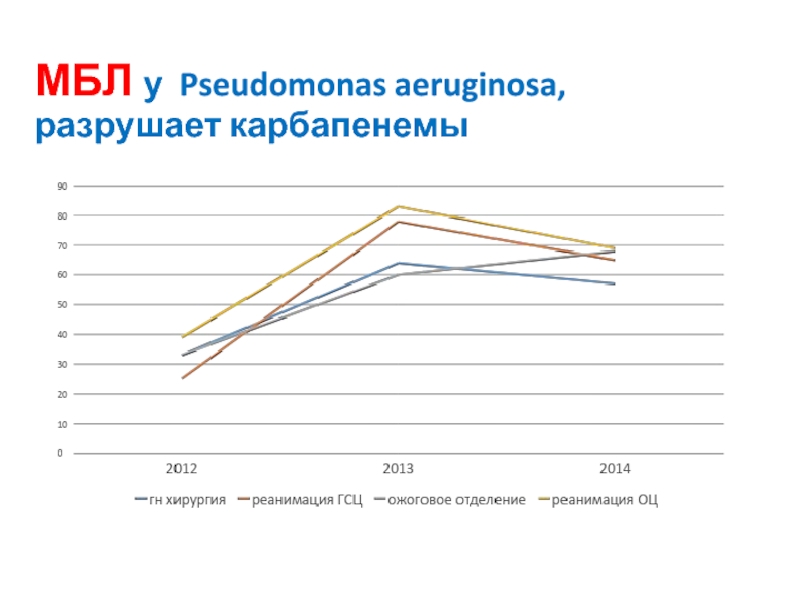
- 21. МБЛ у Pseudomonas aeruginosa, разрушает карбапенемы
- 22. Панрезистентные штаммы Р.aeruginosa, выделенные из раневого отделяемого в ККБ (устойчивость к 12 антибактериальным препаратам)
- 23. Яковлев С.В., материалы научно-практического семинара, Красноярск, 2014.
- 24. Инфекции, вызванные Pseudomonas aeruginosaНет «идеального» антибиотика.Сложности планирования
- 25. Особенности антибактериальной терапии синегнойной инфекцииМонотерапия – недостаточнаОбязательна
- 26. Факторы риска P.aeruginosa и выбор АБТДлительное нахождение
- 27. «Антимикробная резистентность стоит дорого и смертельно опасна»
- 28. Туризм в Индию: заселение кишечника бактериями Enterobacteriaceae
- 29. Алгоритм выбора антимикробных препаратов (эмпирическая АМТ)
- 30. Предположение об этиологии заболевания (стратификация пациентов) Внебольничные
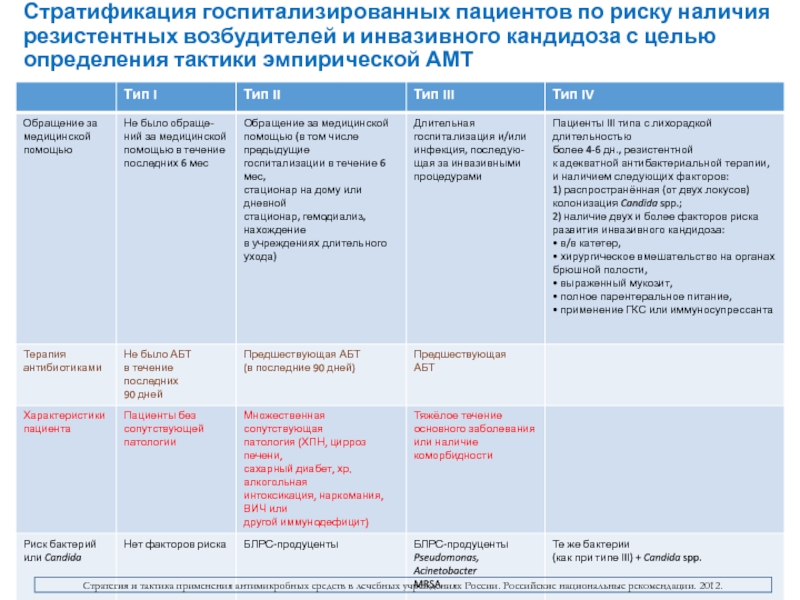
- 31. Стратификация госпитализированных пациентов по риску наличия резистентных
- 32. Резистентность пневмококков в России (ПЕГАС
- 33. Эмпирическая АБТ инфекций кожи и мягких тканей
- 34. Антимикробные препараты, не рекомендованные к применениюСтратегия
- 35. Ошибки микробиологической диагностикиВ спектр действия Азитромицина P.aeruginosa НЕ ВХОДИТ
- 36. Теория ≪параллельного ущерба≫Это селекция полирезистентных микроорганизмов.
- 37. Контроль антибиотикорезистентных штаммов – доказанная эффективность вмешательства
- 38. Оптимизация фармакодинамических параметров способна еще более повысить
- 39. Особенности макроорганизма
- 40. Аллергия на пенициллин в анамнезе Поздние реакции:Синдром
- 41. Аллергия на пенициллин в анамнезеНемедленные или ускоренные
- 42. Возрастные особенностиТетрациклиныНежелательное влияние на костную ткань и
- 43. Выведение антибактериальных препаратовПреимущественно почкамиАминогликозидыПенициллиныВанкомицинФторхтнолоныХинолоныЦефалоспорины (кроме цефоперазона)КарбапенемыПреимущественно печеньюМетронидазолРифампицинЭритромицинЦефоперазонДоксициклинКлиндамицинСульфониламиды
- 44. Дозирование АМП у пациентов с нарушением
- 45. Расчет клиренса креатинина у детей (формула
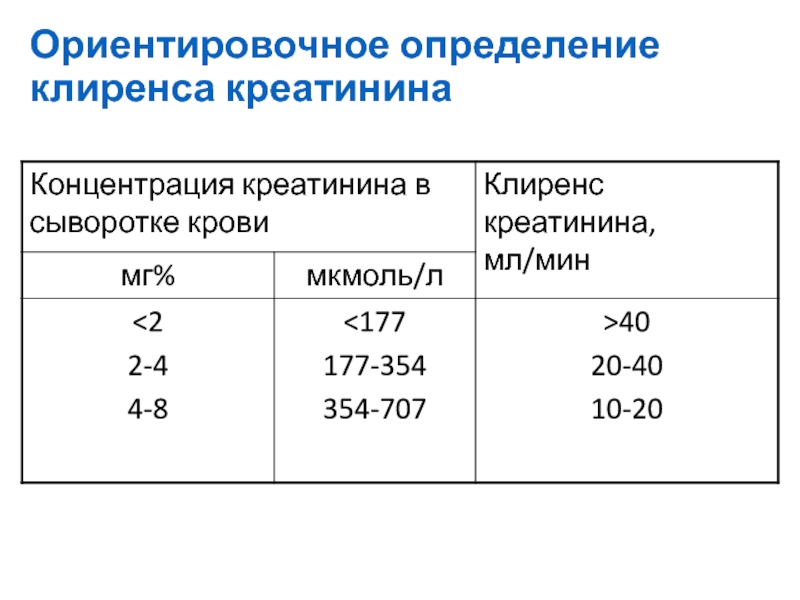
- 46. Ориентировочное определение клиренса креатинина
- 47. Слайд 47
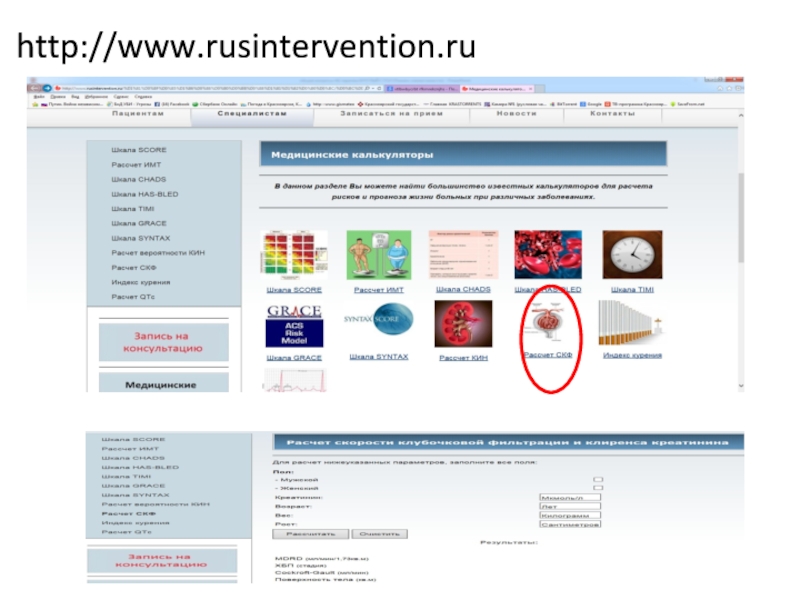
- 48. http://www.rusintervention.ru
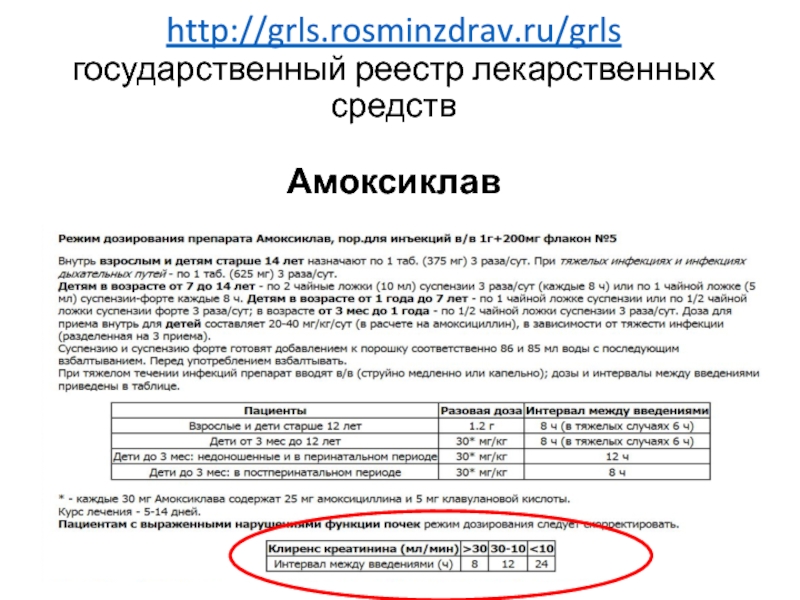
- 49. http://grls.rosminzdrav.ru/grls государственный реестр лекарственных средств Амоксиклав
- 50. Цефоперазон/сульбактамhttp://grls.rosminzdrav.ru/grls государственный реестр лекарственных средств
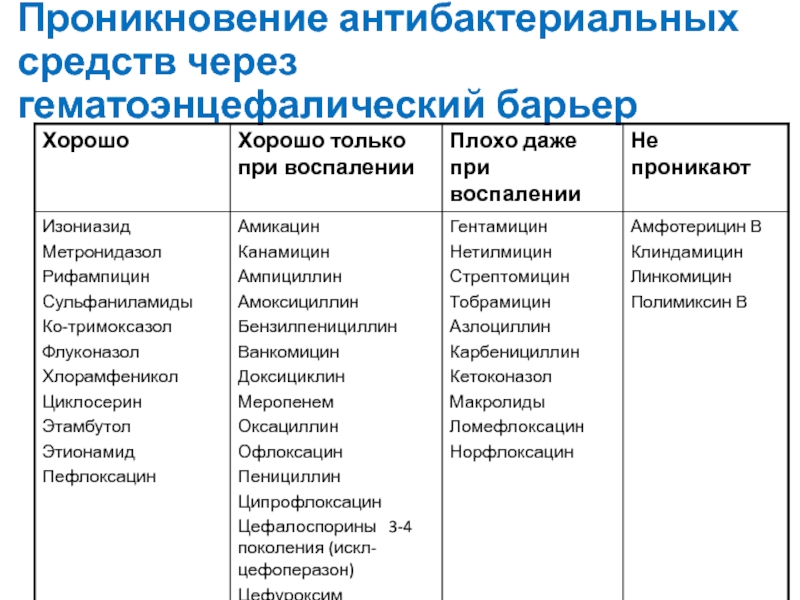
- 51. Проникновение антибактериальных средств через гематоэнцефалический барьер
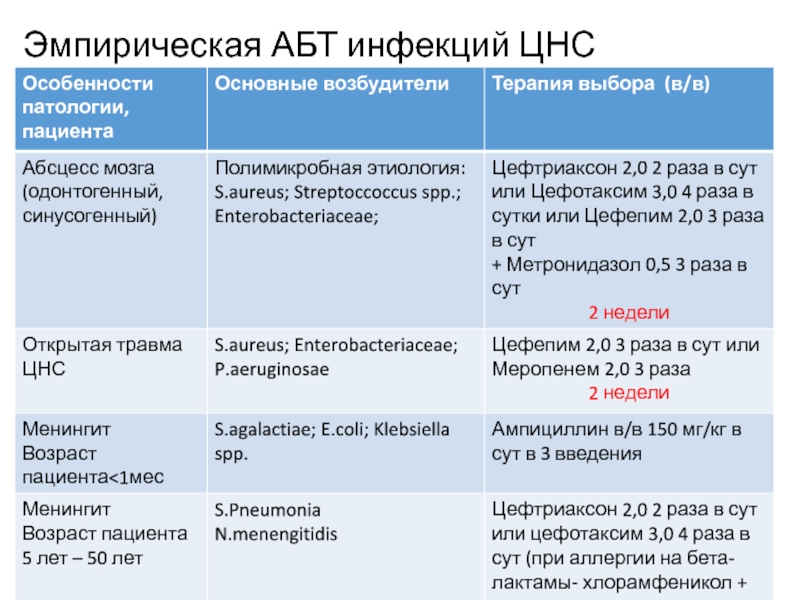
- 52. Эмпирическая АБТ инфекций ЦНС
- 53. Остеотропные антибиотикиОстеотропные (проникающих в костную ткань) антибактериальные препараты: ЛинкозамидыТетрациклиныФторхинолоны (офлоксацин > пефлоксацин > ципрофлоксацин)Макролиды Линезолид
- 54. ЛинкомицинСПЕКТР ДЕЙСТВИЯ: грам+, анаэробыМОЖНО: при аллергии на
- 55. FDA : Классификация лекарственных препаратов по критериям безопасности для плода
- 56. Антибактериальные средства при беременности
- 57. Возможность применения антибиотиков кормящим матерямРазрешеноПенициллиныЦефалоспориныЭритромицинАминогликозидыЛинкосамидыГликопептиды Абсолютно противопоказаныХлорамфениколТетрациклиныСульфониламидыСпирамицин, мидекамицин
- 58. Выбор пути введения АМП (1)Пероральный путь введения
- 59. Выбор пути введения АМП (2)Интратекальное, интравентрикулярное введение
- 60. Мониторинг эффективности терапииДинамика клинических симптомов заболевания
- 61. Причины неэффективности антибиотикотерапииНе бактериальная природа инфекции (вирусная,
- 62. Ступенчатая терапияПоследовательное назначение двух лекарственных форм одного
- 63. Основные показания для использования комбинаций АМПНаличие полимикробных
- 64. Типичные ошибкиИмипенем (торг. наим. Тиенам и др) + метронидазолАмоксициллин/клавуланат (торг. наим. Амоксиклав и др.) + метронидазол
- 65. Профилактика возникновения резистентности доказана только при инвазивной
- 66. Опасность нерационального использования комбинаций АМПАнтагонизм (например: комбинация
- 67. Профилактическое применение антибиотиков (1)Хирургическая антибиотикопрофилактика1 доза- за
- 68. Слайд 68
- 69. Нехирургическая антибиотикопрофилактикаВсем, независимо от факторов риска:При контакте
- 70. Состояния, требующие антибиотикопрофилактики инфекционного эндокардитаВИЧ-инфицированные и больные
- 71. Режимы антибиотикопрофилактики инфекционного эндокардита* В совокупности не
- 72. Взаимодействие антибиотиков с другими ЛП
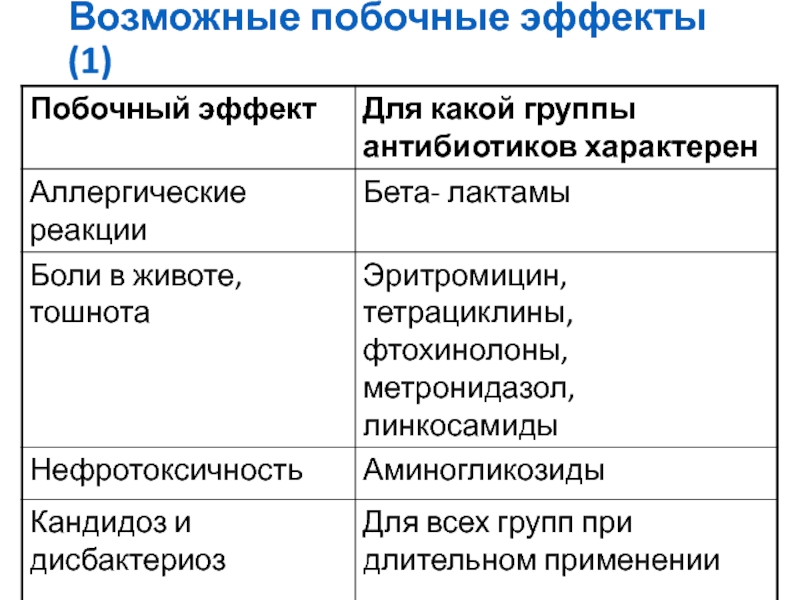
- 73. Возможные побочные эффекты (1)
- 74. Возможные побочные эффекты (2)
- 75. Средства «сопровождения» антимикробной терапииСтратегия и тактика рационального
- 76. Профилактическое назначение противогрибковых препаратов пациентам, получающим антимикробные
- 77. Стратификация госпитализированных пациентов по риску наличия резистентных
- 78. Профилактическое назначение противогрибковых препаратов Практическое руководство по антиинфекционной химиотерапии.2002.Трансплантация печениПовторные перфорации ЖКТ
- 79. Рекомендуемая профилактическая доза флуконазола 50-400 мг/сут Риск
- 80. Диагностически- значимые титры грибов рода Candida
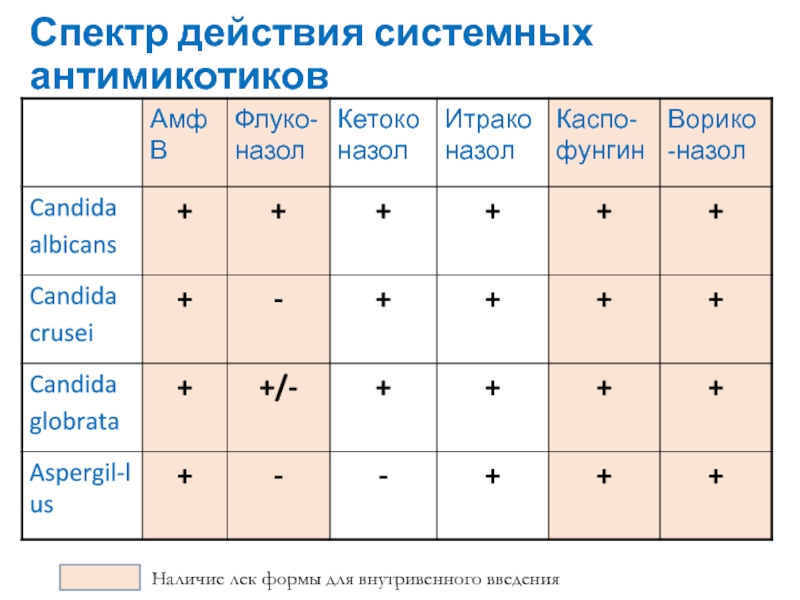
- 81. Спектр действия системных антимикотиковНаличие лек формы для внутривенного введения
- 82. Алгоритм обследования и терапии пациентов при выделении
- 83. КандидурияЭто наличие дрожжеподобных грибов рода Candida
- 84. Вероятные причины кандидурииКонтаминация во время сбора и
- 85. Диагностика кандидурииПовторное исследование мочи с соблюдением всех
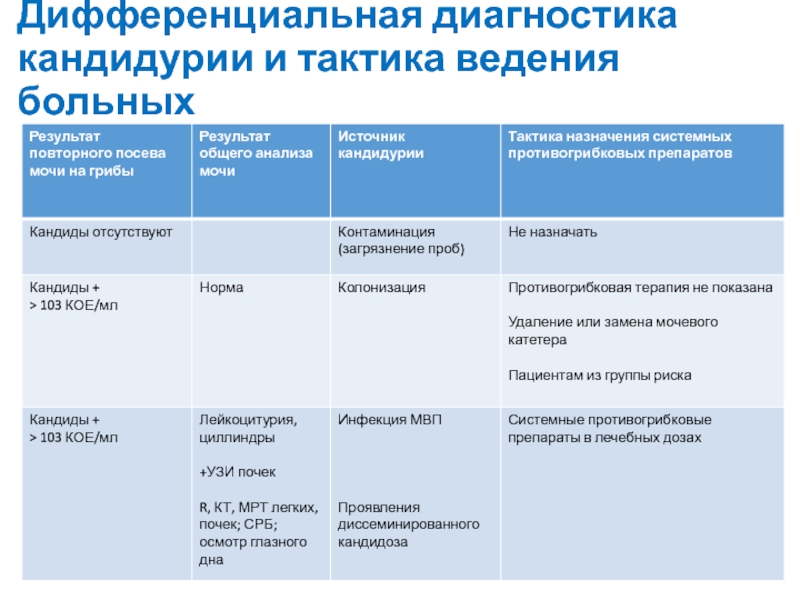
- 86. Дифференциальная диагностика кандидурии и тактика ведения больных
- 87. Показания к противогрибковой терапии при кандидурии:
- 88. Длительность противогрибковой терапииКандидемия и ОДК – 2
- 89. Спасибо за внимание!
- 90. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ОБЩИЕ ВОПРОСЫ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
Бочанова Елена Николаевна
к.м.н., доцент кафедры фармакологии с
курсами клинической фармакологии, фармтехнологии и ПО
Слайд 2Н. Н. Бурденко (1946): «Стремление удалить инфекцию было всегда задачей
врачей — хирургов сначала на основании эмпирического мышления, а затем
научного. Бактериологические средства в тот и другой период играли большую роль».Слайд 3 Антимикробные средства относятся к лекарственным препаратам, эффективность которых является наиболее
очевидной
Снижение летальности при наиболее тяжелых и широко распространенных инфекционных болезнях:
ТуберкулезПневмония
Менингит и др. …
Снижение заболеваемости некоторыми социально значимыми болезнями
Ревматическая лихорадка
Слайд 4Отличительные особенности антибиотиков как лекарственных средств
Мишень действия – микроорганизм.
Не действуют
на клетки макроорганизма.
Снижение активности и эффективности со временем.
Слайд 6История
1906г – противосифилитический антибиотик сальварсан
1936г – первый сульфаниламидный препарат
1941г –
пенициллин, первый природный антибиотик
В настоящее время:
Более 2000 антибиотиков,
Широко применяются
150.Слайд 8Антибиотикорезистентность
- способность микроорганизмов сохранять жизнедеятельность на фоне применения терапевтических
доз антибактериальных препаратов.
Слайд 9Антибиотикорезистентность
ПРИРОДНАЯ
Отсутствие у микроорганизма мишени для действия препарата
Является видовым признаком, используется
для идентификации
ПРИОБРЕТЕННАЯ
Появление в пределах вида микроорганизмов субпопуляции с
существенно более высоким значением для них МПК антибиотикаВсегда связана с каким нибудь биохимическим механизмом
Слайд 10Факторы, способствующие росту антибиотикорезистентности
Использование антибиотиков в сельском хозяйстве
в качестве кормовых добавок.
Использование антибактериальных средств в быту
(мыло, зубная паста с триклозаном, моющие средства с антисептиками).Безрецептурный отпуск антибиотиков.
Нерациональная антибактериальная терапия.
Слайд 11Источники развития резистентности
Микробная клетка делится каждые 20 минут.
За 10 часов
одна бактерия дает 1 000 000 потомков.
Мутации в любом гене
возникают у одной клетки из 10 000 000.Мутантные клетки подвергаются селекции при применении антибиотиков.
Селекция резистентных штаммов может быть причиной клинической неэффективности терапии.
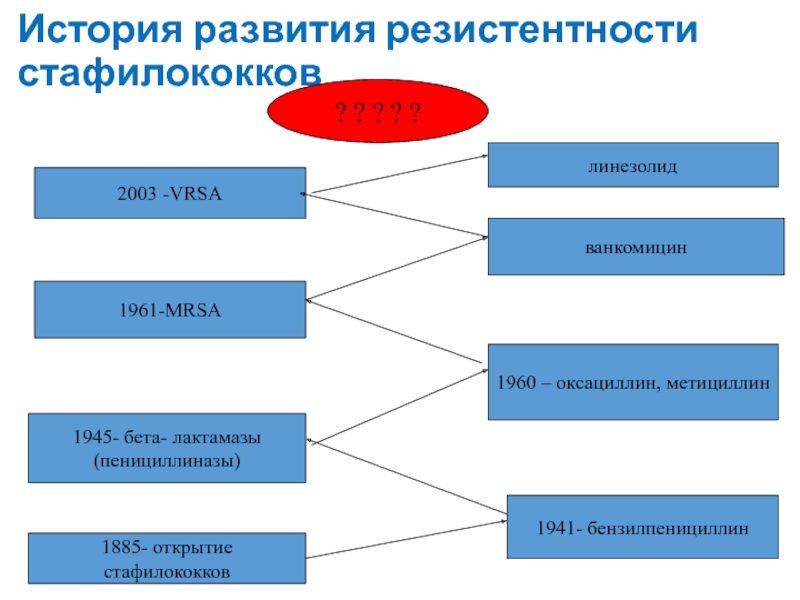
Слайд 12История развития резистентности стафилококков
1885- открытие стафилококков
1941- бензилпенициллин
1945- бета- лактамазы
(пенициллиназы)
1960 – оксациллин, метициллин
1961-MRSA
ванкомицин
2003 -VRSA
линезолид
? ? ? ?
?Слайд 13Модификация мишени – MRSA
(ORSA)
Все β- лактамные антибиотики не эффективны
(в том числе карбапенемы)
Макролиды,
линкозамиды, тетрациклины, аминогликозиды – высокая частота ассоциированной устойчивостиСлайд 14Основные антистафилококковые препараты
MSSA
Оксациллин
Цефазолин
Цефуроксим
Амоксициллин/клавуланат
Макролиды
Фторхинолоны
MRSA
Ванкомицин
Линезолид (Зивокс)
Даптомицин (Кубицин)
Цефтаролин (Зинфоро)
Слайд 16Основной путь передачи MRSA- контактный
Мытье рук
Изоляция пациентов
Обработка фонендоскопов
Проблема сотовых
телефонов…..
Украшения на руках, накладные ногти…..
Санация носителей MRSA
(источники внебольничных MRSA?)
Бактробан – интраназальная мазьХроническое носительство – санация членов семьи, включая домашних животных
Носительство MRSA повышает риск развития аутоимунных заболеваний
Слайд 17Проблемные нозокомиальные возбудители
Глобальная проблема полирезистентных микроорганизмов в ЛПУ: ESCAPE
E
Enterococcus faecium
S Staphylococcus aureus
С Clostridium difficile
A Acinetobacter
baumanii P Pseudomonas aeruginosa
E Enterobacteriaceae (Klebsiella, E.coli)
Яковлев С.В., 2014
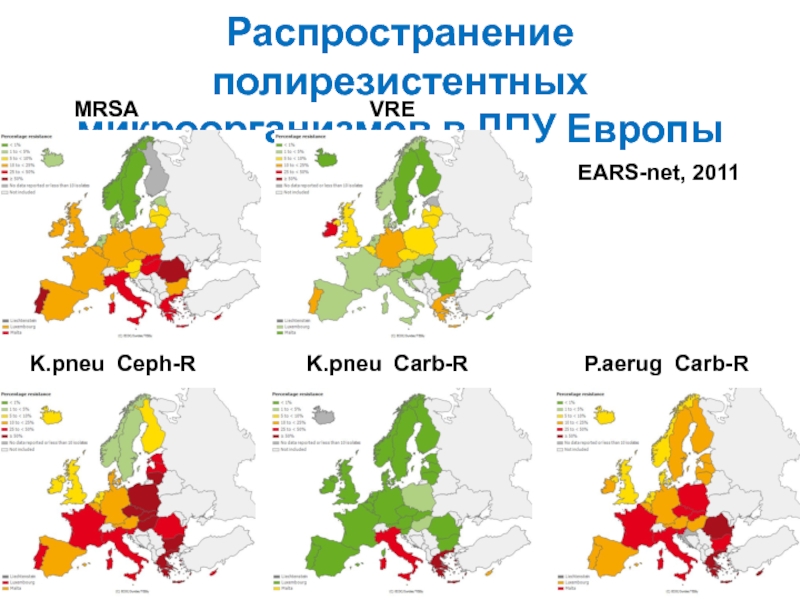
Слайд 18Распространение полирезистентных микроорганизмов в ЛПУ Европы
MRSA
VRE
K.pneu Ceph-R
K.pneu Carb-R
P.aerug
Carb-R
EARS-net, 2011
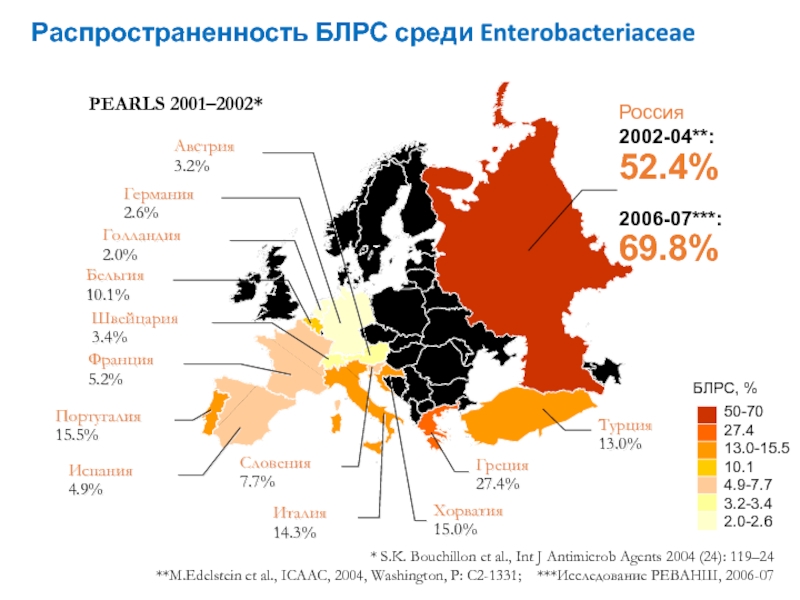
Слайд 19Распространенность БЛРС среди Enterobacteriaceae
* S.K. Bouchillon et al., Int
J Antimicrob Agents 2004 (24): 119–24
**M.Edelstein et al., ICAAC, 2004,
Washington, P: C2-1331; ***Исследование РЕВАНШ, 2006-07 Россия
2002-04**:
52.4%
2006-07***:
69.8%
Слайд 22Панрезистентные штаммы Р.aeruginosa, выделенные из раневого отделяемого в ККБ (устойчивость
к 12 антибактериальным препаратам)
Слайд 24Инфекции, вызванные Pseudomonas aeruginosa
Нет «идеального» антибиотика.
Сложности планирования терапии при отсутствии
данных локального мониторинга устойчивости.
При сохранения чувствительности лечения целесообразно начинать с
антипсевдомонадного цефалоспорина.Оправданы максимальные дозы.
Имипенем и ципрофлоксацин способствуют селекции полирезистентных штаммов.
В случае панрезистентных штаммов целесообразно определение МПК и длительная инфузия антибиотиков.
Слайд 25Особенности антибактериальной терапии синегнойной инфекции
Монотерапия – недостаточна
Обязательна комбинация с другим
антисинегнойным АБ, например:
Цефтазидим 6,0 + амикацин 1,0 в сутки
Цефоперазон 8,0
+ амикацин 1,0 в сутки Ципрофлоксацин 1,2 + амикацин 1,0 в сутки
Цефепим 6,0 + амикацин 1,0 в сутки
Имипенем 2,0 – 3,0 + амикацин 1,0 в сутки
Меропенем 3,0 – 6,0 + амикацин 1,0 в сутки
Амикацин – 15мг/кг в сутки у взрослых, 1 раз в день
Слайд 26Факторы риска P.aeruginosa и выбор АБТ
Длительное нахождение в ОРИТ (>
5 суток), ИВЛ
Иммуносупрессия (цитостатики, глюкокортикоиды, нейтропения)
Бронхоэктазы
Мочевой катетер
Рекомендации по выбору антибиотика
Антибиотики Факторы
риска P.aeruginosaЕсть Нет
Карбапенемы Ими-, Меро-, Дори- Эртапенем
Цефалоспорины Цефтазидим, Цефепим Цефтриаксон, Цефотаксим
Фторхинолоны Ципрофлоксацин Офло-, Пефло-, Мокси-
Левофлоксацин
Стратегия и тактика применения антимикробных средств в лечебных учреждениях России. Практические рекомендации, 2012 г. www.antimicrob.net
Слайд 27«Антимикробная резистентность стоит дорого и смертельно опасна»
Alisson Mc. Geer
Необходимые мероприятия для борьбы с антибиотикорезистентностью:
Обучение
Снижение общей частоты использования антибиотиков.
Исключение безрецептурной продажи.
Инфекционный контроль в стационаре.
Запрет использования в ветеринарии.
Слайд 28Туризм в Индию: заселение кишечника бактериями Enterobacteriaceae - продуцентами Нью-Дели металло-β-лактамаз
(NDM-1)
санация кишечника в течение 3- месяцев
Слайд 30Предположение об этиологии заболевания (стратификация пациентов)
Внебольничные инфекции
Внебольничные инфекции –
тип I
Внебольничные инфекции с факторами риска антибиотико-резистентности – тип II
Нозокомиальные
инфекции (НИ) =Инфекции, связанные с оказанием медицинской помощи (ИСОМП) > 48ч от поступления в стационар
Нозокомиальные инфекции – тип III
Нозокомиальные инфекции с риском развития инвазивного микоза – тип IV
Стратегия и тактика применения антимикробных средств в лечебных учреждениях России. Российские национальные рекомендации. 2012.
Слайд 31Стратификация госпитализированных пациентов по риску наличия резистентных возбудителей и инвазивного
кандидоза с целью определения тактики эмпирической АМТ
Стратегия и тактика применения
антимикробных средств в лечебных учреждениях России. Российские национальные рекомендации. 2012. Слайд 32Резистентность пневмококков
в России (ПЕГАС III )
Пенициллин – 11%
Тетрациклин
– 24,6%
Триметоприм/сульфометаксазол- 39%
Макролиды- 6-8%
Цефуроксим – 2%
Цефтриаксон, цефотаксим – 1%
Амоксициллин/кк –
0,4%Ванкомицин - 0
Респираторные фторхинолоны - 0
Эртапенем – 0
КМАХ, 2010, том 12, №4
Резистентность E. coli
при инфекциях мочевыводящих путей
Триметоприм/сульфометаксазол – 38%
Ампициллин – 37-46%
Амоксициллин/клавуланат – 6%
Цефуроксим – 6%
Нитрофурантоин (фурадонин)- 3%
Гентамицин – 12%
Цефтриаксон – 3%
Фосфомицин –1%
Лечащий врач, 2012, №8
Слайд 34Антимикробные препараты,
не рекомендованные к применению
Стратегия и тактика рационального применения
антимикробных средств в амбулаторной практике. Российские практические рекомендации. Москва, 2014.
Слайд 36Теория ≪параллельного ущерба≫
Это селекция полирезистентных микроорганизмов.
Отличительным
моментом параллельного ущерба как более широкого понятия является селекция резистентности
не только и не столько среди штаммов возбудителей, на которых была направлена антибактериальная терапия, но и среди микроорганизмов, не являвшихся этиологически значимыми, более того – среди микроорганизмов, изначально даже не входивших в спектр активности препарата.Цефалоспорины являются наиболее «неблагонадёжными» антибиотиками, использование которых сопровождается выраженным параллельным ущербом.
Карбапенемы и комбинации бета-лактамов с ингибиторами бета-лактамаз являются в этом смысле относительно безопасными.
Стратегия и тактика применения антимикробных средств в лечебных учреждениях России. Российские национальные рекомендации. 2012.
Слайд 37Контроль антибиотикорезистентных штаммов – доказанная эффективность вмешательства
Уменьшение использования Эффект
Цефалоспоринов III
пок. Снижение частоты БЛРС,
энтерококков
Фторхинолонов
Снижение частоты MRSA,полирезист. P.aeruginosa,
C.difficile
Анти-П карбапенемы Замена на эртапенем (имипенем, меро-; дори-) уменьшение полирезистент- ной P.aeruginosa
Gould I, JAC 2008;61:763-5
Davey P, e.a. Cochrane Database Syst Rev 2005;issue 4:CD003543
Bosso JA, Mauldin PD. AAC 2006;50:2106-12
Charbonneau P, e.a. CID 2006;42:778-84
Goldstein E.J.C., IDSA 2006. Lima A.M., ICAAC 2009
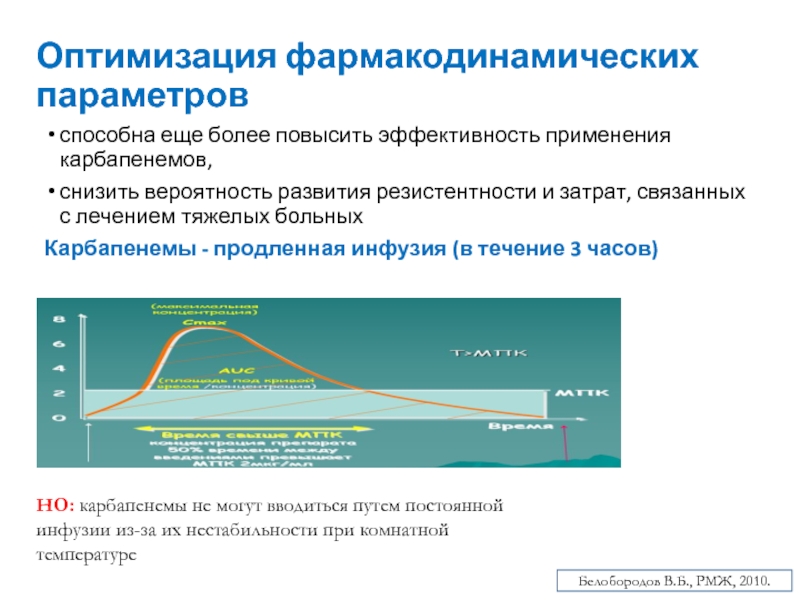
Слайд 38Оптимизация фармакодинамических параметров
способна еще более повысить эффективность применения карбапенемов,
снизить вероятность развития резистентности и затрат, связанных с лечением тяжелых
больных Карбапенемы - продленная инфузия (в течение 3 часов)
Белобородов В.Б., РМЖ, 2010.
НО: карбапенемы не могут вводиться путем постоянной инфузии из-за их нестабильности при комнатной температуре
Слайд 40Аллергия на пенициллин в анамнезе
Поздние реакции:
Синдром Стивенсона – Джонсона
Синдром
Лайелла
Сывороточная болезнь
Интерстициальный нефрит
Избегать назначения всех бета- лактамных антибиотиков (пенициллины, цефалоспорины,
карбапенемы, монобактамы)Слайд 41Аллергия на пенициллин в анамнезе
Немедленные или ускоренные реакции:
Крапивница
Отек Квинке
Избегать применения
антибиотиков, вызывающих перекрестные реакции с пенициллином:
Полусинтетические пенициллины (около 100%)
Цефалоспорины 1
поколения (10%)Карбапенемы (50%)
Цефалоспорины 2-3 поколения – 1-3%
Слайд 42Возрастные особенности
Тетрациклины
Нежелательное влияние на костную ткань и зубы. Противопоказаны до
8 лет
Фторхинолоны
Риск нарушения формирования костно- суставной системы. Официально не разрешены
к применению у детей.Особенности у новорожденных детей
Аминогликозиды
Объем распределения у новорожденных больше, поэтому доза на кг массы тела выше. Период полувыведения увеличен
Хлорамфеникол (Левомицетин)
Инактивация замедлена в связи с дефицитом ферментов цитохрома Р450 – «серый синдром», тяжелые нарушения кроветворения
Цефтриаксон
Конкурентное вытеснение билирубина из связи с белками плазмы крови – риск развития ядерной желтухи
Слайд 43Выведение антибактериальных препаратов
Преимущественно почками
Аминогликозиды
Пенициллины
Ванкомицин
Фторхтнолоны
Хинолоны
Цефалоспорины (кроме цефоперазона)
Карбапенемы
Преимущественно печенью
Метронидазол
Рифампицин
Эритромицин
Цефоперазон
Доксициклин
Клиндамицин
Сульфониламиды
Слайд 44Дозирование АМП у пациентов с нарушением функции почек: только 30% больных
находится в ОРИТ.
ошибки дозирования ЛП в 70% случаев.
Расчет клиренса креатинина
(адаптированная формула Кокрофта и Голта)
У мужчин:
(140- возраст)×масса тела (кг)
0,8 ×креатинин сыворотки крови(мкмоль/л)
Клиренс креатинина у женщин=0,85 × клиренс креатинина у мужчин
При ожирении используется долженствующая масса тела
Слайд 45Расчет клиренса креатинина у детей
(формула Шварца)
Длина тела (см) ×11,3
× к
Креатинин сыворотки(мкмоль/л)
к – возрастной коэффициент перерасчета
0,33 – недоношенные новорожденные
в возрасте до 2 лет0,45 - доношенные новорожденные в возрасте до 2 лет
0,55 – дети в возрасте 2-14 лет
0,55 – девочки старше 14 лет
0,7 – мальчики сарше 14 лет
Слайд 50Цефоперазон/сульбактам
http://grls.rosminzdrav.ru/grls
государственный реестр лекарственных средств
Слайд 53Остеотропные антибиотики
Остеотропные (проникающих в костную ткань) антибактериальные препараты:
Линкозамиды
Тетрациклины
Фторхинолоны (офлоксацин
> пефлоксацин > ципрофлоксацин)
Макролиды
Линезолид
Слайд 54Линкомицин
СПЕКТР ДЕЙСТВИЯ: грам+, анаэробы
МОЖНО: при аллергии на бета-лактамные антибиотики
НЕЛЬЗЯ: назначать
беременным и кормящим
Усиливает действие ЛП для ингаляционного наркоза, миорелаксантов и
опиоидных анальгетиков, повышая риск нервно-мышечной блокады и остановки дыхания.Слайд 57Возможность применения антибиотиков кормящим матерям
Разрешено
Пенициллины
Цефалоспорины
Эритромицин
Аминогликозиды
Линкосамиды
Гликопептиды
Абсолютно противопоказаны
Хлорамфеникол
Тетрациклины
Сульфониламиды
Спирамицин, мидекамицин
Слайд 58Выбор пути введения АМП (1)
Пероральный путь введения при лечении нетяжелых
инфекций (комплайнс, связь с приемом пищи, лекарственные взаимодействия)
Парентеральное введение для
АМП с низкой биодоступностью (ванкомицин, аминогликозиды) – возможность достижения более высоких концентраций. Внутривенно- возможность введения больших концентраций ЛС при небольшом дискомфорте для пациента при угрожающих жизни инфекциях (сепсис), при нарушениях всасывания ЛП.
Слайд 59Выбор пути введения АМП (2)
Интратекальное, интравентрикулярное введение АМП- крайне редко.
В/в
и в/м введение АМП позволяет достичь терапевтических концентраций в плевральной,
перикардиальной, перитонеальной и синовиальной полостях, поэтому введение АМП непосредственно в эти области НЕ рекомендуется.Слайд 60Мониторинг эффективности терапии
Динамика клинических симптомов заболевания (48- 72ч).
Мониторинг
сывороточных концентраций (аминогликозиды).
Определение бактерицидного титра сыворотки крови.
Отсутствие необходимости «плановой» смены
антибиотиков(кроме аминогликозидов в связи с высоким риском развития побочных эффектов)
Слайд 61Причины неэффективности антибиотикотерапии
Не бактериальная природа инфекции (вирусная, грибковая).
Применение АМП неадекватного
спектра действия.
Нарушение кратности дозирования в течение суток.
Применение неадекватных доз АМП.
Выбор
нерационального пути введения.Наличие инородного тела или не дренируемого очага.
Слайд 62Ступенчатая терапия
Последовательное назначение двух лекарственных форм одного антибиотика
в/в →
per os
Преимущества:
Снижение риска постинъекционных осложнений.
Снижение нагрузки на
м/с.Снижение затрат.
Слайд 63Основные показания для использования комбинаций АМП
Наличие полимикробных инфекций (аэробы+ анаэробы).
Альтернатива
– монотерапия: карбапенемы, ингибиторзащищенные пенициллины, антианаэробные фторхинолоны
Эмпирическая терапия у пациентов
с нейтропениями или инфекциями неясной этиологии до получения результатов микробиологического исследования (Альтернатива - монотерапия при использовании карбапенемов и антианаэробных фторхинолонов)Слайд 64Типичные ошибки
Имипенем (торг. наим. Тиенам и др) + метронидазол
Амоксициллин/клавуланат (торг.
наим. Амоксиклав и др.) + метронидазол
Слайд 65Профилактика возникновения резистентности доказана только при инвазивной синегнойной инфекции и
туберкулезе.
Нет данных, подтверждающих снижение токсичности АМП при проведении комбинированной терапии.
Не
снижать дозы каждого антибиотика при проведении комбинированной терапии!Слайд 66Опасность нерационального использования комбинаций АМП
Антагонизм
(например: комбинация 2 бета- лактамных
антибиотиков при лечении синегнойной инфекции)
Нежелательные реакции
(5% пациентов в стационаре)
Существенное
и неоправданное увеличение стоимости.Слайд 67Профилактическое применение антибиотиков (1)
Хирургическая антибиотикопрофилактика
1 доза- за 30 мин до
операции в/в или во время вводного наркоза.
Слайд 69Нехирургическая антибиотикопрофилактика
Всем, независимо от факторов риска:
При контакте с больным дифтерией,
коклюшем (макролиды), менингококковой инфекцией (цефтриаксон)
При вероятности заражения заболеваниями, передающимися половым
путем (фторхинолон+ макролид +метронидазол или цефтриаксон + доксициклин + метронидазол)При укушенных ранах (феноксиметилпенициллин, амоксициллин/клавуланат)
Слайд 70Состояния, требующие антибиотикопрофилактики инфекционного эндокардита
ВИЧ-инфицированные и больные СПИДом пациенты не
относятся к категории более высокого риска, чем здоровые пациенты и
не требуют антибиотикопрофилактики (например, при рутинном стоматологическом лечении)Слайд 71Режимы антибиотикопрофилактики инфекционного эндокардита
* В совокупности не должно превышать дозу
для взрослых
Микробиология и иммунология для стоматологов. М, Практическая медицина,
2010Слайд 75Средства «сопровождения» антимикробной терапии
Стратегия и тактика рационального применения антимикробных средств
в амбулаторной практике. Российские практические рекомендации. Москва, 2014.
Слайд 76Профилактическое назначение противогрибковых препаратов пациентам, получающим антимикробные препараты, необоснованно
Низкий риск развития кандидоза полости рта, половых органов – менее
5%.В случае развития кандидоза терапия не взывает затруднений.
Исключение:
пациенты, имеющие специфические факторы риска (нейтропения на фоне приема цитостатиков, трансплантация печени, почек, кроветворных стволовых клеток)
Слайд 77Стратификация госпитализированных пациентов по риску наличия резистентных возбудителей и инвазивного
кандидоза с целью определения тактики эмпирической АМТ
Стратегия и тактика применения
антимикробных средств в лечебных учреждениях России. Российские национальные рекомендации. 2012. Слайд 78Профилактическое назначение противогрибковых препаратов
Практическое руководство по антиинфекционной химиотерапии.2002.
Трансплантация печени
Повторные
перфорации ЖКТ
Слайд 79Рекомендуемая профилактическая доза флуконазола 50-400 мг/сут
Риск инвазивного кандидоза:
Состояние пациента стабильное,
не было предшествующего применения азолов (флуконазол) – стартовая терапия флуконазол
Состояние
пациента тяжелое, недавнее применение азолов или выделение видов Candida –non –albicans стратовая терапия эхинокандины (каспофунгин и др.)Кандидемия – абсолютное показание к проведению противогрибковой терапии
Стратегия и тактика применения антимикробных средств в лечебных учреждениях России. Российские национальные рекомендации. 2012.
Слайд 82Алгоритм обследования и терапии пациентов при выделении грибов рода Candida≥104
в мокроте повторное исследование мокроты на грибы с соблюдением ВСЕХ
правил забора материала + посев на грибы мазка из ротовой полостиСлайд 83Кандидурия
Это наличие дрожжеподобных грибов рода Candida в моче:
в
концентрации > 103 КОЕ/мл
в 2 ее последовательных исследованиях
У
госпитализированных пациентов 5%, в ОИТ - до 20%
Наличие в общем анализе мочи результата «дрожжевые грибы +++»
не является обоснованием назначения противогрибковых препаратов
Слайд 84Вероятные причины кандидурии
Контаминация во время сбора и транспортировки мочи
Колонизация мочевыводящих
путей (МВП)
(в основном, у пациентов с установленными мочевыми катетерами)Локальная инфекция нижних (цистит, уретрит) и верхних (пиелонефрит) МВП
Диссеминированный кандидоз с поражением МВП
Слайд 85Диагностика кандидурии
Повторное исследование мочи с соблюдением всех правил ее сбора
Микроскопическое
исследование мочи (подсчет лейкоцитов и цилиндров)
При подозрении на диссеминированный кандидоз:
рентгенологическое исследование органов грудной полости, УЗИ почек и др., микробиологическое исследование крови и других возможных источников инфекцииСлайд 87 Показания к противогрибковой терапии при кандидурии: флуконазол 3 мг /кг/сут в
течение 1-2 недель
Кандидурия является одним из проявлений диссеминированной грибковой инфекции
Кандидурия
является проявлением грибкового поражения МВППациент относится к группе риска развития диссеминированной грибковой инфекции (нейтропения, недоношенные дети с низкой массой тела)
Указания на недавно проводившиеся урологические инструментальные вмешательства, перед урологическими манипуляциями;
После трансплантации почки
Практическое руководство по антиинфекционной химиотерапии.2002.
Слайд 88Длительность противогрибковой терапии
Кандидемия и ОДК –
2 нед после исчезновения
всех симптомов
Менингит – 4 нед после исчезновения всех симптомов
Перитонит –
14-21 деньЭндокардит – 6-12 нед
Ретинит – 6-12 нед
Кандидоз пищевода – 14-28 дней
Кандидоз кожи – 7-14 дней
«Резистентная к антибиотикам фебрильная нейтропения» - 7 дней после нормализации температуры тела, а так же после завершения периода агранулоцитоза